Doymamış buhar formülü. Doymuş ve doymamış buhar
Doymamış ve doymuş buharlar
Bir sıvının serbest yüzeyinin üzerinde, her zaman bu sıvının buharlaşma nedeniyle oluşan buharları vardır. Sıvının serbest yüzeyinin üzerindeki boşluk herhangi bir duvarla sınırlı değilse, buharlaşan maddenin molekülleri veya atomları kaotik termal hareket yaparak sıvının yüzeyinden uzaklaşır. Bir sıvının yüzeyinden buhar parçacıklarının uzaklaştırılması, difüzyon olgusunun yanı sıra hava katmanlarının doğal veya yapay konveksiyonu ile kolaylaştırılır. Buhar partikül konsantrasyonu Sabit sıcaklık bu koşullar altında hem azalma hem de artış yönünde geniş bir aralıkta değişebilir. Bu tür çiftlere doymamış denir.
Sıvının serbest yüzeyinin üzerinde sınırlı bir boşluk varsa farklı bir resim gözlemlenir. Buharlaşan sıvının buharları dışında başka gazlı maddelerle dolu olup olmadığı önemli değildir. Kapalı bir alana buharlaşma sürecinin ancak belirli bir sınıra kadar gerçekleşebileceğini belirtmek önemlidir. Buhar halindeki buharlaşan maddenin moleküllerinin veya atomlarının konsantrasyonu ne kadar büyük olursa, bu buharların sabit sıcaklıktaki basıncı o kadar büyük olur. Bu durumda, artan sayıda molekül veya atom serbest yüzeyden sıvıya geri dönebilir. Eğer buhara verilen boşluk yeterince küçük ve sıvı yeterince büyükse, dinamik denge şu şekilde kurulabilir: Birim zamanda sıvıdan ayrılan parçacıkların sayısı, aynı zaman aralığında sıvıya dönen parçacıkların sayısına eşittir. Bu durumda, sıvının üzerinde sabit bir buhar kütlesi olacaktır ve bu koşullar altında parçacıklarının daha yüksek bir konsantrasyonu elde edilemez. Bu tür buhara doymuş denir.
Baskı yapmak doymuş buhar Belirli bir sıcaklıktaki bazı maddelerin bir tanesi olabilir - tek kesin değer.
Belirli bir maddenin doymuş bir buharına sabit bir sıcaklıkta sağlanan alan hacmindeki bir azalma, parçacıklarının konsantrasyonu belirli bir değeri aşamadığından, buharın bir kısmının bir sıvıya yoğunlaşmasına yol açar. Bu izotermal sıkıştırma doymuş buharlar sıradan ideal gazlar gibi davranan doymamış buharların sıkıştırılmasından farklıdır. Bu nedenle Boyle-Mariotte yasası doymuş buharlar için geçerli değildir.
Gay-Lussac yasası doymuş buharlar için de geçerli değildir, çünkü onlara sağlanan hacim sıcaklıktan bağımsızdır.
Doymuş buhar ve Charles yasası için geçerli değildir. artan sıcaklık ile ideal gazlar veya doymamış buharlar izokorik süreçte, ortalama kinetik enerji birbirleriyle ve geminin duvarlarıyla daha sık çarpışmalarına yol açan parçacıkları, yani. basınçta bir artışa.
Belirli bir kapalı kabın tam olarak bir maddenin doymuş buharını içerdiğinden, ancak kap bu maddeyi içinde bulunduruyorsa güvenle konuşmak mümkündür. sıvı hal ve sıvı fazının kütlesi değişmez.
Örneğin önümüze kapalı bir cam kap koyarlar ve herhangi bir ölçüm yapmadan doymuş veya doymamış su buharı içerip içermediğini belirlememizi isterler.
Bu soruyu cevaplamak için, kabın içeriğinin çevredeki hava ile termodinamik dengeye gelmesi için birkaç dakika beklemeniz gerekir. Bunun nedeni, kabın odadan hangi sıcaklıkta getirildiğini bilmememizdir ve sabit bir hacimde buharın sıcaklığındaki bir değişiklik, buharı doymamış bir durumdan doymuş bir duruma getirebilir ve bunun tersi de geçerlidir. . Denge kurulduktan sonra kabın iç duvarlarında su yoğuşması olmazsa, gözlemin yapıldığı sıcaklıkta kabın doymamış buhar içerdiğini söylemeliyiz. Kabın duvarlarında su damlacıkları belirirse, buhar doymuştur.
Havadaki su buharı
Dünyanın atmosferi her zaman su buharı içerir. Onların varlığı çok sık hesaba katılmalıdır. Özellikle kapalı veya yetersiz havalandırılan odalarda, kurutma odalarında vb. hava nemi doğru bir şekilde değerlendirilmelidir.
İçin niceleme havadaki su buharı içeriği, iki değer kullanılır - mutlak nem (f) ve bağıl nem(AT).
Mutlak nem denir fiziksel miktar, bir metreküp havanın içerdiği su buharı kütlesi ile ölçülür. Böylece, mutlak nem yoğunluk boyutuyla örtüşür, ancak pratikte genellikle bir birim kullanırlar - 1 g / m3.
İkinci durum, g/m3 cinsinden ifade edilen mutlak nemin f'nin, aynı koşullar altında milimetre cıva cinsinden ölçülen su buharının kısmi basıncından p sayısal değer olarak çok az farklı olması gerçeğinden kaynaklanmaktadır.
Havadaki su buharının kısmi basıncının p doymuş su buharı basıncına yüzde oranı p n.p. belirli bir sıcaklıkta bağıl nem denir:
Bu formülü kullanarak bağıl nemi hesaplarken, basınç p ve p n.s. aynı birimlerde ölçülmelidir. Genellikle paskal cinsinden değil, milimetre cıva cinsinden ölçülürler. p n.s değeri tablolardan belirlenir.
Soğutma sırasında havanın su buharına doyduğu sıcaklığa çiğ noktası denir.
2. Ders
ISI TRANSFERİNİN TEMELLERİ
Isı transferi, cisimler arasındaki ısı transfer süreçlerinin modellerini ve ısının bir cisim içindeki dağılımını inceleyen bir bilimdir. Makinelerin, motorların, aparatların vb. çalışma süreçlerinde hemen hemen her yerde meydana gelen ısı akışlarını kontrol etmek için ısı transferi yasalarının incelenmesi gereklidir.
Isı transferi teorisinde iki ana soru göz önünde bulundurulur:
I. Belirli koşullar altında bir vücuttan diğerine aktarılan veya vücudun bir bölümünden diğerine geçen ısı miktarının belirlenmesi.
II. Isı transferi sürecinde yer alan vücudun farklı bölgelerindeki sıcaklığın belirlenmesi.
Isı transferi için gerekli ve yeterli bir koşul sıcaklık farkıdır.
Isı üç şekilde aktarılır: iletim, konveksiyon ve radyasyon.
Termal iletkenlik, vücudun ayrı ayrı bölümlerinin farklı sıcaklıklarla doğrudan teması yoluyla termal enerjinin dağıtılması sürecidir.
Konveksiyon, uzayda bir sıcaklıktaki bir alandan farklı bir sıcaklıktaki bir alana sıvı veya gaz hacimlerini taşırken enerji transferi işlemidir.
Radyasyon (radyan ısı transferi), elektromanyetik dalgalarla enerji transferi sürecidir. Radyasyonla ısı transferi, enerjinin çifte dönüşümüdür: daha sıcak bir cisim enerjiyi elektromanyetik salınımlar şeklinde yayar, daha az ısıtılan başka bir cisim enerjiyi emer ve ısıtır.
Genellikle, cisimler arasındaki ısı alışverişi her üç şekilde de aynı anda gerçekleşir. Bunların kombinasyonu en çeşitli olabilir. Bu durumda, ısı transferinin gerçekleştiği koşullara bağlı olarak bir yöntem diğerine üstün gelebilir.
Bununla birlikte, ısı transferi süreçlerini incelerken, farklı yasalara uydukları için çeşitli ısı transferi yöntemlerini (termal iletim, konveksiyon ve radyasyon) açıkça ayırt etmeli ve ayrı ayrı düşünmelisiniz.
Isı mühendisliği cihazlarında ısı transferi işlemleri hem sabit (durağan) hem de kararsız (durağan olmayan) modlarda ilerleyebilir. Sabit (sabit) bir termal rejim, vücudun herhangi bir noktasındaki sıcaklığın zamana bağlı olmadığı bir rejimdir. Durağan bir rejimden önce her zaman durağan olmayan bir rejim gelir.
Durağan olmayan termal koşullar koşullarında (ısıtma ve soğutma süreçleri) meydana gelen süreçler çok karmaşıktır ve bunların dikkate alınması bu dersin programında yer almamaktadır. Bu nedenle burada sadece durağan ısı transfer süreçleri ele alınmaktadır.
TERMAL İLETKENLİK
Temel konseptler
Termal iletkenlik, ısının moleküler olarak aktarılmasıdır. süreklilik bir sıcaklık farkının varlığı nedeniyle.
Bu ısı transferi yöntemi esas olarak katılarda hem bir gövde içinde hem de birbirleriyle temas ettiklerinde iki gövde arasında gerçekleşir. Termal iletkenlik ayrıca bir sıvı veya gaz tabakası aracılığıyla da gerçekleştirilebilir. Bununla birlikte, erimiş metaller hariç, gazlar ve sıvılar çok zayıf ısı iletkenleridir.
sıcaklık alanı. Isı iletimi işlemi ve diğer ısı transferi türleri, yalnızca vücudun farklı noktalarında sıcaklığın aynı olmaması koşuluyla gerçekleştirilir. Bildiğiniz gibi, sıcaklık vücudun durumunun bir parametresidir ve ısınma derecesini karakterize eder. Göz önünde bulundurulan alanın tüm noktalarındaki sıcaklık değerleri kümesi şu an zamana sıcaklık alanı denir. Matematiksel olarak, sıcaklık alanı koordinatların bir fonksiyonu olarak ifade edilir.
Tüm noktalarında sıcaklığı aynı olan bir yüzeye izotermal denir.
Çünkü uzayda aynı anda iki insan aynı noktada olamaz. farklı sıcaklıklar, o zaman farklı izotermal yüzeyler asla kesişmez. Hepsi ya vücudun yüzeyinde biter ya da tamamen içinde bulunur.
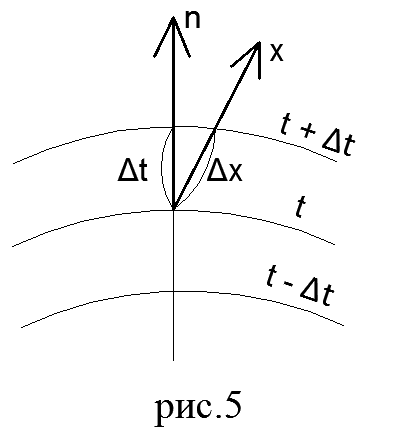 Fourier yasası. Isı akışı, herhangi bir yüzeyden birim zamanda geçen ısı miktarıdır (Q). Isı akısı vektörü daima azalan sıcaklık yönündedir.
Fourier yasası. Isı akışı, herhangi bir yüzeyden birim zamanda geçen ısı miktarıdır (Q). Isı akısı vektörü daima azalan sıcaklık yönündedir.
Nicel olarak, ısı transfer yoğunluğu, ısı akısı yoğunluğu q ile karakterize edilir.
Isı akısı yoğunluğu veya özgül ısı akısı, birim zaman τ başına yüzey birimi F'den geçen ısı miktarıdır:
İlişki (51) termal iletkenliğin temel yasasını ifade eder ve Fourier yasası olarak adlandırılır.
İlişkinin (51) sağ tarafındaki eksi işareti, ısı akısı ve sıcaklık gradyan vektörlerinin zıt yönlerde yönlendirildiği anlamına gelir.
İfadedeki (51) orantılılık katsayısı λ, maddenin termal iletkenlik katsayısı olarak adlandırılan fiziksel bir parametresidir. Bir maddenin ısı iletme yeteneğini karakterize eder.
Termal iletkenlik katsayısının boyutu, ifadeden (51) belirlenir:
Sonuç olarak, termal iletkenlik katsayısının değeri, 1 ° C'lik bir sıcaklık farkıyla birim kalınlıktaki bir duvardan geçen özgül ısı akışına sayısal olarak eşittir. λ ne kadar büyükse, madde o kadar iyi bir ısı iletkenidir.
Metaller iyi ısı iletkenleridir; kuru, durgun hava zayıf bir ısı iletkenidir. Hafif gözenekli malzemeler, gözenekleri hava ile dolu olduğu için ısıyı iyi iletmezler. Isı iletkenliği 0,2 W/(m-deg)'den az olan malzemelere ısı yalıtkanı denir. Suyun termal iletkenliği zayıftır, ancak ıslak bir malzemenin termal iletkenliği, kuru haldeki termal iletkenliğine kıyasla keskin bir şekilde artar. Bunun nedeni suyun ısıyı havadan 20-25 kat daha iyi iletmesidir. Bu nedenle vücuttaki gözeneklerin su ile keskin bir şekilde doldurulması ısı yalıtım özelliklerini azaltır.
Her bir cisim için ısıl iletkenlik katsayısı λ değeri deneysel olarak bulunur. Sonuçlar, hesaplamalarda kullanılan tablolarda özetlenmiştir.
Duvarın termal iletkenliği
Düz tek duvar. Şekil 6, homojen bir malzemeden (tuğla, metal, ahşap veya herhangi bir başka) yapılmış δ kalınlığında düz tek katmanlı bir duvarı göstermektedir.
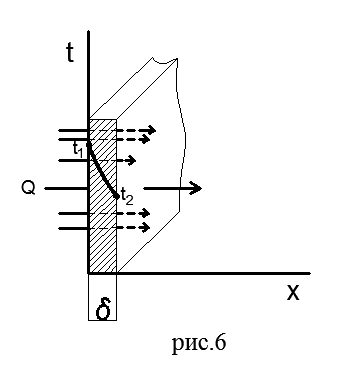 λ malzemesinin ısıl iletkenlik katsayısının sıcaklığa bağlı olmadığını varsayalım. Duvarın dış yüzeylerinde sabit sıcaklıklar t 1 >t 2 korunur; sıcaklık sadece duvar düzlemine dik olan x ekseni yönünde değişir, yani sıcaklık alanı tek boyutludur ve sıcaklık gradyanı dt/dx'e eşittir.
λ malzemesinin ısıl iletkenlik katsayısının sıcaklığa bağlı olmadığını varsayalım. Duvarın dış yüzeylerinde sabit sıcaklıklar t 1 >t 2 korunur; sıcaklık sadece duvar düzlemine dik olan x ekseni yönünde değişir, yani sıcaklık alanı tek boyutludur ve sıcaklık gradyanı dt/dx'e eşittir.
Belirli bir duvardan geçen ısı akışının yoğunluğunu bulalım ve duvar kalınlığı boyunca sıcaklık değişiminin doğasını belirleyelim.
Duvarın içinde, iki izotermal yüzeyle sınırlanmış, dx kalınlığında bir temel katman seçelim. Bu katman için Fourier denklemi şu şekildedir:
Entegrasyondan sonra
Bu denklemden, dikkate alınan duvardan geçen ısı akışının yoğunluğu belirlenebilir. (53) x=δ denklemini koyarsak, t= elde ederiz. t2, nerede
| | (54) |
Düz bir duvardaki ısı akısı yoğunluğu, termal iletkenlik katsayısı λ, sıcaklık farkı () ile doğru orantılı ve duvar kalınlığı δ ile ters orantılıdır. Isı akışının, sıcaklıkların mutlak değeri ile değil, farkları - sıcaklık farkı ile belirlendiği akılda tutulmalıdır.Eşitlik (54) düz bir duvarın termal iletkenliği için hesaplama formülüdür. Dört niceliği q, λ, δ ve : birbirine bağlar:
Duvar kalınlığının ısıl iletkenlik katsayısına δ/λ oranına duvarın ısıl direnci denir.
Denklem (55), özgül ısı akışının sıcaklık farkıyla doğru orantılı ve duvarın ısıl direnciyle ters orantılı olduğunu göstermektedir. Gerçekten de, (55) denklemindeki fraksiyonun paydası ne kadar büyükse, yani δ/λ, ısı akısı yoğunluğu q o kadar düşük olur. Sonuç olarak, duvar kalınlığında δ bir artışla veya termal iletkenlik λ'da bir azalma ile, ısı akısı yoğunluğu q azalır.
Isı akışı yoğunluğunu formül (54) ile belirledikten sonra, τ süresi boyunca F yüzeyi tarafından düz duvardan aktarılan joule cinsinden toplam ısı Q miktarını belirleyebiliriz:
Bu denklem bir doğrunun denklemidir. Böylece, termal iletkenlik katsayısının sabit bir değerinde, sıcaklık homojen bir duvarın kalınlığı boyunca doğrusal olarak değişir. Isıl iletkenliğin sıcaklığa bağlı olduğu durumlarda değişkendir ve hesaplama formülleri biraz daha karmaşıktır.
Ders #2/5 2
26. Konu: “Bir sıvının yapısının modeli. doymuş ve doymamış buharlar. Hava nemi."
1 Akışkan yapısı modeli
sıvı biri toplu durumlar maddeler. Bir sıvının onu diğer kümelenme durumlarından ayıran ana özelliği, pratik olarak hacmi korurken, keyfi olarak küçük bile olsa, teğetsel mekanik streslerin etkisi altında şeklini süresiz olarak değiştirme yeteneğidir.
Şekil 1
Sıvı hal genellikle arasında ara olarak kabul edilir. katı ve gaz : bir gaz ne hacmi ne de şekli korur, ancak bir katı her ikisini de korur.
moleküller sıvıların belirli bir konumu yoktur, ancak aynı zamanda tam hareket serbestliğine de sahip değildirler. Aralarında, onları yakın tutacak kadar güçlü bir çekim vardır.
Sıvı haldeki bir madde belirli bir aralıkta bulunur. sıcaklıklar , bunun altına girerkatı hal(kristalleşme meydana gelir ya da katı hal amorf bir duruma dönüşüm cam), yukarıda gaz halinde (buharlaşma gerçekleşir). Bu aralığın sınırları şunlara bağlıdır: baskı yapmak .
Tüm sıvılar genellikle saf sıvılara bölünür ve karışımlar . Bazı sıvı karışımları yaşam için gereklidir: kan, deniz suyu vb. Sıvılar işlevi gerçekleştirebilirçözücüler.
Akışkanlık, sıvıların ana özelliğidir. Dengedeki bir akışkanın bir bölümüne uygularsanız dış güç , o zaman bu kuvvetin uygulandığı yönde bir sıvı parçacıkları akışı vardır: sıvı akar. Böylece, dengesiz dış kuvvetlerin etkisi altında, sıvı, parçaların şeklini ve göreli düzenini korumaz ve bu nedenle içinde bulunduğu kabın şeklini alır.
Plastik katılardan farklı olarak sıvılardaakma dayanımı: sıvının akması için keyfi olarak küçük bir dış kuvvet uygulamak yeterlidir.
Bir sıvının karakteristik özelliklerinden biri, belirli bir miktar ( değişmeden dış koşullar). Sıvının mekanik olarak sıkıştırılması son derece zordur çünkü aksine gaz moleküller arasında çok az boş alan. Bir kap içinde bulunan bir sıvıya uygulanan basınç, bu sıvının hacminin her noktasına değişmeden iletilir ( pascal yasası , gazlar için de geçerlidir). Bu özellik, çok düşük sıkıştırılabilirlik ile birlikte hidrolik makinelerde kullanılmaktadır.
Sıvıların tipik olarak ısıtıldığında hacmi artar (genişler) ve soğutulduğunda hacmi azalır (büzülür). Ancak, istisnalar vardır, örneğin, su normal basınçta ve 0°C ile yaklaşık 4°C arasındaki sıcaklıklarda ısıtıldığında büzülür.
Ek olarak, sıvılar (gazlar gibi) ile karakterize edilir: viskozite . Parçalardan birinin diğerine göre hareketine karşı koyabilme yeteneği yani iç sürtünme olarak tanımlanır.
Bir sıvının bitişik katmanları birbirine göre hareket ettiğinde, buna ek olarak kaçınılmaz olarak moleküllerin çarpışması meydana gelir.termal hareket. Düzenli hareketi yavaşlatan kuvvetler vardır. Bu durumda, düzenli hareketin kinetik enerjisi, moleküllerin kaotik hareketinin termal enerjisine dönüştürülür.
Kaptaki harekete geçen ve kendi haline bırakılan sıvı yavaş yavaş duracak, ancak sıcaklığı yükselecektir.Bir gaz gibi bir buharda, kohezyon kuvvetlerini pek hesaba katamaz ve hareketi, moleküllerin serbest bir uçuşu ve birbirleriyle ve çevredeki cisimlerle (kabın tabanını kaplayan duvarlar ve sıvı) çarpışması olarak kabul edebilirsiniz. Bir sıvıda, moleküller, bir katıda olduğu gibi, güçlü bir şekilde etkileşime girerek birbirlerini tutarlar. Bununla birlikte, katı bir cisimde her molekül, vücut içinde süresiz olarak belirli bir denge pozisyonunu korurken ve hareketi bu denge pozisyonu etrafındaki salınımlara indirgenirken, bir sıvıdaki hareketin doğası farklıdır. Sıvı moleküller, gaz molekülleri kadar serbest olmasa da katı moleküllerden çok daha serbest hareket eder. Bir sıvıdaki her molekül, komşularından uzaklaşmadan bir süre ileri geri hareket eder. Bu hareket, katı bir molekülün bir denge pozisyonu etrafındaki salınımını andırır. Bununla birlikte, zaman zaman sıvı bir molekül çevresinden kopar ve başka bir yere hareket eder, yeni bir ortama düşer ve yine bir süre için salınım benzeri bir hareket yapar.
Böylece, sıvı moleküllerin hareketi, katı bir cisimdeki ve bir gazdaki hareketlerin bir karışımı gibidir: bir yerdeki "salınımlı" hareket, bir yerden diğerine "serbest" bir geçişle değiştirilir. Buna göre, bir sıvının yapısı, katı bir cismin yapısı ile bir gazın yapısı arasında bir şeydir. Sıcaklık ne kadar yüksekse, yani sıvının moleküllerinin kinetik enerjisi ne kadar büyükse, "serbest" hareketin oynadığı rol o kadar büyük olur: molekülün "salınım" durumunun aralıkları ne kadar kısaysa ve genellikle o kadar "serbest" olur. geçişler, yani sıvı daha çok gaza benzetilir. Yeterli olduğunda Yüksek sıcaklık Her sıvının özelliği (kritik sıcaklık olarak adlandırılır), sıvının özellikleri yüksek oranda sıkıştırılmış gazın özelliklerinden farklı değildir.
2 Doymuş ve doymamış buharlar ve özellikleri
Bir sıvının serbest yüzeyinin üzerinde her zaman bu sıvının buharları vardır. Sıvı içeren kap kapalı değilse, sabit sıcaklıkta buhar parçacıklarının konsantrasyonu, azalma ve artış yönünde geniş bir aralıkta değişebilir.
Kapalı bir alanda buharlaşma süreci(sıvı ile kapalı kap)belirli bir sıcaklıkta ancak belirli bir sınıra kadar meydana gelebilir. Bunun nedeni, buhar yoğunlaşmasının sıvının buharlaşmasıyla aynı anda gerçekleşmesidir. İlk olarak, 1 s içinde sıvıdan yayılan molekül sayısı, daha fazla sayı moleküller geri döner ve yoğunluk ve dolayısıyla buhar basıncı artar. Bu, yoğunlaşma hızında bir artışa yol açar. Bir süre sonra, sıvı üzerindeki buhar yoğunluğunun sabit hale geldiği dinamik denge devreye girer.
Sıvısı ile dinamik dengede olan buhara denir. doymuş buhar. Sıvısı ile dinamik dengede olmayan buhara doymamış buhar denir.
Deneyimler, doymamış buharların her şeye uyduğunu göstermektedir. gaz yasaları ve ne kadar doğru olursa, doygunluktan o kadar uzak olurlar Doymuş buharlar için aşağıdaki özellikler karakteristiktir:
- belirli bir sıcaklıkta doymuş buharın yoğunluğu ve basıncı bunlar, belirli bir sıcaklıkta buharın sahip olabileceği maksimum yoğunluk ve basınçtır;
- doymuş buharın yoğunluğu ve basıncı maddenin türüne bağlıdır. Bir sıvının özgül buharlaşma ısısı ne kadar düşükse, o kadar hızlı buharlaşır ve buharlarının basıncı ve yoğunluğu o kadar büyük olur;
- doymuş buharın basıncı ve yoğunluğu, sıcaklığı ile benzersiz bir şekilde belirlenir (buharın bu sıcaklığa nasıl ulaştığına bağlı değildir: ısıtma veya soğutma sırasında);
- artan sıcaklıkla buhar basıncı ve yoğunluğu hızla artar (Şekil 1, a, b).
Deneyimler, bir sıvı ısıtıldığında, kapalı bir kaptaki sıvının seviyesinin azaldığını göstermektedir. Sonuç olarak, buharın kütlesi ve yoğunluğu artar. İdeal bir gaza kıyasla doymuş buharın basıncında daha güçlü bir artış (Gay-Lussac yasası doymuş buhara uygulanamaz), burada basıncın yalnızca gazın ortalama kinetik enerjisindeki bir artıştan dolayı artmasıyla açıklanır. moleküller (bir ideal gazda olduğu gibi), aynı zamanda moleküllerin konsantrasyonunun artması nedeniyle;
- sabit sıcaklıkta doymuş buharın basıncı ve yoğunluğu hacme bağlı değildir. Şekil 2, ideal gaz (a) ve doymuş buharın (b) izotermlerini karşılaştırma için göstermektedir.

Pirinç. 2
Deneyimler, izotermal genleşme sırasında kaptaki sıvı seviyesinin azaldığını göstermektedir; buhar moleküllerinin sayısı değişir, böylece buhar yoğunluğu sabit kalır.
3 Nem
Su buharı içeren havaya denirıslak . Havadaki su buharı içeriğini karakterize etmek için bir dizi miktar girilir: mutlak nem, su buharı basıncı ve bağıl nem.
mutlak nemρ havaya sayısal olarak 1 m'de bulunan su buharı kütlesine eşit bir değer denir. 3 hava (yani, belirli koşullar altında havadaki su buharının yoğunluğu).
Su buharı basıncı p dır-dir kısmi basıncı havada bulunan su buharı. Mutlak nem ve esneklik için SI birimleri sırasıyla metreküp başına kilogramdır (kg/m 3) ve pascal (Pa).
Yalnızca mutlak nem veya su buharı basıncı biliniyorsa, havanın ne kadar kuru veya nemli olduğuna karar vermek yine de imkansızdır. Hava neminin derecesini belirlemek için su buharının doygunluğa yakın mı yoksa uzak mı olduğunu bilmek gerekir.
bağıl nem hava φ mutlak nemin yoğunluğa yüzde oranı denirρ 0 belirli bir sıcaklıkta doymuş buhar (veya su buharı basıncının basınca oranı) p0 belirli bir sıcaklıkta doymuş buhar):
Bağıl nem ne kadar düşükse, buhar doygunluktan o kadar uzaksa, buharlaşma o kadar yoğun olur. Doymuş buhar basıncı p0 belirli bir sıcaklık tablo değerinde. Su buharının esnekliği (ve dolayısıyla mutlak nem) çiğlenme noktası tarafından belirlenir.
Bir sıcaklığa izobarik soğutma ile tp buhar doymuş hale gelir ve durumu bir nokta ile gösterilir AT . Sıcaklık tp su buharının doygun hale geldiği duruma denirçiğ noktası . Çiy noktasının altına soğutulduğunda buhar yoğunlaşması başlar: sis görünür, çiy düşer, camlar buğulanır.
4 Nem ölçümü
Hava nemini ölçmek için kullanılır ölçü aletleri higrometreler. Birkaç tür higrometre vardır, ancak ana olanlar: saç ve psikrometrik.
Havadaki su buharının basıncını doğrudan ölçmek zor olduğu için havanın bağıl nemi ölçülür.dolaylı bir şekilde.
Çalışma prensibisaç higrometresiyağı alınmış saçın özelliğine göre (insan veya hayvan)uzunluğunu değiştirbulunduğu havanın nemine göre değişir.

Saç metal bir çerçeve üzerine gerilir. Saçın uzunluğundaki değişiklik, ölçek boyunca hareket eden oka iletilir. Kışın saç higrometresi, dış mekan nemini ölçmek için ana araçtır.
Daha doğru bir higrometre, psikrometrik bir higrometredir. psikrometre
(diğer Yunan "psikros" göre soğuk anlamına gelir).
Bağıl nem olduğu bilinmektedir. bağlı olmak buharlaşma oranı.
Hava nemi ne kadar düşük olursa, nemin buharlaşması o kadar kolay olur.

psikrometre vardır iki termometre . Biri sıradan, buna denir kuru. Çevredeki havanın sıcaklığını ölçer. Başka bir termometrenin şişesi bir kumaş fitile sarılır ve bir su kabına indirilir. İkinci termometre havanın sıcaklığını değil, ıslak fitilin sıcaklığını gösterir, dolayısıyla adı nemlendirilmiş termometre. Hava nemi ne kadar düşükse, daha yoğun fitilden nem buharlaşır, ıslak termometreden birim zaman başına ısı miktarı ne kadar büyük olursa, okumaları o kadar küçük olur, bu nedenle kuru ve ıslak termometre okumaları arasındaki fark o kadar büyük olur.
Çiğ noktası higrometreler kullanılarak belirlenir. Yoğuşma higrometresi metal bir kutudur ANCAK , ön duvarİle iyi cilalanmış (Şekil 2) Kutunun içine kolayca buharlaşan bir sıvı eter dökülür ve bir termometre yerleştirilir. Lastik bir ampulle kutudan hava geçirme G , eterin güçlü buharlaşmasına ve kutunun hızlı soğumasına neden olur. Termometre, duvarın cilalı yüzeyinde çiy damlalarının göründüğü sıcaklığı ölçer.İle . Duvara bitişik alandaki basınç, bu alan atmosferle iletişim kurduğundan ve soğutma nedeniyle basınçtaki düşüş, buhar konsantrasyonundaki bir artışla telafi edildiğinden sabit kabul edilebilir. Çiy görünümü, su buharının doymuş hale geldiğini gösterir. Hava sıcaklığını ve çiğlenme noktasını bilerek, su buharının kısmi basıncını ve bağıl nemi bulabilirsiniz.
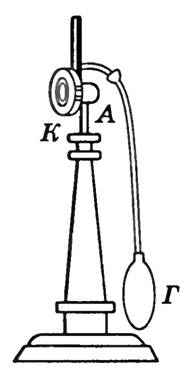
Pirinç. 2
Bağımsız çözüm için 5 Görev
Görev 1
Dışarıda soğuk sonbahar yağmuru yağıyor. Hangi durumda mutfakta asılı olan çamaşırlar daha hızlı kurur: pencere açıkken mi yoksa kapalıyken mi? Neden? Niye?
Görev 2
Nem %78 ve kuru termometre okuması 12°C. Islak termometre termometresi hangi sıcaklığı gösterir?(Cevap: 10 °C.)
Görev 3
Kuru ve ıslak termometre okumaları arasındaki fark 4°C'dir. Bağıl hava nemi %60. Kuru ve ıslak ampul okumaları nelerdir?(Cevap: t c -l9 ° С, t m \u003d 10 ° С.)
Buharlaşma ve yoğuşma süreçleri sürekli ve birbirine paraleldir.
Açık bir kapta sıvı miktarı zamanla azalır çünkü. buharlaşma yoğuşmaya üstün gelir.
Buharlaşmanın yoğuşmaya üstün geldiği sıvının yüzeyinin üzerinde kalan buhara veya sıvının yokluğunda buhara denir. doymamış.
Hermetik olarak kapatılmış bir kapta, sıvı seviyesi zamanla değişmez, çünkü buharlaşma ve yoğuşma birbirini dengeler: sıvıdan kaç molekül uçar, çoğu aynı anda sıvıya döner, buhar ve sıvısı arasında dinamik (hareketli) bir denge oluşur.
Sıvısı ile dinamik dengede olan buhara denir. doymuş.
Belirli bir sıcaklıkta, bir sıvının doymuş buharı, en yüksek yoğunluk ( ) ve maksimum basınç oluşturur ( ) o sıvının buharı o sıcaklıkta olabilir.
Aynı sıcaklıkta doymuş buharın basıncı ve yoğunluğu, maddenin türüne bağlıdır: daha fazla basınç, daha hızlı buharlaşan sıvının doymuş buharını oluşturur.Örneğin, ve
Doymamış buharların özellikleri: Doymamış buharlar Boyle - Mariotte, Gay-Lussac, Charles gaz yasalarına uyar ve ideal gaz hal denklemi onlara uygulanabilir.
Doymuş buhar özellikleri:1. Sabit bir hacimde, artan sıcaklıkla, doymuş buharın basıncı artar, ancak doğru orantılı değildir (Charles yasası yerine getirilmez), basınç ideal bir gazınkinden daha hızlı büyür. , artan sıcaklıkla ( ) , buhar kütlesi artar ve bu nedenle buhar moleküllerinin konsantrasyonu artar () ve doymuş buharın basıncı iki nedenden dolayı erir (
3 1 – doymamış buhar ( Ideal gaz);
2 2 - doymuş buhar; 3 - doymamış buhar,
1 Aynı ortamda doymuş buhardan elde edilen
ısıtıldığında hacim.
2. Sabit sıcaklıkta doymuş buharın basıncı kapladığı hacme bağlı değildir.
Hacimdeki bir artışla, buharın kütlesi artar ve sıvının kütlesi azalır (sıvının bir kısmı buhara geçer), buhar hacminde bir azalma ile daha az olur ve sıvı büyür (kısmen buharın sıvıya geçmesi), doymuş buhar moleküllerinin yoğunluğu ve konsantrasyonu sabit kalır, bu nedenle basınç sabit kalır ().
sıvı
(oturdu. buhar + sıvı)
Doymamış buhar
Doymuş buharlar Boyle - Mariotte, Gay-Lussac, Charles'ın gaz yasalarına uymazlar, çünkü işlemlerdeki buhar kütlesi sabit kalmaz, ancak tüm gaz yasaları sabit kütle için elde edilir. İdeal bir gazın hal denklemi doymuş buhara uygulanabilir.
Yani, doymuş buhar, ısıtılarak doymamış buhara dönüştürülebilir. sabit hacim veya hacmini sabit bir sıcaklıkta arttırmak. Doymamış buhar, sabit bir hacimde soğutularak veya sabit bir sıcaklıkta sıkıştırılarak doymuş buhara dönüştürülebilir.
Kritik durum
Bir sıvıda serbest bir yüzeyin varlığı, maddenin sıvı fazının nerede ve gaz fazının nerede bulunduğunun belirtilmesini mümkün kılar. Bir sıvı ile buharı arasındaki keskin fark, bir sıvının yoğunluğunun bir buharınkinden birçok kez daha büyük olması gerçeğiyle açıklanır. Bir sıvı, hava geçirmez şekilde kapatılmış bir kapta ısıtılırsa, genleşme nedeniyle yoğunluğu azalacak ve üzerindeki buhar yoğunluğu artacaktır. Bu, bir sıvı ile doymuş buharı arasındaki farkın yumuşadığı ve yeterince yüksek bir sıcaklıkta tamamen ortadan kalktığı anlamına gelir. Farklılıkların olduğu sıcaklık fiziksel özellikler Bir sıvı ile doymuş buharı arasındaki ve yoğunluklarının aynı hale gelmesine ne denirKritik sıcaklık.
Gazdan sıvı oluşumu için ortalama potansiyel enerji Moleküllerin çekimi ortalama kinetik enerjilerini aşmalıdır.
Kritik sıcaklık – Maksimum sıcaklık buharın sıvıya dönüştürüldüğü yerdir. Kritik sıcaklık, moleküler etkileşimin potansiyel enerjisine bağlıdır ve bu nedenle farklı gazlar için farklıdır. Su moleküllerinin güçlü etkileşimi nedeniyle, su buharı 0 C sıcaklıkta bile suya dönüşebilir. Aynı zamanda, nitrojen sıvılaşması sadece = -147˚'den daha düşük bir sıcaklıkta meydana gelir, çünkü azot molekülleri birbirleriyle zayıf bir şekilde etkileşime girer.
Buhar-sıvı geçişini etkileyen diğer bir makroskobik parametre basınçtır. Gaz sıkıştırması sırasında dış basınçtaki bir artışla, parçacıklar arasındaki ortalama mesafe azalır, aralarındaki çekim kuvveti artar ve buna bağlı olarak etkileşimlerinin ortalama potansiyel enerjisi.
Baskı yapmakkritik sıcaklığındaki doymuş buhara denir. kritik. Bu, belirli bir maddenin mümkün olan en yüksek doygun buhar basıncıdır.
Maddenin durumu kritik parametrelerle denir kritik(kritik nokta) . Her maddenin kendi kritik sıcaklığı ve basıncı vardır.
AT kritik durumözgül buharlaşma ısısı ve katsayısı yüzey gerilimi sıvılar. Kritik üzerindeki sıcaklıklarda, hatta çok yüksek basınçlar bir gazı sıvıya dönüştürmek imkansızdır, yani. kritik sıcaklığın üzerinde sıvı var olamaz. Süper kritik sıcaklıklarda, maddenin sadece buhar hali mümkündür.
Gazların sıvılaştırılması ancak kritik sıcaklığın altındaki sıcaklıklarda mümkündür. Sıvılaştırma için gazlar, örneğin adyabatik genleşme yoluyla kritik bir sıcaklığa soğutulur ve ardından izotermal olarak sıkıştırılır.
Kaynamak
Dışarıdan, fenomen şöyle görünür: sıvının tüm hacminden hızla büyüyen kabarcıklar yüzeye çıkar, yüzeyde patlar ve buhar çevreye salınır.
MKT kaynamayı şöyle açıklıyor: sıvıda her zaman sıvıdan buharlaşmanın meydana geldiği hava kabarcıkları vardır. Kapalı kabarcık hacminin sadece hava ile değil, aynı zamanda doymuş buharla da doldurulduğu ortaya çıkıyor. Sıvı ısıtıldığında içlerindeki doymuş buharın basıncı, hava basıncından daha hızlı artar. Yeterince ısıtılmış bir sıvıda, kabarcıklardaki doymuş buharın basıncı dış basınçtan daha büyük olduğunda, hacimleri artar ve yerçekimlerini aşan bir kaldırma kuvveti kabarcıkları yüzeye kaldırır. Yüzen kabarcıklar, belirli bir sıcaklıkta, içlerindeki doymuş buharın basıncı sıvının üzerindeki basıncı aştığında patlamaya başlar. Doymuş buharının kabarcıklardaki basıncının, sıvı üzerindeki dış basınca eşit veya daha büyük olduğu bir sıvının sıcaklığına denir. kaynama noktası.
Farklı sıvıların kaynama noktaları farklıdır, çünkü kabarcıklarındaki doymuş buharın basıncı, farklı sıcaklıklardaki aynı dış basınçla karşılaştırılır. Örneğin, kabarcıklardaki doymuş buhar basıncı, 100°C'de su için, 357°C'de cıva için, 78°C'de alkol için, 35°C'de eter için normal atmosfer basıncına eşittir.
Kaynama işlemi sırasında kaynama noktası sabit kalır,çünkü ısıtılan sıvıya verilen tüm ısı buharlaşmaya harcanır.
Kaynama noktası, sıvı üzerindeki dış basınca bağlıdır: artan basınçla sıcaklık yükselir; basınç azaldıkça sıcaklık düşer.Örneğin, deniz seviyesinden 5 km yükseklikte, basıncın atmosfer basıncından 2 kat daha düşük olduğu yerde, buhar basıncının 15 atm olduğu buhar motorlarının kazanlarında suyun kaynama noktası 83 °C'dir. (), su sıcaklığı yaklaşık 200˚С'dir.
hava nemi
Havada her zaman su buharı vardır, bu nedenle aşağıdaki değerlerle karakterize edilen hava nemi hakkında konuşabiliriz:
1.Mutlak nem havadaki su buharının yoğunluğudur (veya bu buharın oluşturduğu basınçtır ( .
Mutlak nem, havanın su buharı ile doyma derecesi hakkında bir fikir vermez. Aynı miktarda su buharı farklı sıcaklık farklı bir nem hissi yaratır.
2.Bağıl nem belirli bir sıcaklıkta havada bulunan su buharının yoğunluğunun (basıncı) aynı sıcaklıkta doymuş buharın yoğunluğuna (basıncına) oranıdır. : veya
belirli bir sıcaklıkta mutlak nemdir; - yoğunluk, aynı sıcaklıkta doymuş buhar basıncı. Herhangi bir sıcaklıkta doymuş su buharının yoğunluğu ve basıncı tabloda bulunabilir. Tablo, hava sıcaklığı ne kadar yüksek olursa, doymuş olması için havadaki su buharının yoğunluğunun ve basıncının o kadar büyük olması gerektiğini gösterir.
Bağıl nemi bilerek, belirli bir sıcaklıkta havadaki su buharının yüzde kaçının doygunluktan uzak olduğunu anlayabilirsiniz. Havadaki buhar doymuşsa, o zaman . Eğer bir , o zaman havada doygunluk durumuna yetecek kadar buhar yoktur.
Havadaki buharın doygun hale gelmesi, sis, çiy şeklindeki nemin görünümü ile değerlendirilir. Havadaki su buharının doygun hale geldiği sıcaklığa denir. çiğ noktası.
Havanın sıcaklığını değiştirmeden sıvının ilave buharlaşmasından dolayı buhar eklenerek veya havadaki buhar miktarı ile sıcaklığı düşürülerek havadaki buhar doymuş hale getirilebilir.
İnsanlar için en uygun olan normal bağıl nem %40 - 60'tır. Büyük önem Hava tahmini için meteorolojide nem bilgisine sahiptir. Dokuma, şekerleme üretiminde, sürecin normal seyri için belirli bir nem gereklidir. Sanat eserlerinin ve kitapların saklanması, nemin gerekli seviyede tutulmasını gerektirir.
Nem aletleri:
1. Yoğuşma higrometresi (çiy noktasını belirlemenizi sağlar).
2. Saç higrometresi (yağsız saçın uzunluğuna karşı neme göre) bağıl nemi yüzde olarak ölçer.
3. Psikrometre, iki kuru ve ıslak termometreden oluşur. Islak ampul, suya batırılmış bir beze sarılır. Kumaştan buharlaşma nedeniyle ıslananın sıcaklığı kuru olanın sıcaklığından daha düşüktür. Termometre okumalarındaki fark, çevredeki havanın nemine bağlıdır: hava ne kadar kuru olursa, kumaştan buharlaşma o kadar yoğun olursa, termometre okumalarındaki fark o kadar büyük olur ve bunun tersi de geçerlidir. Hava nemi %100 ise, o zaman termometrelerin okumaları aynıdır, yani. okumalardaki fark 0'dır. Bir psikrometre kullanarak nemi belirlemek için bir psikrometrik tablo kullanılır.
Erime ve kristalleşme
Eridiğinde sağlam vücut kristal kafesi oluşturan parçacıklar arasındaki mesafe artar ve kafesin kendisi yok olur. Erime işlemi enerji gerektirir. Katı bir cisim ısıtıldığında, titreşen moleküllerin kinetik enerjisi ve buna bağlı olarak salınımlarının genliği artar. denilen belirli bir sıcaklıkta erime noktası, kristallerdeki parçacıkların düzenindeki düzen bozulur, kristaller şekillerini kaybeder. Bir madde erir, katı halden sıvı hale geçer.
kristalizasyon sırasında kristal bir kafes oluşturan moleküllerin yakınsaması vardır. Kristalleşme ancak sıvı enerjiyi serbest bıraktığında meydana gelebilir. Erimiş madde soğutulduğunda ortalama kinetik enerji ve moleküllerin hızı azalır. Çekici kuvvetler, parçacıkları denge konumuna yakın tutabilir. denilen belirli bir sıcaklıkta katılaşma (kristalleşme) sıcaklığı, tüm moleküller kararlı bir denge konumundadır, düzenleri düzenli hale gelir - bir kristal oluşur.
Bir katının erimesi, maddenin katılaştığı sıcaklıkta gerçekleşir.
Her maddenin kendi erime noktası vardır. Örneğin, helyum için erime noktaları -269.6˚С, cıva için -38.9˚С, bakır için 1083˚С'dir.
Erime işlemi sırasında sıcaklık sabit kalır. Dışarıdan verilen ısı miktarı kristal kafesin yıkımına gider.
Kürleme işlemi sırasında ısı alınsa da sıcaklık değişmez. Kristalizasyon sırasında açığa çıkan enerji, sabit bir sıcaklığı korumak için kullanılır.
Tüm madde eriyene veya tüm madde katılaşana kadar, yani. Bir maddenin katı ve sıvı fazları bir arada bulunduğu sürece sıcaklık değişmez.
TV+sıvı sıvı + televizyon
, nerede - ısı miktarı, - maddenin kristalleşmesi sırasında açığa çıkan maddeyi eritmek için gereken ısı miktarı kütle kütlesi
- özgül füzyon ısısı– 1 kg'lık bir maddeyi erime noktasında eritmek için gereken ısı miktarı.
Bir maddenin belirli bir kütlesinin erimesi sırasında ne kadar ısı harcanırsa, bu kütlenin kristalleşmesi sırasında aynı miktarda ısı açığa çıkar.
Olarak da adlandırılır özısı kristalleşme.
Erime noktasında sıvı haldeki bir maddenin iç enerjisi daha büyüktür. içsel enerji katı haldeki maddenin kütlesi aynıdır.
saat Büyük bir sayı Bir madde eridiğinde hacmi artar ve yoğunluğu azalır. Sertleşmede, aksine, hacim azalır ve yoğunluk artar. Örneğin, katı naftalin kristalleri sıvı naftalin içinde batar.
Bazı maddeler, örneğin bizmut, buz, galyum, dökme demir vb., eridiğinde büzülür ve katılaştıklarında genleşir. Bu sapmalar Genel kural kristal kafeslerin yapısal özellikleri ile açıklanmıştır. Bu nedenle su buzdan daha yoğundur, buz suda yüzer. Donma sırasında suyun genleşmesi kayaların tahrip olmasına yol açar.
Eritme ve katılaşma sırasında metallerin hacmindeki değişim, dökümhane işinde esastır.
Tecrübe gösteriyor ki üzerindeki dış basınçtaki değişiklik sağlam maddenin erime noktasını etkiler. Erime sırasında genleşen maddeler için, dış basınçtaki bir artış, erime noktasında bir artışa yol açar, çünkü. erime sürecini engeller. Maddeler erime sırasında sıkıştırılırsa, onlar için dış basınçtaki bir artış, erime sıcaklığında bir azalmaya yol açar, çünkü erime sürecine yardımcı olur. Sadece basınçtaki çok büyük bir artış, erime noktasını gözle görülür şekilde değiştirir. Örneğin, buzun erime noktasını 1˚C düşürmek için basınç 130 atm arttırılmalıdır. Normal bir maddenin erime noktası atmosferik basınç aranan maddenin erime noktası.