Eficiența motorului termic
cicluri. termică și mașini frigorifice. eficienta ciclului Carnot pentru un gaz ideal
Un proces sau ciclu ciclic (circular) este un proces în care stările inițiale și finale ale sistemului coincid.În ciclul prezentat în fig. 8.1, în secțiunea 1-a-2, sistemul efectuează o activitate pozitivă și revine la starea sa inițială pe calea 2-b-1 - negativ, dar mai mic în valoare absolută. în care munca deplina finalizat pe ciclu este pozitiv. Este egală cu aria figurii 1-a-2-b-1 acoperită de ciclul pe P-V diagramă.
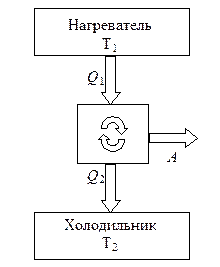 |
|
| Orez. 8.1 | Orez. 8.2 |
Din moment ce energia internă U este o funcție de stare, modificarea sa în procesul ciclic este zero (D U= 0). Apoi, din prima lege a termodinamicii rezultă că munca totală DAR, realizat de sistem pe ciclu, este egal cu cantitatea totală de căldură Q primit de sistem într-un ciclu. Dacă ciclul funcționează DAR este pozitiv, spunem că ciclul este parcurs în directie înainte(în sensul acelor de ceasornic). Astfel de procese ciclice pot fi folosite pentru a crea motoare termice - dispozitive care efectuează lucrări mecanice datorită căldurii primite din rezervoarele termice.
Motorul termic include un corp de lucru, de ex. un sistem care efectuează un ciclu și efectuează lucru și cel puțin două rezervoare de căldură cu care fluidul de lucru schimbă căldură.
Protozoare motor termic prezentat schematic in Fig. 8.2. Rezervoare termice din care fluidul de lucru într-un ciclu direct (la care DAR> 0) primesc o cantitate pozitivă de căldură se numesc încălzitoare. Rezervoarele din care se primește o cantitate negativă de căldură se numesc frigidere. Suma cantităților pozitive de căldură primite de sistem de la încălzitoare în toate etapele ciclului este de obicei notă Q + = Q 1 și suma căldurii negative primite de la frigidere Q - = - Q 2. în care Q 2 se numește cantitatea de căldură cedată de sistem către frigider ( Q 2 > 0).
Lucrul ciclului este egal cu suma algebrică a cantităților de căldură primite de sistem în toate etapele ciclului
A = Q + + Q - = Q 1 – Q 2 .
Coeficientul de performanță (COP) al unui ciclu este raportul dintre munca A efectuată de sistem în timpul parcurgerii ciclului și cantitatea de căldură Q 1 º Q + primită de sistem de la încălzitor
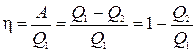 . (8.1)
. (8.1)
Eficiența h calculată în acest fel este uneori numită termodinamică pentru a sublinia diferența sa față de randamentul tehnic, care este întotdeauna mai scăzut din cauza diverselor pierderi care însoțesc funcționarea mașinilor reale.
Dacă direcția ocolirii ciclului este inversată, atunci lucrul și cantitatea de căldură în toate etapele sale se vor schimba semnul. Un astfel de ciclu se numește invers. Când treceți prin ciclul invers, finalizați lucrul DAR arr, perfect de către corpul de lucru, este negativ DAR arr = - DAR(forțele externe care acționează asupra sistemului fac o activitate pozitivă DAR). Sistemul primește o cantitate pozitivă de căldură de la frigider și eliberează căldură către încălzitor.
Mașinile frigorifice funcționează în ciclu invers. Ei consumă energie mecanică, luați căldura de la un corp relativ rece și transferați căldura unui corp mai cald. Dacă scopul mașinii este de a încălzi un corp mai cald (de exemplu, creșterea temperaturii aerului din cameră din cauza căldurii preluate din aerul exterior), se numește pompă de căldură. Eficiența sa este determinată de performanța pompei de căldură x T.N, care este egală cu raportul dintre cantitatea de căldură primită de corpul încălzit și munca cheltuită pentru aceasta.
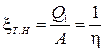 .
.
Efectul util depășește munca cheltuită, x T..N> 1, dar nu există, desigur, nicio încălcare a legii conservării energiei aici. Muncă forțe externe nu se transformă în căldură, dar asigură o „pompare” a căldurii de la un corp mai puțin încălzit la unul mai încălzit.
Dacă sarcina este de a prelua căldura dintr-un corp mai rece, mașina se numește unitate de refrigerare. Eficiența sa este caracterizată de coeficientul de refrigerare x X, egal cu raportul dintre căldura extrasă și munca cheltuită
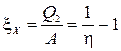 .
.
x coeficienți T.Nși x X sunt utilizate în principal în aplicațiile tehnice ale termodinamicii.
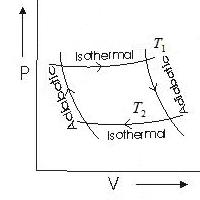
Dintre diferitele procese ciclice, ciclul Carnot are o importanță deosebită în termodinamică. Este format din două izoterme (a-b și c-d) și două adiabate (b-c și d-a) (Figura 8.3).
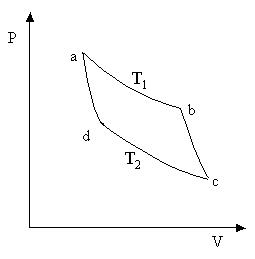 Orez. 8.3 Orez. 8.3 |
Să aflăm eficiența ciclului Carnot, a cărui substanță de lucru este un mol de gaz ideal. Pe secțiunea a-b fluidul de lucru este în contact termic cu un încălzitor având o temperatură T unu . Produs expansiunea izotermă cvasistatică a volumului V a la volum V b. În acest caz, gazul primește de la încălzitor cantitatea de căldură Q ab. Deoarece energia internă a unui gaz ideal depinde numai de temperatură și nu se modifică în timpul unui proces izoterm, atunci, conform primei legi a termodinamicii,
Pe etapa b-c un adiabatic ( Q bc = 0) dilatarea gazelor. Ca urmare, temperatura acestuia scade. Când atinge temperatura frigiderului T 2, gazul este adus în contact termic cu frigiderul, iar procesul de izotermă compresie c-d. Gazul face un lucru negativ. DAR cd și primește o cantitate negativă de căldură Q cd (oferă o cantitate pozitivă de căldură frigiderului)
Din luarea în considerare a etapelor ciclului, se poate observa că gazul primește o cantitate pozitivă de căldură numai la secțiunea a-b, adică Q 1 = Q ab. O cantitate negativă de căldură este primită de gaz secţiunea c-d, înseamnă căldura transmisă frigiderului Q 2 =- Q cd . Apoi eficiența ciclului
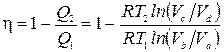 .
.
Scriem ecuațiile adiabatice b-c și d-a, având în vedere că T a = T b= T 1 , T c= T d= T 2 ,
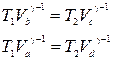 .
.
Împărțind o ecuație la alta, obținem ![]() . Apoi eficiența ciclului Carnot pentru un gaz ideal
. Apoi eficiența ciclului Carnot pentru un gaz ideal
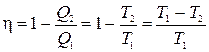 . (8.2)
. (8.2)
Rețineți că din expresia pentru eficiență, scrisă ca , rezultă
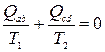 . (8.3)
. (8.3)
Relația (8.3) este caz special egalitățile Clausius (pentru detalii, vezi § 13).
Noi, ca oameni obișnuiți, ne gândim rar la modul în care funcționează motoarele termice și cu atât mai mult - nu încercăm să înțelegem esența a ceea ce se întâmplă în interiorul acestor motoare din punctul de vedere al termodinamicii. Cunoștințele medii ale mecanicilor și tehnicienilor se limitează la faptul că, se pare, ceva din interior se arde și, datorită acestui lucru, pistoanele încep să se miște (la oamenii de rând - „piston”), rotind alte părți și, după cum se spune, „procesul a început”.
Dar, ca întotdeauna, în rândul rasei umane-tribul există cei mai meticuloși reprezentanți care trebuie doar să știe cum se întâmplă totul cu adevărat și de ce depinde totul. Probabil, pe aceste „minuțioase” și „omnipresente”, ca și pe ramurile copacilor, cresc fructele care hrănesc știința.
Deci, să încercăm să ne dăm seama - cum funcționează un motor termic și ce determină eficiența acestuia?
Un pic de teorie.
Un motor termic este o mașină care transformă energia termică în energie mecanică. Adică în interiorul acestor mecanisme, care sunt un sistem, ceva începe să se rotească, să se miște și să se răsucească, dacă temperatura din interiorul acestui sistem este cumva modificată (de regulă, căldura este furnizată fluidului de lucru, care este cel mai adesea un gaz dintr-o serie de motive „bune”).
Ei bine, puțin mai mult - toate motoarele sunt împărțite, în mare, în motoare cu ardere internă și motoare cu ardere externă.
Pentru primul, căldura este furnizată elementului sistemului din interiorul motorului, pentru cel din urmă, undeva în exterior. Privind în viitor, să dăm un exemplu: motoarele cu ardere externă includ, în special, motoarele cu abur, în care căldura către fluidul de lucru (gheață, apă sau abur sau orice lichid) furnizat în afara motorului, prin arderea unui fel de combustibil (cărbune, păcură, lemn de foc etc.)într-un cuptor situat separat sub rezervor (cazan) cu fluidul de lucru. Apoi fluidul de lucru încălzit este introdus în motorul termic (intră în cilindru), și face o muncă utilă, în timp ce degajă căldură.
Motoarele cu ardere internă (ICE) includ (de exemplu) motoarele diesel și motoarele cu carburator familiare tuturor încă din copilărie, în care fluidul de lucru este ars și generează căldură în interiorul sistemului (în cilindru).
În ambele cazuri vorbim despre procesele termodinamice, de ex. procese care provoacă fluctuații de temperatură (sau cauzate de fluctuațiile de temperatură)în interiorul sistemului.
În cazul general, este descrisă esența a ceea ce se întâmplă din punctul de vedere al termodinamicii moderne.
LA începutul XIX de secole, talentatul inginer francez Sadi Carnot (1796-1832) a studiat procesele termodinamice care au loc în motoarele termice folosind un gaz ideal ca fluid de lucru. În același timp, toate procesele din mașini au fost considerate de el ca fiind echilibrate (reversibile).
Proces reversibil- acesta este un proces care decurge atât de lent încât poate fi considerat ca o trecere succesivă de la o stare de echilibru la alta etc., iar întregul proces poate fi realizat în direcție inversă fără a modifica munca efectuată și cantitatea de căldură transferată. (Trebuie remarcat faptul că toate procesele reale sunt ireversibile).
Scopul cercetării lui Carnot a fost acela de a determina condițiile în care este posibil să se obțină maximum de lucru din căldura furnizată motorului termic, adică să se transforme energia termică în energie mecanică cel mai eficient.
La sfârșitul secolului al XVIII-lea - începutul secolului al XIX-lea, singurul tip de motoare termică folosită de omenire în scopuri practice erau motoarele cu ardere externă - adică mașinile cu abur. Eficiența acestor mașini a fost extrem de scăzută - nu mai mult 2 %
, în timp ce nu exista o teorie convingătoare care să indice modalități de îmbunătățire a eficienței acestora.
Carnot a efectuat o analiză amănunțită a diferitelor modalități de transformare a căldurii în lucru pe exemplul unui model idealizat al unui motor cu abur alternativ, în timp ce rezultatele și concluziile trase de el s-au dovedit a fi valabile pentru orice tip de mașină care utilizează energie termică pentru efectua lucrări mecanice.
Ca urmare a concluziilor teoretice, Carnot a ajuns la concluzia că efectul maxim din conversia căldurii în energie mecanică poate fi atins folosind un ciclu circular format din patru procese succesive - izoterme, adiabatice, izoterme și din nou adiabatice, care au completat ciclul. , readucerea sistemului la starea inițială.
Această secvență procese termodinamiceîntr-un motor termic numit ciclul carnot ideal.
Este imposibil să se fabrice un motor real care să transforme energia termică în energie mecanică strict conform ciclului propus de Carnot din motive tehnologice, prin urmare ciclul Carnot este considerat nefezabil și ideal.
Nicolas Leonard Sadie Carnot considerat unul dintre fondatorii termodinamicii. La 28 de ani, el a scris singura lucrare care a ajuns la posteritate - „Reflecții asupra forței motrice a focului și asupra mașinilor capabile să dezvolte această forță”, în care a conturat viziuni fundamental noi pentru acea vreme asupra proceselor din motoarele termice, care s-au reflectat în a doua lege a termodinamicii.
Sadi Carnot a introdus conceptele de bază ale termodinamicii în terminologia științifică - un motor termic ideal, un ciclu ideal, reversibilitatea și ireversibilitatea proceselor termodinamice.
La începutul secolului al XIX-lea se foloseau doar mașini cu abur primitive, a căror eficiență nu depășea câteva procente, deoarece nu exista nicio teorie care să explice cum să crească eficiența utilizării energiei termice în motoare. Lucrarea lui Carnot a servit drept primul ghid pentru ingineri pentru a găsi utilizarea eficientă a căldurii în motoare.
Carnot a murit foarte tânăr, la 36 de ani, de holeră.
Întrucât în acei ani holera era considerată o boală teribilă și incurabilă, trupurile și bunurile morților trebuiau să fie arse. Cu siguranță multe lucrări valoroase ale acestui cel mai talentat inginer au pierit în incendiu. În mod miraculos, doar celebrele „Reflecții asupra forţe motrice foc...”, pe care chiar acest foc, care a distrus toate celelalte lucrări ale lui Carnot și trupul său neînsuflețit, l-a regretat...
Secvența proceselor din ciclul Carnot
Luați în considerare succesiunea de procese termodinamice propusă de Carnot, numită ciclul Carnot ideal.
După cum se știe, munca mecanica poate fi realizat printr-un sistem termodinamic numai în cazul în care are loc un proces care este însoțit de o modificare a volumului fluidului de lucru, adică izoterm, izobar sau adiabatic. În acest caz, toată energia termică poate fi convertită în muncă numai printr-un proces izoterm (cu un proces izobaric și adiabatic, o parte din căldură este cheltuită pentru schimbare energie interna corp de lucru).
Într-un proces izocor (care are loc la un volum constant al fluidului de lucru), este exclusă transformarea căldurii în lucru mecanic.
În starea iniţială a ciclului Carnot ideal, fluidul de lucru (gazul ideal) are nişte parametri p 1 , V 1 , T 1 .
Căldura este furnizată fluidului de lucru dintr-o sursă externă numită încălzitor, care este sistemul (motor termic)începe să fie utilizat prin proces izotermic.
După cum sa menționat mai sus, într-un proces izoterm, variabilele sunt doi parametri principali ai fluidului de lucru - presiunea și volumul, raportul dintre care este invers proporțional. (Model Boyle-Mariotte). În acest caz, toată căldura furnizată fluidului de lucru este cheltuită exclusiv pentru efectuarea lucrărilor mecanice; energia internă a fluidului de lucru rămâne neschimbată și nu necesită căldura primită de la încălzitorul extern. Prin urmare, alegerea primului proces termodinamic din ciclul Carnot conform izotermei este destul de logică - aceasta permite utilizarea maximă a căldurii primite de la încălzitor pentru a efectua lucrări mecanice.
La sfârşitul procesului izoterm, fluidul de lucru are parametrii p 2 , V 2 , T 1 .
Acest proces al ciclului Carnot din diagramă (Fig. 1) este indicat prin cifre 1-2
.
Deoarece ciclul Carnot este reversibil și circular, adică toate procesele termodinamice care au loc în el trebuie să readucă fluidul de lucru la parametrii inițiali, devine evident că cel puțin încă un proces izoterm trebuie să fie prezent în ciclu. În același timp, fluxul său trebuie să fie însoțit de răcirea fluidului de lucru, adică transferul de căldură de la sistem la Mediul extern, altfel nu poți reveni la punctul cu parametrii inițiali. Dacă imediat după primul proces este pornit al doilea proces izoterm, atunci munca totală a ciclului va fi minimă, deoarece zona graficului care caracterizează munca mecanică efectuată de sistem (umbrite în Fig. 1) va fi mic sau chiar zero. (dacă izotermele direct și invers sunt aceleași).

Din acest motiv, S. Carnot a folosit un proces adiabatic ca al doilea proces termodinamic pentru ciclul său, care se desfășoară fără schimb de căldură între sistem și mediu. În acest caz, munca este efectuată datorită unei modificări a energiei interne a fluidului de lucru, care continuă să se extindă și să se răcească până la o temperatură T2. Pe diagrama ciclului Carnot, această secțiune este închisă între numere 2-3
.
Utilizarea unui proces adiabatic după un proces izoterm permite obținerea unor lucrări mecanice din sistem deja fără alimentare de căldură de la încălzitor, datorită utilizării energiei interne a fluidului de lucru.
Parametrii fluidului de lucru la sfârşitul acestui proces sunt p 3 , V 3 , T 2 .
Următoarea verigă a ciclului Carnot este al doilea proces izoterm, care, așa cum sa discutat deja mai sus, trebuie să fie negativ, adică însoțit de transferul de căldură din fluidul de lucru în mediul extern către un alt corp, numit în acest caz frigider. .
Pe diagrama ciclului, acest proces este indicat prin numere. 3-4
.
Cursul procesului este însoțit de o scădere a volumului și o creștere a presiunii fluidului de lucru (compresie), în timp ce temperatura acestuia rămâne constantă datorită transferului de căldură la frigider.
Parametrii fluidului de lucru la sfârşitul acestui proces - p 4 , V 4 , T 2 .
Procesul final al ciclului Carnot, care readuce sistemul la starea inițială cu parametrii inițiali p 1 , V 1 , T 1 este adiabatic.
Transferul de căldură către frigider este oprit. În același timp, fluidul de lucru continuă să scadă în volum (comprimare), datorită efectuării unor lucrări externe asupra acestuia, ceea ce este negativ pentru proces.
În acest caz, energia internă a fluidului de lucru crește, deoarece o parte din munca externă este cheltuită pentru încălzirea acestuia.
Acest proces este indicat prin numere în diagramă. 4-1
.
O analiză a diagramei ciclului p-V circulară obținută de Carnot arată că sistemul a efectuat un lucru mecanic, a cărui valoare este caracterizată de aria cuprinsă între curba delimitată de puncte. 1-2-3 și o curbă delimitată de puncte 3-4-1 . În acest caz, toată munca efectuată de sistem va fi egală cu suma muncii efectuate în timpul fiecăruia dintre cele patru procese termodinamice succesive enumerate mai sus.
Este evident că munca efectuată de corpul de lucru în timpul proceselor adiabatice directe și inverse este egală ca mărime, dar are un semn diferit. (pozitiv în primul proces și negativ în al doilea), adică suma acestor lucrări este egală cu zero. Iar munca efectuată în timpul procesului izoterm direct este mai mare decât munca efectuată în timpul procesului izoterm invers.
Acest lucru este ilustrat grafic zonă diferită diagramă cuprinsă între abscisă și, respectiv, prima și a doua izotermă. Cu cât prima izotermă este mai mare pe diagrama celei de-a doua izoterme (inverse) relative, cu atât fluidul de lucru va face mai multă muncă.
Dacă luăm în considerare diagrama de proces T-V, atunci va reprezenta o figură plată (de exemplu, un romb), în care două izoterme (direct și invers) paralele cu una dintre axe (temperatura), iar adiabatele vor fi paralele între ele.
Rezultă de aici că munca utilă efectuată de sistem va fi cu atât mai mare, cu cât diferența dintre temperatura încălzitorului și temperatura frigiderului este mai mare, adică cu atât diferența de temperatură între T 1 și T 2 este mai mare. (distanța dintre izoterma superioară și inferioară pe diagrama T-V).
Analiza matematică a modelului ciclului ideal propus de Sadi Carnot arată că randamentul termic maxim mașină termică se poate determina din relatia:
η t \u003d 1 - T 2 /T 1;
unde: T 1 și T 2 - temperatura fluidului de lucru (gaz), respectiv, la începutul și sfârșitul ciclului.
Această formulă simplă ne permite să tragem două concluzii principale - despre modul de creștere a eficienței motoarelor termice și că este imposibil să se creeze un motor termic, a cărui eficiență va fi egală cu unitatea, adică 100%. Într-adevăr, fracția T 2 /T 1 poate fi egală cu zero numai dacă numărătorul ei este egal cu zero, sau numitorul este egal cu infinitul. Ambele sunt nerealiste, deoarece este imposibil să răcești un corp material la o temperatură de zero absolut și este imposibil temperatura de pornire a face corpul de lucru infinit, deoarece însuși conceptul de corp în acest caz își va pierde sensul; în plus, este imposibil să se fabrice un motor real, ale cărui părți și componente sunt capabile să reziste la o astfel de temperatură.
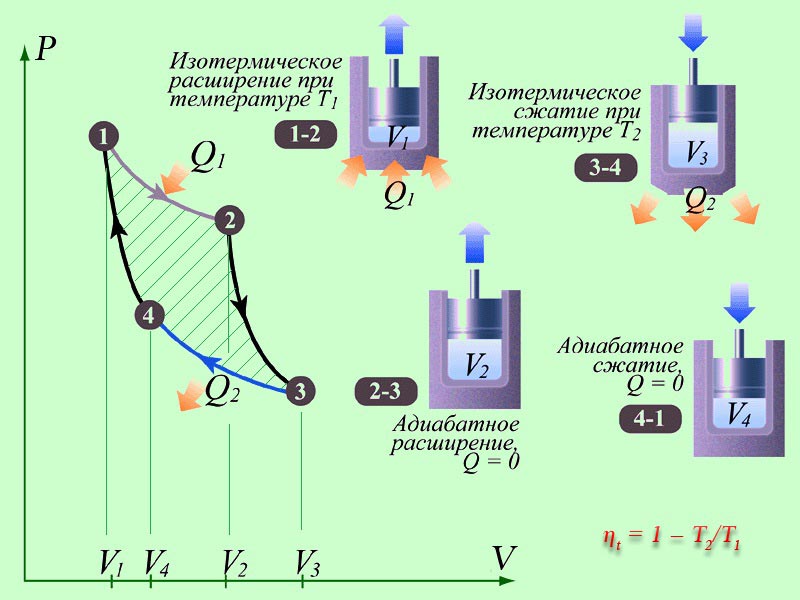
Ciclul Carnot este reperul la care aspiră inginerii care proiectează motoare termice. În condiții de temperaturi reale, a cărei limită superioară este determinată de rezistența materialelor, iar cea inferioară corespunde temperaturii mediu inconjurator, randamentul termic al ciclului Carnot poate ajunge la 0,7…0,8.
Orice motor termic real va fi cu atât mai perfect, cu atât eficiența sa este mai aproape de eficiența calculată a ciclului Carnot, care se desfășoară în aceleași limite de temperatură.
Realitățile moderne implică funcționarea pe scară largă a motoarelor termice. Numeroase încercări de a le înlocui cu motoare electrice au eșuat până acum. Problemele asociate cu acumularea de energie electrică în sistemele autonome sunt rezolvate cu mare dificultate.
Încă relevante sunt problemele tehnologiei pentru fabricarea acumulatorilor de energie electrică, ținând cont de utilizarea lor pe termen lung. Caracteristicile de viteză ale vehiculelor electrice sunt departe de cele ale mașinilor cu motoare cu ardere internă.
Primii pași către crearea motoarelor hibride se pot reduce semnificativ emisii nociveîn megaorașe, rezolvând problemele de mediu.
Un pic de istorie
Posibilitatea de a converti energia aburului în energie de mișcare era cunoscută în antichitate. 130 î.Hr.: Filosoful Heron al Alexandriei a prezentat publicului o jucărie cu abur - aeolipil. O sferă plină cu abur a început să se rotească sub acțiunea jeturilor emanate din ea. Acest prototip de turbine cu abur moderne nu și-a găsit aplicație în acele vremuri.
Timp de mulți ani și secole, dezvoltarea filozofului a fost considerată doar o jucărie distractivă. În 1629, italianul D. Branchi a creat o turbină activă. Aburul a pus în mișcare un disc echipat cu lame.
Din acel moment a început dezvoltarea rapidă a motoarelor cu abur.
motor termic
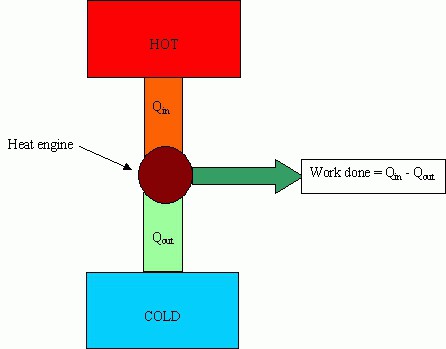
Principalele părți ale mașinilor: un încălzitor (un sistem de obținere a energiei din exterior), un fluid de lucru (realizează o acțiune utilă), un frigider.
Încălzitorul este proiectat pentru a se asigura că fluidul de lucru a acumulat o cantitate suficientă de energie internă pentru a efectua lucrări utile. Frigiderul elimină excesul de energie.
Principala caracteristică a eficienței se numește eficiența motoarelor termice. Această valoare arată ce parte din energia cheltuită pentru încălzire este cheltuită pentru a efectua lucrări utile. Cu cât randamentul este mai mare, cu atât este mai profitabilă funcționarea mașinii, dar această valoare nu poate depăși 100%.
Calculul randamentului
Fie ca încălzitorul să dobândească din exterior energie egală cu Q 1 . Fluidul de lucru a lucrat A, în timp ce energia dată frigiderului a fost Q 2 .
Pe baza definiției, calculăm eficiența:
η= A/Q1. Luăm în considerare faptul că A \u003d Q 1 - Q 2.
De aici, eficiența motorului termic, a cărui formulă are forma η = (Q 1 - Q 2) / Q 1 = 1 - Q 2 / Q 1, ne permite să tragem următoarele concluzii:
- Eficiența nu poate depăși 1 (sau 100%);
- pentru a maximiza această valoare este necesară fie o creștere a energiei primite de la încălzitor, fie o scădere a energiei date frigiderului;
- o creștere a energiei încălzitorului se realizează prin modificarea calității combustibilului;
- reducerea energiei date frigiderului, face posibilă realizarea caracteristicilor de proiectare ale motoarelor.

Motor termic ideal
Este posibil să se creeze un astfel de motor, a cărui eficiență ar fi maximă (ideal, egală cu 100%)? Fizicianul teoretic și talentatul inginer francez Sadi Carnot a încercat să găsească răspunsul la această întrebare. În 1824, calculele sale teoretice despre procesele care au loc în gaze au fost făcute publice.
Ideea principală din spatele unei mașini ideale este de a efectua procese reversibile cu un gaz ideal. Începem cu dilatarea izotermic a gazului la o temperatură T 1 . Cantitatea de căldură necesară pentru aceasta este Q 1. După ce gazul se extinde fără schimb de căldură. După ce a atins temperatura T 2, gazul este comprimat izotermic, transferând energia Q 2 la frigider. Revenirea gazului la starea inițială este adiabatică.
Eficiența unui motor termic Carnot ideal, atunci când este calculată cu precizie, este egală cu raportul dintre diferența de temperatură dintre dispozitivele de încălzire și răcire și temperatura pe care o are încălzitorul. Arată astfel: η=(T 1 - T 2)/ T 1.
Eficiența posibilă a unui motor termic, a cărui formulă este: η= 1 - T 2 / T 1 , depinde numai de temperatura încălzitorului și a răcitorului și nu poate fi mai mare de 100%.
Mai mult, acest raport ne permite să demonstrăm că eficiența motoarelor termice poate fi egală cu unitatea doar atunci când frigiderul atinge temperaturi. După cum știți, această valoare este de neatins.
Calculele teoretice ale lui Carnot fac posibilă determinarea eficienței maxime a unui motor termic de orice proiect.
Teorema demonstrată de Carnot este următoarea. Un motor termic arbitrar nu este în niciun caz capabil să aibă un coeficient de eficiență mai mare decât valoarea similară a eficienței unui motor termic ideal.
Exemplu de rezolvare a problemelor
Exemplul 1 Care este eficiența unui motor termic ideal dacă temperatura încălzitorului este de 800°C și temperatura frigiderului este cu 500°C mai mică?
T 1 \u003d 800 o C \u003d 1073 K, ∆T \u003d 500 o C \u003d 500 K, η -?
Prin definiție: η=(T 1 - T 2)/ T 1.
Nu ni se da temperatura frigiderului, ci ∆T = (T 1 - T 2), de aici:
η \u003d ∆T / T 1 \u003d 500 K / 1073 K \u003d 0,46.
Raspuns: eficienta = 46%.
Exemplul 2 Determinați eficiența unui motor termic ideal dacă se efectuează 650 J de muncă utilă datorită energiei de încălzire dobândite de un kilojoule.Care este temperatura încălzitorului motorului termic dacă temperatura lichidului de răcire este de 400 K?
Q 1 \u003d 1 kJ \u003d 1000 J, A \u003d 650 J, T 2 \u003d 400 K, η -?, T 1 \u003d?
În această problemă, vorbim despre o instalație termică, a cărei eficiență poate fi calculată prin formula:
Pentru a determina temperatura încălzitorului, folosim formula pentru eficiența unui motor termic ideal:
η \u003d (T 1 - T 2) / T 1 \u003d 1 - T 2 / T 1.
După efectuarea transformărilor matematice, obținem:
T 1 \u003d T 2 / (1- η).
T 1 \u003d T 2 / (1- A / Q 1).
Să calculăm:
η= 650 J / 1000 J = 0,65.
T 1 \u003d 400 K / (1- 650 J / 1000 J) \u003d 1142,8 K.
Răspuns: η \u003d 65%, T 1 \u003d 1142,8 K.
Conditii reale
Motorul termic ideal este proiectat având în vedere procesele ideale. Se lucrează numai în procese izoterme, valoarea sa este definită ca aria delimitată de graficul ciclului Carnot.

De fapt, este imposibil să se creeze condiții pentru procesul de schimbare a stării unui gaz fără schimbările însoțitoare de temperatură. Nu există materiale care să excludă schimbul de căldură cu obiectele din jur. proces adiabatic devine imposibil de implementat. În cazul transferului de căldură, temperatura gazului trebuie neapărat să se schimbe.
Eficiența motoarelor termice create în condiții reale diferă semnificativ de eficiența motoarelor ideale. Rețineți că procesele din motoarele reale sunt atât de rapide încât variația energiei termice interne a substanței de lucru în procesul de modificare a volumului acesteia nu poate fi compensată de afluxul de căldură din încălzitor și revenirea la răcitor.
Alte motoare termice
Motoarele reale funcționează pe diferite cicluri:
- Ciclul Otto: procesul la volum constant se modifică adiabatic, creând un ciclu închis;
- Ciclu diesel: izobar, adiabat, isocor, adiabat;
- proces care are loc la presiune constantă, este înlocuit cu adiabatic, închide ciclul.
Creați procese de echilibru în motoarele reale (pentru a le apropia de cele ideale) în condiții tehnologie moderna nu pare posibil. Eficiența motoarelor termice este mult mai scăzută, chiar și ținând cont de aceleași regimuri de temperatură ca într-o instalație termică ideală.
Dar nu ar trebui să reduceți rolul formulei de calcul al eficienței, deoarece aceasta devine punctul de plecare în procesul de lucru pentru creșterea eficienței motoarelor reale.
Modalități de a schimba eficiența
Când comparăm motoarele termice ideale și reale, este de remarcat faptul că temperatura frigiderului celui din urmă nu poate fi nicio. De obicei, atmosfera este considerată a fi un frigider. Temperatura atmosferei poate fi luată doar în calcule aproximative. Experiența arată că temperatura lichidului de răcire este egală cu temperatura gazelor de eșapament din motoare, așa cum este cazul la motoarele cu ardere internă (abreviat motoare cu ardere internă).
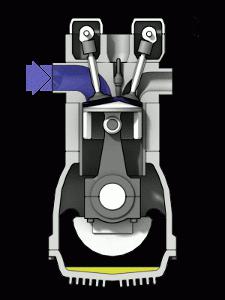
ICE este cel mai comun motor termic din lumea noastră. Eficiența unui motor termic în acest caz depinde de temperatura creată de combustibilul care arde. O diferență esențială între un motor cu ardere internă și motoarele cu abur este îmbinarea funcțiilor încălzitorului și fluidului de lucru al dispozitivului în amestecul aer-combustibil. Arzând, amestecul creează presiune asupra pieselor mobile ale motorului.
O creștere a temperaturii gazelor de lucru se realizează prin modificarea semnificativă a proprietăților combustibilului. Din păcate, nu este posibil să faceți acest lucru la infinit. Orice material din care este realizată camera de ardere a unui motor are propriul punct de topire. Rezistența la căldură a unor astfel de materiale este principala caracteristică a motorului, precum și capacitatea de a afecta semnificativ eficiența.
Valori ale randamentului motorului
Dacă luăm în considerare temperatura aburului de lucru la intrarea căruia este de 800 K, iar gazul de evacuare este de 300 K, atunci eficiența acestei mașini este de 62%. În realitate, această valoare nu depășește 40%. O astfel de scădere apare din cauza pierderilor de căldură în timpul încălzirii carcasei turbinei.

Cea mai mare valoare a randamentului motoarelor cu ardere internă nu depășește 44%. Creșterea acestei valori este o chestiune de viitor apropiat. Schimbarea proprietăților materialelor, combustibililor este o problemă la care lucrează cele mai bune minți ale omenirii.
Luați în considerare un reversibil ciclu Carnot realizat de un motor termic ideal.
Ciclul Carnot constă din patru procese reversibile: două izoterme și două adiabate. Pe fig. 3.10 arată ciclul Carnot direct.
![]()
Orez. 3.10
1. Parcela 1-2. Gazul ideal, situat în cilindrul de sub piston, în proces de dilatare izotermă (T 1 = const) este adus în contact termic cu încălzitorul, care transferă căldura Q 1 gazului ideal.
2. Parcela 2-3. În starea 2, gazul este complet izolat termic de încălzitor. Există o expansiune adiabatică a acesteia, iar temperatura scade la T 2 .
3. Parcul 3-4. În starea 3, gazul ideal este adus în contact cu răcitorul. Are loc compresia izotermă (T 2 = const), în care gazul ideal transferă căldura Q 2 la frigider.
4. Parcela 4-1. În starea 4, gazul este izolat termic de frigider. Apoi există compresia adiabatică. Temperatura gazului crește la T 1 .
Dinamica proceselor termodinamice poate fi observată în modelul computerizat „ciclul Carnot”.
Model de computer „ciclul Carnot”
Modelul este conceput pentru a studia un proces ciclic reversibil într-un gaz ideal, format din două izoterme și două adiabate (ciclul Carnot). La ocolirea ciclului Carnot, substanța de lucru este adusă secvențial în contact termic cu două rezervoare termice - un încălzitor și un frigider. În model, este posibilă modificarea temperaturilor T 1 și T 2 ale încălzitorului și frigiderului. Este prezentată o diagramă energetică, care arată cantitatea de căldură Q primită de gaz, munca efectuată A și modificarea ΔU în energia internă.
Amintiți-vă că un motor termic pornește Ciclul Carnot, are o eficienta maxima la temperaturi date ale incalzitorului si frigiderului.
Munca efectuată de corpul de lucru pe ciclu,
unde T 1 - temperatura încălzitorului; T 2 - temperatura frigiderului.
Formula (3.50) exprimă primul teorema Carnot:
Eficienţă un motor termic ideal care funcționează conform ciclului Carnot depinde doar de temperaturile încălzitorului și frigiderului; nu depinde de dispozitivul mașinii și de tipul fluidului de lucru.
Pentru un motor termic real (conform celei de-a doua teoreme Carnot):
Eficiența oricărui motor termic care funcționează conform ciclului Carnot cu aceleași încălzitoare și temperaturi mai scăzute ca un motor termic ideal nu poate depăși eficiența unui motor ideal,
acestea. Eficienta se gaseste prin formula
|
. |
(3.51) |
Conform ciclului Carnot direct funcționează motoarele cu ardere internă, motoarele diesel etc. Luați în considerare ciclul Carnot invers. Lucrul cu gaz pe ciclu A \u003d (Q 1 -Q2)< 0, где Q 1 < 0 - căldură îndepărtată din frigider; Q2 > 0 - căldură furnizată gazului la T 2< T 1 .
Transferul de căldură de la un corp rece la unul fierbinte are loc datorită muncii forțelor externe.
Eficiența unui motor termic ideal care funcționează pe ciclul Carnot invers este
Toate mașinile frigorifice funcționează în conformitate cu ciclul Carnot invers.
Presupunem că toate moleculele, cu excepția celei luate în considerare, sunt nemișcate. Moleculele vor fi considerate bile cu diametrul d. Ciocnirile vor avea loc ori de câte ori centrul moleculei imobile se află la o distanță mai mică sau egală cu d de linia dreaptă de-a lungul căreia se mișcă centrul moleculei considerate. În timpul coliziunilor, molecula își schimbă direcția de mișcare și apoi se mișcă în linie dreaptă până la următoarea coliziune. Prin urmare, centrul unei molecule în mișcare se mișcă de-a lungul unei linii întrerupte din cauza coliziunilor (Fig. 1).
| orez. unu |
Molecula se va ciocni cu toate moleculele imobile ale căror centre se află într-un cilindru spart cu un diametru de 2d. Într-o secundă, o moleculă parcurge o cale egală cu . Prin urmare, numărul de ciocniri care au loc în acest timp este egal cu numărul de molecule ale căror centre se încadrează în interiorul unui cilindru spart cu lungimea totală și raza d. Vom lua volumul acestuia egal cu volumul cilindrului îndreptat corespunzător, adică egal cu Dacă există n molecule în unitatea de volum a gazului, atunci numărul de ciocniri ale moleculei luate în considerare într-o secundă va fi egal cu
Pentru un gaz ideal. De aceea
| | (3.1.10) |
Aceasta arată că în timpul expansiunii izoterme (compresiei), calea liberă medie crește (descrește). După cum sa menționat în introducere, diametrul efectiv al moleculelor scade odată cu creșterea temperaturii. Prin urmare, la o concentrație dată de molecule, calea liberă medie crește odată cu creșterea temperaturii.Calculul căii libere medii pentru azot (d = 3 10 -10 m) în condiții normale (p = 1,01 10 5 Pa, T = 273,15 K). ) oferă: ![]() , și pentru numărul de coliziuni pe secundă:
, și pentru numărul de coliziuni pe secundă: ![]() . Astfel, calea liberă medie a moleculelor în condiții normale este de fracțiuni de microni, iar numărul de ciocniri este de câteva miliarde pe secundă. Prin urmare, procesele de egalizare a temperaturilor (conductivitate termică), viteze ale straturilor de gaz (frecare vâscoasă) și concentrații (difuzie) sunt destul de lente, ceea ce este confirmat de experiență.
. Astfel, calea liberă medie a moleculelor în condiții normale este de fracțiuni de microni, iar numărul de ciocniri este de câteva miliarde pe secundă. Prin urmare, procesele de egalizare a temperaturilor (conductivitate termică), viteze ale straturilor de gaz (frecare vâscoasă) și concentrații (difuzie) sunt destul de lente, ceea ce este confirmat de experiență.
Moleculă înseamnă cale liberă este distanța medie (notată cu λ) pe care o parcurge particula pe parcursul drumului liber de la o coliziune la alta.
Calea liberă medie a fiecărei molecule este diferită, deci în teoria cinetică este introdus conceptul de cale liberă medie (<λ>). Valoare<λ>este o caracteristică a întregului set de molecule de gaz la valori date de presiune și temperatură.
Unde σ este secțiunea transversală efectivă a moleculei, n este concentrația moleculelor.