Formula e avullit të pangopur. Avull i ngopur dhe i pangopur
Avujt e pangopur dhe të ngopur
Mbi sipërfaqen e lirë të një lëngu ka gjithmonë avuj të këtij lëngu, të cilët formohen për shkak të avullimit. Nëse hapësira mbi sipërfaqen e lirë të lëngut nuk kufizohet nga asnjë mur, molekulat ose atomet e substancës së avulluar, duke bërë lëvizje termike kaotike, largohen nga sipërfaqja e lëngut. Heqja e grimcave të avullit nga sipërfaqja e një lëngu lehtësohet nga fenomeni i difuzionit, si dhe nga konvekcioni natyror ose artificial i shtresave të ajrit. Përqendrimi i grimcave të avullit në temperaturë konstante në këto kushte, ai mund të ndryshojë në një gamë të gjerë, si në drejtim të uljes ashtu edhe në rritje. Çifte të tilla quhen të pangopura.
Një pamje tjetër vërehet nëse ka një hapësirë të kufizuar mbi sipërfaqen e lirë të lëngut. Nëse është e mbushur me ndonjë lëndë tjetër të gaztë, përveç avujve të lëngut avullues, apo jo, nuk ka rëndësi. Është e rëndësishme të theksohet se procesi i avullimit në një hapësirë të mbyllur mund të ndodhë vetëm deri në një kufi të caktuar. Sa më i madh të bëhet përqendrimi i molekulave ose atomeve të substancës avulluese në gjendje avulli, aq më i madh do të jetë presioni i këtyre avujve në një temperaturë konstante. Në këtë rast, një numër në rritje i molekulave ose atomeve mund të kthehen përmes sipërfaqes së lirë përsëri në lëng. Nëse sasia e hapësirës që i jepet avullit është mjaft e vogël dhe lëngu është mjaftueshëm i madh, mund të vendoset ekuilibri dinamik: numri i grimcave që largohen nga lëngu për njësi të kohës është i barabartë me numrin e grimcave që kthehen në lëng në të njëjtën kohë. . Në këtë rast, një masë konstante avulli do të jetë mbi lëngun dhe një përqendrim më i lartë i grimcave të tij në këto kushte nuk mund të arrihet. Një avull i tillë quhet i ngopur.
Presioni avull i ngopur e një substance në një temperaturë të caktuar mund të ketë një - të vetmen vlerë të caktuar.
Një rënie në vëllimin e hapësirës që i jepet një avulli të ngopur të një substance të caktuar në një temperaturë konstante çon në kondensimin e një pjese të avullit në një lëng, pasi përqendrimi i grimcave të tij nuk mund të kalojë një vlerë të caktuar. Ky kompresim izotermik avujt e ngopur ndryshon nga ngjeshja e avujve të pangopur, të cilët sillen si gazra të zakonshëm idealë. Prandaj, ligji Boyle-Mariotte nuk vlen për avujt e ngopur.
Ligji i Gay-Lussac gjithashtu nuk zbatohet për avujt e ngopur, pasi vëllimi i dhënë atyre është i pavarur nga temperatura.
Nuk zbatohet për avujt e ngopur dhe ligjin e Charles. Me rritjen e temperaturës gazet ideale ose avujt e pangopur në procesin izokorik, mesatarja energjia kinetike grimcat e tyre, gjë që çon në përplasjet e tyre më të shpeshta me njëra-tjetrën dhe me muret e enës, d.m.th. ndaj rritjes së presionit.
Është e mundur të flitet me besim se një enë e caktuar e mbyllur përmban saktësisht avullin e ngopur të një substance vetëm nëse ena përmban këtë substancë në gjendje e lëngshme dhe masa e fazës së tij të lëngshme nuk ndryshon.
Për shembull, na vendosin një enë qelqi të mbyllur përpara dhe na kërkojnë të përcaktojmë pa asnjë matje nëse përmban avuj uji të ngopur apo të pangopur.
Për t'iu përgjigjur kësaj pyetjeje, duhet të prisni disa minuta në mënyrë që përmbajtja e enës të ketë kohë për të ardhur në ekuilibër termodinamik me ajrin përreth. Kjo shkaktohet nga fakti se ne nuk e dimë se në çfarë temperature është sjellë ena nga dhoma, dhe një ndryshim në temperaturën e avullit në një vëllim konstant mund ta sjellë avullin nga një gjendje e pangopur në një gjendje të ngopur dhe anasjelltas. . Nëse, pasi vendoset ekuilibri, nuk ka kondensim të ujit në muret e brendshme të enës, duhet të themi se në temperaturën në të cilën bëhet vëzhgimi, ena përmban avull të pangopur. Nëse pikat e ujit shfaqen në muret e enës, avulli është i ngopur.
Avujt e ujit në ajër
Atmosfera e Tokës gjithmonë përmban avujt e ujit. Prania e tyre duhet të llogaritet shumë shpesh. Në veçanti, lagështia e ajrit duhet të vlerësohet me saktësi në dhomat e mbyllura ose të ajrosura dobët, dhomat e tharjes, etj.
Për kuantifikimi Përmbajtja e avullit të ujit në ajër përdor dy vlera - lagështia absolute (f) dhe lagështia relative (B).
Lagështia absolute quhet sasi fizike, e matur me masën e avullit të ujit që përmbahet në një metër kub ajër. Në këtë mënyrë, lagështia absolute përkon me dimensionin e densitetit, por në praktikë ata zakonisht përdorin një njësi - 1 g / m 3.
Rrethana e fundit është për faktin se lagështia absolute f, e shprehur në g/m 3, ndryshon pak në vlerë numerike nga presioni i pjesshëm i avullit të ujit p në të njëjtat kushte, i matur në milimetra merkur.
Raporti në përqindje i presionit të pjesshëm p të avullit të ujit në ajër me presionin e avullit të ujit të ngopur p n.p. në një temperaturë të caktuar quhet lagështia relative:
Gjatë llogaritjes së lagështisë relative duke përdorur këtë formulë, presioni p dhe p n.s. duhet të maten në të njëjtat njësi. Zakonisht ato maten jo në paskale, por në milimetra merkur. Vlera e p n.s përcaktohet nga tabelat.
Temperatura në të cilën ajri bëhet i ngopur me avujt e ujit gjatë ftohjes quhet pika e vesës.
Leksioni #2
BAZAT E TRANSFERIMIT TË NXEHTËSISË
Transferimi i nxehtësisë është një shkencë që studion modelet e proceseve të transferimit të nxehtësisë midis trupave dhe shpërndarjen e nxehtësisë brenda një trupi. Studimi i ligjeve të transferimit të nxehtësisë është i nevojshëm për të kontrolluar rrjedhat e nxehtësisë që ndodhin pothuajse kudo në proceset e punës së makinave, motorëve, aparateve, etj.
Në teorinë e transferimit të nxehtësisë, merren parasysh dy pyetje kryesore:
I. Përcaktimi i sasisë së nxehtësisë që bartet nga një trup në tjetrin ose kalon nga një pjesë e trupit në tjetrën në kushte të dhëna.
II. Përcaktimi i temperaturës në pjesë të ndryshme të trupit të përfshira në procesin e transferimit të nxehtësisë.
Një kusht i domosdoshëm dhe i mjaftueshëm për transferimin e nxehtësisë është ndryshimi i temperaturës.
Nxehtësia transmetohet në tre mënyra: përçueshmëri, konvekcion dhe rrezatim.
Përçueshmëria termike është procesi i shpërndarjes së energjisë termike me kontakt të drejtpërdrejtë të pjesëve individuale të trupit me temperatura të ndryshme.
Konvekcioni është procesi i transferimit të energjisë gjatë lëvizjes së vëllimeve të lëngut ose gazit në hapësirë nga një zonë me një temperaturë në një zonë me një temperaturë të ndryshme.
Rrezatimi (transferimi i nxehtësisë rrezatuese) është procesi i transferimit të energjisë nga valët elektromagnetike. Transferimi i nxehtësisë nga rrezatimi është një transformim i dyfishtë i energjisë: një trup më i nxehtë rrezaton energji në formën e lëkundjeve elektromagnetike, një trup tjetër më pak i nxehtë thith energjinë dhe nxehet.
Zakonisht, shkëmbimi i nxehtësisë midis trupave ndodh në të tre mënyrat njëkohësisht. Kombinimi i tyre mund të jetë më i larmishëm. Në këtë rast, njëra metodë mund të mbizotërojë mbi tjetrën, në varësi të kushteve në të cilat ndodh transferimi i nxehtësisë.
Sidoqoftë, kur studiohen proceset e transferimit të nxehtësisë, duhet të dallohen qartë dhe të merren parasysh veçmas metoda të ndryshme të transferimit të nxehtësisë (përçimi termik, konvekcioni dhe rrezatimi), pasi ato u binden ligjeve të ndryshme.
Proceset e transferimit të nxehtësisë në pajisjet e inxhinierisë së nxehtësisë mund të vazhdojnë si në modalitete të qëndrueshme (stacionare) dhe të paqëndrueshme (jo stacionare). Një regjim termik i palëvizshëm (i qëndrueshëm) është një regjim në të cilin temperatura në çdo pikë të trupit nuk varet nga koha. Një regjim stacionar gjithmonë i paraprin një regjim jostacionar.
Proceset që ndodhin në kushtet e kushteve termike jo-stacionare (proceset e ngrohjes dhe ftohjes) janë shumë komplekse dhe shqyrtimi i tyre nuk përfshihet në programin e këtij kursi. Prandaj, këtu merren parasysh vetëm proceset stacionare të transferimit të nxehtësisë.
PËRÇUESHMËRI TERMIKE
Konceptet bazë
Përçueshmëria termike është transferimi molekular i nxehtësisë brenda vazhdimësi për shkak të pranisë së një ndryshimi të temperaturës.
Kjo metodë e transferimit të nxehtësisë ndodh kryesisht në trupat e ngurtë si brenda një trupi ashtu edhe midis dy trupave kur ata bien në kontakt me njëri-tjetrin. Përçueshmëria termike mund të kryhet edhe përmes një shtrese lëngu ose gazi. Megjithatë, gazet dhe lëngjet, me përjashtim të metaleve të shkrirë, janë përcjellës shumë të dobët të nxehtësisë.
fusha e temperaturës. Procesi i përcjelljes së nxehtësisë, si dhe llojet e tjera të transferimit të nxehtësisë, kryhet vetëm me kushtin që temperatura të mos jetë e njëjtë në pika të ndryshme të trupit. Siç e dini, temperatura është një parametër i gjendjes së trupit dhe karakterizon shkallën e ngrohjes së tij. Seti i vlerave të temperaturës në të gjitha pikat e hapësirës së konsideruar në ky moment koha quhet fusha e temperaturës. Matematikisht, fusha e temperaturës shprehet në funksion të koordinatave
Një sipërfaqe në të gjitha pikat e së cilës temperatura është e njëjtë quhet izotermale.
Sepse dy njerëz nuk mund të jenë në të njëjtën pikë në hapësirë në të njëjtën kohë. temperatura të ndryshme, atëherë sipërfaqe të ndryshme izotermike nuk kryqëzohen kurrë. Të gjithë ata ose përfundojnë në sipërfaqen e trupit, ose ndodhen tërësisht brenda tij.
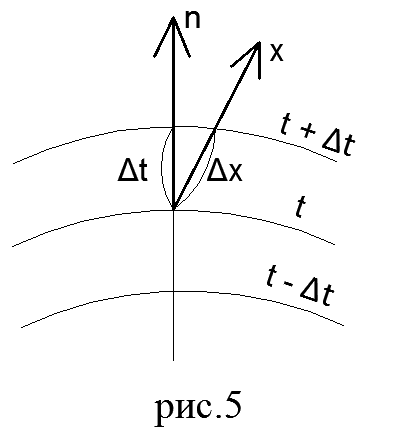 Ligji i Furierit. Rrjedha e nxehtësisë është sasia e nxehtësisë Q që kalon për njësi të kohës nëpër një sipërfaqe arbitrare. Vektori i fluksit të nxehtësisë është gjithmonë i drejtuar në drejtim të uljes së temperaturës.
Ligji i Furierit. Rrjedha e nxehtësisë është sasia e nxehtësisë Q që kalon për njësi të kohës nëpër një sipërfaqe arbitrare. Vektori i fluksit të nxehtësisë është gjithmonë i drejtuar në drejtim të uljes së temperaturës.
Në mënyrë sasiore, intensiteti i transferimit të nxehtësisë karakterizohet nga densiteti i fluksit të nxehtësisë q.
Dendësia e fluksit të nxehtësisë ose fluksi specifik i nxehtësisë është sasia e nxehtësisë që kalon nëpër njësinë e sipërfaqes F për njësi të kohës τ:
Relacioni (51) shpreh ligjin bazë të përçueshmërisë termike dhe quhet ligji i Furierit.
Shenja minus në anën e djathtë të relacionit (51) do të thotë se vektorët e fluksit të nxehtësisë dhe gradientit të temperaturës janë të drejtuar në drejtime të kundërta.
Koeficienti i proporcionalitetit λ në shprehjen (51) është një parametër fizik i substancës, i quajtur koeficienti i përçueshmërisë termike. Karakterizon aftësinë e një substance për të përcjellë nxehtësinë.
Dimensioni i koeficientit të përçueshmërisë termike përcaktohet nga shprehja (51):
Rrjedhimisht, vlera e koeficientit të përçueshmërisë termike është numerikisht e barabartë me fluksin specifik të nxehtësisë përmes një muri me trashësi njësi në një ndryshim temperature prej 1 o C. Sa më i madh λ, aq më mirë substanca është një përcjellës nxehtësie.
Metalet janë përcjellës të mirë të nxehtësisë; ajri i thatë dhe i qetë është një përcjellës i dobët i nxehtësisë. Materialet poroze të lehta nuk e përcjellin mirë nxehtësinë, pasi poret e tyre janë të mbushura me ajër. Materialet përçueshmëria termike e të cilave është më pak se 0,2 W / (m-deg) quhen izolues të nxehtësisë. Uji ka përçueshmëri të dobët termike, megjithatë, përçueshmëria termike e një materiali të lagësht rritet ndjeshëm në krahasim me përçueshmërinë e tij termike në një gjendje të thatë. Kjo për faktin se uji e përcjell nxehtësinë 20-25 herë më mirë se ajri. Prandaj, mbushja e poreve të trupit me ujë ul ndjeshëm vetitë e tij izoluese termike.
Vlera e koeficientit të përçueshmërisë termike λ për çdo trup gjendet në mënyrë eksperimentale. Rezultatet janë përmbledhur në tabela që përdoren në llogaritjet.
Përçueshmëria termike e murit
Mur i sheshtë i vetëm. Figura 6 tregon një mur të sheshtë me një shtresë me trashësi δ të bërë nga një material homogjen (tulla, metal, dru ose ndonjë tjetër).
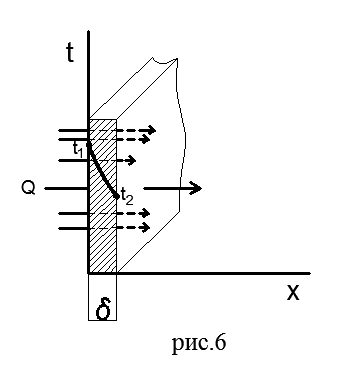 Le të supozojmë se koeficienti i përçueshmërisë termike të materialit λ nuk varet nga temperatura. Temperaturat konstante t 1 >t 2 ruhen në sipërfaqet e jashtme të murit; temperatura ndryshon vetëm në drejtim të boshtit x, i cili është pingul me rrafshin e murit, d.m.th., fusha e temperaturës është njëdimensionale dhe gradienti i temperaturës është i barabartë me dt/dx.
Le të supozojmë se koeficienti i përçueshmërisë termike të materialit λ nuk varet nga temperatura. Temperaturat konstante t 1 >t 2 ruhen në sipërfaqet e jashtme të murit; temperatura ndryshon vetëm në drejtim të boshtit x, i cili është pingul me rrafshin e murit, d.m.th., fusha e temperaturës është njëdimensionale dhe gradienti i temperaturës është i barabartë me dt/dx.
Le të gjejmë densitetin e fluksit të nxehtësisë që kalon nëpër një mur të caktuar dhe të përcaktojmë natyrën e ndryshimit të temperaturës përgjatë trashësisë së murit.
Le të zgjedhim brenda murit një shtresë elementare me trashësi dx të kufizuar nga dy sipërfaqe izotermike. Ekuacioni i Furierit për këtë shtresë ka formën
Pas integrimit
Nga ky ekuacion, mund të përcaktohet dendësia e fluksit të nxehtësisë që kalon nëpër murin e konsideruar. Duke vendosur në ekuacionin (53) x=δ, marrim t= t2, ku
| | (54) |
Dendësia e fluksit të nxehtësisë në një mur të sheshtë është drejtpërdrejt proporcionale me koeficientin e përçueshmërisë termike λ, ndryshimin e temperaturës () dhe në proporcion të zhdrejtë me trashësinë e murit δ. Duhet të kihet parasysh se rrjedha e nxehtësisë nuk përcaktohet nga vlera absolute e temperaturave, por nga ndryshimi i tyre - ndryshimi i temperaturës.Ekuacioni (54) është formula e llogaritjes për përçueshmërinë termike të një muri të sheshtë. Ai lidh katër sasi q, λ, δ dhe :
Raporti i trashësisë së murit me koeficientin e përçueshmërisë termike δ/λ quhet rezistenca termike e murit.
Ekuacioni (55) tregon se fluksi specifik i nxehtësisë është drejtpërdrejt proporcional me ndryshimin e temperaturës dhe në përpjesëtim të zhdrejtë me rezistencën termike të murit. Në të vërtetë, sa më i madh të jetë emëruesi i fraksionit në ekuacionin (55), d.m.th., δ/λ, aq më i ulët është densiteti i fluksit të nxehtësisë q. Rrjedhimisht, me një rritje të trashësisë së murit δ ose me një ulje të përçueshmërisë termike λ, densiteti i fluksit të nxehtësisë q zvogëlohet.
Pasi të kemi përcaktuar densitetin e fluksit të nxehtësisë me formulën (54), mund të përcaktojmë sasinë totale të nxehtësisë Q në xhaul të transferuar përmes murit të sheshtë nga sipërfaqja F gjatë kohës τ:
Ky ekuacion është ekuacioni i një vije të drejtë. Kështu, në një vlerë konstante të koeficientit të përçueshmërisë termike, temperatura ndryshon në mënyrë lineare mbi trashësinë e një muri homogjen. Në rastet kur përçueshmëria termike varet nga temperatura, ajo është një variabël dhe formulat e llogaritjes janë disi më të komplikuara.
Mësimi #2/5 2
Tema nr.26: “Modeli i strukturës së një lëngu. Të ngopur dhe avujt e pangopur. Lagështia e ajrit”.
1 Modeli i strukturës së lëngut
Lëngu është një nga gjendjet agregate substancave. Vetia kryesore e një lëngu, e cila e dallon atë nga gjendjet e tjera të grumbullimit, është aftësia për të ndryshuar formën e tij për një kohë të pacaktuar nën veprimin e streseve mekanike tangjenciale, qoftë edhe në mënyrë arbitrare të vogla, duke ruajtur praktikisht vëllimin.
Fig.1
Gjendja e lëngshme zakonisht konsiderohet e ndërmjetme ndërmjet të ngurtë dhe të gaztë : një gaz nuk ruan as vëllimin as formën, por një e ngurtë i ruan të dyja.
molekulat lëngjet nuk kanë një pozicion të caktuar, por në të njëjtën kohë nuk kanë liri të plotë të lëvizjes. Mes tyre ka një tërheqje, aq e fortë sa për t'i mbajtur pranë.
Një substancë në gjendje të lëngshme ekziston në një interval të caktuar temperaturat , poshtë së cilës futetgjendje e ngurtë(ndodh kristalizimi ose transformimi në një gjendje amorfe në gjendje të ngurtë - xhami), sipër - në të gaztë (bëhet avullimi). Kufijtë e këtij intervali varen nga presion .
Të gjitha lëngjet zakonisht ndahen në lëngje të pastra dhe përzierjet . Disa përzierje lëngjesh janë thelbësore për jetën: gjaku, uji i detit etj. Lëngjet mund të kryejnë funksionin tretës.
Fluiditeti është vetia kryesore e lëngjeve. Nëse aplikoni në një seksion të një lëngu në ekuilibër forcë e jashtme , atëherë ka një rrjedhje të grimcave të lëngut në drejtimin në të cilin zbatohet kjo forcë: lëngu rrjedh. Kështu, nën veprimin e forcave të jashtme të çekuilibruara, lëngu nuk ruan formën dhe rregullimin relativ të pjesëve, dhe për këtë arsye merr formën e enës në të cilën ndodhet.
Ndryshe nga lëndët e ngurta plastike, lëngjet nuk kanëforca e rendimentit: mjafton të aplikoni një forcë të jashtme arbitrarisht të vogël që lëngu të rrjedhë.
Një nga vetitë karakteristike të një lëngu është se ai ka sasi e caktuar ( me të pandryshuar kushtet e jashtme). Lëngu është jashtëzakonisht i vështirë për t'u ngjeshur mekanikisht sepse, ndryshe nga gazit , midis molekulave ka shumë pak hapesire e lire. Presioni i ushtruar në një lëng të mbyllur në një enë transmetohet pa ndryshim në secilën pikë të vëllimit të këtij lëngu ( ligji i paskalit , gjithashtu i vlefshëm për gazrat). Kjo veçori, së bashku me kompresueshmërinë shumë të ulët, përdoret në makinat hidraulike.
Lëngjet zakonisht rriten në vëllim (zgjerohen) kur nxehen dhe ulen në vëllim (kontraktohen) kur ftohen. Megjithatë, ka përjashtime, për shembull, ujë tkurret kur nxehet, në presion normal dhe në temperatura ndërmjet 0°C dhe afërsisht 4°C.
Përveç kësaj, lëngjet (si gazet) karakterizohen nga viskozitetit . Përkufizohet si aftësia për t'i rezistuar lëvizjes së njërës prej pjesëve në lidhje me tjetrën - domethënë si fërkim i brendshëm.
Kur shtresat ngjitur të një lëngu lëvizin në lidhje me njëra-tjetrën, në mënyrë të pashmangshme ndodh një përplasje e molekulave përveç asaj për shkak tëlëvizje termike. Ka forca që ngadalësojnë lëvizjen e urdhëruar. Në këtë rast, energjia kinetike e lëvizjes së porositur shndërrohet në energji termike - energjia e lëvizjes kaotike të molekulave.
Lëngu në enë, i vënë në lëvizje dhe i lënë në vetvete, gradualisht do të ndalet, por temperatura e tij do të rritet.Në një avull, si një gaz, pothuajse mund të injorohen forcat e kohezionit dhe ta konsiderojnë lëvizjen si një fluturim të lirë të molekulave dhe përplasjen e tyre me njëri-tjetrin dhe me trupat përreth (muret dhe lëngu që mbulojnë pjesën e poshtme të enës). Në një lëng, molekulat, si në një të ngurtë, ndërveprojnë fort, duke mbajtur njëra-tjetrën. Megjithatë, ndërsa në një trup të ngurtë secila molekulë ruan një pozicion të caktuar ekuilibri pafundësisht të gjatë brenda trupit dhe lëvizja e saj reduktohet në lëkundje rreth këtij pozicioni ekuilibri, natyra e lëvizjes në një lëng është e ndryshme. Molekulat e lëngshme lëvizin shumë më lirshëm se molekulat e ngurta, megjithëse jo aq lirshëm sa molekulat e gazit. Çdo molekulë në një lëng lëviz përpara dhe mbrapa për ca kohë, pa u larguar, megjithatë, nga fqinjët e saj. Kjo lëvizje të kujton lëkundjen e një molekule të ngurtë rreth një pozicioni ekuilibri. Megjithatë, herë pas here një molekulë e lëngshme del nga mjedisi i saj dhe zhvendoset në një vend tjetër, duke rënë në një mjedis të ri, ku përsëri kryen një lëvizje të ngjashme me lëkundjen për disa kohë.
Kështu, lëvizja e molekulave të lëngshme është diçka si një përzierje lëvizjesh në një trup të ngurtë dhe në një gaz: lëvizja "osciluese" në një vend zëvendësohet nga një kalim "i lirë" nga një vend në tjetrin. Në përputhje me këtë, struktura e një lëngu është diçka ndërmjet strukturës së një trupi të ngurtë dhe strukturës së një gazi. Sa më e lartë të jetë temperatura, d.m.th., sa më e madhe të jetë energjia kinetike e molekulave të lëngut, aq më i madh është roli që luan lëvizja "e lirë": aq më të shkurtra janë intervalet e gjendjes "osciluese" të molekulës dhe aq më shpesh "e lirë". "Tranzicionet, d.m.th., aq më shumë lëngu i ngjan një gazi. Kur mjafton temperaturë të lartë karakteristikë e çdo lëngu (e ashtuquajtura temperaturë kritike), vetitë e lëngut nuk ndryshojnë nga vetitë e një gazi shumë të ngjeshur.
2 Avujt e ngopur dhe të pangopur dhe vetitë e tyre
Mbi sipërfaqen e lirë të një lëngu ka gjithmonë avuj të këtij lëngu. Nëse ena me lëngun nuk është e mbyllur, atëherë përqendrimi i grimcave të avullit në një temperaturë konstante mund të ndryshojë në një gamë të gjerë në drejtim të uljes dhe rritjes.
Procesi i avullimit në një hapësirë të mbyllur(enë e mbyllur me lëng)mund të ndodhë në një temperaturë të caktuar vetëm deri në një kufi të caktuar. Kjo për faktin se kondensimi i avullit ndodh njëkohësisht me avullimin e lëngut. Së pari, numri i molekulave të emetuara nga lëngu në 1 s, më shumë numër molekulat që kthehen prapa, dhe dendësia, dhe si rrjedhim presioni i avullit, rritet. Kjo çon në një rritje të shkallës së kondensimit. Pas ca kohësh, vendoset ekuilibri dinamik, në të cilin dendësia e avullit mbi lëng bëhet konstante.
Një avull që është në ekuilibër dinamik me lëngun e tij quhet avull i ngopur. Një avull që nuk është në ekuilibër dinamik me lëngun e tij quhet i pangopur.
Përvoja tregon se avujt e pangopur u binden të gjithëve ligjet e gazit , dhe sa më të sakta, aq më larg ngopjes.Për avujt e ngopur janë karakteristike këto veti:
- dendësia dhe presioni i avullit të ngopur në një temperaturë të caktuar janë dendësia dhe presioni maksimal që mund të ketë avulli në një temperaturë të caktuar;
- dendësia dhe presioni i avullit të ngopur varen nga lloji i substancës. Sa më e ulët të jetë nxehtësia specifike e avullimit të një lëngu, aq më shpejt ai avullohet dhe aq më i madh është presioni dhe dendësia e avujve të tij;
- presioni dhe dendësia e avullit të ngopur përcaktohen në mënyrë unike nga temperatura e tij (ato nuk varen nga mënyra se si avulli arriti këtë temperaturë: gjatë ngrohjes ose ftohjes);
- Presioni i avullit dhe dendësia rriten me shpejtësi me rritjen e temperaturës (Fig. 1, a, b).
Përvoja tregon se kur një lëng nxehet, niveli i lëngut në një enë të mbyllur zvogëlohet. Rrjedhimisht, masa dhe dendësia e avullit rriten. Një rritje më e fortë e presionit të avullit të ngopur në krahasim me një gaz ideal (ligji Gay-Lussac nuk është i zbatueshëm për avujt e ngopur) shpjegohet me faktin se këtu presioni rritet jo vetëm për shkak të rritjes së energjisë mesatare kinetike të molekulat (si në një gaz ideal), por edhe për shkak të rritjes së përqendrimit të molekulave;
- në temperaturë konstante, presioni dhe dendësia e avullit të ngopur nuk varen nga vëllimi. Figura 2 tregon për krahasim izotermat e gazit ideal (a) dhe avullit të ngopur (b).

Oriz. 2
Përvoja tregon se gjatë zgjerimit izotermik niveli i lëngut në enë zvogëlohet, ndërsa gjatë ngjeshjes rritet, d.m.th. numri i molekulave të avullit ndryshon në mënyrë që dendësia e avullit të mbetet konstante.
3 Lagështia
Ajri që përmban avujt e ujit quhet i lagur . Për të karakterizuar përmbajtjen e avullit të ujit në ajër, futen një sërë sasish: lagështia absolute, presioni i avullit të ujit dhe lagështia relative.
lagështia absoluteρ ajri quhet një vlerë numerikisht e barabartë me masën e avullit të ujit që përmbahet në 1 m 3 ajri (d.m.th. dendësia e avullit të ujit në ajër në kushte të caktuara).
Presioni i avullit të ujit p është presion i pjesshëm avujt e ujit që gjenden në ajër. Njësitë SI për lagështinë absolute dhe elasticitetin janë, përkatësisht, kilogram për metër kub (kg/m 3) dhe paskal (Pa).
Nëse dihet vetëm lagështia absolute ose presioni i avullit të ujit, është ende e pamundur të gjykohet se sa i thatë ose i lagësht është ajri. Për të përcaktuar shkallën e lagështisë së ajrit, është e nevojshme të dihet nëse avulli i ujit është afër ose larg ngopjes.
lageshtia relative ajri φ quhet raporti i përqindjes së lagështisë absolute ndaj densitetitρ 0 avulli i ngopur në një temperaturë të caktuar (ose raporti i presionit të avullit të ujit ndaj presionit p0 avulli i ngopur në një temperaturë të caktuar):
Sa më e ulët të jetë lagështia relative, aq më i madh është avulli nga ngopja, aq më intensiv është avullimi. Presioni i avullit të ngopur p0 në një temperaturë të caktuar - një vlerë tabelare. Elasticiteti i avullit të ujit (dhe rrjedhimisht lagështia absolute) përcaktohet nga pika e vesës.
Me ftohje izobarike në një temperaturë tp avulli bëhet i ngopur dhe gjendja e tij përfaqësohet me një pikë AT . Temperatura t p në të cilën avulli i ujit bëhet i ngopur quhet pika e vesës . Kur ftohet nën pikën e vesës, fillon kondensimi i avullit: shfaqet mjegull, vesa bie, dritaret mjegullohen.
4 Matja e lagështisë
Përdoret për të matur lagështinë e ajrit instrumente matëse higrometra. Ekzistojnë disa lloje të higrometrave, por më kryesorët janë: flokët dhe psikometrike.
Meqenëse është e vështirë të matet drejtpërdrejt presioni i avullit të ujit në ajër, matet lagështia relative e ajritnë mënyrë indirekte.
Parimi i funksionimithigrometër i flokëvebazuar në vetinë e flokëve të dhjamosur (njerëz ose kafshë)ndryshoni gjatësinë e sajvarësisht nga lagështia e ajrit në të cilin ndodhet.

Flokët shtrirë mbi një kornizë metalike. Ndryshimi në gjatësinë e flokëve transmetohet në shigjetën që lëviz përgjatë shkallës. Higrometri i flokëve në dimër është instrumenti kryesor për matjen e lagështisë së jashtme.
Një higrometër më i saktë është një higrometër psikrometrik - psikometër
(sipas grekëve të tjerë "psychros" do të thotë i ftohtë).
Dihet se lagështia relative varet shkalla e avullimit.
Sa më e ulët të jetë lagështia e ajrit, aq më e lehtë është që lagështia të avullojë.

Psikrometri ka dy termometra . Njëra është e zakonshme, quhet thatë. Ai mat temperaturën e ajrit përreth. Balona e një termometri tjetër mbështillet me një fitil pëlhure dhe ulet në një enë me ujë. Termometri i dytë nuk tregon temperaturën e ajrit, por temperaturën e fitilit të lagësht, prandaj emri i lagur termometri. Sa më e ulët të jetë lagështia e ajrit, aq më intensive lagështia avullohet nga fitili, sa më e madhe të hiqet sasia e nxehtësisë për njësi të kohës nga termometri i lagur, aq më të vogla janë leximet e tij, prandaj, aq më i madh është ndryshimi midis leximeve të termometrave të thatë dhe të lagur.
Pika e vesës përcaktohet duke përdorur higrometra. Higrometri i kondensimit është një kuti metalike POR , muri ballor te e cila është e lëmuar mirë (Fig. 2) Një lëng që avullohet lehtë - eter - derdhet në kuti dhe futet një termometër. Kalimi i ajrit përmes kutisë me një llambë gome G , shkaktojnë avullim të fortë të eterit dhe ftohje të shpejtë të kutisë. Termometri mat temperaturën në të cilën shfaqen pikat e vesës në sipërfaqen e lëmuar të murit. te . Presioni në zonën ngjitur me murin mund të konsiderohet konstant, pasi kjo zonë komunikon me atmosferën dhe ulja e presionit për shkak të ftohjes kompensohet nga një rritje në përqendrimin e avullit. Shfaqja e vesës tregon se avulli i ujit është ngopur. Duke ditur temperaturën e ajrit dhe pikën e vesës, mund të gjeni presionin e pjesshëm të avullit të ujit dhe lagështinë relative.
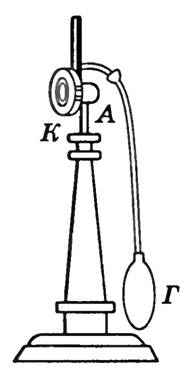
Oriz. 2
5 Detyra për zgjidhje të pavarur
Detyra 1
Jashtë po bie shi i ftohtë vjeshte. Në cilin rast rrobat e varura në kuzhinë do të thahen më shpejt: kur dritarja është e hapur apo kur është e mbyllur? Pse?
Detyra 2
Lagështia është 78% dhe leximi i llambës së thatë është 12°C. Çfarë temperature tregon një termometër me llambë të lagësht?(Përgjigje: 10 °C.)
Detyra 3
Dallimi midis leximeve të termometrit të thatë dhe të lagësht është 4°C. Lagështia relative e ajrit 60%. Cilat janë leximet e llambave të thata dhe të lagështa?(Përgjigje: t c -l9 ° С, t m \u003d 10 ° С.)
Proceset e avullimit dhe të kondensimit janë të vazhdueshme dhe paralele me njëri-tjetrin.
Në një enë të hapur, sasia e lëngut zvogëlohet me kalimin e kohës, sepse. avullimi mbizotëron mbi kondensimin.
Avulli që është mbi sipërfaqen e një lëngu kur avullimi mbizotëron mbi kondensimin, ose avulli në mungesë të lëngut, quhet të pangopura.
Në një enë të mbyllur hermetikisht, niveli i lëngut nuk ndryshon me kalimin e kohës, sepse avullimi dhe kondensimi kompensojnë njëra-tjetrën: sa molekula fluturojnë nga lëngu, pasi shumë prej tyre kthehen në të në të njëjtën kohë, ndodh një ekuilibër dinamik (i lëvizshëm) midis avullit dhe lëngut të tij.
Një avull që është në ekuilibër dinamik me lëngun e tij quhet e ngopur.
Në një temperaturë të caktuar, avulli i ngopur i një lëngu ka dendësia më e lartë ( ) dhe krijon presion maksimal ( ) që avulli i atij lëngu mund të ketë në atë temperaturë.
Presioni dhe dendësia e avullit të ngopur në të njëjtën temperaturë varet nga lloji i substancës: më shumë presion krijon avull të ngopur të lëngut që avullon më shpejt. Për shembull, dhe
Karakteristikat e avujve të pangopur: Avujt e pangopur u binden ligjeve të gazit të Boyle - Mariotte, Gay-Lussac, Charles, dhe ekuacioni ideal i gjendjes së gazit mund të zbatohet për ta.
Karakteristikat e avullit të ngopur:1. Me një vëllim konstant, me rritjen e temperaturës, presioni i avullit të ngopur rritet, por jo në proporcion të drejtë (ligji i Charles nuk plotësohet), presioni rritet më shpejt se ai i një gazi ideal. , me rritjen e temperaturës ( ) , masa e avullit rritet, dhe për këtë arsye përqendrimi i molekulave të avullit rritet () dhe presioni i avullit të ngopur do të shkrihet për dy arsye (
3 1 - avull i pangopur ( gaz ideal);
2 2 - avull i ngopur; 3 - avull i pangopur,
1 marrë nga avulli i ngopur në të njëjtën
vëllimi kur nxehet.
2. Presioni i avullit të ngopur në një temperaturë konstante nuk varet nga vëllimi që ai zë.
Me një rritje të vëllimit, masa e avullit rritet, dhe masa e lëngut zvogëlohet (një pjesë e lëngut kalon në avull), me një ulje të vëllimit të avullit, bëhet më pak, dhe lëngu bëhet më i madh (pjesë i avullit kalon në lëng), dendësia dhe përqendrimi i molekulave të avullit të ngopur mbeten konstante, prandaj, dhe presioni mbetet konstant ().
lëngshme
(u ul. avull + lëng)
Të pangopura avulli
Avujt e ngopur nuk u binden ligjeve të gazit të Boyle - Mariotte, Gay-Lussac, Charles, sepse masa e avullit në procese nuk mbetet konstante, por e gjitha ligjet e gazit të marra për një masë konstante. Ekuacioni i gjendjes për një gaz ideal mund të zbatohet për avullin e ngopur.
Kështu që, avulli i ngopur mund të shndërrohet në avull të pangopur, qoftë duke e ngrohur atë në vëllim konstant ose duke rritur vëllimin e tij në një temperaturë konstante. Avulli i pangopur mund të shndërrohet në avull të ngopur ose duke e ftohur në një vëllim konstant ose duke e ngjeshur në një temperaturë konstante.
Situata kritike
Prania e një sipërfaqe të lirë në një lëng bën të mundur që të tregohet se ku ndodhet faza e lëngshme e substancës dhe ku ajo e gaztë. Dallimi i mprehtë midis një lëngu dhe avullit të tij shpjegohet me faktin se dendësia e një lëngu është shumë herë më e madhe se ajo e një avulli. Nëse një lëng nxehet në një enë të mbyllur hermetikisht, atëherë për shkak të zgjerimit, densiteti i tij do të ulet dhe densiteti i avullit mbi të do të rritet. Kjo do të thotë që ndryshimi midis një lëngu dhe avullit të tij të ngopur zbutet dhe zhduket fare në një temperaturë mjaft të lartë. Temperatura në të cilën diferencat në vetitë fizike midis një lëngu dhe avullit të tij të ngopur, dhe dendësia e tyre bëhet e njëjtë, quhettemperaturë kritike.
Për formimin e lëngut nga gazi, mesatarja energji potenciale tërheqja e molekulave duhet të tejkalojë energjinë mesatare kinetike të tyre.
Temperatura kritike – Temperatura maksimale në të cilin avulli shndërrohet në lëng. Temperatura kritike varet nga energjia potenciale e bashkëveprimit molekular dhe për këtë arsye është e ndryshme për gazra të ndryshëm. Për shkak të ndërveprimit të fortë të molekulave të ujit, avulli i ujit mund të shndërrohet në ujë edhe në një temperaturë prej . Në të njëjtën kohë, lëngëzimi i azotit ndodh vetëm në një temperaturë më të vogël se = -147˚, sepse molekulat e azotit ndërveprojnë dobët me njëra-tjetrën.
Një tjetër parametër makroskopik që ndikon në tranzicionin avull-lëng është presioni. Me një rritje të presionit të jashtëm gjatë kompresimit të gazit, distanca mesatare midis grimcave zvogëlohet, forca e tërheqjes midis tyre rritet dhe, në përputhje me rrethanat, energjia mesatare potenciale e ndërveprimit të tyre.
Presioniavulli i ngopur në temperaturën e tij kritike quhet kritike. Ky është presioni më i lartë i mundshëm i avullit të ngopjes së një substance të caktuar.
Gjendja e çështjes me parametra kritikë quhet kritike(pikë kritike) . Çdo substancë ka temperaturën dhe presionin e vet kritik.
AT gjendje kritike nxehtësia specifike e avullimit dhe koeficienti tensioni sipërfaqësor lëngjeve. Në temperatura mbi kritike, madje edhe në shumë presione të lartaështë e pamundur të shndërrohet gazi në lëng, d.m.th. mbi temperaturën kritike, lëngu nuk mund të ekzistojë. Në temperaturat superkritike, vetëm gjendja e avullit të materies është e mundur.
Lëngëzimi i gazeve është i mundur vetëm në temperatura nën temperaturën kritike. Për lëngëzimin, gazrat ftohen në një temperaturë kritike, për shembull, nga zgjerimi adiabatik, dhe më pas kompresohen në mënyrë izotermale.
Duke zier
Nga jashtë, fenomeni duket si ky: Nga i gjithë vëllimi i lëngut, flluska me rritje të shpejtë ngrihen në sipërfaqe, ato shpërthejnë në sipërfaqe dhe avulli lëshohet në mjedis.
MKT e shpjegon vlimin si kjo: në lëng ka gjithmonë flluska ajri, në të cilat ndodh avullimi nga lëngu. Vëllimi i mbyllur i flluskave rezulton të jetë i mbushur jo vetëm me ajër, por edhe me avull të ngopur. Presioni i avullit të ngopur në to kur lëngu nxehet rritet më shpejt se presioni i ajrit. Kur presioni i avullit të ngopur në flluska në një lëng të ngrohur mjaftueshëm bëhet më i madh se presioni i jashtëm, ato rriten në vëllim dhe forca e lëvizjes, e cila tejkalon gravitetin e tyre, i ngre flluskat në sipërfaqe. Flluskat e notuara fillojnë të shpërthejnë kur, në një temperaturë të caktuar, presioni i avullit të ngopur në to tejkalon presionin mbi lëngun. Temperatura e një lëngu në të cilën presioni i avullit të tij të ngopur në flluska është i barabartë ose më i madh se presioni i jashtëm në lëng quhet pikë vlimi.
Pika e vlimit të lëngjeve të ndryshme është e ndryshme, sepse presioni i avullit të ngopur në flluskat e tyre krahasohet me të njëjtin presion të jashtëm në temperatura të ndryshme. Për shembull, presioni i avullit të ngopjes në flluska është i barabartë me presionin normal atmosferik për ujin në 100°C, për merkurin në 357°C, për alkoolin në 78°C, për eterin në 35°C.
Pika e vlimit mbetet konstante gjatë procesit të vlimit, sepse e gjithë nxehtësia që i jepet lëngut të ndezur shpenzohet në avullim.
Pika e vlimit varet nga presioni i jashtëm në lëng: me rritjen e presionit, temperatura rritet; me uljen e presionit, temperatura zvogëlohet. Për shembull, në një lartësi prej 5 km mbi nivelin e detit, ku presioni është 2 herë më i ulët se presioni atmosferik, pika e vlimit të ujit është 83 ° C, në kaldaja e motorëve me avull, ku presioni i avullit është 15 atm. (), temperatura e ujit është rreth 200˚С.
Lagështia e ajrit
Gjithmonë ka avull uji në ajër, kështu që mund të flasim për lagështinë e ajrit, e cila karakterizohet nga vlerat e mëposhtme:
1.Lagështia absoluteështë dendësia e avullit të ujit në ajër (ose presioni që krijon ky avull (.
Lagështia absolute nuk jep një ide për shkallën e ngopjes së ajrit me avujt e ujit. Sasia e njëjtë e avullit të ujit temperatura të ndryshme krijon një ndjenjë të ndryshme lagështie.
2.Lageshtia relativeështë raporti i densitetit (presionit) të avullit të ujit që përmbahet në ajër në një temperaturë të caktuar me densitetin (presionin) e avullit të ngopur në të njëjtën temperaturë : ose
është lagështia absolute në një temperaturë të caktuar; - dendësia, presioni i avullit të ngopur në të njëjtën temperaturë. Dendësia dhe presioni i avullit të ujit të ngopur në çdo temperaturë mund të gjenden në tabelë. Tabela tregon se sa më e lartë të jetë temperatura e ajrit, aq më e madhe duhet të jetë dendësia dhe presioni i avullit të ujit në ajër në mënyrë që ai të jetë i ngopur.
Duke ditur lagështinë relative, mund të kuptoni se sa përqind e avullit të ujit në ajër në një temperaturë të caktuar është larg ngopjes. Nëse avulli në ajër është i ngopur, atëherë . Nese nje , atëherë nuk ka avull të mjaftueshëm në ajër deri në një gjendje të ngopjes.
Fakti që avulli në ajër bëhet i ngopur gjykohet nga shfaqja e lagështirës në formën e mjegullës, vesës. Temperatura në të cilën avulli i ujit në ajër bëhet i ngopur quhet pika e vesës.
Avulli në ajër mund të bëhet i ngopur duke shtuar avull për shkak të avullimit shtesë të lëngut pa ndryshuar temperaturën e ajrit, ose duke ulur temperaturën e tij me sasinë e avullit në ajër.
Lagështia relative normale, më e favorshme për njerëzit, është 40 - 60%. Rëndësi e madhe ka njohuri për lagështinë në meteorologji për parashikimin e motit. Në thurjen, prodhimin e ëmbëlsirave, një lagështi e caktuar është e nevojshme për ecurinë normale të procesit. Ruajtja e veprave të artit dhe librave kërkon ruajtjen e lagështisë në nivelin e kërkuar.
Instrumentet e lagështirës:
1. Higrometër i kondensimit (ju lejon të përcaktoni pikën e vesës).
2. Higrometri i flokëve (bazuar në gjatësinë e flokëve pa yndyrë kundrejt lagështisë) mat lagështinë relative në përqindje.
3. Psikrometri përbëhet nga dy termometra të thatë dhe të lagësht. Llamba e lagësht mbështillet me një leckë të zhytur në ujë. Për shkak të avullimit nga pëlhura, temperatura e të njomurit është më e ulët se ajo e të thatit. Dallimi në leximet e termometrit varet nga lagështia e ajrit përreth: sa më i thatë të jetë ajri, aq më intensiv është avullimi nga pëlhura, aq më i madh është ndryshimi në leximet e termometrit dhe anasjelltas. Nëse lagështia e ajrit është 100%, atëherë leximet e termometrit janë të njëjta, d.m.th. diferenca në lexime është 0. Për të përcaktuar lagështinë duke përdorur një psikrometër, përdoret një tabelë psikometrike.
Shkrirja dhe kristalizimi
Kur shkrihet trup i fortë distanca midis grimcave që formojnë rrjetën kristalore rritet, dhe vetë rrjeta shkatërrohet. Procesi i shkrirjes kërkon energji. Kur një trup i ngurtë nxehet, energjia kinetike e molekulave vibruese rritet dhe, në përputhje me rrethanat, amplituda e lëkundjeve të tyre. Në një temperaturë të caktuar, të quajtur pika e shkrirjes, Rendi në renditjen e grimcave në kristale është i shqetësuar, kristalet humbasin formën e tyre. Substanca shkrihet nga gjendje e ngurtë në gjendje të lëngshme.
Gjatë kristalizimit ka një konvergjencë të molekulave që formojnë një rrjetë kristalore. Kristalizimi mund të ndodhë vetëm kur lëngu lëshon energji. Kur substanca e shkrirë ftohet, energjia mesatare kinetike dhe shpejtësia e molekulave zvogëlohen. Forcat tërheqëse mund t'i mbajnë grimcat pranë pozicionit të ekuilibrit. Në një temperaturë të caktuar, të quajtur temperatura e ngurtësimit (kristalizimit), të gjitha molekulat janë në një pozicion të ekuilibrit të qëndrueshëm, rregullimi i tyre bëhet i renditur - formohet një kristal.
Shkrirja e një trupi të ngurtë ndodh në të njëjtën temperaturë në të cilën substanca ngurtësohet.
Çdo substancë ka pikën e vet të shkrirjes. Për shembull, pikat e shkrirjes për heliumin janë -269,6˚С, për merkurin -38,9˚С, për bakrin 1083˚С.
Gjatë procesit të shkrirjes, temperatura mbetet konstante. Sasia e nxehtësisë e furnizuar nga jashtë shkon në shkatërrimin e rrjetës kristalore.
Gjatë procesit të tharjes, edhe pse nxehtësia hiqet, temperatura nuk ndryshon. Energjia e çliruar gjatë kristalizimit përdoret për të mbajtur një temperaturë konstante.
Derisa të shkrihet e gjithë substanca ose derisa të ngurtësohet e gjithë substanca, d.m.th. Për sa kohë që fazat e ngurta dhe të lëngëta të një lënde ekzistojnë së bashku, temperatura nuk ndryshon.
TV + lëng lëng + tv
, ku - sasia e nxehtësisë, - sasia e nxehtësisë e nevojshme për shkrirjen e substancës së çliruar gjatë kristalizimit të masës së lëndës.
- nxehtësia specifike e shkrirjes– sasia e nxehtësisë që nevojitet për të shkrirë një lëndë 1 kg në pikën e shkrirjes së saj.
Çfarë sasie nxehtësie harxhohet gjatë shkrirjes së një mase të caktuar të një lënde, e njëjta sasi nxehtësie lirohet gjatë kristalizimit të kësaj mase.
Gjithashtu i quajtur ngrohje specifike kristalizimi.
Në pikën e shkrirjes, energjia e brendshme e një lënde në gjendje të lëngshme është më e madhe energjia e brendshme masë e njëjtë e materies në gjendje të ngurtë.
Në një numër i madh Kur një substancë shkrihet, vëllimi i saj rritet dhe densiteti i saj zvogëlohet. Me ngurtësim, përkundrazi, vëllimi zvogëlohet dhe densiteti rritet. Për shembull, kristalet e ngurta të naftalinës zhyten në naftalinë të lëngët.
Disa substanca, për shembull, bismuti, akulli, galiumi, gize, etj., tkurren kur shkrihen dhe zgjerohen kur ngurtësohen. Këto devijime nga rregull i përgjithshëm shpjegohet me veçoritë strukturore të rrjetave kristalore. Prandaj, uji është më i dendur se akulli, akulli noton në ujë. Zgjerimi i ujit gjatë ngrirjes çon në shkatërrimin e shkëmbinjve.
Ndryshimi në vëllimin e metaleve gjatë shkrirjes dhe ngurtësimit është thelbësor në biznesin e shkritores.
Përvoja e tregon këtë Ndryshimi i presionit të jashtëm në të ngurta ndikon në pikën e shkrirjes së substancës. Për ato substanca që zgjerohen gjatë shkrirjes, rritja e presionit të jashtëm çon në rritjen e pikës së shkrirjes, sepse. pengon procesin e shkrirjes. Nëse substancat kompresohen gjatë shkrirjes, atëherë për to një rritje e presionit të jashtëm çon në uljen e temperaturës së shkrirjes, sepse ndihmon në procesin e shkrirjes. Vetëm një rritje shumë e madhe e presionit ndryshon dukshëm pikën e shkrirjes. Për shembull, për të ulur pikën e shkrirjes së akullit me 1˚C, presioni duhet të rritet me 130 atm. Pika e shkrirjes së një lënde në normale presioni atmosferik thirrur pika e shkrirjes së substancës.






