Një substancë që është në gjendje të ngurtë. Pra, presioni total është i barabartë. Presioni nën sipërfaqen e lakuar
Rendi me rreze të shkurtër (fluiditeti, moskompresibiliteti, kuazi-kristaliniteti, energjia potenciale e molekulave).
tensioni sipërfaqësor.
Presioni nën një sipërfaqe të lakuar.
Veting.
dukuritë kapilare.
Tensioni sipërfaqësor.
Energjia potenciale e një molekule brenda një lëngu është më e vogël se jashtë lëngut. Shtresa sipërfaqësore është në kushte të ndryshme. Për të transferuar molekulat në sipërfaqe, duhet të kapërcehet një pengesë e caktuar potenciale.
Është e pamundur të bësh një filxhan balte pa hyrë në një kategori tjetër - do të jetë vetëm një filxhan pa shkop. Kosterlitz dhe Tauuss konsideruan fenomene që ndodhin në shtresa shumë të holla, pothuajse dy-dimensionale. Haldane studioi gjithashtu vetitë e materies në formën e strukturave pothuajse njëdimensionale - zinxhirët e atomeve.
Për një kohë të gjatë, shkencëtarët besonin se edhe në temperaturën e biskotës zero absolute, luhatjet termike shkatërrojnë të gjithë rendin në një shtresë të hollë të materies. Dhe nëse nuk ka faza të renditura, nuk ka as kalime fazore. Topologjike tranzicioni fazor jo si kalimi i zakonshëm i akullit në ujë. Roli kryesor luhet nga vorbulla të vogla në një material të sheshtë. Në temperatura të ulëta, ato formojnë çifte të lidhura ngushtë. Kur temperatura rritet, ndodh një tranzicion fazor - vorbullat papritmas largohen nga njëra-tjetra dhe "lundrojnë" mbi materialin.
r- rrezja e veprimit molekular (sfera e veprimit molekular).
Forca që rezulton brenda lëngut është 0. Në sipërfaqen e gazit - veprimi i tij mund të neglizhohet. Forca që rezulton është zvogëluar. E gjithë shtresa e shtrirë pranë sipërfaqes së lëngut i nënshtrohet forcave të drejtuara normalisht në lëng. Shtresa sipërfaqësore ushtron presion mbi lëngun - presion molekular.
Ka gjetur aplikim, për shembull, në fizika atomike dhe mekanika statistikore. Kjo është vërtetuar edhe eksperimentalisht. David Thouless dhe Duncan Haldane prezantuan një inovative punë teorike, e cila hedh dyshime mbi teoritë aktuale se cilat materiale mund të përcjellin elektricitetin. Doli se këto ndryshime mund të marrin vetëm vlera të plota të përcaktuara rreptësisht pa gjendje të ndërmjetme. Topologjia doli të ishte çelësi i duhur për të shpjeguar këtë enigmë: elektronet në shtresën përcjellëse midis shtresave gjysmëpërçuese lëvizin lirshëm, duke krijuar të ashtuquajturin lëng kuantik topologjik.
Masa e lëngut, mbi të cilën nuk veprojnë forcat e jashtme, duhet të marrë një formë sferike. Nga të gjitha trupat gjeometrikë Një sferë ka sipërfaqen më të vogël për një vëllim të caktuar. Sipërfaqja e një lëngu është si një film i shtrirë. Për të shtrirë një film, zakonisht një forcë duhet të zbatohet në kufirin e tij  tangjente me sipërfaqen e lëngut, e quajtur forca e tensionit sipërfaqësor. Këto forca janë sa më të mëdha, aq më e gjatë është gjatësia e kufirit të filmit:
tangjente me sipërfaqen e lëngut, e quajtur forca e tensionit sipërfaqësor. Këto forca janë sa më të mëdha, aq më e gjatë është gjatësia e kufirit të filmit:
Ndryshimet në rezistencë janë kuantike - ato ndodhin gradualisht, jo vazhdimisht. Megjithatë, Haldane priste një efekt më të veçantë. Doli se vetitë e tyre janë krejtësisht të ndryshme në varësi të natyrës së magneteve atomike, të cilat ndahen në dy kategori - çift dhe tek. Siç tregoi Haldane, magnetet çift formojnë qarqe topologjike, ndërsa ato tek janë të palogjikshme.
Kërkimet e mëtejshme në këtë fushë çuan në zbulimin e gjendjeve topologjike që lidhen jo vetëm me zinxhirët ose shtresat e holla, por edhe me materialet konvencionale tre-dimensionale. Izoluesit topologjikë, superpërçuesit ose metalet janë ndër temat "e nxehta" të kërkimit.
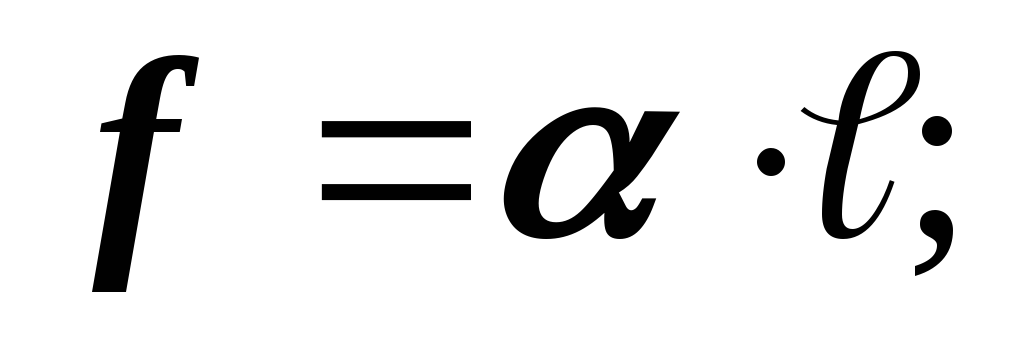
 - Koeficient tensioni sipërfaqësor. NGAT
- Koeficient tensioni sipërfaqësor. NGAT dhe
dhe  . NëT
. NëT  T Kreta.
T Kreta.
 0
. Le
0
. Le  - disa platforma.
- disa platforma.  - punoni për të krijuar forcën e sajF.
- punoni për të krijuar forcën e sajF.
Falë zbulimeve të laureatëve Çmimi Nobël Këtë vit, fizikantët i kanë kuptuar më mirë vetitë e materies. Progresi teorik mund të përkthehet në zhvillimin e materialeve të reja dhe përparim në ndërtimin e pajisjeve të tilla si kompjuterët kuantikë. Pjesë e një organizimi më të lartë të materies. Asnjë vëllim i vdekur, as forma e tij, nuk përfaqëson shtrirjen më të madhe, por ngjeshshmërinë më të madhe. Forcat tërheqëse midis grimcave të gazit janë të dobëta, kohezioni i degazuar midis grimcave është shumë i vogël, si dhe dendësia. Shpejtësia e difuzionit është në përpjesëtim të zhdrejtë me masën e grimcave dhe proporcionale me presionin e gazit.

pastaj

Kjo punë shkon për të rritur energjinë e filmit:


Ata quhen avull i ngopur. Varet nga vëllimi i gazit në të cilin ndodhet lëngu. Tensioni sipërfaqësor shfaqet në lëngje. Rrjedha është një veti specifike për lëngjet. Kimia e kristalit Faktorët që ndikojnë struktura kristalore- vëllimi i grimcave - polarizimi - natyra e forcave të ndërveprimit - elektromagnetike. Kur avullimi ndodh në të gjithë masën e lëngut, procesi quhet zierje. Presioni në të cilin një lëng bashkëjeton në një temperaturë të caktuar quhet presion i avullit.
Këto janë struktura kompakte. Shtresë pranë murit të një enë të palëvizshme. Kristalet kufizohen nga faqet dhe skajet që takohen në qoshe. Paketim kristali. Grimcat janë rregulluar në mënyrë që ato të mund të zënë plotësisht hapësirën. Për të ndërtuar një rrjet, konsideroni atomet ose jonet e përbëra si grimca. Sasia e nxehtësisë e nevojshme për të transformuar një mol avulli të lëngshëm quhet nxehtësia molare e avullimit. të tjerat rrjedhin me shpejtësi në rritje derisa të arrihet shpejtësia maksimale. që nënkupton numrin maksimal të grimcave të vendosura në hapësirën më të vogël të mundshme.
Energjia e tensionit sipërfaqësor.
Energjisë - është një pjesë energjia e brendshme film, i cili shndërrohet në punë gjatë një procesi izotermik.
Energji e lirë
Tensioni sipërfaqësor shpjegon: formimin e pikave:

Leva është e orientuar nga pjesa e brendshme e lëngut në brendësi dhe tenton të zvogëlojë sipërfaqen e lëngut. Viskoziteti i një lëngu shprehet me një koeficient viskoziteti që përfaqëson forcën e fërkimit midis dy shtresave paralele të lëngut të zhvendosjes relative në një bllok sipërfaqësor. Procesi me të cilin një lëng avullon quhet avullim. Një lëng tjetër që shfaqet në lëngje është rezistenca e brendshme, e cila përfaqëson forcën e deaerimit. molekulat e gazta në një distancë më të vogël se rrezja e veprimit të forcave ndërmolekulare.
Për një pikë:

Presioni nën sipërfaqen e lakuar
Konsideroni sipërfaqen e lëngut, bazuar në një kontur të sheshtë.

Nëse sipërfaqja e lëngut nuk është e sheshtë, atëherë tendenca e tij për t'u tkurrur do të çojë në shtimin e presionit në raport me lëngun e sheshtë.
Kapilariteti është procesi i rritjes së lëngjeve në tuba të ngushtë për të formuar sipërfaqe të lakuara të quajtura meniskur. Zhvendosja e lëngut kundërshton stabilitetin dhe viskozitetin e brendshëm të lëngjeve. Në varësi të ngjitjes së lëngut në muret e enës, formohen shenja konkave dhe konvekse. Tërheqje të ngurta - tërheqëse midis përbërësve - rezistencë ndaj nxehtësisë dhe deformimit termik. Përkufizimi në kristal - karakterizohet nga një shpërndarje e renditur e grimcave të grimcave amorfe - një shpërndarje e rregullsisë së grimcave.

Në rastin e një sipërfaqe konvekse, ky presion është pozitiv, në rastin e një sipërfaqeje konkave, është negativ.


Llogaritni
 për një sipërfaqe të lëngshme sferike.
për një sipërfaqe të lëngshme sferike.

Për shkak të tensionit sipërfaqësor, të dy hemisferat tërhiqen.


Këto forca shtypin të dy hemisferat në sipërfaqe dhe ato shkaktojnë presion shtesë:

Lakimi i sipërfaqes:
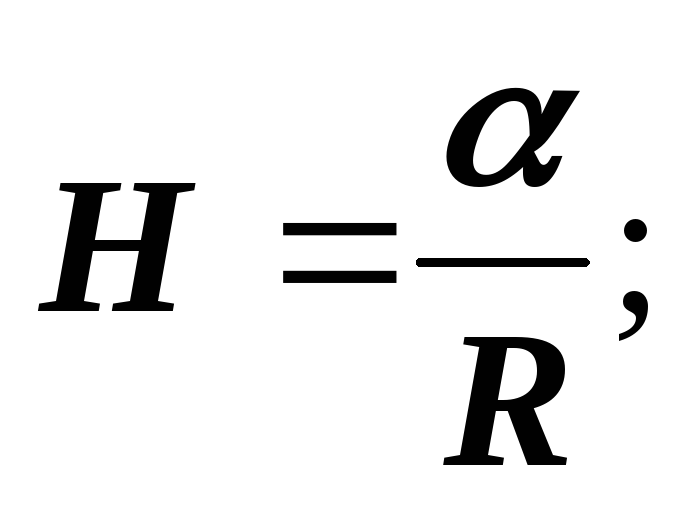
Në gjeometri, vërtetohet se gjysma e rrezeve reciproke të lakimit të çdo çifti seksionesh reciproke pingule ka të njëjtën vlerë H :
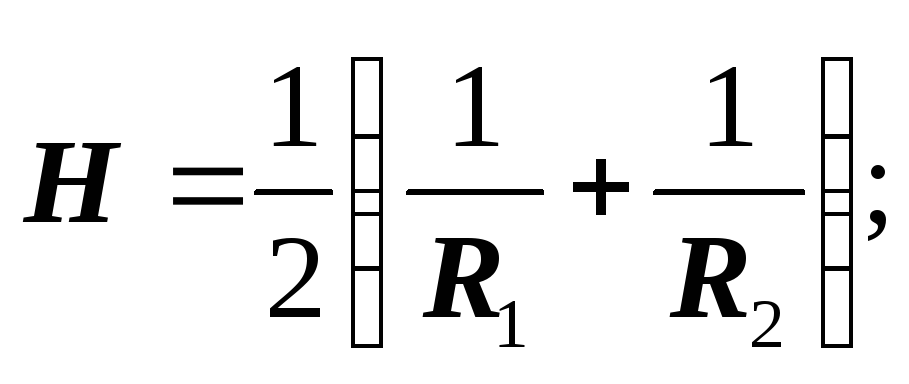
Për sferën: R 1 = R 2 = R :

Laplace vërtetoi se formulat janë të vlefshme për një sipërfaqe të çdo forme, nëse H nënkupton lakimin mesatar të sipërfaqes në pikën në të cilën përcaktohet presioni shtesë.
Lakim mesatar

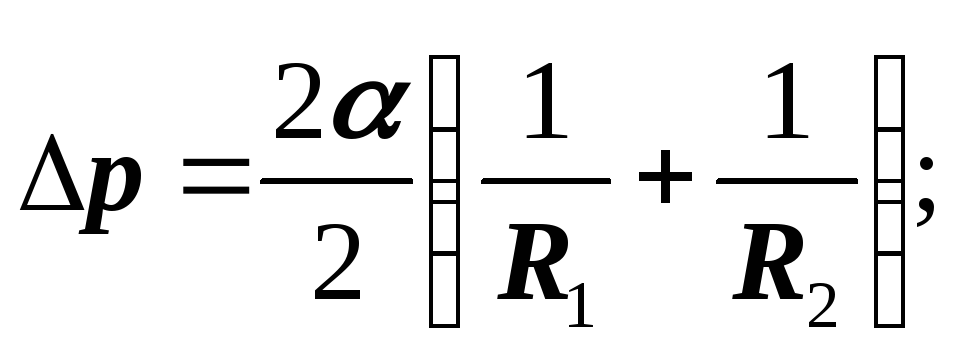
Formula Laplace
Presioni shtesë ndryshon nivelin e lëngut në tubat e ngushtë (kapilarët), i cili nganjëherë quhet presion kapilar.
Lundrimi i trupave të vegjël në sipërfaqe shpjegohet me presionin Laplace.
duke u lagur
Kur merren parasysh dukuritë në kufirin lëng-ngurtë, është e nevojshme të merret parasysh energjia totale sipërfaqësore e dy substancave.
Nëse kufizohen tre substanca: të lëngshme, të ngurta dhe të gazta. Atëherë i gjithë konfigurimi korrespondon energji totale minimale (sipërfaqja, në fushën e lëngshme).
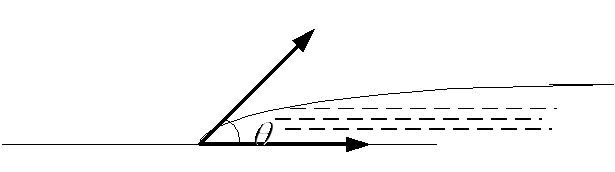
Këndi midis sipërfaqes së një trupi të ngurtë dhe tangjentes me lëngun
 - këndi i skajit.
- këndi i skajit.
Nese nje
 më pak se π/2 lëngu lag trupin.
më pak se π/2 lëngu lag trupin.
Nese nje
 më shumë se π/2 lëngu nuk e lag trupin.
më shumë se π/2 lëngu nuk e lag trupin.
Në
 zero njomje totale.
zero njomje totale.
Në
 i plotë pa lagështirë.
i plotë pa lagështirë.
Mos lagja mund të çojë në fenomene kurioze: një gjilpërë nuk zhytet në yndyrë. Në mënyrë të ngjashme, ju mund të mbani ujë në një sitë nëse sita nuk laget nga uji (mbuloni fijet e sitës me parafinë), nëse nuk ka shumë ujë.
Dukuritë kapilare
Ekzistenca e këndit të kontaktit çon në lakimin e sipërfaqes së lëngshme pranë mureve të enës. Në një tub të ngushtë kapilar, sipërfaqja rezulton të jetë e lakuar.
Lëngu lag sipërfaqen:
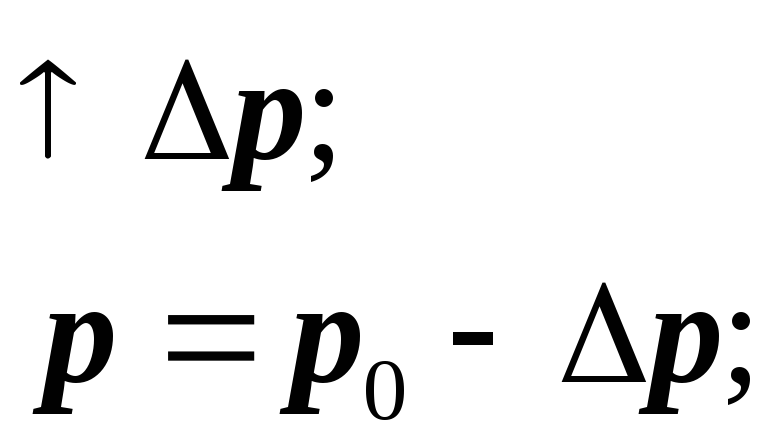
Nëse lëngu nuk laget:

Nëse sipërfaqja e lëngut është e lakuar, atëherë forcat e tensionit sipërfaqësor krijojnë presion shtesë mbi lëngun:
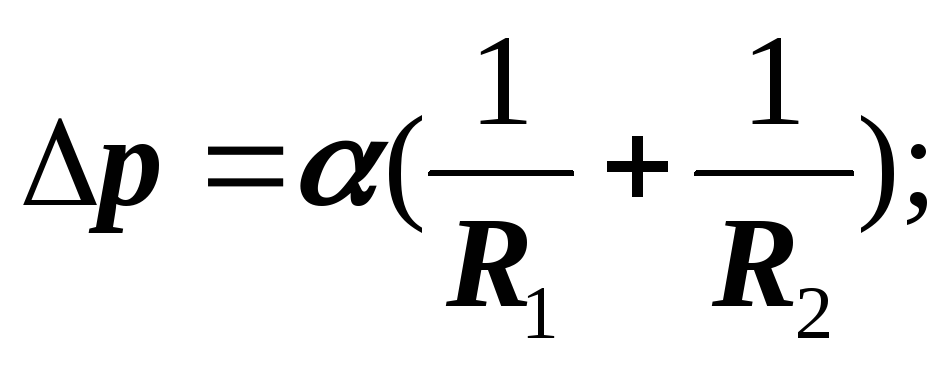
Pra, presioni total është:

 kapilar, presion laplasian.
kapilar, presion laplasian.
Nëse kapilari zhytet me një skaj në një lëng, atëherë kur kapilari laget, niveli i lëngut do të jetë më i lartë se niveli në enë, dhe kur nuk laget, do të jetë më i ulët.

Ndryshimi i lartësisë së nivelit në tubat e ngushtë - kapilariteti.

Nëse kapilarët janë seksion i rrumbullakët, pastaj:
 dhe
dhe


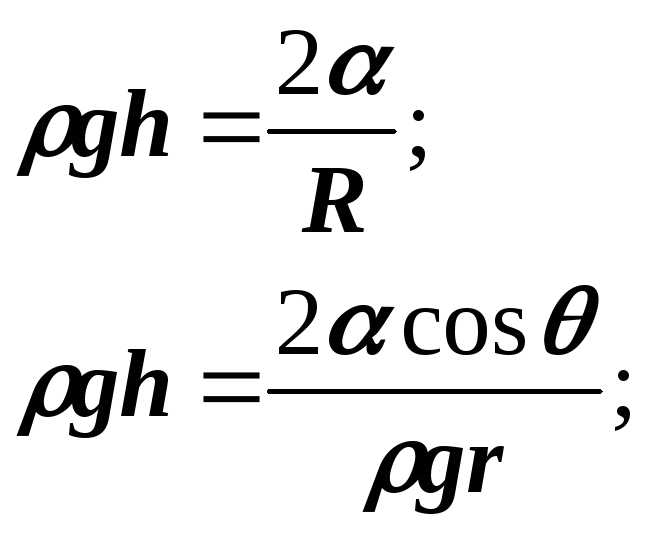

Nëse kapilari është i vogël, atëherë me lagështi të plotë
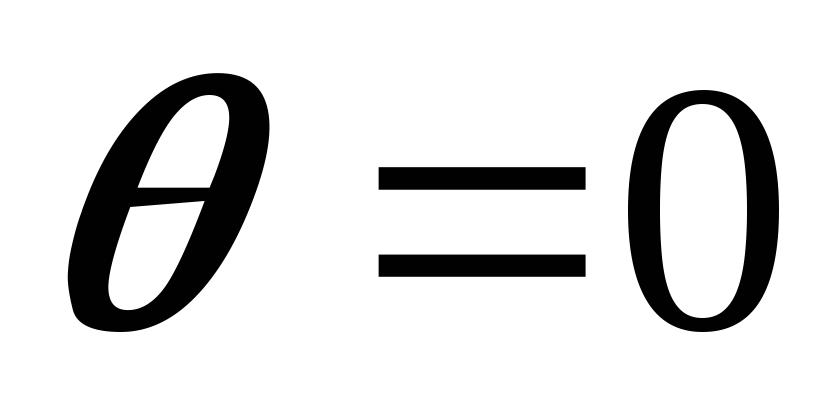 :
:
R = r

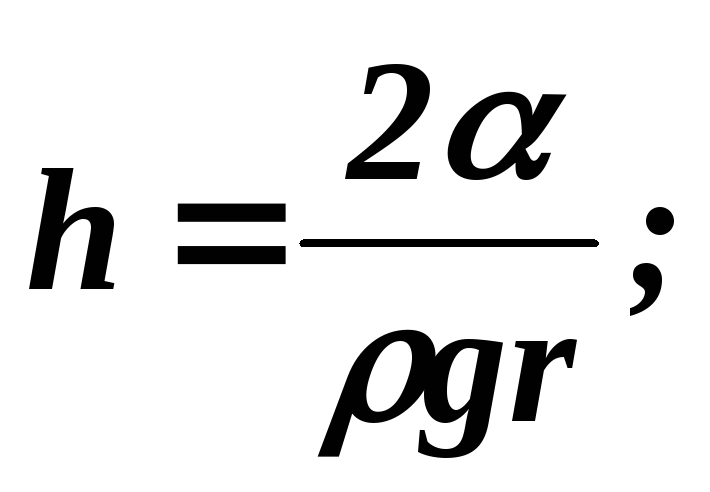
Liquid - gjendja e grumbullimit të lëndës, e ndërmjetme midis të ngurtë dhe të gaztë. Lëngjet kanë pronësinë e natyrshme të trupave të ngurtë - të ruajnë vëllimin e tyre, të formojnë një sipërfaqe, transparencë, forcë në tërheqje. Gazrat: marrin formën e një ene, vazhdimisht shndërrohen në gaz pa kërcim.
Një numër karakteristikash të veçanta vetëm për të: Veçori - rrjedhshmëri. Lëngjet janë pothuajse të pakompresueshme. Testimi i lëngjeve me rrezet x tregoi se strukturën e brendshme kanë shumë të përbashkëta me strukturën e trupave të ngurtë.
Në rregullimin e grimcave të lëngshme, ekziston porosi me rreze të shkurtër .
Vetia kryesore e një lëngu që e dallon atë nga të tjerët gjendjet agregate, është aftësia për të ndryshuar në mënyrë të pakufizuar formën nën veprimin e sforcimeve mekanike tangjenciale, qoftë edhe në mënyrë arbitrare të vogla, duke ruajtur praktikisht vëllimin. Substanca në gjendje e lëngshme ekziston në një diapazon të caktuar temperaturash, nën të cilin kalon në gjendje të ngurtë (kristalizimi ose shndërrimi në gjendje të ngurtë amorfe - qelqi), sipër - në gjendje të gaztë (ndodh avullimi). Kufijtë e këtij intervali varen nga presioni.
3.1 Vetitë fizike të lëngjeve:
ü Fluiditeti(Vetësia themelore.Ndryshe nga plastika të ngurta, lëngu nuk ka pikë rendimenti: mjafton të aplikoni një të vogël në mënyrë arbitrare forca e jashtme për të lënë lëngun të rrjedhë.
ü Ruajtja e vëllimit. Një nga vetitë karakteristike të një lëngu është se ai ka një vëllim të caktuar (me konstante kushtet e jashtme). Një lëng është jashtëzakonisht i vështirë për t'u ngjeshur mekanikisht, sepse, ndryshe nga një gaz, ka shumë pak hapësirë midis molekulave. hapesire e lire. Lëngjet zakonisht rriten në vëllim (zgjerohen) kur nxehen dhe ulen në vëllim (kontraktohen) kur ftohen.
ü Viskoziteti. Përveç kësaj, lëngjet (si gazrat) karakterizohen nga viskoziteti. Përkufizohet si aftësia për t'i rezistuar lëvizjes së njërës prej pjesëve në lidhje me tjetrën - domethënë si fërkim i brendshëm.Kur shtresat ngjitur të një lëngu lëvizin në raport me njëra-tjetrën, në mënyrë të pashmangshme ndodh një përplasje e molekulave përveç asaj që shkaktohet. ndaj lëvizjes termike. Lëngu në enë, i vënë në lëvizje dhe i lënë në vetvete, gradualisht do të ndalet, por temperatura e tij do të rritet.
ü Formimi i lirë i sipërfaqes dhe tensioni i sipërfaqes.Për shkak të ruajtjes së vëllimit, lëngu është në gjendje të formojë një sipërfaqe të lirë. Një sipërfaqe e tillë është sipërfaqja e ndarjes së fazës së një lënde të caktuar: nga njëra anë është një fazë e lëngshme, nga ana tjetër - një fazë e gaztë (avull) Nëse fazat e lëngëta dhe të gazta të së njëjtës substancë janë në kontakt, lindin forca që priren të zvogëlojnë forcat e tensionit të sipërfaqes së ndërfaqes. Ndërfaqja sillet si një membranë elastike që tenton të tkurret.
ü Avullimi dhe kondensimi
ü Duke zier
ü duke u lagur - fenomen sipërfaqësor, që ndodh kur një lëng kontakton një sipërfaqe të ngurtë në prani të avullit, domethënë në ndërfaqet e tre fazave.
ü Përzierje- aftësia e lëngjeve për t'u tretur në njëri-tjetrin. Një shembull i lëngjeve të përziera: uji dhe alkooli etilik, një shembull i lëngjeve të papërziershme: uji dhe vaji i lëngshëm.
ü Difuzioni. Kur dy lëngje të përzier janë në një enë, si rezultat i lëvizjes termike, molekulat fillojnë të kalojnë gradualisht përmes ndërfaqes, dhe kështu lëngjet gradualisht përzihen. Ky fenomen quhet difuzion (ndodh edhe në substanca në gjendje të tjera grumbullimi).
ü Mbinxehje dhe hipotermi. Një lëng mund të nxehet mbi pikën e vlimit në mënyrë të tillë që të mos ndodhë vlimi. Kjo kërkon ngrohje uniforme, pa dallime të konsiderueshme të temperaturës brenda volumit dhe pa ndikime mekanike si dridhjet. Nëse në lëng i mbinxehur hedh diçka, ajo vlon në çast. Uji i mbinxehur është i lehtë për t'u marrë në një furrë me mikrovalë.Nënftohja është ftohja e një lëngu nën pikën e ngrirjes pa u kthyer në një gjendje të ngurtë grumbullimi.






