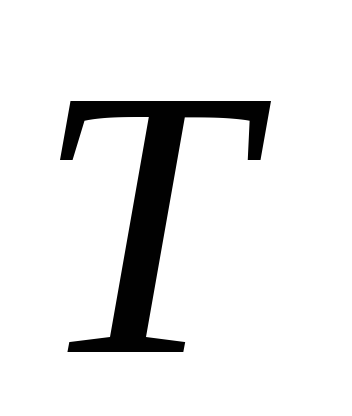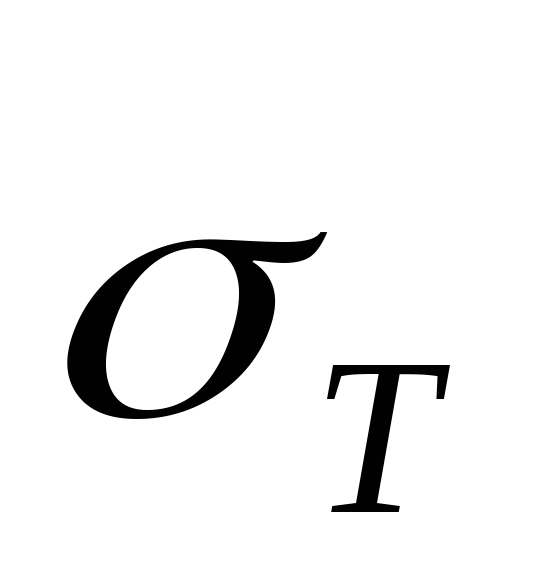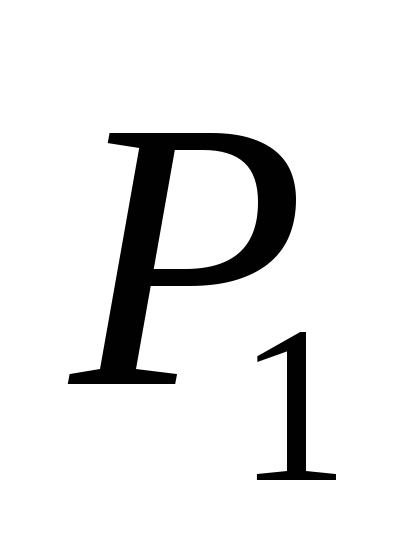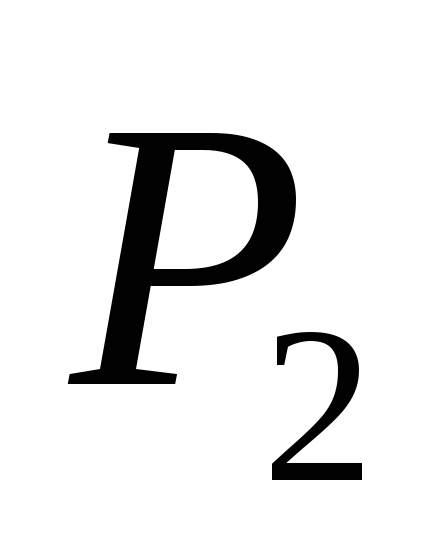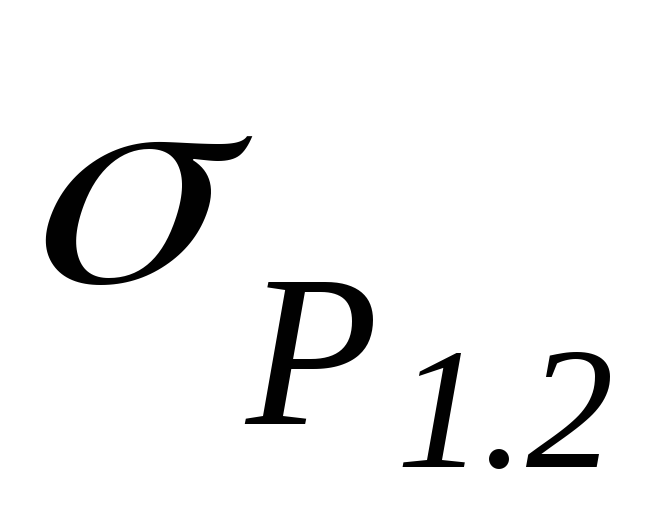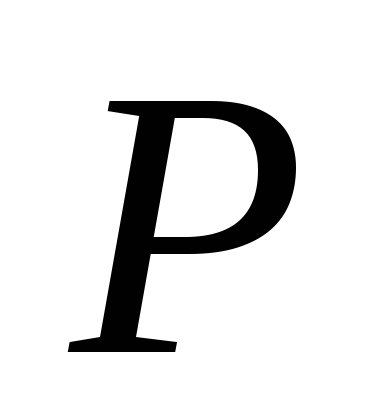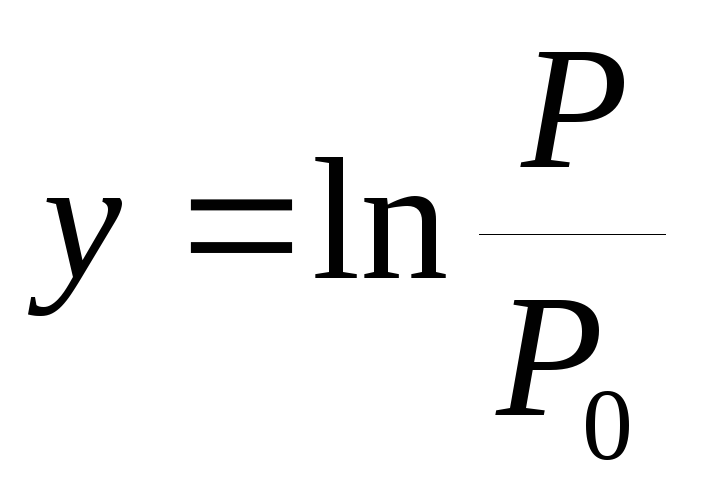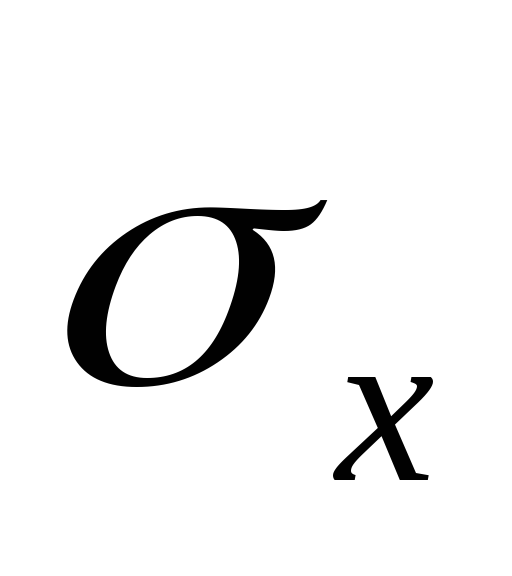Su buharı yoğuşmasının özgül ısı kapasitesi. Buharlaşmanın özgül ısısının belirlenmesi
Laboratuvar çalışması №4.
Bir sıvının buharlaşma ısısının belirlenmesi
1. Kısa teori
Buharlaşma, bir maddenin sıvı halden gaz hale geçmesidir. Buharlaşma sırasında, moleküller sıvının yüzeyinden uçar ve üzerinde buhar oluşturur. Sadece en hızlı moleküller, sıvının yüzey tabakasında hareket eden çekici kuvvetlerin üstesinden gelebildikleri için, sıvıdan çevreleyen alana uçabilir. Hızlı moleküllerin ayrılması sonucunda sıvı soğutulur. Sıcaklığını sabit tutmak için bir ısı kaynağı gereklidir.
Bir maddenin başka bir maddeye dönüşmesi için verilmesi gereken ısı miktarı sıvı hal gaz halinde Sabit sıcaklık ve sabit basınç, buharlaşma ısısı (veya buharlaşma ısısı) olarak adlandırılır.
Sıvıların buharlaşma ısısı doğrudan bir kalorimetre ile ölçülebilir. Ancak bu yöntem, küçük hale getirilmesi zor olan kontrolsüz ısı kaybı nedeniyle doğru sonuçlar vermemektedir. Bu yazıda, buharlaşma ısısını belirlemek için Clausius-Clapeyron denklemine dayanan dolaylı bir yöntem kullanıyoruz:
 . (1)
. (1)
Burada P
sıcaklıktaki sıvının doymuş buhar basıncıdır. T
,T sıvı ve buharın mutlak sıcaklığı, 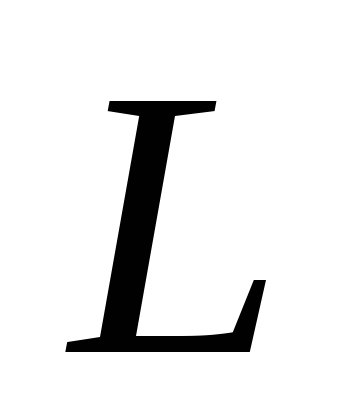 - sıvının özgül buharlaşma ısısı,
- sıvının özgül buharlaşma ısısı, 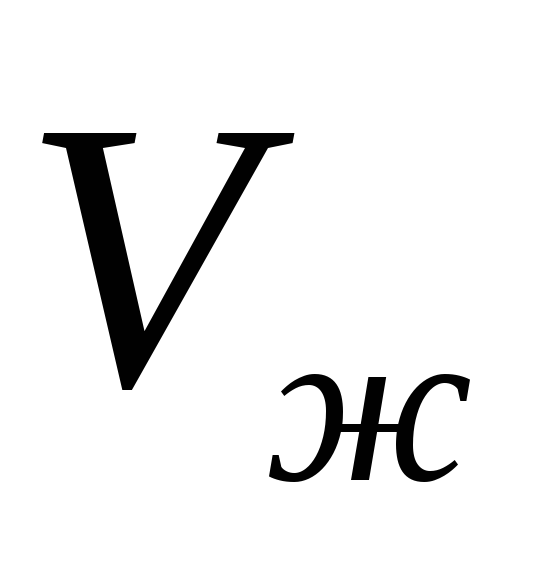 - özgül sıvı hacmi,
- özgül sıvı hacmi, 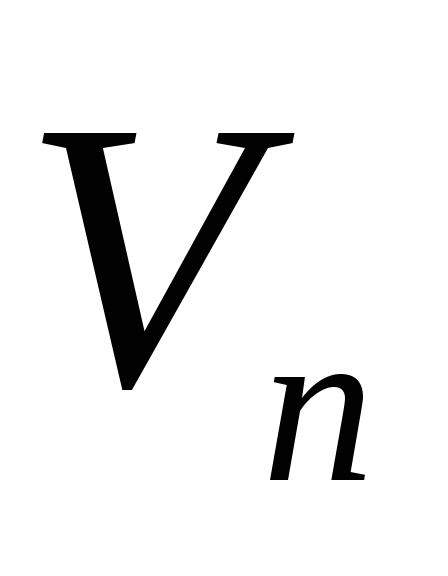 - belirli buhar hacmi.
- belirli buhar hacmi.
Özgül buharlaşma ısısının bağımlılığı biliniyorsa 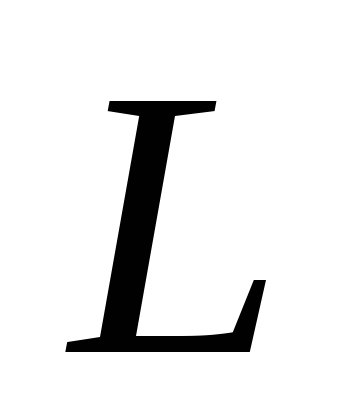 ve belirli hacimler
ve belirli hacimler 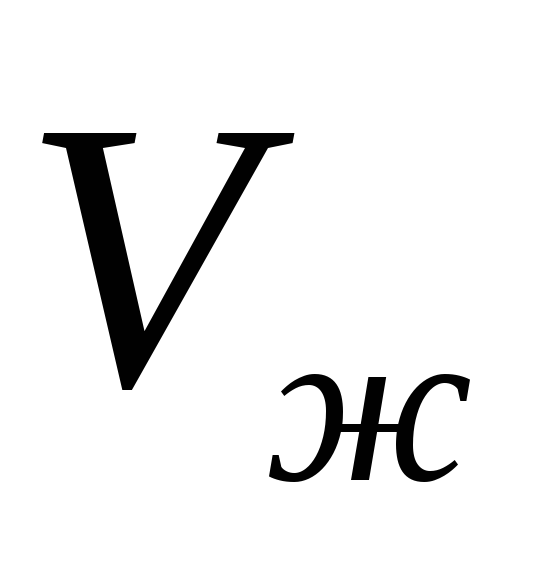 ve
ve 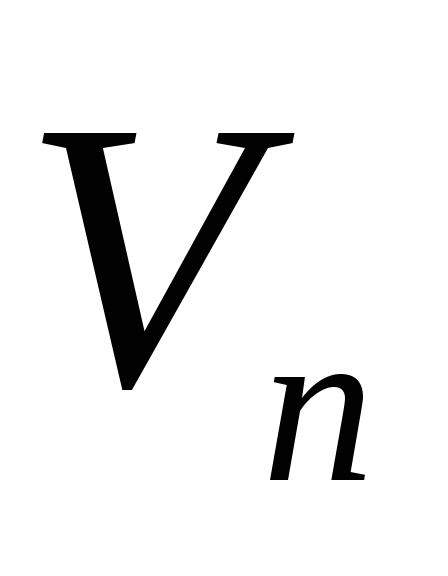 sonra denklem (1) entegre edilebilir ve doymuş buhar basıncının sıcaklığa bağımlılığı açıkça bulunabilir. En kaba yaklaşımda, değerin
sonra denklem (1) entegre edilebilir ve doymuş buhar basıncının sıcaklığa bağımlılığı açıkça bulunabilir. En kaba yaklaşımda, değerin 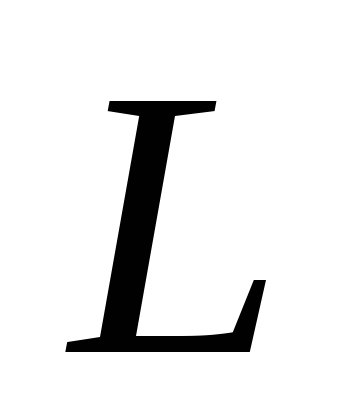 sıcaklığa bağlı değildir ve özgül buhar hacmine kıyasla sıvının özgül hacmi ihmal edilebilir. Ek olarak, ideal gaz hal denkleminin (Mendeleev-Clapeyron denklemi) ifade ettiğimiz buhara uygulanabilir olduğunu varsayabiliriz. belirli hacimçift:
sıcaklığa bağlı değildir ve özgül buhar hacmine kıyasla sıvının özgül hacmi ihmal edilebilir. Ek olarak, ideal gaz hal denkleminin (Mendeleev-Clapeyron denklemi) ifade ettiğimiz buhara uygulanabilir olduğunu varsayabiliriz. belirli hacimçift: 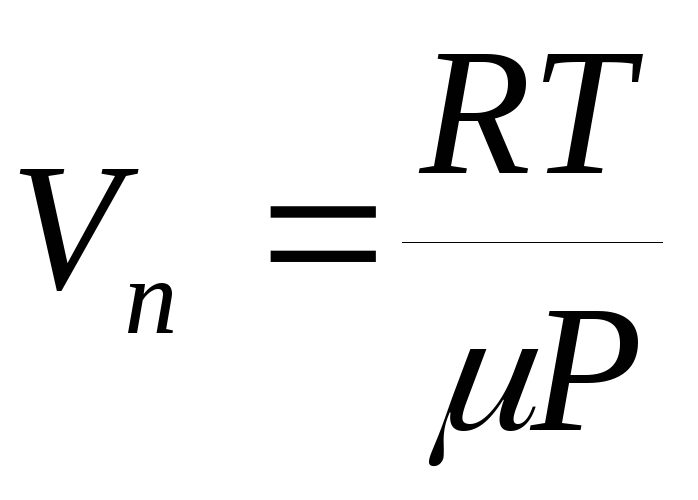 .
.
Kabul edilen yaklaşımda, denklem (1) bir diferansiyel denkleme dönüşecektir:
 ,
,
hangisini entegre edersek, şunu elde ederiz:
 , (2)
, (2)
nerede 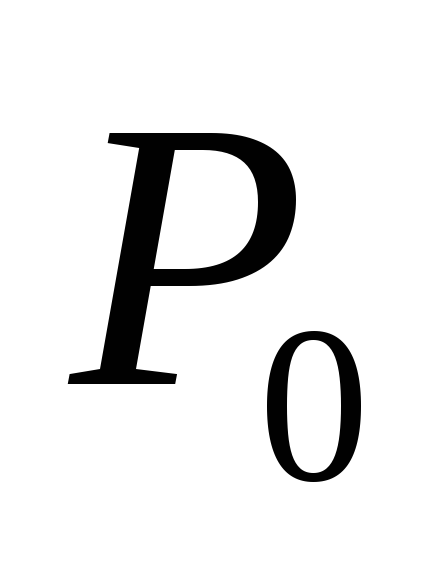
 .
.
İlişki (2), doymuş buhar basıncının sıcaklığa bağımlılığını bilerek, özgül buharlaşma ısısını belirlemeyi mümkün kılar. Mevcut laboratuvar çalışması, suyun özgül buharlaşma ısısının belirlenmesine ayrılmıştır.
2. Deneysel kurulum. deneysel teknik
Deney, şekilde şematik olarak gösterilen kurulum üzerinde gerçekleştirilir. Kurulum, suyla doldurulmuş bir termostat, ısıtma elemanları, bir soğutma sistemi (şekilde gösterilmemiştir), test gazlı iki şişe ve ölçüm cihazlarından oluşur.
H  ısıtma elemanları H sistemdeki sıcaklığı arttırmaya yarar. Sistemin eşit şekilde ısıtılması için su, kompresör tarafından sağlanan hava ile sürekli olarak karıştırılır. İle. Isıtma elemanlarının ve kompresörün açılması ve kapatılması kontrol paneli kullanılarak gerçekleştirilir. PU. Vinçleri çalıştırmadan önce İle 1
ve İle 2
aç, sonra kapat. Bu, ilk anda şişelerdeki basıncın atmosfer basıncına eşit olması için gereklidir. Termometre sıcaklığı ölçer T kuru ve nemli hava içeren şişelerin daldırıldığı su. Kurulum parametreleri, suyun yavaş ısınması ve şişelerdeki gazın sistemdeki su ile aynı sıcaklığa ısınması için zamana sahip olacak şekildedir. Basınç ölçerler M 1
ve M 2
sırasıyla kuru ve nemli hava ile şişelerdeki aşırı basıncı gösterin.
ısıtma elemanları H sistemdeki sıcaklığı arttırmaya yarar. Sistemin eşit şekilde ısıtılması için su, kompresör tarafından sağlanan hava ile sürekli olarak karıştırılır. İle. Isıtma elemanlarının ve kompresörün açılması ve kapatılması kontrol paneli kullanılarak gerçekleştirilir. PU. Vinçleri çalıştırmadan önce İle 1
ve İle 2
aç, sonra kapat. Bu, ilk anda şişelerdeki basıncın atmosfer basıncına eşit olması için gereklidir. Termometre sıcaklığı ölçer T kuru ve nemli hava içeren şişelerin daldırıldığı su. Kurulum parametreleri, suyun yavaş ısınması ve şişelerdeki gazın sistemdeki su ile aynı sıcaklığa ısınması için zamana sahip olacak şekildedir. Basınç ölçerler M 1
ve M 2
sırasıyla kuru ve nemli hava ile şişelerdeki aşırı basıncı gösterin.
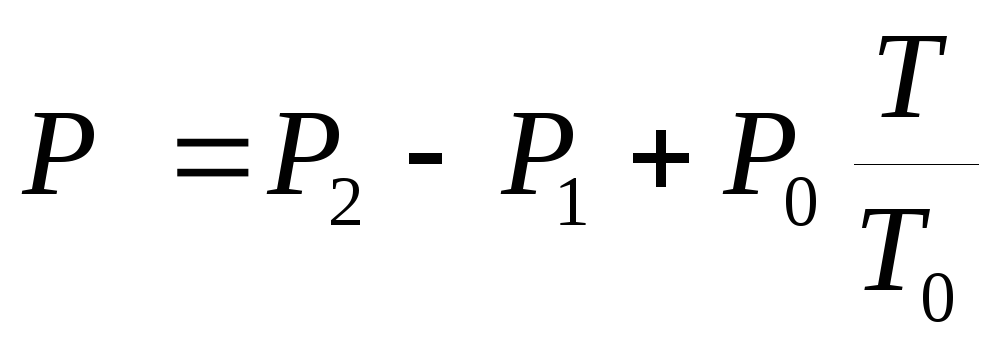 , (3)
, (3)
nerede P 1
ve P 2
- manometre göstergeleri M 1
ve M 2
sırasıyla, T– sistemdeki sıcaklık 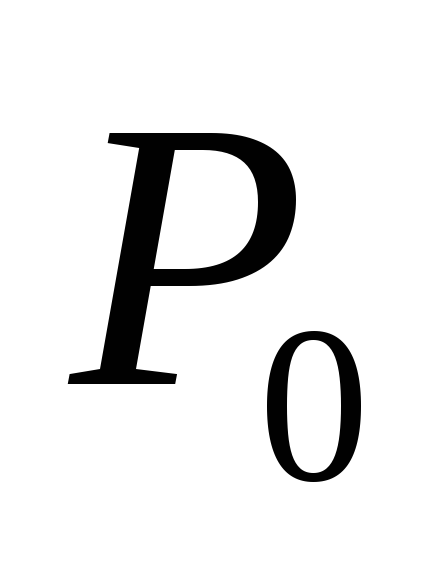 başlangıç sıcaklığında doymuş buhar basıncı
başlangıç sıcaklığında doymuş buhar basıncı  (bu değer bilindiği kabul edilir).
(bu değer bilindiği kabul edilir).
Deneyime göre, bir bağımlılık grafiği oluşturulur  itibaren
itibaren 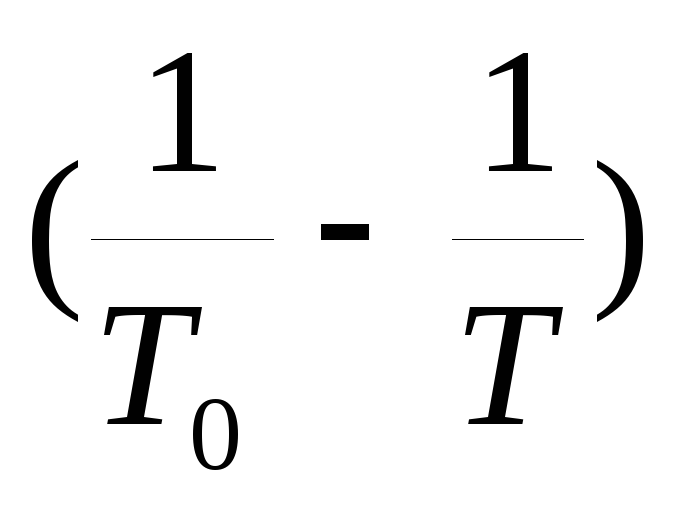 .
.
Denklem (2)'ye göre, deney noktaları orijinden geçen düz bir çizgi üzerinde uzanmalıdır. Grafiğe göre bu doğrunun eğimi belirlenir.  ve suyun özgül buharlaşma ısısı bulunur.
ve suyun özgül buharlaşma ısısı bulunur.
Denklem (2) şunu gösterir:  ve dolayısıyla:
ve dolayısıyla: 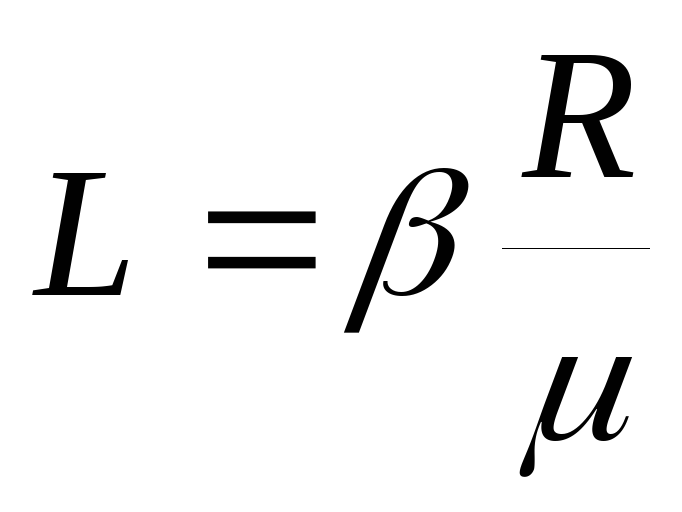 .
.
3. Ölçümler. Ölçüm sonuçlarının işlenmesi
1. Kurulum cihazı ve elemanları hakkında bilgi edinin.
2. Basınç göstergelerinin bağımlılığını ortadan kaldırın P 1 ve P 2 ve her sıcaklık için doygunluk buhar basıncını hesaplayın P formül (3) kullanılarak. Deneyiminize göre bir tablo yapın:
|
| ||||||
|
| ||||||
|
| ||||||
|
| ||||||
|
| ||||||
|
| ||||||
|
|
3. Doygunluk buhar basıncını sıcaklığa karşı çizin P(T) ve basınç oranlarının logaritmasının bir grafiği y=  değerden x =
değerden x =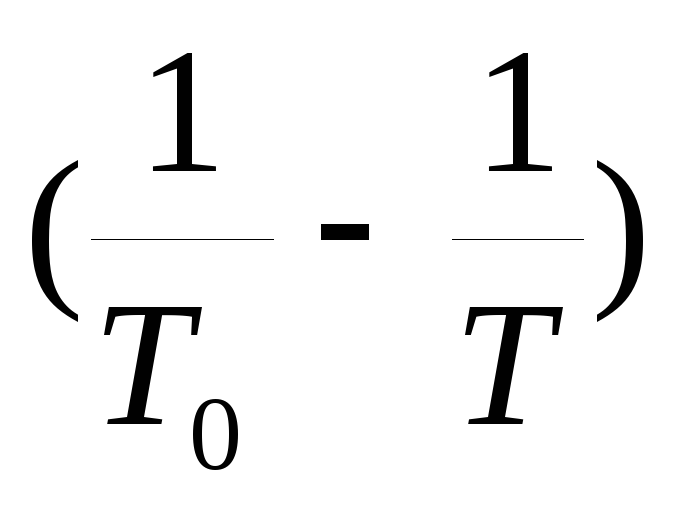 .
.
Son grafiği oluşturmak için tabloyu doldurmanız gerekir:
|
| ||||||
|
| ||||||
|
| ||||||
|
|
İle açısal katsayı grafik buharlaşma ısısını belirler L ve sonucun hatasını tahmin edin.
4. Sonucu tablo değeriyle karşılaştırın.
4. Güvenlik soruları
Bir sıvının özgül buharlaşma ısısına ne denir?
Clausius-Clapeyron denklemini türetiniz.
(2) ilişkisini türetirken hangi varsayımlar yapıldı? Bu oranı türet.
azeotropik- termodinamik denge koşulları altında sıvı ve gaz fazları aynı bileşime sahip olan bir sıvı karışımını belirtmek için kullanılan bir terim. Karışımın kaynama noktası sabittir.
azeotropi noktası- bir sıvı karışımının kaynadığı ve sıvı karışımla aynı bileşimdeki buharın oluştuğu sıcaklık.
Vakum(veya nadir gaz) - basıncının atmosferik basınçtan önemli ölçüde düşük olduğu gazlı bir ortamın durumu.
balgam söktürücü - buharın kısmi yoğunlaşması için ısı eşanjörü. Damıtma kolonlarında kolonun kontak elemanlarının sulanması için gerekli olan geri akışın oluşturulmasına hizmet eder.
buharlaşma Buharlaşma, bir sıvının serbest yüzeyinden meydana gelir. Aynı sıcaklıktaki bir sıvının molekülleri farklı hızlarda hareket eder. Yeterince hızlı bir molekül sıvının yüzeyindeyse, komşu moleküllerin çekimini yenebilir ve sıvıdan dışarı fırlayabilir. Sıvının yüzeyinden kaçan moleküller buhar oluşturur. Buharlaşma ile eş zamanlı olarak, moleküller buhardan sıvıya aktarılır. Buharın bir sıvıya dönüşmesi olgusuna yoğuşma denir.
Sıvıya dışarıdan enerji akışı yoksa, buharlaşan sıvı soğutulur. Buharın yoğunlaşmasına enerji salınımı eşlik eder.
Bir sıvının buharlaşma hızı, sıvının türüne ve sıcaklığına, yüzey alanına, sıvının yüzeyi üzerindeki hava kütlelerinin (rüzgar) hareketine bağlıdır.
Kaynamak- sıvının tüm hacminde meydana gelen buharlaşma süreci. Kaynama sırasında, sıvı içinde çözünmüş hava kabarcıkları halinde buharlaşma meydana gelir. Kabarcıklarda artan basınçla yüzeye çıkar ve patlar. Bu kabarcıklar sadece havayı değil, aynı zamanda bu kabarcıkların içindeki sıvı buharlaştığı için su buharını da içerir.
Kaynama Merkezi Oluşumu- sıvı ile temas halindeki ısıtılmış yüzeyde buhar kabarcıklarının görünümü ve büyümesi.
Kaynama noktası normal basınçta kaynama noktasıdır.
buharlaşma - faz geçişi birinci tür; bir maddenin bir sıvıdan geçişi veya katı hal gaz durumuna geçer.
Kapalı bir hacimde, buharlaşma, sıvı veya katının üzerindeki boşluk, belirli bir sıcaklıkta (doyma basıncı) denge basıncına sahip buharla dolana kadar devam eder. Buharlaşma ısısının büyük bir kısmı partiküller arasındaki bağları kırmak için harcanır, bir kısmı da buharın genleşmesi sırasında yapılan işe gider.
kaynama sıcaklığı sıvının kaynadığı sıcaklıktır.
Kaynama sıcaklığı:
Akışkanın doğasına ve dış basınca bağlıdır; ve
arasında yer alır üçlü nokta ve kritik sıcaklık.
Sabit basınçta her sıvının kendi kaynama noktası vardır.
Atmosfer basıncının artmasıyla sıvının kaynama noktası yükselir ve özgül buharlaşma ısısı düşer.
Buharlaşma ısısı- sabit sıcaklıkta sıvı halden gaz hale geçmek için bir maddeye verilmesi gereken ısı miktarı.
Buharlaşma ısısı- Sabit basınç ve sıcaklıktaki bir maddeyi sıvı halden gaz haline geçirmek için verilmesi gereken ısı miktarı.
SI'de buharlaşma ısısı J cinsinden ölçülür.
Özgül buharlaşma ısısı- sabit sıcaklıkta sıvı halden gaz hale geçmek için 1 kg maddeye verilmesi gereken ısı miktarı.
Buharlaşmanın özgül ısısı J/kg olarak ölçülür.
Özgül buharlaşma ısısı 1 kg sıvıyı sabit sıcaklıkta buhara dönüştürmek için gereken ısı miktarıdır. Bu değer L harfi veya r harfi ile gösterilir ve kilogram başına joule (J / kg) olarak ifade edilir.
Artan sıcaklıkla, değer özısı buharlaşma azalır.
Özgül buharlaşma ısısı - bir maddenin birim kütlesi başına hesaplanan buharlaşma ısısı.
Buharlaşmanın özgül ısısı artan sıcaklıkla azalır ve kritik sıcaklıkta sıfır olur.
Buharlaşmanın özgül ısısı, kaynama sıcaklığında alınan bir kilogram sıvıyı bu sıcaklıkta tamamen buhara dönüştürmek için ne kadar enerji verilmesi gerektiğini gösterir (yoğunlaşma için: bir kilogram buhar tarafından ne kadar enerji açığa çıkar? yoğunlaşma sıcaklığı, tamamen sıvıya dönüşüyor).
Aynı basınçta aynı maddenin kaynama noktası ve yoğuşma noktası aynıdır.
Buhar yoğunlaşması - buhar moleküllerinin bir sıvıya geri döndürülmesi işlemine buhar yoğuşması denir.
kondansatör- soğutucuya ısı verirken buharların yoğunlaştığı bir ısı eşanjörü.
su kondansatörü Soğutma sıvısı olarak su kullanan bir kondansatör.
BORU İÇİ KONDENSER BORUSU- buharın çoğunlukla dairesel boşlukta dolaştığı ve soğutucunun merkezi boruda olduğu iki eş merkezli borudan oluşan bir kondansatör.
Isı değişimi veya ısı transferi- geçiş süreci içsel enerji iş yapmadan termal temas sonucu bir vücuttan diğerine.
Termal denge- makroskopik parametrelerinin zamanla değişmediği sistemin durumu. Termal dengede hacim ve basınç değişmez, ısı değişimi olmaz, sıvılar ve gazlar, sıvılar ve sıvılar arasında karşılıklı dönüşüm yoktur. katılar, Dur kimyasal reaksiyonlar ve diğerleri Termal denge durumunda, sistemin tüm bölümlerinde sıcaklık aynıdır.
Özısı- (küçük harf c) - 1 kg maddeyi 1 derece ısıtmak için ne kadar ısı gerektiğini gösteren (veya 1 kg madde 1 derece soğuduğunda açığa çıkan) bir maddenin özelliği. J/kg K veya J/kg 0C olarak ölçülür. Tablo verileri.
ısı eşanjörü- birbirinden ayrılmış iki ortam arasında ısı aktarmak için tasarlanmış bir cihaz.
Kabuk ve borulu ısı eşanjörü- bir mahfaza içine yerleştirilmiş bir boru demeti, biri borulardan geçen akışkanlardan, diğeri borular ile mahfazanın iç yüzeyi arasındaki boşluktan oluşan bir ısı eşanjörü.
ısı borusu- genellikle bir tüp şeklinde, kısmen bir sıvı ve buharları ile doldurulmuş ve sıcak bölümde sıvıyı buharlaştırarak ve soğukta buharı yoğunlaştırarak iki uç bölümü arasında ısıyı aktarmak için kullanılan kapalı bir hacim. Yoğunlaşan sıvı, fitil görevi gören uygun bir cihaz aracılığıyla yerçekimi veya kılcal kuvvetler ile sıcak noktaya geri döndürülür.
Kısmi basıncı- (partialis - kısmi) - bir gaz karışımının parçası olan bir gazın tek başına aynı sıcaklıktaki karışımın hacmine eşit bir hacmi işgal etmesi durumunda sahip olacağı basınç.
çiy noktası Havadaki su buharının doymuş hale geldiği sıcaklık.
Evre- farklı olan maddenin denge durumu fiziksel özellikler aynı maddenin diğer olası durumlarından Bir maddenin fazları vardır: biri gaz, biri sıvı ve birkaç katı faz (örneğin, buz beş farklı modifikasyonda olabilir, yani beş katı faza sahiptir).
faz geçişi- bir maddenin bir fazdan diğerine geçişi.
Sıcaklık gradyanının fiziksel anlamı mesafe boyunca maksimum sıcaklık artışı oranıdır. Bu, mesafeye göre sıcaklığın birinci türevine sayısal olarak eşit, artan sıcaklık yönünde yönlendirilen bir vektördür. Sıcaklık gradyanı metre başına derece cinsinden ölçülür. Sıcaklık farkı varsa, sıcaklık gradyanı sıfır değildir.
ejektör- oluşturmak için daralan bir bölümde bir ortamın akış hızını artıran bir cihaz Indirgenmiş basınç ve böylece orada başka bir ortamın akışına neden olur.
Şurup Genellikle su içinde bir şeker çözeltisi.
Salamura- genellikle suda bir tuz çözeltisi.
Öğrencilere kaynama olgusunu tanıtın. Moleküler temelde kaynama sürecini açıklamayı öğretmek - Kinetik teori. Kaynamanın fiziksel özelliklerini düşünün. İncelenen süreçte ısı hesaplama yöntemini belirleyin.
İndirmek:
Slayt başlıkları:
Sunum fizik öğretmeni Starkova Evgenia Evgenievna MOU Burevestnikovskaya ortaokulu tarafından hazırlandı.
Ders konusu:
Buharlaşma olarak adlandırılan süreç nedir?
Buharlaşma nedir?
Buharlaşma hangi sıcaklıkta gerçekleşir?
1. Su neden bir tabaktan bir kaseden daha hızlı buharlaşır?
2. Terazinin dengesi neden bozuldu?
3. Neden birkaç gün sonra farklı sıvıların seviyeleri farklılaştı?
Hangi sürece yoğunlaşma denir?
Yoğuşma sırasında enerji emilir veya serbest bırakılır mı?
Kaynama, belirli bir sıcaklıkta sıvının tüm hacmi boyunca buhar kabarcıklarının oluşmasıyla meydana gelen bir sıvının buhara yoğun bir geçişidir.
Bazı maddelerin kaynama noktası, 0C (normalde atmosferik basınç)
Hidrojen
-253
su
100
Oksijen
-183
Merkür
357
Süt
100
Öncülük etmek
1740
Eter
35
Bakır
2567
Alkol
78
Ütü
2750
Kaynama noktası, sıvının serbest yüzeyine uygulanan basınca bağlıdır.
Basınç azaldıkça bir sıvının kaynama noktası düşer.
Basınç arttıkça bir sıvının kaynama noktası artar.
Özgül buharlaşma ısısı.
Fiziksel miktar 1 kg kütleli bir sıvıyı, sıcaklığını değiştirmeden buhara dönüştürmek için ne kadar ısı gerektiğini gösteren, öz buharlaşma ısısı olarak adlandırılır.
Buharlaşmanın özgül ısısı, J / kg cinsinden ölçülen L ile gösterilir.
Belirli maddelerin özgül buharlaşma ısısı, J / kg (kaynama noktasında ve normal atmosfer basıncında)
1 kg maskeli suyu 100 0C sıcaklıkta buhara dönüştürmek için 2,3*106 J enerji gerekir.
Yoğunlaşan buhar, oluşumuna giren enerji miktarını verir.
Bir sıvıyı buhara dönüştürmek için gereken ısı miktarının hesaplanması
Kaynama noktasında alınan herhangi bir kütledeki bir sıvıyı buharlaştırmak için gereken ısı miktarını hesaplamak için, özgül buharlaşma ısısını kütle ile çarpmanız gerekir.
Q=lm
Q – ısı miktarı, J L – özgül buharlaşma ısısı, J/kg m – vücut ağırlığı, kg
Kaynama noktasında yoğunlaşan buhar tarafından salınan ısı miktarı aynı formülle belirlenir.
Q
3*106J
?
4,5*107J
L
2.3*106 J/kg
2.3*106 J/kg
?
m
?
0.8kg
19 kg
1,3 kg
1.84 * 106J
2.3 * 106 J/kg
Grafikler, aynı kütledeki su ve alkolün ısıtılması ve kaynatılması işlemlerini göstermektedir.
20
40
60
80
100
ANCAK
AT
İTİBAREN
İle
M
t, 0c
t, s
1. Alkol için oluşturulmuş ısıtma ve kaynama grafiğini belirtin
2. MC işlemi sırasında emilen ısı miktarını hesaplayın. Su kütlesinin 5 kg olduğu varsayılmaktadır.
Ders Kitabı A.V. Peryshkin§18, §20Ex. 10 Hayır 3.4
Ön izleme:
8. sınıf fizik dersi.
Başlık: Kaynamak. Özgül buharlaşma ve yoğunlaşma ısısı.
Dersin amacı: Öğrencilere kaynama olgusunu tanıtın. Moleküler-kinetik teori temelinde kaynama sürecini açıklamayı öğretmek. Kaynamanın fiziksel özelliklerini düşünün. İncelenen süreçte ısı hesaplama yöntemini belirleyin.
Demolar:1 .Cam şişede su ısıtma ve kaynatma işleminin gözlemlenmesi (Video)
2 . Düşük basınçta kaynar su (video).
3 . Yoğunlaşma sürecinin gözlemlenmesi (video).
Teçhizat: bilgisayar, multimedya projektörü.
Ders adımları:
- E Bilgiyi güncellemek için dokunun
- motivasyon aşaması
- Yeni bilgi yaratma aşaması
- Edinilen bilgiyi uygulama aşaması
- Ev ödevi
ders yapısı
- Bilgiyi güncelleme aşaması.
Kuruluş anı.
muayene ev ödevi sözlü anket şeklinde:
Son derste iki tane öğrendik fiziksel olaylar Bunlar buharlaşma ve yoğunlaşmadır. Ne olduklarını hatırlayalım.
Slayt 2. Buharlaşma olarak adlandırılan süreç nedir?
Buharlaşma nedir?
Buharlaşma hangi sıcaklıkta gerçekleşir?
Slayt 3. Buharlaşma hızı birkaç faktöre bağlıdır. Aşağıdaki soruları cevaplayarak bunları netleştirelim:
Bu nedenle, buharlaşma hızı şunlara bağlıdır:
- yüzey alanından.
- sıvının sıcaklığına bağlıdır.
- Bir çeşit sıvıdan.
slayt 4. Ekranda ne görüyorsun? (çiğ ve bulutlar).
Çiy ve bulutların oluşmasına neden olan süreç nedir?
Hangi sürece yoğunlaşma denir?
Yoğuşma sırasında enerji emilir veya serbest bırakılır mı? (öne çıkıyor).
- motivasyon aşaması.
Aferin! Şimdi ekranda sunulan görüntülere bakalım:
Slayt 5. Söyle bana ne görüyorsun? ( su buharı üzerinde)
slayt 6. Burada ne görüyoruz? (kaynar su, suyun üstünde buhar)
7. Slayt Görüntü verilerini birleştiren nedir? ( buhar )
İyi! Son derste, bir sıvının içine geçmesinin iki yolu olduğunu öğrendik. gaz hali, buharlaşma ve kaynama.
Bugün buhar oluşumunun ikinci yöntemini ele alacağız - kaynama.
- Yeni bilgi yaratma aşaması.
slayt 8. "Bir cam şişede su ısıtma ve kaynatma" deneyimine sahip bir video gösteriyorum.
Isıtıldığında, suyun yüzeyden buharlaşması artar, bazen üzerinde sis bile fark edebilirsiniz. Bu su buharı soğudukça havada yoğunlaşır.
Sıcaklığın daha da artmasıyla, suda çok sayıda küçük kabarcıkların ortaya çıktığını fark edeceğiz. Boyutları yavaş yavaş büyüyor. Bunlar suda çözünen hava kabarcıklarıdır. Isıtıldığında, fazla hava sudan kabarcıklar şeklinde salınır. İçerdikleri doymuş buhar su buharlaşarak bu hava kabarcıklarına dönüşür.
Su ısındıkça kabarcıklar büyür ve sayıları artar. Kabarcıkların boyutu arttıkça Arşimet kuvveti de artar, onları sudan dışarı iter ve yüzerler. Bu noktada, genellikle kaynamadan önce bir ses duyulur. Belirli bir sıcaklıkta sıvının yüzeyine yaklaştıkça kabarcıkların hacmi keskin bir şekilde artar. Yüzeyde patlarlar ve içlerindeki doymuş buhar atmosfere kaçar - su kaynar.
Ruh lambasını şişenin altından çıkarıyoruz. Ne görüyoruz? (kaynama durur)
Kaynamaya devam etmek için kaynayan sıvıya enerji sağlamak gerekir.
slayt 9. Kaynama, belirli bir sıcaklıkta sıvının tüm hacmi boyunca buhar kabarcıklarının oluşmasıyla meydana gelen bir sıvının buhara yoğun bir geçişidir. (deftere yazmak)
Bir sıvının kaynadığı sıcaklığa kaynama noktası denir. (deftere yazmak)
slayt 10. Kaynama sırasında sıvının sıcaklığı değişmez.
Farklı sıvıların farklı kaynama noktaları vardır.
Slayt 11. Kaynama noktası, sıvının serbest yüzeyine uygulanan basınca bağlıdır.
"Düşük basınç altında kaynama" deneyimine sahip bir video gösteriyorum
Basınç azaldıkça sıvının kaynama noktası düşer
(Yüksek rakımlı dağlık bölgelerde, düşük atmosferik basınçta su 100 santigrat derecenin altındaki sıcaklıklarda kaynar. Böyle bir yemeğin pişmesini beklemek daha uzun sürer.)
Basınç arttıkça sıvının kaynama noktası artar
(Pişirirken, tencerenin içindeki basınç - "düdüklü tencere" - yaklaşık 200 kPa'dır ve böyle bir tenceredeki çorba çok daha hızlı pişecektir).
slayt 12. Özgül buharlaşma ısısı.
slayt 13. Buharlaşmanın özgül ısısı maddeden maddeye değişir.
slayt 14. Soğuk bir cisimle temas ettiğinde su buharı yoğunlaşır. Bu durumda buhar oluşumu sırasında emilen enerji açığa çıkar.
"Yoğuşma sürecinin gözlemlenmesi" deneyimine sahip bir video gösteriyorum.
Yoğunlaşan buhar, oluşumuna giren enerji miktarını verir.
slayt 15. Bir sıvıyı buhara dönüştürmek için gereken ısı miktarının hesaplanması.
- Edinilen bilgiyi uygulama aşaması.
(Yeni materyal sunduktan sonra, güçlendirme görevlerinin yapılması tavsiye edilir)
slayt 16.
Herhangi bir kütledeki bir sıvıyı buhara dönüştürmek için gereken ısı miktarını hesaplamak için bir formülle çalışmak
S = Lm.
Yanıtlar:
slayt 17. Grafiklerle çalışmak.
Sonuç . Bugün derste kaynama fenomeni ile tanıştık. Kaynama sürecini moleküler-kinetik teori temelinde açıklamayı öğrendik. Kaynamanın fiziksel özelliklerini göz önünde bulundurduk ve incelenen süreçte ısı hesaplama yöntemini belirledik.
- Ev ödevi
(Öğretmen en aktif öğrencileri not eder)