Atom çekirdeğini oluşturan parçacıkları tanımlar. Atom çekirdeğinin özellikleri

Obninsk Devlet Teknik Üniversitesi
nükleer enerji
Nükleer Fizik Bölümü
L.N. Pustynsky
ders notları nükleer Fizik
"Nükleer ve Nötron Fiziği" dersi için ders kitabı.
Elektronik versiyon.
Obninsk, 2003
Pustynsky L.N. Nükleer fizik üzerine derslerin özeti. "Nükleer ve nötron fiziği" dersi için ders kitabı. Elektronik versiyon. - Obninsk, IATE, 2003. -215s.
El kitabı, yazarın 1999-2003 akademik yıllarında çeşitli üniversite uzmanlıkları için "Nükleer Fizik" ve "Nükleer ve Nötron Fiziği" derslerinde verdiği ders notlarının elektronik bir versiyonunu sunmaktadır. Kılavuz, çalışma programlarına tam olarak uygun olarak yazılmıştır ve okutulan derslerde sınavı geçmeye hazırlanırken ana kılavuz olarak önerilebilir. Yazar, Prof. VS. Stavinsky'ye değerli ve faydalı açıklamalar için teşekkür eder ve anısını onurlandırır.
© L.N. Pustynsky, 2003
Bölüm 1. Yapı ve ana özellikler atom çekirdeği
Artık kesin olarak kurulmuştur ve atomun elektronlardan (J. Thomson, 1897) ve bir çekirdekten (E. Rutherford, 1911) oluştuğuna şüphe yoktur. Atom çekirdeği, tek tek kimyasal elementlerin çekirdeklerini birbirinden ayırt etmeyi mümkün kılan bir dizi bireysel özelliğe sahiptir ve aynı zamanda Genel özellikleri tüm çekirdekler için.
Atom çekirdeği olabilir kararlı, yani süresiz yaşamak ve dengesiz spontan (kendiliğinden) radyoaktif dönüşümler yaşıyor.
Tüm atom çekirdekleri aşağıdaki özelliklere sahiptir: çekirdekteki nükleon sayısı; çekirdeğin elektrik yükü; çekirdek kütlesi; çekirdeğin bağlanma enerjisi; çekirdek boyutu; nükleer spin; çekirdeğin manyetik ve elektriksel momentleri; dalga fonksiyonunun paritesi; izotopik dönüş; İstatistik.
Kararsız çekirdekler, radyoaktif dönüşümün türü, ortalama yaşam süresi ve bozunma sırasında açığa çıkan enerji gibi bir dizi ek özelliğe sahiptir.
Çekirdekler farklı enerji durumlarında olabilir ve herhangi bir kuantum sistemi gibi, yalnızca belirli bir çekirdeğin çekirdeğine, enerji seviyeleri sistemine özgü kendi bireysel özelliklerine sahiptirler. Çekirdeğin en düşük enerjili durumuna denir. temel, geri kalan - heyecanlı. Uyarılmış durumdaki çekirdekler kararsızdır ve temel durumların aksine, sınırlı bir süre için uyarılmış durumlarda olabilir ve daha düşük enerjili durumlara kendiliğinden geçişler yaşayabilir.
Aşağıda gösterilecektir (bakınız §1.7), kararlı, kararsız ve uyarılmış çekirdeklere bölünme, bir dizi ortak özellik ile karakterize edilebildiklerinden, bir dereceye kadar koşulludur.
§1.1. Çekirdeğin proton-nötron yapısı.
Tüm maddeler moleküllerden oluşur. Moleküller de atomlardan oluşur. Bir atom, bir çekirdek ve bir elektron kabuğundan oluşur. Bir atomun boyutu elektron kabuğu tarafından belirlenir ve ≈ 10 -8'e eşittir. santimetre. Çekirdek - atomun merkezi büyük kısmı ≈ 10 -13 10 12 boyutlarına sahiptir. santimetre(1 – 10FM(fermi)). Sonuç olarak, çekirdeğin boyutu atomdan 10 4 - 105 kat daha küçüktür.
Çekirdek özel parçacıklardan oluşur (Heisenberg, Ivanenko) - protonlar(Rutherford, 1919) ve nötronlar(Chadwick, 1932). Protonun bir pozitif temel elektrik yükü vardır ve nötronun elektrik yükü sıfırdır. Herhangi bir çift kombinasyonundaki bu parçacıklar arasında, aşağıdakilere bağlı olmayan özel (nükleer) kuvvetler vardır. elektrik şarjı tek tek protonların ve nötronların çekirdekle bağlantısını sağlayan parçacıklar. Bu nedenle, nükleer fizikte genel terim kullanılır. nükleon, hem bir proton hem de bir nötron olan çekirdeği oluşturan parçacıklardan herhangi birini belirtir.
Çekirdekteki nükleon sayısı A harfi ile gösterilir ve buna denir. kütle Numarası .
Çekirdekteki proton sayısı Z harfi ile gösterilir. Ayrıca Z, atom elektriksel olarak nötr olduğu için çekirdeği Z protonu olan bir atomdaki elektron sayısıdır. Çünkü Kimyasal özellikler elementler atomdaki elektron sayısı ile belirlenir, yani Z aynı zamanda sıralı veya atomik numara periyodik tablodaki element.
Çekirdekteki nötron sayısı N harfi ile gösterilir. Bu nedenle çekirdekteki nötron sayısı N=A–Z'dir.
(Z,N), (N,A) veya (A,Z) sayı çiftlerinden herhangi biri, çekirdeğin bileşimini benzersiz şekilde belirler. Genellikle aşağıda belirtilecek nedenlerden dolayı bir çift sayı (A, Z) kullanılır.
Belirli A ve Z değerlerine sahip çekirdeğe sahip bir atoma denir. nüklid, ve aynı Z-'ye sahip nüklidler kümesi kimyasal element. Z sayısı kimyasal elementi tamamen belirler ve Z ve A sayıları nüklidi belirler. Bir nüklidi belirtmek için iki gösterim biçimi kullanılır: (A, Z) veya 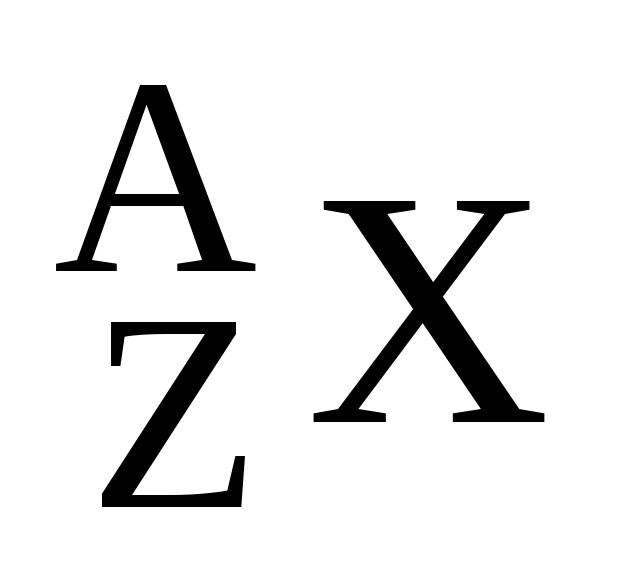 , burada X bir kimyasal elementin sembolüdür. Örneğin, (12.6) veya
, burada X bir kimyasal elementin sembolüdür. Örneğin, (12.6) veya 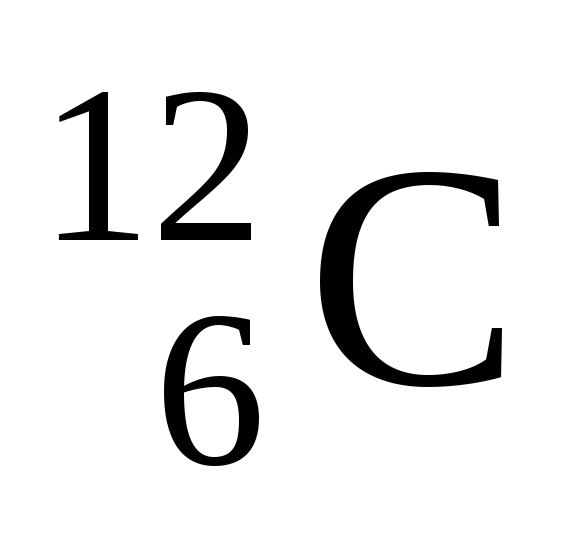 karşılık gelen karbon nüklididir. Bir kimyasal elementin sembolü benzersiz bir şekilde Z ile ilişkili olduğundan, genellikle bir kimyasal elementin sembolünü gösteren bir kayıt biçimindeki atom numarası atlanır ve basitçe yazılır.
karşılık gelen karbon nüklididir. Bir kimyasal elementin sembolü benzersiz bir şekilde Z ile ilişkili olduğundan, genellikle bir kimyasal elementin sembolünü gösteren bir kayıt biçimindeki atom numarası atlanır ve basitçe yazılır. 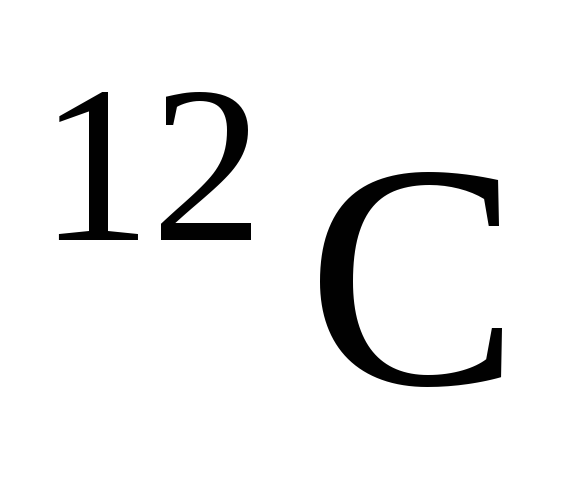 . Aynı gösterim çekirdekler için de kullanılır.
. Aynı gösterim çekirdekler için de kullanılır.
Çekirdekleri aynı sayıda protona sahip olan ancak A nükleon sayıları farklı olan nüklidlere denir. kimyasal bir elementin izotopları. Bileşimlerinde izotop atomları bulunan maddeler aynı kimyasal özelliklere sahiptir, ancak yoğunluk, erime noktası, kaynama noktası vb. farklıdır, yani. fiziksel özelliklerde farklılık gösterir. Örneğin: 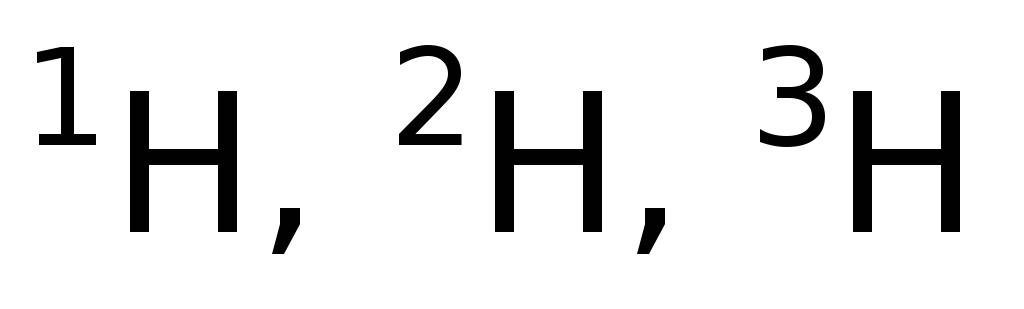 hidrojen izotopları. 1H - protiyum (hafif hidrojen); 1 H - döteryum (ağır hidrojen, çekirdek için D sembolünü de kullanın - d); 3H - trityum (süper ağır hidrojen, çekirdek için T sembolünü de kullanın d); 233 U, 235 U, 238 U uranyum izotoplarıdır. Bununla birlikte, bir kimyasal elemente ait olduğunu ima ederek bir izotop hakkında konuşmak mantıklıdır. Bu nedenle, 235 U, uranyumun bölünebilir bir izotopu değil, bölünebilir bir uranyum nüklididir. Aynı şekilde, 3H bir radyoaktif hidrojen nüklididir ve bir radyoaktif izotop değildir, çünkü bu durumda, atomun karşılık gelen kimyasal özellikleri değil, çekirdeğin fiziksel özellikleri ima edilir.
hidrojen izotopları. 1H - protiyum (hafif hidrojen); 1 H - döteryum (ağır hidrojen, çekirdek için D sembolünü de kullanın - d); 3H - trityum (süper ağır hidrojen, çekirdek için T sembolünü de kullanın d); 233 U, 235 U, 238 U uranyum izotoplarıdır. Bununla birlikte, bir kimyasal elemente ait olduğunu ima ederek bir izotop hakkında konuşmak mantıklıdır. Bu nedenle, 235 U, uranyumun bölünebilir bir izotopu değil, bölünebilir bir uranyum nüklididir. Aynı şekilde, 3H bir radyoaktif hidrojen nüklididir ve bir radyoaktif izotop değildir, çünkü bu durumda, atomun karşılık gelen kimyasal özellikleri değil, çekirdeğin fiziksel özellikleri ima edilir.
Çekirdekleri aynı sayıda nükleon içeren (A kütle numarası aynı), proton sayıları farklı Z olan nüklitlere denir. izobarlar. Örneğin: 3 H ve 3 He, trityum ve helyum izobarlarıdır, 10 Be, 10 B, 10 C berilyum, bor ve karbon izobarlarıdır.
Çekirdeğinde aynı sayıda nötron bulunan nüklidlere denir. izotonlar. Örneğin 2H ve 3 He hidrojen ve helyumun izotonlarıdır.
İTİBAREN  çeşitli nüklidlerin çekirdeklerinin özellikleri kullanılarak sistematize edilebilir. proton-nötron diyagramı(Segre diyagramları) - satırları aynı sayıda protona sahip nüklidlere ve sütunlar aynı sayıda nötrona sahip nüklidlere karşılık gelen bir tablo. Şekil 1.1.1, hafif çekirdekli nüklidler örneğini kullanarak bir proton-nötron diyagramı oluşturma ilkesini göstermektedir. Bilinen tüm nüklidler için proton-nötron diyagramı Şekil 1.1.2'de gösterilmiştir.
çeşitli nüklidlerin çekirdeklerinin özellikleri kullanılarak sistematize edilebilir. proton-nötron diyagramı(Segre diyagramları) - satırları aynı sayıda protona sahip nüklidlere ve sütunlar aynı sayıda nötrona sahip nüklidlere karşılık gelen bir tablo. Şekil 1.1.1, hafif çekirdekli nüklidler örneğini kullanarak bir proton-nötron diyagramı oluşturma ilkesini göstermektedir. Bilinen tüm nüklidler için proton-nötron diyagramı Şekil 1.1.2'de gösterilmiştir.
Atom çekirdeğinin proton-nötron diyagramından çıkan aşağıdaki ampirik gerçekleri ve düzenlilikleri not ediyoruz.
1 . 2000'den fazla nüklid bilinmektedir, bunlardan 265'i stabil nüklidlerdir.
. 2000'den fazla nüklid bilinmektedir, bunlardan 265'i stabil nüklidlerdir.
2. Resmi adlara sahip nüklidler, 0'dan (nötron) 109'a (meitnerium) kadar Z'ye sahiptir. Doğada bulunan çekirdekler için Z, 1 (hidrojen) ile 92 (uranyum) arasında değişir.Çekirdeklerin geri kalanı yapay olarak elde edilir. Z= 0, 43, 61 ve Z84 ile kararlı nüklid yoktur.
3. Nüklitler, 1'den 263'e kadar olan A nükleonlarının sayısı ile bilinir. A = 5.8 ve A210'da kararlı nüklidler yoktur.
4. β-kararlı nüklidlerin bulunduğu proton-nötron diyagramının bölgesi (Şekil 1.1.2'de gölgeli çubuk 1) istikrar yolu. Hafif kararlı nüklidler (Z≤ 20'ye kadar) çekirdekte yaklaşık olarak eşit sayıda proton ve nötron içerir. A kütle numarası arttıkça, nötronların bağıl kesri de artar. Örneğin, hafif bir nüklid için 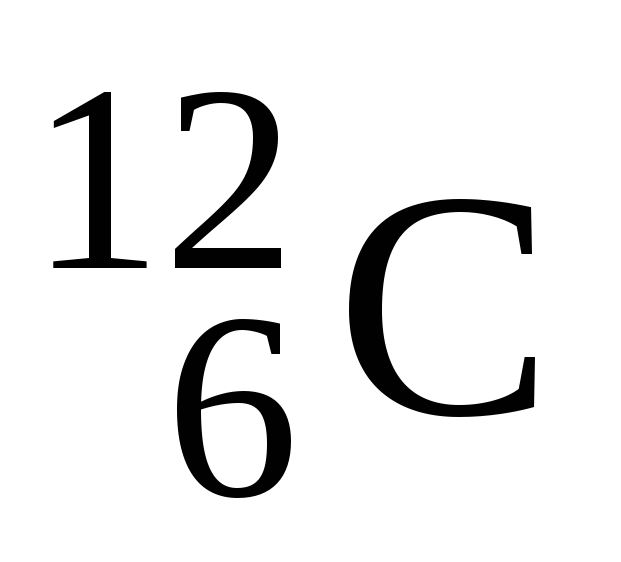 N/Z = 1; ortalama nüklid için
N/Z = 1; ortalama nüklid için 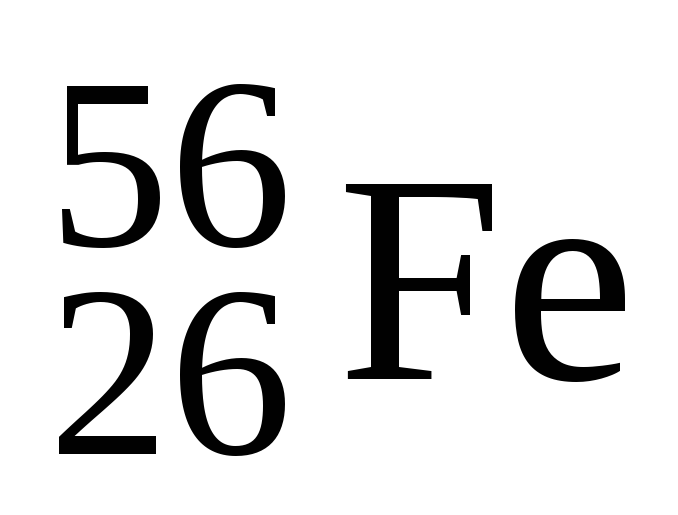 N/Z
= 1.15; ağır bir nüklid için
N/Z
= 1.15; ağır bir nüklid için 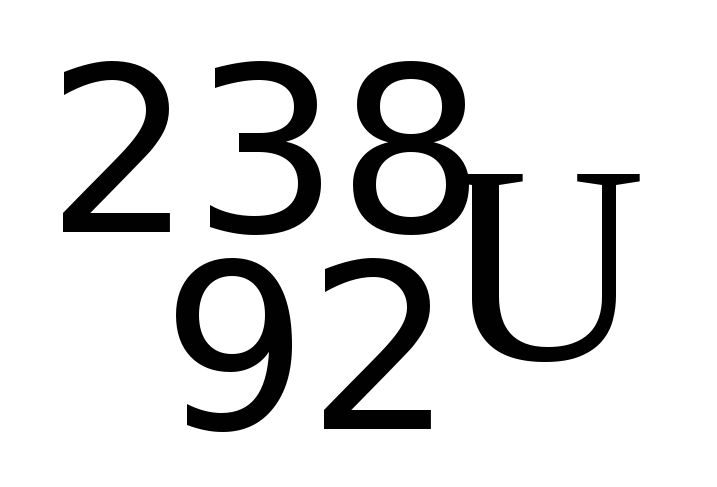 N/Z =
59. Büyük A'daki nötron sayısındaki önde gelen artış, çekirdekteki protonların karşılıklı itilmesine yönelik uzun menzilli Coulomb kuvvetlerinin etkisinden kaynaklanır.
N/Z =
59. Büyük A'daki nötron sayısındaki önde gelen artış, çekirdekteki protonların karşılıklı itilmesine yönelik uzun menzilli Coulomb kuvvetlerinin etkisinden kaynaklanır.
5. Çoğu kimyasal elementin birkaç kararlı ve -aktif nüklidi vardır. Bazı elementlerin her biri sadece bir kararlı nüklide (9 Be, 19 F, 23 Na) sahiptir (bkz. Şekil 1.1.1), geri kalanların her biri 2 ÷ 3 kararlı nüklide sahiptir. Kalay (Sn) on kararlı nüklide sahiptir.
6. Stabilite yolunun üstünde β + -aktif nüklidler, altında - β - -aktif nüklidler bulunur.
7. Çekirdeklerin özellikleri esas olarak Z ve N sayılarının paritesine bağlıdır. En fazla sayıda kararlı nüklid (265'ten 155'i) çift-çift çekirdeklere (Z-çift, N-çift), eşit derecede kararlı nüklidlere (her biri 53) ve çekirdeklerinde çift-tek ve tek-çift sayıda nükleon içerir. Ve tek-tek bir çekirdek bileşimine sahip sadece dört kararlı nüklid (2 H, 6 Li, 10 V ve 14 N) vardır.
Hafif hidrojen atomu hariç herhangi bir atomun çekirdeği parçacıklardan oluşur - nükleonlar iki tip: Z protonlar ve N nötronlar. Nötron, 1932'de James Chadwick, aynı zamanda Karl Anderson - pozitron tarafından keşfedildi. Hafif hidrojen atomunun çekirdeği bir protondan oluşur.
Proton açık, yüklü bir parçacıktır - qp = +e. Bir protonun kütlesi m p= 1.67265 10 -27 kg. Nükleer fizikte, parçacıkların enerjisini, kütleyi ışık hızının karesiyle çarptıkları enerji birimlerinde (eV) ifade etmek gelenekseldir. c2, daha sonra proton kütlesi p = 938.26 MeV. Protonun spini şuna eşittir: s = 1/2.
Nötron ayrıca spin var s= 1/2. Kütlesi bir protonun kütlesine yakındır ve mn\u003d 1.67495 10 -27 kg veya enerji birimi (eV) p = 939.55 MeV. Ancak nötronun elektrik yükü yoktur. Serbest durumda, nötron radyoaktiftir, kendiliğinden bozunur ve bir protona dönüşür. Bu durumda, bir antineutrino serbest bırakılır.
Nötron çekirdekte kararlıdır.
Bir atom bir yük numarası ile karakterize edilir Z(çekirdekteki proton sayısına eşittir). Sayı Z periyodik tablodaki atom numarasını belirler. Kütle Numarası A=N+Zçekirdekteki toplam nükleon sayısını gösterir. Tüm nükleonların kütlesi A tüm atomun kütlesine ana katkıyı yapar. Çekirdeğe nüklid de denir. Nüklidin benimsenen şeması aşağıdaki forma sahiptir: Çekirdekte nükleonlar dışında başka parçacık yoktur. Ancak nükleonlar temel parçacıklar değildir: her biri başka bir derste tartışılacak olan üç kuarktan oluşur.
Çekirdekleri aynı yük sayısına sahip atomlar Z ve çeşitli kütle numaraları A, aynı kimyasal özelliklere sahiptir ve izotop olarak adlandırılır. Aynı kimyasal elementin izotopları, yalnızca çekirdekteki nötron sayısı ile birbirinden farklıdır. Aynı atoma sahip maddelerin çoğu Z farklı izotopların karışımıdır. Yani hidrojen, karbon ve oksijenin her biri 3 izotopa sahiptir: - sıradan hidrojen, - döteryum, - trityum; ![]() ;
; ![]() ; Kalay 10 izotopa sahiptir.
; Kalay 10 izotopa sahiptir.
Çekirdekleri aynı kütle numaralarına sahip atomlar A, arandı izobarlar. İzobarlar, yani farklı çekirdekler Z, çeşitli atomların çekirdeklerine karşılık gelir kimyasal elementler.
Rutherford'un saçılma deneylerinde α -maddenin atomları üzerindeki parçacıklar, çekirdeklerin sonlu bir boyuta sahip olduğu bulundu. O andan bu yana çok zaman geçti, ancak atom çekirdeği üzerindeki parçacıkların saçılmasıyla ilgili deneyler, çekirdeğin boyutunu belirlemede hala en çok tercih edilen deneylerdir. Elektronlar çekirdeklerle yalnızca elektrostatik etkileşim yaşadıklarından, çekirdeğin içindeki yük dağılımı elektron saçılımı kullanılarak incelenir. Çekirdek içindeki nükleer maddenin dağılımı, nötronların saçılması ile değerlendirilir, çünkü bu durumda parçacıklar arasındaki etkileşim sadece belirli bir nükleer olana indirgenir. Çekirdeğin gelen parçacığı "hissetmesi" için, kütleler dikkate alındığında elektronun enerjisi en az 124 MeV ve nötronun enerjisi en az 8 MeV olmalıdır. Çeşitli (ancak belirtilen koşulları karşılayan) enerjilerdeki elektronlar ve nötronlarla yapılan deneyler, bir çekirdeğin hacminin, bileşimindeki nükleon sayısıyla orantılı olduğunu gösterdi:
1'e eşit veya daha büyük spinli çekirdeklerde, gerçekten de küresel şekilden bir sapma gözlemlenir. Bu tür çekirdekler sıkıştırılabilir veya dönüş elipsoidlerini çoğaltabilir ve büyük ve küçük eksenleri arasındaki fark hiçbir zaman %20'yi geçmez ve kural olarak çok daha küçüktür. İlk yaklaşımda, çekirdek bir top olarak kabul edilebilir, çekirdeğin yarıçapı şu şekildedir: (13.3)
Devamlı R0≈ 1.3·10 –15 m Yaklaşık değeri, nükleer maddenin dağılımından elde edilen çekirdeğin yarıçapının değerinin, yük dağılımından elde edilen yarıçapın değerinden farklı olmasından kaynaklanmaktadır. Bu, yükün ve maddenin çekirdeğin içinde farklı bir şekilde dağıldığı anlamına gelir.
Nükleer teori çerçevesinde, miktar kullanılır 1 fermi = 1 f= 10-15 m.
O zaman çekirdek yarıçapı ![]() .
.
Nükleer spin I, çekirdeğin toplam açısal momentumudur. Kütle numarası olan bir çekirdek için Aşuna eşittir: 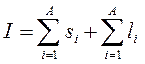 (13.4)
(13.4)
Bu ifadede, sağdaki ilk terim nükleonların toplam dönüş momentine, ikinci terim ise çekirdekteki nükleonların toplam yörünge momentine eşittir. değerler Si ve ben ben karşılık gelen kuantum sayılarının değerleri ile belirlenir: s p = s n= 1/2 ve ben = 0, 1, 2, ...
Çekirdeğin manyetik momenti μ ben protonların ve nötronların içsel manyetik momentleri ile protonların yörüngesel manyetik momentlerinin toplamıdır (bir nötronun herhangi bir yörünge manyetik momenti sıfırdır). ben).
Yani çekirdek içerir A nükleonlar. Bununla birlikte, tüm proton ve nötron kombinasyonları kararlı çekirdekler oluşturmaz. Bu nükleer enerji seviyelerinin varlığından kaynaklanmaktadır. Hem protonlar hem de nötronlar fermiyon olduğundan (spin s = 1/2), o zaman her seviyede ikiden fazla proton ve iki nötron olamaz. Seviyeler, birleşik parçacıklar sistemini en aza indirme ilkesine göre doldurulur. Örneğin, iki izotopu düşünün ve . İlk iki seviyesi (Şekil 13.1) aynı şekilde doldurulur.
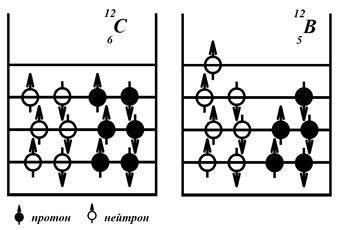
Pirinç. 13.1 Karbonun kararlı izotopu ve boronun kararsız izotopu
Son seviyede, 12. nötron nüklidde bulunurken, aynı zamanda bir önceki seviyede tamamen dolana kadar yeterli proton yoktur. Üç nötron ve bir protondan oluşan bir sistemin enerjisi, iki proton ve iki nötrondan oluşan bir sistemin enerjisinden daha büyük olacaktır. Bu nedenle izotop kararlı olmayacak ve oldukça hızlı bir şekilde bozunacaktır. Aynı zamanda izotop (5 proton ve 6 nötron içeren) kararlıdır.
Hafif çekirdeklerde ( A< 20), как правило, число протонов и нейтронов одинаково (или отличается не единицу в случае ядер с нечетным числом нуклонов, причем число нейтронов обязательно daha fazla sayı protonlar). Ağır çekirdeklerde, nötronların oranı büyüyor. Bu tür çekirdeklerde, enerji minimizasyonu ilkesine ek olarak, protonların Coulomb itmesinin önemli olduğu ortaya çıkıyor. 10'dan fazla protona sahip çekirdeklerde bu itme o kadar güçlüdür ki, çekirdeğin kararlılığı için bu kuvvetin bir şey tarafından telafi edilmesi gerekir. Nötronlar arasında sadece çekici nükleer kuvvetler hareket eder. Bu nedenle, çekirdeğin bileşimindeki nötron sayısındaki bir artış, bir kuvvet dengesine, yani. çekirdek kararlılığı için.
13.2. Çekirdek modeller: damla ve kabuk
Çekirdeklerin özelliklerini, katılımlarıyla meydana gelen süreçleri açıklamak ve olası yeni etkileri tahmin etmek için, tüm nükleer fenomenleri doğru ve tam olarak tanımlayacak böyle bir çekirdek teorisi oluşturmak gerekir. Çekirdeğin özgüllüğü, iç süreçler ve yapı hakkında bilgi edinmenin basit yollarına izin vermediğinden, bu çok zor bir iştir. Ayrıca, çekirdek bir sistemdir. Büyük bir sayı parçacıklar. Zaten 3 - 4 etkileşimli cisim durumunda olan matematiksel problem, ancak yüksek performanslı bilgisayar teknolojisinin yardımıyla çözülebilir hale gelir. Nitel modellerin oluşturulması, çekirdeklerin özelliklerini tanımlamak için nispeten basit matematiksel yasaların kullanılmasına izin veren bir geçici çözümdür.
Bu modellerden biri damla modeli- 1939'da Ya. I. Frenkel tarafından önerildi ve daha sonra N. Bor tarafından geliştirildi. Frenkel, bir sıvı damlasındaki moleküller gibi, çekirdekteki nükleonların sınırlı sayıda yakındaki parçacıklarla etkileşime girdiğine dikkat çekti. Nükleer maddenin son derece düşük sıkıştırılabilirliği, bir sıvı ile analojiyi tamamladı. Çekirdeğin belirli sayıda pozitif yüklü proton içerdiği düşünüldüğünde, bu model çerçevesinde çekirdeğin elektriklenmiş bir damla olduğu düşünülmelidir.
Pirinç. 13.2. Çekirdeğin damla modeli
Damla modeli, çekirdekteki bağlanma enerjisi için yarı deneysel bir formül türetmeyi mümkün kılar. Nükleon sistemi, bağlanma enerjisinin maksimum değerine sahip durumu tercih eder. Bu durumda, varlığı toplam enerjinin değerini azaltan bir takım kuvvetler vardır.
Bir çekirdeğin özgül bağlanma enerjisinin nükleon sayısına bağımlılığını belirlemek için, enerjiyi tanıtmak gerekir. sen, her nükleon-nükleon bağını karakterize eder. Bir çift nükleonun her biri bu enerjinin yarısını oluşturur. Geometrik değerlendirmelerden, her nükleonun 12 kısa menzilli nükleonla çevrili olduğu sonucu çıkar. O halde çekirdeğin hacim enerjisi: ![]() (13.5)
(13.5)
nerede Açekirdekteki nükleon sayısını, ürünü koyduk 6U = a.
Aslında, her çekirdekte, bazı nükleonlar çekirdeğin yüzeyinde bulunur ve 12'den az "komşu"ya sahiptir. Bu nedenle, yüzey enerjisi dikkate alınmalıdır. Nükleonların çoğunun yüzeyde olduğu hafif çekirdeklerde önemli bir rol oynar.
(13.3) formülü dikkate alındığında, çekirdeğin yüzey alanının şuna eşit olduğunu elde ederiz: ![]() (13.6)
(13.6)
Yüzey enerjisi negatiftir ve çekirdeğin yüzey alanıyla orantılıdır, dolayısıyla:
![]() (13.7)
(13.7)
Yüzey enerjisinin varlığı, çekirdeğin, minimum yüzey alanını ve dolayısıyla belirli bir hacim (nükleon sayısı) için minimum yüzey enerjisi değerini sağlayan küresel bir şekil alma eğilimini belirler. Böylece küresel şekil, çekirdeğin toplam bağlanma enerjisindeki minimum azalmaya karşılık gelir. Aynı şekilde kuvvetler yüzey gerilimiÜzerine herhangi bir dış kuvvet etki etmiyorsa, bir sıvı damlasının küre şeklini almasına neden olur.
Çekirdekteki her bir proton çifti arasındaki elektrostatik itici kuvvetler, çekirdeğin toplam bağlanma enerjisine yönelik başka bir düzeltmeyi belirler. Sonsuzluktan bir araya getirmek için yapılması gereken işe eşdeğerdir. Z protonlar, çekirdeğin hacmine eşit bir hacme sahiptir. İçerdiği çekirdekte Z protonlar, bu iş proton çiftlerinin sayısı ile orantılı ve çekirdeğin yarıçapı ile ters orantılıdır (13.3):
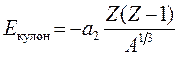 (13.8)
(13.8)
Coulomb enerjisi de negatiftir, çünkü nükleonların itilmesinden kaynaklanır, yani. çekirdekteki bağları kırmayı amaçlar.
toplam enerjiçekirdek bağlantılar Avustralya, Brezilya ve Kuzey Amerika ülkelerinin kullandığı saat uygulaması kütle, yüzey ve Coulomb enerjilerinin toplamıdır:
Çekirdeğin özgül bağlanma enerjisi nereden geliyor, yani. nükleon başına enerji:
Şek. 13.3 gösteri deneysel bağımlılıklar farklı şekillerçekirdekteki nükleon sayısı kadar enerji.
Çekirdeğin düşme modeli çerçevesinde elde edilen teorik bağımlılıklarla karşılık gelen eğrileri karşılaştırarak, bu teorinin çekirdeğin bazı parametrelerinin teorik hesaplamalarında ve bir takım etkileri açıklamak için kullanılabileceğini söyleyebiliriz.
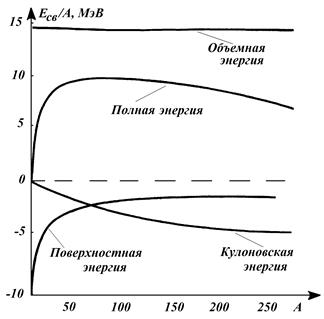
13.3. Bir atom çekirdeğinin özgül bağlanma enerjisinin nükleon sayısına bağımlılığı
Kabuk modeli ödül sahipleri tarafından geliştirildi Nobel Ödülü Amerikalı Maria Goeppert-Mayer ve Alman Johan H. D. Jensen.
Bu modele göre, çekirdekteki nükleonlar birbirleriyle etkileşmezler (düşürme modelinde varsayıldığı gibi), ancak ortalama merkezi simetrik kuvvet alanı. Benzer bir durum, her elektronun hareketinin çekirdeğin ve diğer elektronların ortalama alanında meydana geldiği çok elektronlu bir atomda gerçekleşir. Model çerçevesinde nükleonlar bazı noktalarda yer almaktadır. enerji seviyeleri kabuklar halinde gruplandırılmıştır. Nükleonlar, elektronlar gibi Fermi parçacıklarıdır, yani her seviyede antiparalel dönüşlü iki nükleon olabilir.
Çekirdekteki nükleon sayısının artmasıyla kabuklar kademeli olarak doldurulurken, çekirdeğin bazı özellikleri duruma bağlı olarak periyodik olarak tekrarlanır. Z(proton sayısı) ve N(nötron sayısı), tıpkı atomların özelliklerinin periyodik olarak değişmesi gibi Z. 2, 10, 18, 36, 54 ve 86 elektronlu atomlarda tüm kabukların tamamen tamamlandığını hatırlayın (bkz. Bölüm 8). Bu tür atomlar inert gazlardır ve elektronik konfigürasyonlar oldukça kararlı, bu da kimyasal inertliklerini açıklıyor.
Çekirdeklerde durum şöyledir: 2, 8, 20, 28, 50, 82 ve 126'ya eşit nötron veya proton sayısına sahip çekirdekler daha fazladır. Bu numaralar denir büyülü. Sihirli sayıda proton veya nötron içeren çekirdeklerin daha kararlı olduğunu varsaymak mantıklıdır - bu tür çekirdeklere ayrıca denir büyülü. Proton ve nötron sayıları sihirli olan çekirdeklere denir. iki kez büyülü. Özellikle dayanıklıdırlar. Bu tür yalnızca beş çekirdek vardır:
(Z = 2, N = 2)
(Z = 8, N = 8)
(Z = 20, N = 20)
(Z = 20, N = 28)
(Z = 82, N = 126)
Özellikle helyum çekirdeği o kadar kararlıdır ki, radyoaktif bozunma sırasında ağır çekirdekler tarafından bir bütün olarak yayılabilir (bkz. aşağıdaki Bölüm 14). Helyum çekirdeği denir α -parçacık.
Çekirdeğin enerji durumlarının doldurulması Pauli ilkesine göre gerçekleştiğinden (bkz. Bölüm 8), çekirdeklerin çift sayıda proton ve nötron içerdiğini varsaymak mantıklı olacaktır ( "çift-çift"çekirdekler), yani her iki türden de dolu seviyelere sahip olmak, proton ve nötron türlerinin seviyeleri yarı dolu olan "tek-tek" çekirdeklerden daha kararlı olacaktır. Bu, 160 kararlı "çift-tek" nüklid olduğu gerçeğiyle doğrulanırken, "tek-tek" nüklidler arasında sadece dördü kararlıdır: , , ve .
Kabuk modeline göre, atomlar gibi çekirdekler de uyarılmış durumlara sahip olabilir. Bu durumlardan birine geçiş, eylem altında mümkündür. dış enerji. Buna göre, uyarımın giderilmesi aynı enerjinin radyasyonu ile gerçekleşir. Atomların aksine, nükleer geçişlerin karakteristik enerjileri birkaç MeV (1 MeV = 106 eV) mertebesindedir. Tanım enerji geçişleriçekirdekte kabuk modelinin kullanılması deneysel verilerle iyi bir uyum içindedir.
Böylece, dikkate alınan modeller bir yandan gerçeğe yakın olarak kabul edilebilir, çünkü deneysel olarak doğrulandı. Öte yandan birbirleriyle çelişiyorlar. Düşme modeli çerçevesinde nükleonların birbirleriyle etkileştiği (çarpıştığı) kabul edilirken, kabuk modeli çerçevesinde nükleonlar birbirinden bağımsız olarak kuvvet alanında hareket eder. Yoğun bir şekilde paketlenmiş bir çekirdekte bile, Pauli dışlama ilkesi nedeniyle nükleon-nükleon çarpışmaları yoktur. Bir çarpışmada, bir nükleon enerjisini başka bir nükleona aktararak daha düşük enerjili bir duruma geçerken, ikinci nükleon daha yüksek enerjili bir duruma geçmelidir. Bununla birlikte, tüm düşük enerji durumları zaten işgal edilmiştir ve bu tür bir enerji transferi ancak Pauli ilkesi ihlal edilirse, yani. gerçekleşemez.
Çok farklı yaklaşıma rağmen, hem sıvı damla modeli hem de çekirdeğin kabuk modeli, çekirdeğin çok sayıda özelliğini açıklamayı mümkün kılar. Son zamanlarda, bu modellerin her birinin esasına sahip teoriler oluşturmak için başarılı girişimlerde bulunulmuştur. En başarılılarından biri genelleştirilmiş model damla ve kabuk modellerinin ilkelerini birleştiren .
nükleer kuvvetler
Bahsedilen nükleer kuvvetler, denilen temel etkileşimlerden birini karakterize eder. güçlü etkileşim. 4 tür temel etkileşim vardır - azalan kuvvet sırasına göre: güçlü, elektromanyetik, zayıf ve yerçekimi (ikincisi evrenseldir ve herhangi bir parçacık arasında hareket eder, ancak mikro parçacıklar dünyasında önemli bir rol oynamaz).
Nükleer kuvvetler kuvvettir cazibe. Oldukça etkileyici Coulomb itme gücüne rağmen nükleonları çekirdekte tutan onlardır. 0,5 Fermi'den daha küçük mesafelerde, çekimin yerini itme alır, böylece çekirdekteki nükleonlar birbirine yapışmaz.
Nükleer kuvvetler kısa mesafe– bu, yalnızca çok kısa mesafelerde (~ 10-15 m) çalıştıkları anlamına gelir. Bu nedenle, normal koşullar altında, farklı atomların çekirdekleri birbirini "fark etmez".
Farklı nükleon çiftleri arasında ortaya çıkan tüm kuvvetler aynıdır. Şarj Bağımsızlığı nükleer kuvvetler- bu, nükleer etkileşimin elektrostatik olmayan bir yapıya sahip olmasının bir sonucudur. Nükleer kuvvetin büyüklüğü, nükleon üzerinde bir elektrik yükünün varlığına veya yokluğuna bağlı değildir.
nükleer kuvvetler merkezi değil iki nükleonu birbirine bağlayan düz bir çizgi boyunca yönlendirildikleri gibi temsil edilemezler.
Nükleonlar arasındaki etkileşim kuvvetlerinin özelliği doyma. Bu, her nükleonun sınırlı sayıda komşu nükleonla etkileşime girdiği anlamına gelir. Coulomb itmesi çekirdeğin tüm hacmi üzerinde önemli olduğundan, ağır çekirdeklerdeki nötronlar bu itmeyi tam olarak telafi edemezler. Bu nedenle, doğada 209'dan fazla nükleon içeren ve 83'ten fazla proton içermeyen kararlı çekirdek yoktur.Periyodik tablodaki son kararlı elementin seri numarası 83'tür - bu bir bizmut izotopudur. Tüm ağır çekirdekler radyoaktiftir, emisyonla kendiliğinden daha hafif çekirdeklere dönüşürler. α -parçacıklar.
Çekirdekteki nükleonlar arasındaki etkileşim, π mezonları adı verilen özel parçacıkların değişimi yoluyla gerçekleştirilir. Bu nedenle, bu etkileşim değişim karakteri. Serbest durumdaki tüm π-mezonlar, elektrik yükü, kütle ve ömür açısından birbirinden farklı olan üç gruba ayrılır: π 0 , π + , π – . Serbest durumda olmak, aşağıdaki özelliklere sahiptir:
m π±= 273.2 ben, elektrik şarjı q= ± e, ömür τ = 2,6 10 –8 sn,
m π0 = 264.2 ben, elektrik şarjı q= 0, ömür boyu τ = 1,9 10 –16 sn,
nerede ben elektronun kütlesidir.
Protonlar ve nötronlar baryon yüküne sahiptir. B= +1. π mezonların baryon yükü yoktur ( AT= 0), bu nedenle, bu parçacıkların değişimi sırasında nükleonların baryon yükü korunur, doğanın temel bir yasasıdır.
İki nükleon arasında bir etkileşim varsa bu, bu iki nükleonun birbirleriyle sürekli olarak diğer parçacıkları değiştirdiği anlamına gelir. Böylece, nükleonlar ve protonlar sürekli olarak yayar ve emer. π mezonlar, daha doğrusu:
a) bir nötron, yayan π – -meson, negatif bir elektrik yükünü kaybeder ve nötrden pozitif yüklü bir nükleona dönüşür, yani. bir protona; nötron sırasıyla sadece absorbe edebilir π + -meson, bir protona dönüşüyor;
b) proton, aksine, sadece yayar π + -meson, sırasıyla, pozitif yüklü bir nötr nükleondan döner, yani. bir nötrona; sadece bir protonu emebilir π – -meson, böylece elde negatif yük, kendi pozitifliğini telafi ederek ve bir nötron haline gelerek;
c) protonlar ve nötronlar da yayabilir ve soğurabilir π 0 -meson, karşılıklı dönüşümler gerçekleşmezken - proton bir proton, nötron - bir nötron olarak kalır.
π mezonları nükleondan nükleona o kadar hızlı geçer ki onları geçiş durumunda görmek imkansızdır. Onları kaydetmek için, muazzam enerji gerektiren çekirdeğin bütünlüğünü yok etmek gerekir.
π-mezon değişimi teorisi, aşağıdakileri içeren bir takım avantajlara sahiptir: 1) kısa menzilli nükleer kuvvetlerin varlığının açıklaması, 2) nükleer kuvvetlerin etkisinin büyüklükten bağımsızlığının nedeninin açıklaması ve elektrik yükünün işareti. Aynı zamanda, 0.2 Fermi'den daha küçük mesafelerde nükleonlar arasında itici kuvvetlerin ortaya çıkmasının fiziksel nedeni henüz açıklanmadı, nükleer kuvvetlerin doygunluğunun fiziksel nedeni açıklanmadı ve nükleon dönüşünün etkisi aralarındaki etkileşimin özellikleri dikkate alınmamıştır. Sonuç olarak, nükleer kuvvetlerin doğası üzerine çalışmalar devam etmektedir.
Atom çekirdeğinin özellikleri, bileşimlerine ve yapılarına göre belirlenir.
1) çekirdekteki proton ve nötron sayıları;
2) bu parçacıkların özellikleri; aralarındaki etkileşimin doğası;
3) çekirdeğin içindeki proton ve nötronların göreceli düzeni ve hareketi.
Çekirdeklerin bileşenleri olarak protonlar ve nötronlar birleşir yaygın isim- nükleonlar; çekirdekteki nükleon sayısıdır.
Çekirdekler genellikle şemaya göre çekirdeğin içeriğini gösteren sayılarla donatılmış elementin kimyasal sembolü ile gösterilir.
Örneğin, 11 proton ve 12 nötron içeren bir sodyum çekirdeği şöyle yazılır:
267'si stabil olan yaklaşık 1300 çekirdek bilinmekte ve çalışılmaktadır. Kararlı çekirdeklerin çoğu çift değerlere sahiptir.Bunlardan 159'u çift-çift, yani hem çift hem de çekirdekleri çift-tek tek-çift ve sadece 5 kararlı çekirdek tek-tek:
(ancak vanadyum çok uzun bir yarı ömre sahiptir - yaklaşık yıl). Bu bilgi, kararlı çekirdeklerin iç yapısını tamamlarken proton ve nötron sayılarının paritesinin büyük önem taşıdığını göstermektedir. Şu özelliklere sahip çekirdekler:
1) aynı fakat farklı olanlara izotop denir;
2) aynı fakat farklı olanlara izotop denir;
3) farklı ama aynı olana izobar denir. Ek olarak, aynı bileşime sahip ancak bazı özelliklerde, özellikle yarı ömürlerde farklılık gösteren çekirdekler olabilir. Bu tür çekirdeklere izomer denir.
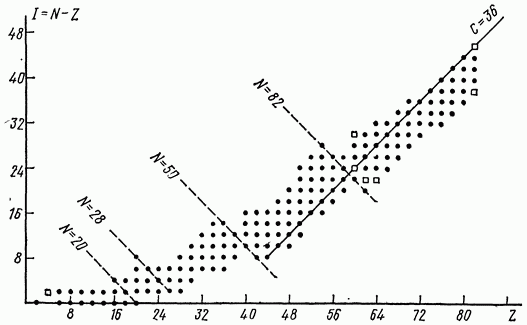
Araştırma ekipmanlarında çekirdekler, özellikle ağır olanlar, çevreleriyle birlikte incelenir. elektron kabuğu. Bunu göz önünde bulundurarak, yeni bir nüklid terimi tanıtıldı - yükünü nötralize eden bir elektron kabuğu ile birlikte bir çekirdek. bir atom var kimyasal kavram; çoğu durumda, bir kimyasal element bir izotop karışımıdır (dolayısıyla nötr atomlar, aynı sayıda protona sahip nüklidlerin bir karışımıdır).
Sayı, çekirdekteki nötron fazlalığını gösterir. Negatif bir değere sahip sadece bir çekirdek vardır (helyum-3 çekirdeklerin geri kalanına sahiptir, nötronların fazlalığı pozitif bir sayıdır ve artan atom numarası ile artar. Şekil IV. 100, kararlı çift-çift çekirdeklerin dağılımını gösterir. Kareler, yarı ömrü çok büyük (104 yıl veya daha fazla) radyoaktif çekirdekleri gösterir. Aynı sayıda nötrona (izotop) sahip çekirdekler, koordinat eksenlerine 45°'lik bir açıyla çizilen düz çizgiler üzerinde bulunur. N = 20, 28, 50 ve 82'ye karşılık gelen bu tür sadece birkaç çizgi çizilir. Çizgilere dik düz çizgiler üzerinde bulunan çekirdekler aynı büyüklük değerine sahiptir (C, nötron sayısıdır.
çekirdeğe eklenmelidir, böylece içindeki nötron sayısı proton sayısının iki katı olur). Pirinç. IV. 100, çekirdek ailelerinin ailelerden daha fazla olduğunu ve
Birinin proton sayısı diğerinin nötron sayısına eşit olan iki çekirdek
aynalar denir. Bunlar, örneğin,
19 çift ayna çekirdeği vardır; bu çiftlerin 16'sında bir çekirdeğin kararlı, ikincisinin radyoaktif olması karakteristiktir (diğer üç çiftte her iki çekirdek de radyoaktiftir).
Proton veya nötron sayısının 2, 8, 20, 28, 50, 82 (ve nötronlar için de 126) olduğu çekirdekler çok yaygındır ve komşu çekirdekler arasında ana özelliklerinde keskin bir şekilde öne çıkar. Bu çekirdeklere sihirli denir. Her iki sayının da sihirli olduğu çekirdeklere ikili büyü denir; bunlar arasında, örneğin,
Örneklemek için, doğal element - kromdaki izotopların nispi içeriğini çeşitli değerlerde sunuyoruz.
En basit atomun çekirdeği olan hidrojen atomu bir taneden oluşur. temel parçacık proton denir. Diğer tüm atomların çekirdeği, protonlar ve nötronlar olmak üzere iki tür parçacıktan oluşur. Bu parçacıklara nükleon denir. Proton. Protonun yükü ve kütlesi vardır
Karşılaştırma için, bir elektronun kütlesinin eşit olduğunu belirtiyoruz.
(66.1) ve (66.2) karşılaştırmasından, -protonun yarıya eşit bir dönüşe ve kendi manyetik momentine sahip olduğu sonucu çıkar.
![]()
Nükleer magneton adı verilen bir manyetik moment birimi. (33.2) ile karşılaştırıldığında, Bohr magnetonundan 1836 kat daha az olduğu sonucuna varılır. Sonuç olarak, protonun içsel manyetik momenti, elektronun manyetik momentinden yaklaşık 660 kat daha azdır.
Nötron. Nötron, 1932'de İngiliz fizikçi D. Chadwick tarafından keşfedildi. Elektrik yükü sıfırdır ve kütlesi
protonun kütlesine çok yakındır.
Nötron ve proton kütleleri arasındaki fark 1.3 MeV'dir, yani.
Nötron, yarıya eşit bir dönüşe ve (elektrik yükü olmamasına rağmen) kendi manyetik momentine sahiptir.
![]()
(eksi işareti, içsel mekanik ve manyetik momentlerin yönlerinin zıt olduğunu gösterir). Bu şaşırtıcı gerçeğin bir açıklaması § 69'da verilecektir.
Deneysel değerlerin oranının büyük ölçüde doğruluk -3/2'dir. Bu, ancak teorik olarak böyle bir değer elde edildikten sonra fark edildi.
Serbest durumda, nötron kararsızdır (radyoaktif) - kendiliğinden bozunur, bir protona dönüşür ve bir elektron ve bir antineutrino adı verilen başka bir parçacık yayar (bkz. § 81). Yarı ömür (yani, orijinal nötron sayısının yarısının bozunması için geçen süre) yaklaşık 12 dakikadır. Bozunma şeması aşağıdaki gibi yazılabilir:
![]()
Antineutrino'nun kütlesi sıfırdır. Bir nötronun kütlesi bir protonun kütlesinden daha büyüktür Bu nedenle, nötronun kütlesi denklemin (66.7) sağ tarafında görünen parçacıkların toplam kütlesini, yani 0.77 MeV'yi aşıyor. Bu enerji, formdaki bir nötronun bozunması sırasında serbest bırakılır. kinetik enerji oluşan parçacıklar.
Atom çekirdeğinin özellikleri. Atom çekirdeğinin en önemli özelliklerinden biri yük sayısı Z'dir. Çekirdeği oluşturan protonların sayısına eşittir ve eşit olan yükünü belirler Z sayısı kimyasal elementin sıra sayısını belirler Mendeleev'in periyodik tablosunda. Bu nedenle, çekirdeğin atom numarası olarak da adlandırılır.
Çekirdekteki nükleon sayısı (yani toplam proton ve nötron sayısı) A harfi ile gösterilir ve çekirdeğin kütle numarası olarak adlandırılır. Çekirdekteki nötron sayısı ise
Çekirdekleri belirtmek için kullanılan sembol
burada X, elementin kimyasal sembolüdür. Kütle numarası sol üstte, atom numarası sol altta yer alır (son simge genellikle atlanır).
Bazen kütle numarası kimyasal element sembolünün soluna değil sağına yazılır.
Aynı Z'ye sahip ancak farklı A'ya sahip çekirdeklere izotop denir. Çoğu kimyasal elementin birkaç kararlı izotopu vardır. Örneğin oksijenin üç kararlı izotopu vardır: kalayda on tane vb.
Hidrojenin üç izotopu vardır:
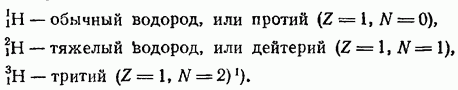
Protium ve döteryum stabildir, trityum radyoaktiftir.
Aynı kütle numarası A olan çekirdeklere izobar denir. Aynı sayıda nötrona sahip çekirdeklere örnek olarak izoton denir.Son olarak, aynı Z ve A'ya sahip, yarı ömürleri farklı olan radyoaktif çekirdekler vardır. Bunlara izomer denir. Örneğin, çekirdeğin iki izomeri vardır, bunlardan birinin yarı ömrü 18 dakika, diğerinin yarı ömrü 4.4 saattir.
Z veya A veya her ikisinde de farklılık gösteren yaklaşık 1500 çekirdek bilinmektedir. Bu çekirdeklerin yaklaşık 1/5'i kararlı, geri kalanı radyoaktiftir. Nükleer reaksiyonlar kullanılarak yapay olarak birçok çekirdek elde edildi.
Doğada, teknetyum ve prometyum hariç 1'den 92'ye kadar Z atom numarasına sahip elementler vardır.Plütonyum, yapay olarak elde edildikten sonra, doğal bir mineral - reçine harmanında ihmal edilebilir miktarlarda bulunmuştur. Transuranyum (yani, transuranyum) elementlerinin geri kalanı (Z ile 93 ila 107 arasında) çeşitli nükleer reaksiyonlar yoluyla yapay olarak elde edildi.
Transuranyum elementleri curium, einsteinium, fermium) ve mendelevium) seçkin bilim adamları P. ve M. Curie, A. Einstein, E. Fermi ve D. I. Mendeleev'in onuruna adlandırıldı. Lawrencium, adını siklotron E. Lawrence'ın mucidinden almıştır. Kurchatovy) adını seçkin Sovyet fizikçisi I. V. Kurchatov'un onuruna aldı.
Kurchatovium ve 106 ve 107 numaralı elementler de dahil olmak üzere bazı transuranyum elementleri, Sovyet bilim adamı G. N. Flerov ve işbirlikçileri tarafından Dubna'daki Ortak Nükleer Araştırma Enstitüsü'nün Nükleer Reaksiyonlar Laboratuvarında elde edildi.
Çekirdek boyutları. İlk yaklaşımda, çekirdek, yarıçapı formülle oldukça doğru bir şekilde belirlenen bir küre olarak kabul edilebilir.
(Fermi, nükleer fizikte kullanılan uzunluk biriminin adıdır, cm'ye eşittir). Formül (66.8)'den, çekirdeğin hacminin, çekirdekteki nükleon sayısıyla orantılı olduğu sonucu çıkar. Böylece, tüm çekirdeklerdeki maddenin yoğunluğu yaklaşık olarak aynıdır.
Çekirdeğin dönüşü. Nükleonların dönüşleri, çekirdeğin sonuçtaki dönüşüne eklenir. Nükleonun spini bu nedenle kuantum sayısı nükleer spin l, tek sayıda nükleon A için yarı tamsayı ve hatta A için tamsayı veya sıfır olacaktır. Çekirdek l'nin dönüşleri birkaç birimi geçmez. Bu, çekirdekteki çoğu nükleonun dönüşlerinin antiparalel olarak birbirini iptal ettiğini gösterir. Tüm çift-çift çekirdekler (yani, çift sayıda proton ve çift sayıda nötron içeren çekirdekler) sıfır dönüşe sahiptir.