Yuzaki hodisalar bunga misoldir. Boshqa lug'atlarda "Yuza hodisalari" nima ekanligini ko'ring
Yuzaki Hodisalar
Yuzaki Hodisalar
Ortiqchalik tufayli yuzaga kelgan hodisalar erkin energiya chegara qatlamida - sirt energiyasi, sirt qatlami molekulalarining faolligi va orientatsiyasi kuchayishi, uning tuzilishi va tarkibining xususiyatlari. P. i. kimyo ekanligi bilan ham aniqlanadi. va jismoniy jismlarning ta'siri birinchi navbatda sirt qatlamlarida sodir bo'ladi. Asosiy P. i. sirt maydoniga mutanosib ravishda sirt energiyasining pasayishi bilan bog'liq. Shunday qilib, suyuq tomchilar yoki gaz pufakchalarining muvozanat shakllarining shakllanishi, shuningdek, ularning o'sishi davomida kristallar doimiy oqimdagi minimal erkin energiya bilan belgilanadi. hajmi. P. I., molekulyar kuchlarning birgalikdagi ta'siridan kelib chiqadi ( sirt tarangligi va namlash) va ext. kuchlar (tortishish) va suyuqlik interfeyslarining egriligiga olib keladigan, deyiladi. kapillyar hodisalar.
P. i. televizorda. jismlar birinchi navbatda tashqi muhitda joylashadi. tana yuzasi. Bularga quyidagilar kiradi: yopishish (birikish), (yopishish), ishqalanish. Kristalning minimal erkin sirt energiyasi shartlaridan, parchalanish bo'yicha. tarangligi har xil bo'lgan yuzlari matematik jihatdan kristalning barcha mumkin bo'lgan shakllari olinadi. ko'p yuzli geomda o'rganilgan. kristallografiya.
P. i. ichki qismida sodir bo'ladi. kristall nuqsonlar asosida rivojlanayotgan yuzalar. panjaralar. Televizorning har qanday buzilishi. tanasi, uning kuchini yengish bilan bog'liq, mohiyatan P. I., chunki u yangi interfeysning shakllanishida ifodalanadi. da joylashgan dastlab bir hil muhitda yangi faza yadrolarining shakllanishi va rivojlanishi metastabil holat, shuningdek, P. I tomonidan belgilanadi. (bu kichik tomchilar va kristallarning eruvchanligining oshishi va ular ustidagi bosimning oshishi bilan bog'liq to'yingan bug '; (qarang: KELVIN TENGLAMA)).
vositalari. guruh P.I. adsorbsion hodisalarni tashkil qiladi, bunda kimyoviy o'zgaradi. sirt qatlamining tarkibi (qarang: ADSORPTION). Bu hodisalar guruhi dek. faollashtirilgan va kimyo holatlari. adsorbsiya, sirt kimyosiga aylanishi. kimyoviy sirt qatlami shakllanishi bilan reaktsiyalar. ulanishlar. Bunga diff kiradi. Topochem. (masalan, uning tuzlari eritmasidan metallni qaytarganda yuzalarda metall nometall hosil bo'lishi, qizdirilgan yuzalarda shkala hosil bo'lishi va boshqalar). Kimyosorbsion monomolekulyar qatlamlarning hosil bo'lishi tanadagi monomolekulyar-yuzaki yorug'lik va uning ta'sirining tabiatini o'zgartirishning samarali usuli hisoblanadi. muhit. Adsorbsion qatlamlar emulsiyalar, ko'piklar, suspenziyalarning barqarorligini sezilarli darajada oshirishi mumkin, bu chegarada strukturaviy va mexanik bilan bog'liq. bu qatlamlarning azizlari (yuqori, elastiklik va quvvat).
Sirt qatlamlarida issiqlik harakatining xususiyatlari iskalaga olib keladi. yorug'likning sirtlar tomonidan tarqalishi. Boshqa hodisalar guruhiga quyidagilar kiradi: termion emissiya, potentsial sakrashlarning paydo bo'lishi va interfeysda qo'sh elektr qatlamining shakllanishi. Bu P.I. ionlar va dipol molekulalarining adsorbsiyasi bilan bog'liq. P. i. termodinamikaga ta'sir qiladi. fazalar muvozanati faqat kolloid tizimlarda ularning ajralish yuzasi juda rivojlangan taqdirdagina. Issiqlik uzatish va massa almashish jarayonlarining tezligi - erish, kondensatsiya, heterojen kimyo. jarayonlar (masalan, korroziya) - kattaligi va Sankt bilan belgilanadi siz interfeysi va shuning uchun keskin iskala bog'liq. bu sirtning tabiati va tuzilishi. Adsorbsion qatlamlar mavjudotlarni chaqirishi mumkin. o'zgarishi, interfaal almashinuv jarayonlarini sekinlashtiradi. Masalan, ba'zi sirt faol moddalarning mono qatlamlari. suv yuzasida setil spirti uning bug'lanishini sezilarli darajada sekinlashtirishi mumkin. Xuddi shu narsa ta'siri ostida korroziya jarayonlarining sekinlashishi sirt qatlamlari ingibitorlar yoki oksidlarning himoya plyonkalari va boshqalar kimyoviy. metall yuzasida birikmalar.
P. i. interfeyslarning harakati (tomchilar, pufakchalar va suyuqlik oqimlari, tomchilarga bo'linish, kapillyar) paytida chegara sharoitlarining xususiyatlarini aniqlash. Adsorbsion fillar sirt tarangligidagi mahalliy farqlarning paydo bo'lishi, ya'ni chegara gidrodinamikasining o'zgarishi tufayli kapillyar to'lqinlarning susayishiga olib keladi. sharoitlar.
P. i. ma'lum bir muhitda materiallar va tuzilmalarning chidamliligini aniqlash. Nafaqat erish va korroziya, balki qayta tiklanadigan korroziya ham deformatsiyalarni bartaraf etish va qattiq moddalarning yo'q qilinishiga olib keladi. jismlar, yangi sirtlarni shakllantirish ishini kamaytiradi. Kichik aralashmalar ichkariga singib, monomol hosil qiladi. interfeyslardagi qatlamlar ko'pchilikni boshqarishga imkon beradi. Aziz siz materiallar. Monomolekulyar sirt qatlamlarini o'rganish molekulalarni o'rganish va ularning o'lchamlarini aniqlashning yangi usullariga olib keladi. P. i. tog' jinslarining parchalanishi va tuproq hosil bo'lishi, namlikning bug'lanishi va kondensatsiyasi va boshqalarni aniqlash. tirik organizmlardagi jarayonlar. P.dan foydalanish boʻyicha I. ko'plab texnologik asoslarni yaratdi jarayonlar (moylash, namlash, flotatsiya va boshqalar).
Jismoniy ensiklopedik lug'at. - M.: Sovet Entsiklopediyasi. . 1983 .
Yuzaki Hodisalar
-
hodisalar, adsorbsiya, sirt energiyasining paydo bo'lishi, sirt tarangligi, sirt elektr. Yuzaki qatlamlar molekulyar o'lchamlar shkalasi bo'yicha heterojen bo'lib, fazalarning agregatsiya holatidan qat'i nazar, anizotropdir; ular fizikaning ommaviy fazalaridan farq qiladi. xossalari (zichlik, yopishqoqlik, kristallar va bo'shliqlar mikroskopikdir. Sirtda ikki o'lchovli fazali o'tishlar mavjud bo'lganda, shuningdek, sirtlarning kesishmasida interfaza chiziqlari hosil bo'ladi - fazalararo sirtlarning bir o'lchovli analoglari, chiziqli hodisalar. mavjudligi bilan bog'liq.Bir hil bo'lmagan chiziqli mintaqa sirt qatlamining bir o'lchovli analogi bo'lib, chiziqli taranglikka, chiziqli erkin energiyaga va boshqalarga ega. Masofaviy chiziqli termodinamik potentsiallar sirt birliklaridan faqat birlik uzunligiga tegishliligi bilan farq qiladi. (J/m bilan o'lchanadi).Chiziqli hodisalar faqat juda kichik jismlar uchun ahamiyatlidir (ikki o'lchovli fazalar yadrolari, . P.).
P.I. qoidalari. Laplas qonuni va Yang tenglamasi bilan tavsiflanadi (qarang. namlash), shuningdek, umumiy Gibbs ur-Niemadsorbtsiyasi:
kesish orqali sirt birligini shakllantirish ishi qayerda (qarang. sirt tarangligi), - uradi entropiya (qarang Yuzaki energiya), - sirt taranglik tenzori, - birlik tenzori, - tensor deformatsiyalar(“:” belgisi tenzorlarning skalyar ko‘paytmasini bildiradi),- kimyoviy potentsiallar
molekulalar (yoki ionlarning elektrokimyoviy potentsiallari), G i- ularning adsorbsiyasi, yig'indisi barcha komponentlar bo'yicha amalga oshiriladi, buning uchun massa fazasi va sirt qatlami o'rtasida muvozanat bo'lishi mumkin. Suyuq yuzalar uchun - sirt tarangligi va deformatsiya. a'zosi yo'qolgan. Gibbsning adsorbsiyasi ur-siyasi eng muhim P.I. o'rtasidagi aloqani o'rnatadi. - adsorbsiya va sirt faolligi (qarang sirt faol moddalar).
Muhim ta'sir P.I. makrotizimlarning xossalari. Bu bunday tizimlarda sirt maydonining ko'payishi, kapillyar hodisalar bilan bog'liq. Faqat egri sirtlari bo'lgan geterogen tizimda Gibbs faza qoidasi uning klassikasida dispers tizimlarning barqarorligiga hissa qo'shadigan yupqa plyonkalarning takoz bosimi (o'z belgisi bilan) (plyonkadagi tashqi bosim va bir vaqtning o'zida plyonkaning tarkibiy qismlaridan tashkil topgan ommaviy fazadagi bosim o'rtasidagi farq sifatida aniqlanadi). plyonkadagi kabi harorat va kimyoviy qiymatlar.P.I.ning muhim guruhi elektrosirt hodisalari: sirt, sirt elektr, emissiya va boshqalar. Ularning barchasi interfeysdagi hosil bo'lish bilan bog'liq. ikki qavatli elektr qatlami emissiya natijasida yoki o'ziga xos. P.I.ga. bog'lash birlashish, yopishish, gözenekli jismlarni namlash, moylash va yuvish, ishqalanish, emdirish. P. i. ta'sir qiladi (masalan, adsorbsiya kuchini pasaytirish - Rehbinder effekti). P. i. fazali jarayonlarda muhim rol o'ynaydi. ular orasidagi issiqlik va massa uzatish tezligi. Yuzaki qatlamlar va plyonkalarning o'tkazuvchanligi, ularning molekulyar tuzilishi bilan bog'liq bo'lib, biolda ayniqsa muhim bo'lgan membrana hodisalarini keltirib chiqaradi. tizimlari. Lit.: Rusanov A.I., Fazaviy muvozanat va sirt hodisalari, L., 1967; Adameon A., Fizik kimyo yuzalar, LEKIN. I. Rusanov.
Jismoniy ensiklopediya. 5 jildda. - M.: Sovet Entsiklopediyasi. Bosh muharrir A. M. Proxorov. 1988 .
Boshqa lug'atlarda "SURFACE FENOMENA" nima ekanligini ko'ring:
Zamonaviy entsiklopediya
Yuzaki hodisalar- Yuzaki Hodisalar, maxsus jismoniy va tufayli kimyoviy xossalari jismlar chegarasidagi yupqa materiya qatlamlari (o'rtalar, fazalar). Eng muhim sirt hodisasi adsorbsiyadir. Materiallarning mustahkamligi va chidamliligini aniqlang. Sirt bilan ... Illustrated entsiklopedik lug'at
Jismni tashkil etuvchi zarralar orasidagi o'zaro ta'sir kuchlari uning yuzasida kompensatsiyalanmaganligi bilan bog'liq hodisalar guruhi. Yuzaki hodisalarga sirt tarangligi, kapillyar hodisalar, sirt faolligi kiradi ... Katta ensiklopedik lug'at
sirt hodisalari- - jismoniy kimyoviy hodisalar, interfeys yaqinida erituvchi va erigan moddalar molekulalarining notekis taqsimlanishi tufayli. umumiy kimyo: darslik / A.V.Jolnin ... Kimyoviy atamalar
Yuzaki Hodisalar- sirt qatlamida, muhitlar orasidagi interfeyslarda yuzaga keladigan va sirt qatlami molekulalarining faolligi va orientatsiyasining kuchayishi, uning tuzilishi va tarkibining xususiyatlari, shuningdek kimyoviy ta'siridan kelib chiqadigan hodisalar. va jismoniy o'zaro ta'sirlar ... Katta politexnika entsiklopediyasi
fizika. kimyo. suyuqliklar va qattiq jismlarning sirt qatlamlarining maxsus (quyma bilan solishtirganda) xususiyatlariga bog'liq bo'lgan hodisalar. Naib. Bu qatlamlarda umumiy va muhim sv - ortiqcha svob. energiya F \u003d sS, bu erda s - sirt (interfasial) kuchlanish, ... ... uchun. Kimyoviy entsiklopediya
Yuzaki hodisalar fazalar interfeysidagi nozik materiya qatlamlarining maxsus xossalari bilan bog'liq hodisalar to'plami. Yuzaki hodisalarga interfeysda, oraliq yuzada sodir bo'ladigan jarayonlar kiradi ... ... Vikipediya
Yuzaki qatlamlarning, ya'ni jismlar (media, fazalar) orasidagi interfeysdagi nozik materiya qatlamlarining maxsus xususiyatlarini ifodalash. Bu xususiyatlar sirt qatlamining ortiqcha erkin energiyasi (qarang. Erkin energiya), uning xususiyatlari ... ... Buyuk Sovet Entsiklopediyasi
Yuzaki- ikkita aloqa vositasi o'rtasidagi interfeys
Yuzaki hodisalar- qo'shni moddalar chegarasida fizik va kimyoviy xossalarga bog'liq hodisalar majmui.
Ya'ni, bular sirt energiyasi tufayli yuzaga keladigan hodisalardir.
Materialning er osti qatlamlari quyi tizim sifatida qaraladi umumiy tizim deformatsiyalanadigan material.
Maxsus sirt maydoni: S urish = S/V
Yuzaki hodisalarga quyidagilar kiradi:
2) kapillyar hodisalar(suyuqlikning boshqa muhit bilan chegarasida, uning sirtining egriligi bilan bog'liq bo'lgan sirt hodisalari)
Laplas funktsiyasi (kapillyar bosim formulasi) P = s(dS/dV)
3) yopishish(bir fazadagi moddaning boshqa fazaga yopishishini tavsiflaydi) va uyg'unlik(bir xil jismning qismlarini yopishishi (suyuq yoki qattiq))
4) ishqalanish
5) adsorbsiya va desorbsiya hodisalari
Gibbs adsorbsion tenglamasi: D = -(∂s/∂m) T
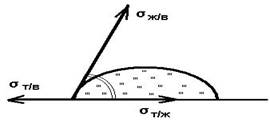
6) namlash(uchunchi faza, gaz (bug ) yoki birinchi bilan aralashmaydigan boshqa suyuqlik mavjud bo'lganda suyuqlik qattiq jism bilan aloqa qilganda kuzatiladigan sirt hodisasi. Xususiyat namlash - uch fazali aloqa liniyalarining mavjudligi (namlash liniyalari).
Namlanishning asosiy termodinamik xarakteristikalari muvozanat ho'llash burchagi q 0 , yopishish ishi W a , ho'llash issiqligi q W dir. Namlanishning muvozanatli aloqa burchagi suyuqlik (masalan, tomchilar) yuzasining u namlangan qattiq jism yuzasiga moyilligi bilan aniqlanadi; burchakning tepasi namlash chizig'ida. Muvozanatning aloqa burchagi Young tenglamasi bilan aniqlanadi:
cosq 0 \u003d (s s -s sl) / s sl,
qayerda s s va s sl - mos ravishda. qattiq jismning gaz bilan chegarasida va namlovchi suyuqlik bilan aloqada bo'lgan o'ziga xos sirt energiyasi, s l - suyuqlikning sirt tarangligi.
Yuzaki termodinamika:
sirt hodisalari odatda termodinamikaning birinchi va ikkinchi qonunlarining birlashgan tenglamasiga muvofiq tasniflanadi.
Bu tenglama quyidagicha yoziladi:
qayerda sdS – sirt energiyasi[J/m^2=N/m]
Yuzaki energiya - interfeysda to'plangan energiya, hajmdagi energiyaga nisbatan ortiqcha. Kristalli moddalar sirt energiyasi anizotropiyasi bilan tavsiflanadi: eng past sirt energiyasiga yuzlar ega eng yuqori zichlik zarralar.
Yuzaki taranglik: s = (dG/dS) T , p , ni
Ya'ni, sirt tarangligi muvozanatdagi ikki faza o'rtasidagi interfeysning termodinamik xarakteristikasi bo'lib, harorat, tizim hajmi va barcha kimyoviy potentsiallarni hisobga olgan holda, ushbu interfeysning birlik maydonining teskari izotermokinetik shakllanishi ishi bilan belgilanadi. ikkala fazadagi komponentlar doimiy bo'lib qoladi.
Sirt energiyasining minimal darajaga moyilligi suyuqlik yuzasining egriligiga olib keladi. Shuning uchun biz sirt energiyasi va shakl o'rtasida bog'liqlik mavjudligini taxmin qilishimiz mumkin.
Elektron xususiyatlar yuzalar ommaviy bo'lganlardan, xususan, elektron mavjudligi bilan farq qiladi sirt holatlari. Elektronlarning mos keladigan to'lqin funktsiyalari sirtdan masofa bilan eksponent ravishda parchalanadi.
Yupqa plyonkalar va filamentlar, tor teshiklar va teshiklar, tomchilar, kristallar va mikroskopik o'lchamdagi bo'shliqlar kabi sirt qatlamlari bilan bog'liq bo'lgan kichik (hech bo'lmaganda bir o'lchamdagi) ob'ektlar ham maxsus xususiyatlarga ega. Yupqa plyonkalar va monomolekulyar qatlamlarni o'rganish molekulalararo o'zaro ta'sirning tabiati va molekulalarning tuzilishi haqida ma'lumot beradi.
Ikki o'lchovli bo'lsa fazali o'tishlar, shuningdek, sirtlar kesishganda, interfasial chiziqlar hosil bo'ladi - interfasial yuzalarning bir o'lchovli analoglari, ularning mavjudligi chiziqli hodisalar bilan bog'liq. Bir hil bo'lmagan chiziqli mintaqa sirt qatlamining bir o'lchovli analogidir va chiziqli taranglikka, chiziqli erkin energiyaga va boshqalarga ega. Maxsus chiziqli termodinamik potensiallar sirtdan farq qiladi, chunki ular uzunlik birligiga (J / m bilan o'lchanadi) tegishlidir. Chiziqli hodisalar faqat juda kichik ob'ektlar (ikki o'lchovli fazalar yadrolari, namlovchi mikrotomchilar va boshqalar) uchun ahamiyatlidir.
Adsorbsiya va desorbsiya hodisalari
Gazlarni qattiq jismlarga adsorbsiyasida adsorbat va adsorbent molekulalarining o'zaro ta'sirini tavsiflash juda murakkab muammodir, chunki ularning adsorbsiya xarakterini belgilovchi o'zaro ta'sirining tabiati har xil bo'lishi mumkin. Shuning uchun muammo odatda ikkita ekstremal holatni ko'rib chiqish orqali soddalashtiriladi, bunda adsorbsiya fizik yoki kimyoviy kuchlar ta'sirida yuzaga keladi - mos ravishda fizik va kimyoviy adsorbsiya.
jismoniy adsorbsiya van der Vaals o'zaro ta'siri tufayli yuzaga keladi. U haroratning oshishi bilan teskari va adsorbsiyaning pasayishi bilan tavsiflanadi, ya'ni. ekzotermiklik va fizik adsorbsiyaning issiqlik effekti odatda adsorbatning suyuqlanish issiqligiga yaqin (10 – 80 kJ/mol). Bu, masalan, ko'mirga inert gazlarning adsorbsiyasi.
Kimyoviy adsorbsiya(xemisorbtsiya) tomonidan amalga oshiriladi kimyoviy o'zaro ta'sir adsorbent va adsorbat molekulalari. Xemisorbtsiya odatda qaytarilmas; kimyoviy adsorbsiya, fizik adsorbsiyadan farqli o'laroq, mahalliylashtirilgan; adsorbat molekulalari adsorbent yuzasida harakatlana olmaydi. Chunki kimyosorbtsiya kimyoviy jarayon, 40 - 120 kJ / mol darajasidagi faollashtirish energiyasini talab qiladigan haroratning oshishi uning paydo bo'lishiga yordam beradi. Kimyoviy adsorbsiyaga misol qilib kislorodning volfram yoki kumushga yuqori haroratda adsorbsiyasini keltirish mumkin.
Jismoniy va kimyoviy adsorbsiya hodisalari juda kam hollarda aniq farqlanadi. Oraliq variantlar odatda, adsorbsiyalangan moddaning asosiy qismi nisbatan zaif bog'langanda va faqat kichik qismi mustahkam bog'langanda amalga oshiriladi. Masalan, past haroratlarda metallardagi kislorod yoki nikeldagi vodorod fizik adsorbsiya qonuniyatlari bo’yicha adsorbsiyalanadi, lekin harorat ko’tarilishi bilan kimyoviy adsorbsiya sodir bo’la boshlaydi. Haroratning oshishi bilan ma'lum bir haroratdan kimyoviy adsorbsiyaning ortishi fizik adsorbsiyaning pasayishi bilan ustma-ust tusha boshlaydi, shuning uchun bu holda adsorbsiyaning haroratga bog'liqligi aniq belgilangan minimumga ega.
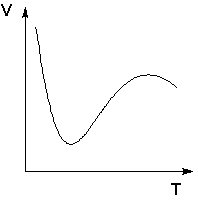
Nikel tomonidan adsorbsiyalangan vodorod hajmining haroratga bog'liqligi
Adsorbsiya turlari:
Lengmyorning monomolekulyar adsorbsiya nazariyasi
Amerikalik kimyogari I.Langmyur tomonidan ishlab chiqilgan monomolekulyar adsorbsiya nazariyasi quyidagi qoidalarga asoslanadi.
1) Adsorbsiya mahalliylashtirilgan va kimyoviy kuchlarga yaqin kuchlar ta'sirida yuzaga keladi.
2) Adsorbsiya adsorbentning butun yuzasida emas, balki faol markazlarda sodir bo'ladi, ular adsorbent yuzasida o'simtalar yoki bo'shliqlar deb ataladigan narsaning mavjudligi bilan tavsiflanadi. erkin valentliklar. Faol markazlar mustaqil (ya'ni, bitta faol markaz boshqalarning adsorbsion qobiliyatiga ta'sir qilmaydi) va bir xil hisoblanadi.
3) Har bir faol markaz faqat bitta adsorbat molekulasi bilan ta'sir o'tkazishga qodir; natijada sirtda adsorbsiyalangan molekulalarning faqat bitta qatlami hosil bo'lishi mumkin.
4) Adsorbsiya jarayoni teskari va muvozanatli - adsorbsiyalangan molekula faol markaz tomonidan ma'lum vaqt ushlab turiladi, shundan so'ng u desorbsiyalanadi; shunday qilib, ma'lum vaqt o'tgach, adsorbsiya va desorbsiya jarayonlari o'rtasida dinamik muvozanat o'rnatiladi.
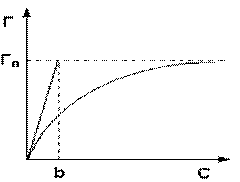
Monomolekulyar adsorbsiya izotermasi
Muvozanat holatida adsorbsiya tezligi desorbsiya tezligiga teng. Desorbsiya tezligi ishg'ol qilingan faol markazlar ulushiga (x) to'g'ridan-to'g'ri proportsionaldir va adsorbsiya tezligi adsorbat konsentratsiyasining mahsulotiga va erkin faol markazlarning ulushiga (1 - x) to'g'ridan-to'g'ri proportsionaldir:
Tenglamaning o'ng tomonidagi pay va maxrajni k A ga bo'lib, biz quyidagilarga erishamiz:

Adsorbsiyaning maksimal mumkin bo'lgan qiymati T o barcha faol markazlarni adsorbat molekulalari egallashi sharti bilan erishiladi, ya'ni. x = 1. Bundan kelib chiqadiki, x = r / r o.
Tenglama monomolekulyar adsorbsiya izotermasi bo‘lib, u G adsorbsion qiymatini adsorbat konsentratsiyasiga C bog‘laydi. Bu yerda b ma’lum adsorbent-adsorbat juftligi uchun qandaydir doimiy qiymat (desorbsiya va adsorbsiya tezligi konstantalari nisbati), son jihatdan adsorbat konsentratsiyasiga teng, faol markazlarning yarmi ishg'ol qilingan. Langmuir adsorbsion izotermining grafigi rasmda ko'rsatilgan. C = 0 nuqtada adsorbsion izotermaga teginish o'tkazish yo'li bilan b doimiyni grafik tarzda aniqlash mumkin.
Tenglamada gazlarning adsorbsiyasi jarayonini tavsiflashda konsentratsiyani proportsional qiymat bilan almashtirish mumkin. qisman bosim gaz:
Lengmyurning monomolekulyar adsorbsiya nazariyasi adsorbatning past bosimida (kontsentratsiyasida) gazlar va erigan moddalarning adsorbsiyasining ba'zi jarayonlarini tavsiflash uchun qo'llaniladi.
Polanyining polimolekulyar adsorbsiya nazariyasi
Amalda, ko'pincha (ayniqsa, bug'larning adsorbsiyasida) deb ataladigan narsalar mavjud. S-shaklidagi adsorbsion izotermalar, ularning shakli ma'lum bir bosim qiymatidan boshlab adsorbsiyalangan molekulalarning adsorbat bilan mumkin bo'lgan o'zaro ta'sirini ko'rsatadi.

Polimolekulyar adsorbsiya izotermasi
Bunday adsorbsion izotermalarni tavsiflash uchun M. Polyani quyidagi asosiy qoidalarga asoslangan polimolekulyar adsorbsiya nazariyasini taklif qildi:
1. Adsorbsiya sof jismoniy kuchlar ta’sirida yuzaga keladi.
2. Adsorbent yuzasi bir hil, ya'ni. unda faol markazlar yo'q; adsorbsion kuchlar adsorbent yuzasi yaqinida uzluksiz kuch maydoni hosil qiladi.
3. Adsorbsion kuchlar masofada harakat qiladi, kattaroq adsorbat molekulalari. Boshqacha qilib aytganda, adsorbent yuzasi yaqinida ma'lum bir adsorbsiya hajmi mavjud bo'lib, u adsorbsiya jarayonida adsorbat molekulalari bilan to'ldiriladi.
Sirt qatlamining atom tuzilishining xususiyatlari:
Qattiq jismlar yuzasiga yaqin joylashgan atom tuzilishining o'ziga xosligi sirtning bo'shashishi va qayta tiklanishi deb ataladigan narsada namoyon bo'ladi. Bo'shashish vaqtida sirtlarga parallel bo'lgan atom tekisliklarining tuzilishi massadagi kabi qoladi, lekin sirt yaqinidagi tekisliklar orasidagi masofalar o'zgaradi. Qayta qurish jarayonida sirtga yaqin hududdagi panjaraning simmetriyasi katta hajmdagidan keskin farq qiladi. Bu hodisa birinchi navbatda kovalent aloqaga ega bo'lgan kristallar uchun xarakterlidir (masalan, Si va Ge). Kovalent o'zaro ta'sirning yuqori anizotropik tabiati tufayli sirtning shakllanishi paytida panjara davriyligini buzish sirt yaqinidagi atomlararo bog'lanishlar geometriyasini tubdan o'zgartirishga olib keladi. Bir qator o'tish va olijanob metallarning sirtini qayta tiklash ham topildi.
Yuzaki bo'shashish - kristallning sirtga yaqin qatlamining modifikatsiyasi, bunda yuqori qatlamning atom tuzilishi hajmdagi mos keladigan atom tekisliklari bilan bir xil bo'lib qoladi, lekin birinchi va ikkinchi qatlamlar orasidagi masofa yoki ularning o'zaro joylashuvi bir-biridan farq qiladi. hajmdagilar.
Dam olish quyidagilarga bo'linadi normal va lateral, parallel yoki tangensial deb ham ataladi. Oddiy bo'shashish, yuqori qatlamning atom tuzilishi massadagi kabi bo'lgan holatga to'g'ri keladi, lekin yuqori va ikkinchi qatlamlar orasidagi masofa massadagi tekisliklar orasidagi masofadan farq qiladi (a-rasm). Uning sof shaklida metallarda normal bo'shashish kuzatiladi. Ko'pgina hollarda, birinchi qatlamlararo masofada pasayish kuzatiladi; chuqurroq qatlamlar uchun qatlamlararo masofaning ommaviy qiymatidan og'ish chuqurlik bilan kamayadi. Ba'zan sirtga parallel ravishda yuqori qatlamning bir xil siljishi ham mavjud (b-rasm); bu holda parallel yoki tangensial gevşeme haqida gapiradi. U asosan atomlar kontsentratsiyasi past bo'lgan yuqori indeksli tekisliklarda kuzatiladi.
Yuzaki hodisalar
Yuzaki hodisalar- fazalar interfeysidagi nozik materiya qatlamlarining maxsus xossalari bilan bog'liq hodisalar to'plami. Yuzaki hodisalarga fazalar chegarasida, fazalararo sirt qatlamida sodir bo'ladigan va konjugatsiyalangan fazalarning o'zaro ta'siri natijasida yuzaga keladigan jarayonlar kiradi.
Yuzaki hodisalar fazalararo chegaralardagi sirt qatlamlarida turli xil tarkib va kontakt fazalarining tuzilishi va shunga mos ravishda sirt atomlari va molekulalarining turli fazalar tomondan bog'lanishlaridagi farq tufayli atomlararo, molekulalararo kuchlarning to'yinmagan maydoni mavjud. Natijada, sirt qatlamlaridagi atomlar va molekulalar maxsus tuzilish hosil qiladi va modda turli xossalari bilan fazalar hajmida o'z holatidan farq qiladigan maxsus holatni oladi. Yuzaki hodisalarni kolloid kimyo o'rganadi.
Yuzaki hodisalarning tasnifi
Yuzaki hodisalar odatda asosiy energiya turlarini o'z ichiga olgan termodinamikaning birinchi va ikkinchi qonunlarining kombinatsiyalangan tenglamasiga muvofiq tasniflanadi. Har qanday heterojen tizim uchun uni quyidagi shaklda yozish mumkin:
Bu tenglama Gibbs energiyasining o'sishini boshqa turdagi energiyalarning algebraik yig'indisi orqali ko'rsatadi. Ko'rinib turibdiki, sirt energiyasi quyidagi energiya turlariga aylanishga qodir:
- Gibbs energiyasi
- kimyoviy energiya
- mexanik energiya
- Elektr energiyasi
Sirt energiyasining sanab o'tilgan energiya turlaridan biriga aylanishi ma'lum sirt hodisalariga mos keladi, masalan, dispersiya, yopishish va namlanishning o'zgarishi bilan reaktivlikning o'zgarishi, kapillyarlik, adsorbsiya, elektr hodisalari.
Yuzaki hodisalarning ahamiyati
Yuzaki hodisalar kimyoviy muhandislikda keng tarqalgan. Deyarli har qanday kimyoviy ishlab chiqarish dispers tizimlar va sirt hodisalari yordamida amalga oshiriladi. Qoida tariqasida, kimyoviy texnologiyadagi barcha heterojen jarayonlar da amalga oshiriladi maksimal sirt fazali aloqa. Buning uchun moddalar sistemalari suspenziyalar, kukunlar, emulsiyalar, tumanlar, changlar holatiga o'tkaziladi. Xom ashyo va oraliq mahsulotlarni maydalash, boyitish jarayonlari dispers tizimlarda boradi, ularda namlanish, kapillyarlik, adsorbsiya, cho'kish, koagulyatsiya kabi hodisalar muhim rol o'ynaydi. Kimyoviy texnologiyada g'ovak adsorbentlar va katalizatorlar keng qo'llaniladi. dispers tizimi qattiq dispersion muhit bilan.
Yuzaki hodisalarning borishi qonuniyatlari, xususan, strukturaning shakllanishi xizmat qiladi nazariy asos kerakli xususiyatlarga ega bo'lgan materiallarni olish: keramika, tsement, shisha-keramika, sorbentlar, katalizatorlar, polimerlar, kukunlar, dori-darmonlar va boshqalar.
Adabiyot
Frolov Yu.G. Xo'sh kolloid kimyo. - MChJ TID "Alliance", 2004. - 464 p. - ISBN 5-98535-003-7
Wikimedia fondi. 2010 yil.
Boshqa lug'atlarda "Yuza hodisalari" nima ekanligini ko'ring:
Sirt energiyasining chegaraviy qatlamida erkin energiyaning ortiqcha bo'lishi, sirt qatlami molekulalarining faolligi va orientatsiyasining kuchayishi, uning tuzilishi va tarkibining xususiyatlaridan kelib chiqadigan hodisalar. P. i. kimyo ekanligi bilan ham aniqlanadi. va jismoniy vz…… Jismoniy entsiklopediya
Zamonaviy entsiklopediya
Yuzaki hodisalar- YUZA HODISALARI jismlar chegarasidagi yupqa materiya qatlamlarining maxsus fizik-kimyoviy xossalari (omiyotlar, fazalar) bilan bog'liq. Eng muhim sirt hodisasi adsorbsiyadir. Materiallarning mustahkamligi va chidamliligini aniqlang. Sirt bilan ... Illustrated entsiklopedik lug'at
Jismni tashkil etuvchi zarralar orasidagi o'zaro ta'sir kuchlari uning yuzasida kompensatsiyalanmaganligi bilan bog'liq hodisalar guruhi. Yuzaki hodisalarga sirt tarangligi, kapillyar hodisalar, sirt faolligi kiradi ... Katta ensiklopedik lug'at
sirt hodisalari- - interfeys yaqinida erituvchi va erigan moddalar molekulalarining notekis taqsimlanishi natijasida yuzaga keladigan fizik-kimyoviy hodisalar. Umumiy kimyo: darslik / A.V.Jolnin ... Kimyoviy atamalar
Yuzaki Hodisalar- sirt qatlamida, muhitlar orasidagi interfeyslarda yuzaga keladigan va sirt qatlami molekulalarining faolligi va orientatsiyasining kuchayishi, uning tuzilishi va tarkibining xususiyatlari, shuningdek kimyoviy ta'siridan kelib chiqadigan hodisalar. va jismoniy o'zaro ta'sirlar ... Katta politexnika entsiklopediyasi
fizika. kimyo. suyuqliklar va qattiq jismlarning sirt qatlamlarining maxsus (quyma bilan solishtirganda) xususiyatlariga bog'liq bo'lgan hodisalar. Naib. Bu qatlamlarda umumiy va muhim sv - ortiqcha svob. energiya F \u003d sS, bu erda s - sirt (interfasial) kuchlanish, ... ... uchun. Kimyoviy entsiklopediya
Yuzaki qatlamlarning, ya'ni jismlar (media, fazalar) orasidagi interfeysdagi nozik materiya qatlamlarining maxsus xususiyatlarini ifodalash. Bu xususiyatlar sirt qatlamining ortiqcha erkin energiyasi (qarang. Erkin energiya), uning xususiyatlari ... ... Buyuk Sovet Entsiklopediyasi
Jismni tashkil etuvchi zarralar orasidagi o'zaro ta'sir kuchlari uning yuzasida kompensatsiyalanmaganligi bilan bog'liq hodisalar guruhi. Yuzaki hodisalarga sirt tarangligi, kapillyar hodisalar, sirt faolligi, ... ... ensiklopedik lug'at
Yuzaki Hodisalar- qo'shni jismlar orasidagi chegaradagi sirt qatlamlarining maxsus xususiyatlari bilan bog'liq hodisalar to'plami. Yuzaki hodisalar sirt energiyasining mavjudligi bilan bog'liq. Yuzaki hodisalarga sirt tarangligi, ... ... Metallurgiya lug'ati
Kitoblar
- Fizik kimyo. Yuzaki hodisalar va dispers tizimlar. Darslik, A. G. Morachevskiy. Fizik kimyo. Yuzaki hodisalar va dispers sistemalar: Uch. nafaqa, 2-nashr, o'chirilgan. ISBN: 978-5-81141-857-2…
Yuzaki hodisalar- fazalar interfeysidagi nozik materiya qatlamlarining maxsus xossalari bilan bog'liq hodisalar to'plami. Yuzaki hodisalarga fazalar chegarasida, fazalararo sirt qatlamida sodir bo'ladigan va konjugatsiyalangan fazalarning o'zaro ta'siri natijasida yuzaga keladigan jarayonlar kiradi.
Yuzaki hodisalar fazalararo chegaralardagi sirt qatlamlarida aloqa qiluvchi fazalarning har xil tarkibi va tuzilishi tufayli va shunga mos ravishda turli fazalardagi sirt atomlari va molekulalarining bog'lanishlaridagi farq tufayli yuzaga keladi. atomlararo, molekulalararo kuchlarning to'yinmagan maydoni. Natijada, sirt qatlamlaridagi atomlar va molekulalar maxsus tuzilish hosil qiladi va modda turli xossalari bilan fazalar hajmida o'z holatidan farq qiladigan maxsus holatni oladi. Yuzaki hodisalarni kolloid kimyo o'rganadi.
Yuzaki hodisalarning tasnifi
Yuzaki hodisalar odatda asosiy energiya turlarini o'z ichiga olgan termodinamikaning birinchi va ikkinchi qonunlarining kombinatsiyalangan tenglamasiga muvofiq tasniflanadi. Har qanday heterojen tizim uchun uni quyidagi shaklda yozish mumkin:
d G = − S d T + V d P + s d s _ + S m i d n i + ph d q (\displaystyle dG=-SdT+VdP+(\tagi chizilgan (\sigma ds))+\Sigma \mu _(i)dn_ (i)+\varphi dq)Bu tenglama Gibbs energiyasining o'sishini boshqa turdagi energiyalarning algebraik yig'indisi orqali ko'rsatadi. Ko'rinib turibdiki, sirt energiyasi quyidagi energiya turlariga aylanishga qodir:
- Gibbs energiyasi
- kimyoviy energiya
- mexanik energiya
- Elektr energiyasi
Sirt energiyasining sanab o'tilgan energiya turlaridan biriga aylanishi ma'lum sirt hodisalariga mos keladi, masalan, dispersiya, yopishish va namlanishning o'zgarishi bilan reaktivlikning o'zgarishi, kapillyarlik, adsorbsiya, elektr hodisalari.
Yuzaki hodisalarning ahamiyati
Yuzaki hodisalar kimyoviy muhandislikda keng tarqalgan. Deyarli har qanday kimyoviy ishlab chiqarish dispers tizimlar va sirt hodisalari yordamida amalga oshiriladi. Qoida tariqasida, kimyoviy texnologiyadagi barcha heterojen jarayonlar maksimal fazali aloqa yuzasida amalga oshiriladi. Buning uchun moddalar sistemalari suspenziyalar, kukunlar, emulsiyalar, tumanlar, changlar holatiga o'tkaziladi. Xom ashyo va oraliq mahsulotlarni maydalash, boyitish jarayonlari dispers tizimlarda boradi, ularda namlanish, kapillyarlik, adsorbsiya, cho'kish, koagulyatsiya kabi hodisalar muhim rol o'ynaydi. Kimyoviy texnologiyada qattiq dispersion muhitga ega dispers tizim bo'lgan g'ovakli adsorbentlar va katalizatorlar keng qo'llaniladi.
Yuzaki hodisalarning, xususan, strukturaning shakllanishining qonuniyatlari kerakli xususiyatlarga ega bo'lgan materiallarni olish uchun nazariy asos bo'lib xizmat qiladi: keramika, tsement, shisha-keramika, sorbentlar, katalizatorlar, polimerlar, kukunlar, dori-darmonlar va boshqalar.
Suv sathidagi hodisalar
Vizual tekshirishda neft-suv interfeysining soddaligi va uning darajadagi murakkabligi o'rtasida aniq kontrast mavjud. mikroskopik shkala en , bu chegaraning molekulyar tuzilishida va uning vodorod aloqalari dinamikasida namoyon bo'ladi. Puasson va Maksvelldan boshlab, suvning tuzilishi va uning interfeysdagi reaktivligini o'rganishga bag'ishlangan katta hajmdagi ishlar, ammo ko'p suvli janjal tufayli suv tuzilishi mavzusi ilmiy faoliyatning pasayishiga olib keldi.
Neft-suv chegarasidagi yuza hodisalari bir qator muhim kimyoviy, fizik va biologik jarayonlar, jumladan mitsella va membrana hosil bo'lishi, oqsillarni buklanish, kimyoviy ajralish, neftni olish, nanozarrachalar hosil bo'lishi va interfeysida polimerlanish uz.
Interfeysda yuzaga keladigan "kengaytirilgan" hidrofobik yuzalar bilan aloqa qiladigan suvning tuzilishi, masalan, geksan emulsiyasida, undan juda farq qiladi. hidratsiya qobig'i metan kabi oddiy eritmalar. Metanning bir hil eritmasida molekulalar suv qobig'i metan molekulasi sferasiga tangensial yo'naltirilgan; geksan emulsiyasida esa er usti suvlarining taxminan 25% molekulalari bitta vodorod aloqasini yo'qotadi va natijada erkin guruhlar Oh geksan mitselasiga kirib boradi. Kimyogarlar Y. Chon va R. A. Markuslarning gipotezasiga ko'ra, erkin guruhlarning mavjudligi Oh ba'zilarining sababidir suv yuzasida organik reaktsiyalar en yuzlab marta tezlashtirilgan.
Shuningdek qarang
Eslatmalar
Adabiyot
- Frolov Yu.G. Kolloid kimyo kursi. - MChJ TID "Alliance", 2004. - 464 p. - ISBN 5-98535-003-7.
- Chaplin, M. Kolloid yuzalarda suvning tuzilishi // Biotibbiyot va atrof-muhit fanida sirt kimyosi: [Ingliz ] / J. P. Blits, V. M. Gun'ko (Tahrirlar). - Springer Niderlandiya, 2006. - B. 1-10. - DOI: 10.1007/1-4020-4741-X_1 .
- Jung, Y.
Interfeysda sodir bo'ladigan jarayonlar sirt hodisalari deb ataladi. Yuzaki hodisalarning sababi to'g'ridan-to'g'ri interfeysga ulashgan qatlamlardagi molekulalarning maxsus holatidir, chunki Bu qatlamlar bir-biridan farq qiladi ichki qatlamlar ularning fizik-kimyoviy xossalari (o'ziga xos energiya, zichlik, yopishqoqlik, elektr o'tkazuvchanligi, tarkibi). Bundan tashqari, o'ziga xoslik qanchalik katta tizim energiyasi, xususiyatlar qanchalik kuchli farqlanadi va sirt hodisalarining butun tizimning xatti-harakatlariga ta'siri shunchalik kuchli bo'ladi.
Molekulyar bosim. Faza hajmida va sirt qatlamida modda molekulalarining energiya holati bir xil emas. Faza hajmida joylashgan molekulalar uni o'rab turgan molekulalardan bir xil tortishish (va itarilish) ni boshdan kechiradi va shuning uchun molekulyar kuchlarning natijasi nolga teng. Masalan, A nuqtadagi suyuqlik molekulasi. Fazalar chegarasida joylashgan molekulada (B nuqtasi), turli (qo‘shni) dan.
gaz fazasining jozibador kuchlaridan ko'proq. Agar gaz molekulalarining tortilishini e'tiborsiz qoldirish mumkin bo'lsa, u holda sirtning tortishish kuchi suyuqlik molekulalari, 1 m 2 maydonni egallagan, chuqur qatlamlarning molekulalari tomonidan suyuqlikning ichki (molekulyar) bosimiga teng, ya'ni. hajmdagi suyuqlik molekulalari orasidagi tortishish kuchi. Suyuqlikning ichki bosimining kattaligi juda katta va suyuqlikning qutbliligiga bog'liq. Moddalar qanchalik qutbli bo'lsa va ularning molekulalarini jalb qilish qanchalik kuchli bo'lsa, ichki bosim shunchalik yuqori bo'ladi. Masalan, suv uchun 14800 atm., Va benzol uchun - 3800 atm.
sirt tarangligi. Erkin sirt energiyasi. Suyuqlikning sirtini oshirish uchun (ya'ni, moddaning faza hajmidan sirt qatlamiga o'tishi) ichki bosim kuchini engib, ishni bajarish kerak. Bu ish qanchalik katta bo'lsa, yaratilgan sirtning maydoni qanchalik katta va sirt tarangligi shunchalik yuqori bo'ladi. Molekulalarning sirt qatlamining bir tomonlama tarangligiga sirt tarangligi deyiladi ( σ ). Bu ma'lum holatdagi ma'lum bir moddaning molekulalari orasidagi birikish kuchlarining ifodasidir.
Sirtni yaratish uchun sarflangan energiya molekulalarni faza chuqurligidan yuzaga chiqarish uchun energiyani oshirishga sarflanadi. Sirt molekulalarining ichki molekulalar energiyasiga nisbatan sirt birligidagi ortiqcha energiyasi erkin sirt energiyasi deyiladi: F= s. . S (J / m 2 yoki erg / sm 2 da o'lchanadi). Ko'rinib turganidek
formuladan sirt tarangligi son jihatdan birlik sirt maydoni yoki solishtirma erkin energiya hosil qilish ishiga teng: . Bu bor energiya ifodasi sirt tarangligi. Kuch ta'rifi sirt tarangligi: bu sirtda unga tangensial ravishda ta'sir qiluvchi va tananing erkin yuzasini eng kichik chegaralarga kamaytirishga intiladigan kuch. Bunday holda, u N / m da o'lchanadi.
Termodinamikaning II qonuniga ko'ra, sistemaning erkin sirt energiyasi o'z-o'zidan minimumga intiladi. Bu sirt maydonini kamaytirish yoki sirt tarangligini kamaytirish orqali erkin sirt energiyasini kamaytirish mumkinligini anglatadi. Molekulyar bosim kuchlari ta'sirida sirt maydonining pasayishi faqat suyuqliklar uchun mumkin, chunki uning molekulalarining biriktiruvchi kuchlari unchalik katta emas. Shuning uchun kichik tomchilar kattaroqlarga birlashadi va aerozollar, tumanlar va emulsiyalardagi suyuq tomchilar sharsimon shaklga ega.
Sirt tarangligining pasayishi tufayli erkin sirt energiyasining kamayishi suyuqliklarga ham, qattiq jismlarga ham xosdir. Sirt tarangligi boshqa moddaning, xususan, sirt faol moddasining molekulalarining yuzasida to'planishi tufayli kamayishi mumkin. Ushbu molekulalar o'zlarining tortishishlari bilan ma'lum bir fazaning sirt molekulalarining hajmning ichki qismiga qaytarilishini qisman qoplaydi va tizim yanada barqaror bo'ladi.
Erkin sirt energiyasi va sirt tarangligi haroratga, fazalarning tabiatiga, erigan moddalarning tabiatiga va konsentratsiyasiga bog'liq.
Haroratning oshishi bilan sirt tarangligi pasayadi, chunki molekulalarning o'zaro tortishishi kamayadi. Kritik nuqtada sirt tarangligi nolga etadi, chunki bu holda farqlar va faza chegarasi yo'qoladi.
Bosimning oshishi sirt tarangligini faqat "gaz-suyuqlik" tizimida kamaytiradi, chunki shu bilan birga, gaz fizik-kimyoviy xossalari bo'yicha suyuqlikka yaqinlashadi.
Shuni ham ta'kidlash kerakki, faqat suyuqliklar sirt tarangligini o'lchashi mumkin. Qattiq jismlar uchun bu mumkin emas, chunki qattiq jismning sirtini uning buzilishi tufayli sun'iy ravishda cho'zish mumkin emas. Qattiq jismlarning sirt tarangligi hisoblash yo'li bilan aniqlanadi. Suyuqliklarning sirt tarangligini o'lchash uchun statik (kapillyar ko'tarilish, yotgan yoki osilgan tomchilar usullari), yarim statik usullar (gaz pufakchasining maksimal bosimi usuli, halqani yirtib tashlash usuli, stalagmometrik usul (usul) tortish yoki hisoblash tomchilari) qo'llaniladi.Bulardan oddiy va yetarlicha stalagmometrik usul aniq bo'lib, tortishish ta'sirida suyuqlik tomchisining kapillyar uchidan ajralish momentida uning og'irligi amalda bo'lishiga asoslanadi. kuchga teng kapillyarning atrofiga qo'llaniladigan sirt tarangligi.
Zichligi suvning zichligidan ozgina farq qiladigan suyultirilgan eritmalar uchun sirt tarangligini tenglama (mJ / m 2) yordamida hisoblash mumkin: ![]() .
.
yopishish va birlashish. Yuzaki hodisalar farmatsiyada muhim ahamiyatga ega, chunki ko'pchilik dori vositalari - kukunlar, planshetlar, emulsiyalar, suspenziyalar, aerozollar, malhamlar va boshqalar dispers tizimlardir. Dori vositalarini ishlab chiqarishda ko'pincha adsorbsiya, namlanish va yopishish kabi hodisalar bilan shug'ullanish kerak.
Ikki oʻxshash (qattiq yoki suyuq) jismlar oʻzaro aloqada boʻlganda ular oʻrtasida yuzaga keladigan tortishish adezyon (lotincha adhaesio tortishish, yopishish) deyiladi. U o'xshash bo'lmagan moddalarning yopishish kuchini tavsiflaydi va bir faza molekulalarini boshqa faza molekulalaridan ajratish uchun sarflangan ish bilan o'lchanadi (J / m 2 da o'lchanadi). Ushbu ish Dupre-Young tenglamasi bo'yicha hisoblanadi: W A \u003d s well-g (1 + cosÖ). Yopishtiruvchi moddalar, bog'lovchilar, qoplamalarning harakati yopishqoqlik hodisalariga asoslanadi. Tabletkalarning parchalanishiga, qobiqlarning mustahkamligiga, qattiq dozalash shakllarining erishiga ta'sir qiladi va jarrohlik va stomatologiyada ishlatiladigan materiallarni tavsiflash uchun ishlatiladi.
Bir faza doirasida molekulalararo, atomlararo va ionlararo tortishishning barcha turlarini o'z ichiga olgan bir jinsli molekulalar, atomlar, ionlarning yopishishi kogeziya (lot. “bog'”) deb ataladi. U moddaning kuchini tavsiflaydi va moddani sindirish (molekulalar orasidagi biriktiruvchi kuchlarni engish) va ikkita yangi sirt birligini yaratish uchun zarur bo'lgan ish bilan o'lchanadi. Yopishqoqlik qiymati son jihatdan sirt tarangligining ikki barobar qiymatiga teng: W tishli. = 2s.
Adsorbsion jarayonlar haqida asosiy tushunchalar. Qattiq yoki sirtida adsorbsiya sodir bo'ladigan suyuqlik adsorbent, adsorbsiyalangan modda esa adsorbat yoki adsorbat deb ataladi. Moddaning chegarada oʻz-oʻzidan toʻplanish jarayoni adsorbsiya (D) deyiladi. U birlik sirt yoki massa (mol/m2, mol/g) tomonidan adsorbsiyalangan moddaning miqdori bilan ifodalanadi. Van-der-Vaals kuchlari va vodorod bog'lari ta'sirida amalga oshiriladigan adsorbsiya deyiladi. jismoniy. Hodisaga asoslangan adsorbsiya kovalent aloqalar adsorbent va adsorbent molekulalari orasidagi deyiladi kimyoviy yoki kimyosorbtsiya. Jismoniy adsorbsiya teskari jarayon bo'lib, desorbsiya (sirtning adsorblangan moddadan ozod bo'lishi) bilan birga keladi. Adsorbsiya va desorbsiya o'rtasida dinamik muvozanat o'rnatiladi, uning holati haroratga bog'liq. Haroratning oshishi fizik adsorbsiyani pasaytiradi va kimyoviy adsorbsiyani kuchaytiradi. Desorbsiya adsorbentning yo'q qilinishi, haroratning o'zgarishi va adsorbsion o'zaro ta'sir kuchlarining kamayishi bilan amalga oshiriladi. Ikkinchisi elyusiya shaklida keng qo'llaniladi. Elutsiya - moddani desorbsiyalash uchun adsorbentga, masalan, eritmaga tutashgan fazaning o'zgarishi. Elyusiya jarayonida adsorbsiyalangan modda adsorbentdan yangi erituvchi molekulalari tomonidan yoki yangi eritmada erigan moddalarning adsorbsion yaqinligining pasayishi natijasida (ko'pincha adsorbent va adsorbent molekulalarining zaryadini o'zgartirish natijasida) siqib chiqariladi. eritmaning pH yoki ion kuchining o'zgarishi).
Adsorbsiyaning xarakterli xususiyati uning selektivligi (o'ziga xosligi)dir. Bu shuni anglatadiki, har bir adsorbent bir yoki bir nechta o'ziga xos moddalarni adsorbsiya qiladi. Adsorbsiyaning selektivligi adsorbent va adsorbent molekulalarining elektron zichligini "kalit - qulf" turiga ko'ra taqsimlashda tasodifiy tasodifni nazarda tutadi, ya'ni. adsorbent va adsorbat o'rtasidagi kimyoviy yaqinlik.






