Gazsimon holatdagi molekulalarning xossalari. Suyuqliklarda molekulalarning joylashishi
Suyuqliklarda molekulalarning joylashishi. Suyuqliklardagi molekulalar molekulalarning o'lchamiga teng masofada joylashgan bo'lib, qisqa masofali tartib deb ataladigan tartibni saqlaydi, shuning uchun suyuqliklar hajmini saqlab qoladi. Molekulalar doimo harakatlanib, sakrab turadi, shuning uchun suyuqliklar oqadi, tomir shaklini oladi.
"Materiyaning 3 holati" taqdimotidan 9-rasm mavzu bo'yicha fizika darslariga " issiqlik hodisalari»O'lchamlari: 960 x 720 piksel, format: jpg. Rasm bepul yuklab olish uchun fizika darsi, rasmni o'ng tugmasini bosing va "Rasmni boshqa saqlash ..." tugmasini bosing. Darsdagi rasmlarni ko'rsatish uchun siz "Materaning 3 holati.ppt" taqdimotini zip arxividagi barcha rasmlar bilan bepul yuklab olishingiz mumkin. Arxiv hajmi 2714 KB.
Taqdimot yuklab olishissiqlik hodisalari
"Maddalarning tarqalishi" - Geraklit. Kuzatishlar. Texnologiya va tabiatdagi diffuziya. Biologiya sevuvchilar uchun vazifalar. Diffuziya hodisasi. Biz muammolarni hal qilamiz. Demokrit. Olimlar Qadimgi Gretsiya. Hikmatlar. Diffuziya. Miletlik Thales. Gazlardagi diffuziya. Xushbo'y barglar. To'q rang.
"Materaning 3 holati" - Xususiyatlar qattiq moddalar. Muz. Qiziq faktlar. Kondensatsiya. Suyuqliklarning xossalari. Gazlardagi molekulalarning joylashishi. Modda. Suyuqliklarda molekulalarning joylashishi. Krossvordni yeching. Jarayonga misollar. davlatlar. Bug'lanish. Kristallanish. Qattiq jismlarda molekulalarning joylashishi. Zarrachalar harakati va o'zaro ta'sirining xarakteri.
"Tabiatdagi diffuziya" - Sabzavot va mevalarni saqlashda oziq-ovqat sanoatida keng qo'llaniladi. Po'latni eritishda. Diffuziya hodisasi tabiatda muhim ko'rinishlarga ega bo'lib, fan va ishlab chiqarishda qo'llaniladi. tabiatdagi diffuziya. Diffuziyaga gazlar yoki suyuqliklarning aralashishi misol bo'la oladi. Nafasda diffuziya.
"Materiyaning agregat holatlarini o'zgartirish" - Qaynatish. Erish va kristallanish harorati. Qaynatish harorati. bug'lanish shartlari. yig'indisi o'zgarishlar. Maxsus issiqlik bug'lanish. erish va qotib qolish jarayoni. Erish jarayonini tushuntirish. Bug'lanish. Moddaning agregat transformatsiyalari. Uchta davlat. Issiqlik miqdorini hisoblash.
"Erilish paytidagi issiqlik hodisalari" - Kimyogar. Hodisalar. Eritilish. Molekulalarning o'zaro kirib borishi. Sizga fizika va kimyo qonunlarini yanada chuqurroq bilishda muvaffaqiyatlar tilaymiz. Xonadoshingizni tekshiring. Amaliy topshiriqlar. Yechimlarning qiymati. Fizika - kimyoviy jarayon. Dars davomida o'zingizni qanday his qildingiz? ekzotermik jarayon. Kimyoviy reaksiyalarning belgilari.
"Molekulalarning o'zaro ta'siri" - Repulsiya to'liq konvergentsiyani oldini oladi. gazsimon moddalar. Ikki bo'lak temir mixni ulash mumkinmi? I variant Tabiiy aralashmalar tarkibiga kirmaydi: a) gil; b) sement; c) tuproq. Darsning maqsad va vazifalari: Moddalarni hosil qiluvchi zarralar haqidagi bilimlarni kengaytirish. Attraktsion zarralarni birga ushlab turadi.
Mavzu bo'yicha jami 23 ta taqdimot
To'liq matnli qidiruv:
Fizika->Laboratoriya ishi
dagi jarayonlarni o'rganish elektr zanjiri Bilan parallel ulanish induktiv va sig'imli elementlarni o'z ichiga olgan qabul qiluvchilar, boshqa nisbat bilan ... to'liq>>
Fizika->Laboratoriya ishi
Ketma-ket o'z ichiga olgan bir fazali sinusoidal kuchlanish zanjirining elektr parametrlariga lasan indüktansının ta'sirini tekshirish ... to'liq>>
Bosh sahifa > Annotatsiya >Fizika
1 Saqlash………………………………………………………..2
2 Asosiy tana
2.1 Suyuqlikning tuzilishi. Suyuqlik molekulalarining harakati………3
2.2 Suyuqlikdagi bosim…………………………………….4
2.3 Arximed qonuni ………………………………………….5
2.4 Bug‘lanish…………………………………………………6
2.5 Qaynatish………………………………………………….7
2.6 Suyuqlikning sirt tarangligi………………………….8
2.7 Suyuq plyonkalar………………………………………9
2.8 Namlash va namlanmaslik…………………………….10
2.9 Kapillyar hodisalar……………………………………..12
2.10 Elektr toki suyuqliklarda………………………..13
3 Xulosa……………………………………………………..14
Adabiyotlar……………………………………………………16
1.Kirish
Kundalik hayotda biz odatda materiyaning uch fazali holatiga duch kelamiz - qattiq, suyuq va gazsimon. Biz gazlar va qattiq kristall jismlarning tuzilishi haqida aniq tasavvurga egamiz. Gaz - bu bir-biridan mustaqil ravishda barcha yo'nalishlarda tasodifiy harakatlanadigan molekulalar yig'indisidir. Qattiq jismda barcha molekulalar uzoq vaqt davomida o'zlarining o'zaro joylashishini saqlab qoladilar va ma'lum muvozanat pozitsiyalari atrofida faqat kichik tebranishlarni amalga oshiradilar.
Ushbu inshoda men batafsilroq ko'rib chiqaman suyuqlik holati moddalar. Asosiy xususiyat Bu agregatsiya holati gazlar va kristallar o'rtasida oraliq pozitsiyani egallagan suyuqlik holati bu ikkala holatning ba'zi xususiyatlarini birlashtiradi. Xususan, suyuqliklar uchun, shuningdek, kristall jismlar uchun ma'lum hajmning mavjudligi xarakterlidir va shu bilan birga, suyuqlik, gaz kabi, o'zi joylashgan idish shaklini oladi. Aksariyat odamlar suyuqlikning o'ziga xos shakli yo'q deb o'ylashadi. Lekin bu haqiqat emas. Har qanday suyuqlikning tabiiy shakli shardir. Odatda, tortishish kuchi suyuqlikning bu shaklni olishiga to'sqinlik qiladi, suyuqlik sirt ustida yupqa qatlamda tarqaladi yoki ichiga quyilsa, idish shaklini oladi.
Suyuqliklarning oraliq holati suyuqlik holatining xossalari bo'yicha ayniqsa murakkab bo'lganligi bilan bog'liq. Suyuqliklar hech bo'lmaganda Arximed davridan beri, ya'ni 2200 yil oldin ilmiy tadqiqot mavzusi bo'lgan bo'lsa-da, suyuqliklarning xatti-harakatlarini tahlil qilish hali ham amaliy fanning eng qiyin yo'nalishlaridan biri hisoblanadi. Hozirgacha suyuqliklarning to'liq to'liq va umumiy qabul qilingan nazariyasi mavjud emas.
2 .Asosiy qism.
Moddaning suyuqlik holatining asosiy xossalari va qonuniyatlarini tushunish uchun quyidagi jihatlarni hisobga olish kerak:
2.1.Suyuqlikning tuzilishi. Suyuqlik molekulalarining harakati.
Suyuqlik - bu oqishi mumkin bo'lgan narsa.
Suyuq zarrachalarning joylashishida qisqa masofali tartib deb ataladigan narsa kuzatiladi. Bu shuni anglatadiki, har qanday zarrachaga nisbatan uning eng yaqin qo'shnilarining joylashuvi tartibga solinadi. Biroq berilgan zarrachadan uzoqlashgan sari boshqa zarralarning unga nisbatan joylashuvi tobora kamroq tartibli bo'lib boradi va zarrachalarning joylashish tartibi tezda butunlay yo'qoladi. Suyuq molekulalar gaz molekulalari kabi erkin bo'lmasa ham, qattiq molekulalarga qaraganda ancha erkin harakat qiladi. Suyuqlikning har bir molekulasi ma'lum vaqt davomida qo'shnilaridan uzoqlashmasdan, bu erda va u erda harakat qiladi. Ammo vaqti-vaqti bilan suyuqlik molekulasi o'z muhitidan chiqib, boshqa joyga boradi, yangi muhitga kiradi va u erda yana bir muncha vaqt tebranishlarga o'xshash harakatlar qiladi. Suyuq holat nazariyasining bir qator muammolarini ishlab chiqishda sovet olimi Ya.I.Frenkelning xizmatlari katta. Frenkelning fikricha, suyuqliklardagi issiqlik harakati quyidagi xususiyatga ega. Har bir molekula ma'lum vaqt davomida ma'lum bir muvozanat holatida tebranadi. Vaqti-vaqti bilan molekula o'zining muvozanat joyini o'zgartirib, yangi holatga o'tadi, avvalgisidan molekulalarning o'lchamlari bo'yicha masofa bilan ajralib turadi. Ya'ni molekulalar suyuqlik ichida faqat sekin harakat qiladi, vaqtning bir qismini ma'lum joylarga yaqin joyda qoladi.Shunday qilib, suyuqlik molekulalarining harakati qattiq va gazdagi harakatlar aralashmasiga o'xshaydi: bir joyda tebranish harakati almashtiriladi. bir joydan ikkinchi joyga erkin o'tish orqali.
2.2 Suyuqlikdagi bosim
Kundalik tajriba bizga suyuqliklar ular bilan aloqa qilgan qattiq jismlar yuzasida ma'lum kuchlar bilan harakat qilishini o'rgatadi. Bu kuchlar suyuqlik bosimi kuchlari deb ataladi.
Ochiq suv jo'mrakining ochilishini barmoq bilan qoplagan holda, biz suyuqlikning barmoq ustidagi bosimini his qilamiz. Suzuvchining katta chuqurlikka sho'ng'ish paytida boshdan kechiradigan quloqlardagi og'riqlar quloq pardasidagi suv bosimining kuchlari tufayli yuzaga keladi. Chuqur dengiz termometrlari juda kuchli bo'lishi kerak, shunda suv bosimi ularni ezib tashlamaydi.
Suyuqlikdagi bosim uning hajmining o'zgarishi - siqilish bilan bog'liq. Suyuqliklar hajmining o'zgarishiga nisbatan elastiklikka ega. Suyuqlikdagi elastik kuchlar bosim kuchlaridir. Shunday qilib, agar suyuqlik u bilan aloqa qiladigan jismlarga bosim kuchlari bilan ta'sir qilsa, bu uning siqilganligini anglatadi. Siqilish paytida moddaning zichligi ortib borayotganligi sababli, suyuqliklar zichlikning o'zgarishiga nisbatan elastiklikka ega deyish mumkin.
Suyuqlikdagi bosim suyuqlikda joylashgan har qanday sirtga perpendikulyar. H chuqurligidagi suyuqlikdagi bosim sirtdagi bosim yig'indisiga va chuqurlikka mutanosib qiymatga teng:
Suyuqliklar statik bosimni o'tkazishi mumkinligi sababli, ular zichligidan deyarli kam bo'lmagan holda, ular kuchga ega bo'lgan qurilmalarda qo'llanilishi mumkin: gidravlik press.
2.3.Arximed qonuni
Bosim kuchlari suyuqlikka botgan qattiq jismning yuzasiga ta'sir qiladi. Bosim chuqurlik bilan ortib borayotganligi sababli, suyuqlikning pastki qismidagi yuqoriga ko'tariladigan bosim kuchlari yuqoridagi pastga tushadigan kuchlardan kattaroqdir va bosim kuchlarining natijasi yuqoriga qarab bo'lishini kutishimiz mumkin. Suyuqlikka botirilgan jismga ta’sir etuvchi bosim kuchi suyuqlikning tayanch kuchi deyiladi.
Agar suyuqlikka botgan jism o'z-o'zidan qolsa, u holda u cho'kib ketadi, muvozanat holatida qoladi yoki suyuqlik yuzasiga suzib ketadi, bu tayanch kuchi tanaga ta'sir qiluvchi tortishish kuchidan kichik bo'ladimi, teng. u yoki undan kattaroq.
Arximed printsipi shuni ko'rsatadiki, suyuqlikdagi jismga ko'chirilgan suyuqlikning og'irligiga teng yuqoriga ko'taruvchi kuch ta'sir qiladi. Suyuqlikka botgan jismga suzuvchi kuch ta'sir qiladi (Arximed kuchi deb ataladi)
bu yerda r - suyuqlik (gaz) zichligi, tezlanish erkin tushish, a V- suvga botgan jismning hajmi (yoki jism hajmining sirt ostidagi qismi).
Agar suyuqlikka botgan jism tarozida osilgan bo'lsa, u holda tarozida tananing havodagi og'irligi va ko'chirilgan suyuqlikning og'irligi o'rtasidagi farq ko'rsatiladi. Shuning uchun Arximed qonuniga ba'zan quyidagi formula beriladi: suyuqlikka botgan jism o'z vaznini u bilan almashtirilgan suyuqlik qanchalik og'irlashtirsa, shuncha yo'qotadi.
Yana bir kattaroq suyuqlik ichida bo'lgan bunday eksperimental haqiqatni ta'kidlash qiziq solishtirma og'irlik, Arximed qonuniga ko'ra suyuqlik o'z vaznini "yo'qotadi" va tabiiy, sharsimon shaklni oladi.
2.4 Bug'lanish
Sirt qatlamida va suyuqlik yuzasiga yaqin joyda sirt mavjudligini ta'minlaydigan va molekulalarning suyuqlik hajmini tark etishiga yo'l qo'ymaydigan kuchlar ta'sir qiladi. Issiqlik harakati tufayli molekulalarning bir qismi suyuqlikdagi molekulalarni ushlab turadigan kuchlarni engib, suyuqlikni tark etish uchun etarlicha yuqori tezlikka ega. Bu hodisa bug'lanish deb ataladi. Har qanday haroratda kuzatiladi, lekin harorat oshishi bilan uning intensivligi ortadi.
Agar suyuqlikni tark etgan molekulalar suyuqlik yuzasiga yaqin bo'shliqdan chiqarilsa, oxir-oqibat barcha suyuqlik bug'lanadi. Agar suyuqlikni tark etgan molekulalar olib tashlanmasa, ular bug' hosil qiladi. Suyuqlik yuzasiga yaqin hududga tushgan bug 'molekulalari tortishish kuchlari bilan suyuqlikka tortiladi. Bu jarayon kondensatsiya deb ataladi.
Shunday qilib, molekulalar olib tashlanmasa, bug'lanish tezligi vaqt o'tishi bilan kamayadi. Bug 'zichligining yanada oshishi bilan ma'lum bir vaqt ichida suyuqlikni tark etadigan molekulalar soni bir vaqtning o'zida suyuqlikka qaytadigan molekulalar soniga teng bo'ladigan holatga erishiladi. Dinamik muvozanat holati keladi. Suyuqlik bilan dinamik muvozanat holatidagi bug 'to'yingan deb ataladi.
Harorat, zichlik va bosimning oshishi bilan to'yingan bug ' kattalashtirish; ko'paytirish. Harorat qanchalik yuqori bo'lsa, suyuqlik molekulalarining soni shunchalik ko'p bug'lanish uchun etarli energiyaga ega bo'ladi va kondensatsiya bug'lanish teng bo'lishi uchun bug 'zichligi qanchalik katta bo'lishi kerak.
2.5 Qaynatish
Suyuqlik bosim bo'ladigan haroratgacha qizdirilganda to'yingan bug'lar tashqi bosimga teng, suyuqlik va uning o'rtasida muvozanat o'rnatiladi to'yingan bug '. Suyuqlikka qo'shimcha issiqlik miqdori berilganda, suyuqlikning mos keladigan massasi darhol bug'ga aylanadi. Bu jarayon qaynatish deb ataladi.
Qaynatish suyuqlikning kuchli bug'lanishi bo'lib, u nafaqat sirtdan, balki butun hajmida, hosil bo'lgan bug 'pufakchalari ichida sodir bo'ladi. Suyuqlikdan bug'ga o'tish uchun molekulalar ularni suyuqlikda ushlab turadigan jozibali kuchlarni engish uchun zarur bo'lgan energiyani olishlari kerak. Masalan, 1 g suvni 100 ° C haroratda va dengiz sathida atmosfera bosimiga mos keladigan bosimda bug'lantirish uchun 2258 J sarflash kerak bo'ladi, shundan 1880 tasi suyuqlikdan molekulalarni ajratish uchun ketadi, qolganlari esa ketadi. atmosfera bosimi kuchlariga qarshi tizim egallagan hajmni oshirish uchun ishlash (100 ° C haroratda 1 g suv bug'i va normal bosim 1,673 sm 3 hajmni egallaydi, bir xil sharoitlarda 1 g suv esa atigi 1,04 sm 3 ni tashkil qiladi. ).
Qaynash nuqtasi bug 'bosimi tashqi bosimga teng bo'ladigan haroratdir. Bosim ortishi bilan qaynash nuqtasi ortadi, bosim pasayganda esa pasayadi.
Suyuqlikdagi bosimning uning ustunining balandligi bilan o'zgarishi tufayli suyuqlikda turli darajadagi qaynash, aniq aytganda, har xil haroratlarda sodir bo'ladi. Qaynayotgan suyuqlik yuzasidan faqat to'yingan bug' ma'lum bir haroratga ega. Uning harorati faqat tashqi bosim bilan belgilanadi. Aynan shu harorat qaynash nuqtasi haqida gapirganda nazarda tutilgan.
Turli suyuqliklarning qaynash nuqtalari bir-biridan juda farq qiladi va bu texnologiyada, masalan, neft mahsulotlarini distillashda keng qo'llaniladi.
Suyuqlikning ma'lum miqdorini izotermik ravishda bug'ga aylantirish uchun berilishi kerak bo'lgan issiqlik miqdori uning to'yingan bug'lari bosimiga teng tashqi bosimda bug'lanishning yashirin issiqligi deyiladi. Odatda bu qiymat bir gramm yoki bir mol bilan bog'liq. Bir mol suyuqlikning izotermik bug'lanishi uchun zarur bo'lgan issiqlik miqdori molyar deb ataladi yashirin issiqlik bug'lanish. Agar bu qiymat molekulyar massaga bo'linsa, bug'lanishning o'ziga xos yashirin issiqligi olinadi.
2.6 Suyuqlikning sirt tarangligi
Suyuqlikning sirtini minimal darajaga tushirish xususiyati sirt tarangligi deyiladi. Sirt tarangligi suyuqlikdagi molekulyar bosim hodisasi bo‘lib, sirt qatlami molekulalarining suyuqlik ichidagi molekulalarga tortilishi natijasida yuzaga keladi. Suyuqlik yuzasida molekulalar nosimmetrik bo'lmagan kuchlarni boshdan kechiradi. Suyuqlik ichidagi molekulada o'rtacha tortishish kuchi, kogeziya har tomondan o'rtacha bir xilda ta'sir qiladi. Agar suyuqlik yuzasi kattalashtirilsa, u holda molekulalar ushlab turish kuchlarining ta'siriga qarshi harakat qiladi. Shunday qilib, suyuqlikning sirtini qisqartirishga moyil bo'lgan kuch sirtdagi tashqi tortish kuchiga teskari yo'nalishda harakat qiladi. Bu kuch sirt taranglik kuchi deb ataladi va quyidagi formula bilan hisoblanadi:
 - sirt taranglik koeffitsienti
- sirt taranglik koeffitsienti
 (
( )
)
 - suyuqlik yuzasi chegarasining uzunligi
- suyuqlik yuzasi chegarasining uzunligi
E'tibor bering, oson bug'lanadigan suyuqliklar (efir, spirt) uchuvchan bo'lmagan suyuqliklarga (simob) qaraganda pastroq sirt tarangligiga ega. Suyuq vodorod va ayniqsa suyuq geliyning sirt tarangligi juda past. Suyuq metallar uchun sirt tarangligi aksincha, bu juda katta. Suyuqliklarning sirt tarangligidagi farq turli molekulalarning biriktiruvchi kuchlarining farqi bilan izohlanadi.
Suyuqlikning sirt tarangligini o'lchash shuni ko'rsatadiki, sirt tarangligi faqat suyuqlikning tabiatiga emas, balki uning haroratiga ham bog'liq: harorat oshishi bilan suyuqlik zichligidagi farq kamayadi va shuning uchun koeffitsient kamayadi. sirt tarangligi - pasayadi.
Sirt tarangligi tufayli suyuqlikning har qanday hajmi sirt maydonini kamaytirishga intiladi, shuning uchun potentsial energiya kamayadi. Yuzaki taranglik suvda to'lqinlarning harakatlanishi uchun mas'ul bo'lgan elastik kuchlardan biridir. Bo'shliqlarda sirtning tortishish kuchi va sirt tarangligi suv zarralarini pastga qarab tortadi va sirtni yana silliq qilishga intiladi.
2.7 Suyuq plyonkalar
Sovunli suvdan ko'pikni olish qanchalik oson ekanligini hamma biladi. Ko'pik - suyuqlikning eng nozik plyonkasi bilan chegaralangan havo pufakchalari to'plami. Ko'pik hosil qiluvchi suyuqlikdan alohida plyonka osongina olinishi mumkin.
Bu filmlar juda qiziq. Ular juda nozik bo'lishi mumkin: eng nozik qismlarida qalinligi millimetrning yuz mingdan bir qismidan oshmaydi. Ularning nozikligiga qaramay, ular ba'zan juda barqaror. Sovun plyonkasi cho'zilishi va deformatsiyalanishi mumkin va suv oqimi sovun plyonkasi orqali uni yo'q qilmasdan oqishi mumkin.
Filmlarning barqarorligini qanday tushuntirish mumkin? Plyonka hosil bo'lishining ajralmas sharti - unda eriydigan moddalarning toza suyuqlikka qo'shilishi, bundan tashqari, sirt tarangligini sezilarli darajada kamaytiradigan moddalar.
Tabiat va texnologiyada biz odatda alohida filmlar bilan emas, balki filmlar to'plami - ko'pik bilan uchrashamiz. Siz tez-tez oqimlarda ko'rishingiz mumkin, bu erda kichik oqimlar sokin suvga tushadi, ko'pikning mo'l shakllanishi. Bunday holda, suvning ko'piklanish qobiliyati suvda o'simliklarning ildizidan ajralib chiqadigan maxsus organik moddaning mavjudligi bilan bog'liq. Qurilish uskunalarida uyali tuzilishga ega bo'lgan materiallar, masalan, ko'pik ishlatiladi. Bunday materiallar arzon, engil, issiqlik va tovushni yaxshi o'tkazmaydi va etarlicha kuchli. Ularni ishlab chiqarish uchun qurilish materiallari hosil bo'ladigan eritmalarga ko'pik hosil bo'lishiga yordam beradigan moddalar qo'shiladi.
2.8 Namlash
Shisha plastinka ustiga qo'yilgan mayda simob tomchilari sharsimon shaklga ega bo'ladi. Bu suyuqlik sirtini kamaytirishga moyil bo'lgan molekulyar kuchlarning natijasidir. Qattiq jism yuzasiga joylashtirilgan simob har doim ham dumaloq tomchilarni hosil qilmaydi. U sink plastinka ustiga tarqaladi va tomchining umumiy yuzasi shubhasiz ortadi.
Anilin tomchisi ham shisha idish devoriga tegmagandagina sharsimon bo'ladi. U devorga tegishi bilanoq, u darhol stakanga yopishadi, uning bo'ylab cho'ziladi va katta umumiy sirtga ega bo'ladi.
Bu qattiq jism bilan aloqa qilganda suyuqlik molekulalarining qattiq jism molekulalari bilan yopishish kuchlari muhim rol o'ynay boshlashi bilan izohlanadi. Suyuqlikning harakati qaysi biri kattaroq bo'lishiga bog'liq bo'ladi: suyuqlik molekulalari orasidagi yopishish yoki suyuqlik molekulasining qattiq molekulaga yopishishi. Simob va shisha holatida simob va shisha molekulalari orasidagi bog'lanish kuchlari simob molekulalari orasidagi biriktiruvchi kuchlarga nisbatan kichik bo'lib, simob tomchilab yig'iladi. Bunday suyuqlik deyiladi namlanmaydigan qattiq. Simob va ruxda suyuqlik va qattiq jismning molekulalari orasidagi biriktiruvchi kuchlar suyuqlik molekulalari o'rtasida ta'sir qiluvchi kogeziya kuchlaridan oshib ketadi va suyuqlik qattiq jismga tarqaladi. Bunday holda, suyuqlik deyiladi namlash qattiq.
Bundan kelib chiqadiki, suyuqlik yuzasi haqida gap ketganda, nafaqat suyuqlik havo bilan chegaradosh sirtni, balki boshqa suyuqliklar yoki qattiq jism bilan chegaradosh sirtni ham nazarda tutish kerak.
Suyuqlik idishning devorlarini namlaydimi yoki yo'qmi, qattiq devor va gaz bilan aloqa qilish joyidagi suyuqlik yuzasining shakli u yoki bu shaklga ega. Nam bo'lmagan holda, suyuqlik yuzasining chetidagi shakli yumaloq, qavariq. Namlash holatida, chekkadagi suyuqlik konkav shaklini oladi.
2.9.Kapillyar hodisalar.
Hayotda biz ko'pincha ko'plab kichik kanallar (qog'oz, ip, teri, turli qurilish materiallari, tuproq, yog'och) tomonidan teshilgan jismlar bilan shug'ullanamiz. Suv yoki boshqa suyuqliklar bilan aloqa qilganda, bunday jismlar ko'pincha ularni o'zlashtiradi. Bu qo'llarni quritganda sochiqning ta'siri, kerosin lampasidagi tayoqning ta'siri va boshqalar uchun asosdir. Shu kabi hodisalar tor shisha naychalarda ham kuzatilishi mumkin. Tor naychalar kapillyar yoki soch deb ataladi.
Bunday trubka bir uchi bilan keng idishga keng idishga botirilganda, quyidagilar sodir bo'ladi: agar suyuqlik trubaning devorlarini ho'llasa, u idishdagi suyuqlik darajasidan yuqoriga ko'tariladi va bundan tashqari, balandroq bo'lsa, trubka torroq bo'ladi; agar suyuqlik devorlarni ho'llamasa, unda, aksincha, trubadagi suyuqlik darajasi keng idishga qaraganda pastroq o'rnatiladi. Tor quvurlar yoki bo'shliqlarda suyuqlik darajasining balandligining o'zgarishi deyiladi kapillyarlik. Keng ma'noda kapillyar hodisalar deganda sirt tarangligi mavjudligi sababli barcha hodisalar tushuniladi.
Kapillyar naychalarda suyuqlikning ko'tarilish balandligi naychadagi kanalning radiusiga, sirt tarangligiga va suyuqlikning zichligiga bog'liq. Kapillyardagi suyuqlik va keng tomir o'rtasida shunday daraja farqi h o'rnatiladi, shunda gidrostatik bosim gh kapillyar bosimni muvozanatlashtiradi:
bu yerda - suyuqlikning sirt tarangligi
R - kapillyar radius.
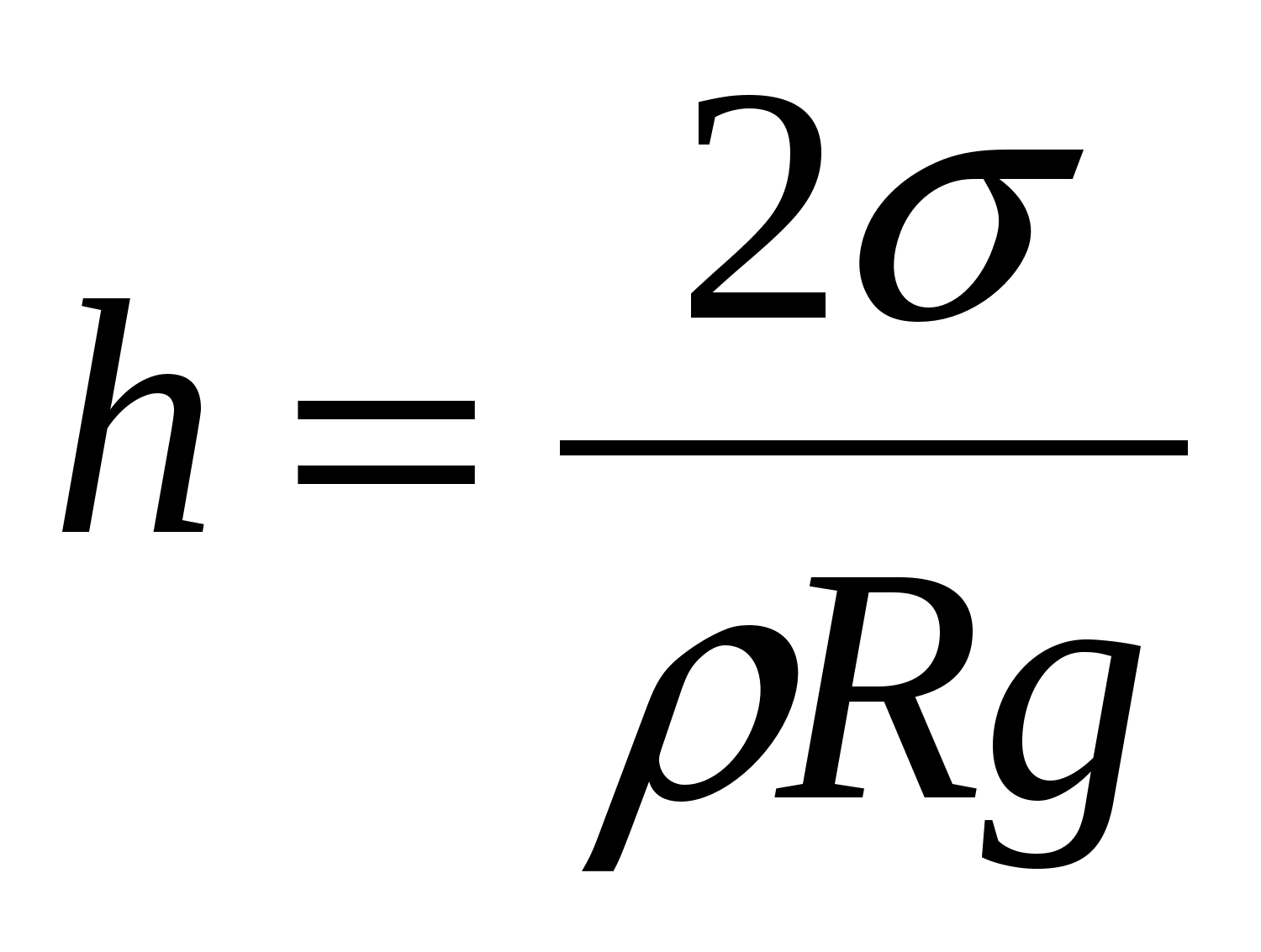
Kapillyardagi suyuqlikning ko'tarilish balandligi uning sirt tarangligiga proportsional va kapillyar kanalning radiusi va suyuqlik zichligiga teskari proportsionaldir (Yurin qonuni).
2.10.Suyuqliklardagi elektr toki.
Sof suyuqliklar elektr tokini o'tkazmaydi, ya'ni ular dielektriklardir, chunki suyuqlik molekulalarining har biri neytral bo'lib, elektr maydonida harakat qilmaydi.
Elektr tokini o'tkazadigan suyuqliklarga elektrolitlar deyiladi. Suyuqliklardagi elektr toki tuz ionlarining yo'naltirilgan harakati natijasida hosil bo'ladi. Elektrolitdan tok o`tganda moddaning elektrodlarga chiqishi hodisasi elektroliz deb ataladi. Salbiy zaryadlangan elektrodda katod zarrachalarning (atomlar, molekulalar, kationlar) elektrokimyoviy qisqarishi mavjud va musbat zaryadlangan elektrodda - anod zarrachalarning (atomlar, molekulalar, anionlar) elektrokimyoviy oksidlanishi mavjud. 1832 yilda Faraday elektrodda chiqarilgan moddaning M massasi elektrolitdan o'tgan Q elektr zaryadiga to'g'ridan-to'g'ri proportsional ekanligini aniqladi:
agar u elektrolit orqali t vaqt davomida o'tkazilsa D.C. joriy I bilan.
Proportsionallik koeffitsienti k moddaning elektrokimyoviy ekvivalenti deyiladi. Bu elektrolit orqali bitta elektr zaryadining o'tishida ajralib chiqadigan moddaning massasiga son jihatdan teng va moddaning kimyoviy tabiatiga bog'liq.
Faradayning ikkinchi qonuni shunday deydi: Turli moddalarning elektrokimyoviy ekvivalentlari ularning kimyoviy ekvivalentlari sifatida qaraladi. Ionning kimyoviy ekvivalenti bu ionning A molyar massasining z valentligiga nisbati. Shuning uchun elektrokimyoviy ekvivalent:
![]() ,
,
Bu erda F - Faraday doimiysi
Elektroliz hodisasi zamonaviy sanoatda keng qo'llaniladi. Xususan, elektroliz vodorod, shuningdek, natriy gidroksid, xlor, xlororganik birikmalar, marganets dioksidi va vodorod periksni sanoat ishlab chiqarish usullaridan biridir. Rudalardan katta miqdordagi metallar ajratib olinadi va elektroliz (elektrotekstraksiya, elektr tozalash) yordamida qayta ishlanadi. Elektroliz oqava suvlarni tozalash uchun ishlatiladi (elektrokoagulyatsiya, elektroekstraktsiya, elektroflotatsiya jarayonlari).
3. Xulosa
Shunday qilib, suyuqlik qattiq va gazsimon holatlar orasidagi moddaning oraliq holatidir. Bu suyuqliklarning qattiq va gazsimon holatlarga xos bo'lgan xususiyatlarga ega bo'lishiga olib keladi. Suyuq va qattiq xolatlar xossalarini o`zida mujassam etgan moddaning holatiga yorqin misol qilib sanoat va texnikada keng qo`llaniladigan suyuq kristalllarni keltirish mumkin (suyuq kristall displeylar). Shu munosabat bilan suyuqlik holatini tavsiflashda qattiq va gazsimon holatlarni tasvirlashda qo‘llaniladigan matematik usullarni sintez qilish talab etiladi, bu esa ko‘plab fizikaviy va kimyoviy hodisalarni to‘liq tasvirlashni murakkablashtiradi va qiyinlashtiradi.
Hozirgi vaqtda suyuqliklarning ko'pgina xususiyatlari sanoat va texnologiyada keng qo'llaniladi. Masalan, suyuqlikning butun hajmida bosimni oshirish xususiyati gidravlika bilan boshqariladigan yuk ko'taruvchi mashinalarda qo'llaniladi. Ammo materiyaning suyuq holati nazariyasini yanada chuqur o'rganish ham zarur. Shunday qilib, qaynoq suyuqlik oqimini o'rganishning dolzarbligi atom energiyasiga bo'lgan ehtiyoj, elektr stantsiyalarining xavfsizligi muammosi bilan bog'liq.
Suyuq holatda jismoniy va kimyoviy jarayonlarni o'rganishga alohida qiziqish uyg'otadi, chunki biz o'zimiz 90% suv, Yerdagi eng keng tarqalgan suyuqlikdir. Va hayvondagi barcha hayotiy jarayonlar va flora suyuqlikda, ya'ni suvda uchraydi. Shuning uchun materiyaning bu holatini o'rganish barcha odamlar uchun muhim va dolzarbdir.
Adabiyotlar ro'yxati:
I.V. Savelyev "Umumiy fizika kursi"
Cl.E. Svarts "Oddiy hodisalarning favqulodda fizikasi"
Fizika boshlang'ich darsligi, akademik G.S. Landsberg
T.I. Trofimov "Fizika kursi"
MEN VA. Perelman "Qiziqarli fizika"
Qattiq jismlarda molekulalarning joylashishi. Qattiq jismlarda molekulalar orasidagi masofalar molekulalarning kattaligiga teng, shuning uchun qattiq jismlar o'z shakllarini saqlab qoladi. Molekulalar kristall panjara deb ataladigan ma'lum bir tartibda joylashtirilgan, shuning uchun normal sharoitda qattiq moddalar o'z hajmini saqlab qoladi.
"Materiyaning 3 holati" taqdimotidan 5-rasm"Issiqlik hodisalari" mavzusidagi fizika darslarigaO'lchamlari: 960 x 720 piksel, format: jpg. Fizika darsi uchun rasmni bepul yuklab olish uchun rasmni o'ng tugmasini bosing va "Rasmni boshqa saqlash ..." tugmasini bosing. Darsdagi rasmlarni ko'rsatish uchun siz "Materaning 3 holati.ppt" taqdimotini zip arxividagi barcha rasmlar bilan bepul yuklab olishingiz mumkin. Arxiv hajmi 2714 KB.
Taqdimot yuklab olishissiqlik hodisalari
"Tabiatdagi diffuziya" - Sabzavot va mevalarni saqlashda oziq-ovqat sanoatida keng qo'llaniladi. Po'latni eritishda. Diffuziyaga gazlar yoki suyuqliklarning aralashishi misol bo'la oladi. Diffuziya nima? Nafasda diffuziya. Diffuziya hodisasi tabiatda muhim ko'rinishlarga ega bo'lib, fan va ishlab chiqarishda qo'llaniladi.
"Materiyaning agregat holatlarini o'zgartirish" - Materiyaning agregat o'zgarishlari. Bug'lanishning o'ziga xos issiqligi. Qaynatish harorati. Qaynatish. Suvning agregat holatidagi o'zgarishlarning harorat grafigi. Erish va kristallanish harorati. bug'lanish shartlari. yig'indisi o'zgarishlar. Bug'lanish. Issiqlik miqdorini hisoblash. erish va qotib qolish jarayoni.
"Materaning 3 holati" - Krossvordni yeching. Kristallanish. Qattiq jismlarda molekulalarning joylashishi. Jarayonga misollar. davlatlar. Modda. Gazlarning xossalari. Bug'lanish. Krossvord uchun savollar. Suyuqliklarning xossalari. Suyuqliklarda molekulalarning joylashishi. Muz. Qattiq jismlarning xossalari. Kondensatsiya. Zarrachalar harakati va o'zaro ta'sirining xarakteri.
"Maddalarning tarqalishi" - Xushbo'y barglar. To'q rang. Hikmatlar. Miletlik Thales. Geraklit. Biz muammolarni hal qilamiz. Qadimgi Yunoniston olimlari. Texnologiya va tabiatdagi diffuziya. Biologiya sevuvchilar uchun vazifalar. Diffuziya. Diffuziya hodisasi. Demokrit. Kuzatishlar. Gazlardagi diffuziya.
"Erilish paytidagi issiqlik hodisalari" - D.I. Mendeleev. Brifing. Kaliy permanganatning suvda erishi. ekzotermik jarayon. Xonadoshingizni tekshiring. Sizga fizika va kimyo qonunlarini yanada chuqurroq bilishda muvaffaqiyatlar tilaymiz. diffuziya tezligi. Issiqlik harakati deb ataladigan narsa. Molekulalarning o'zaro kirib borishi. Yechimlarning qiymati. Amaliy topshiriqlar.
"Molekulalarning o'zaro ta'siri" - Ikki bo'lak temir mixni ulash mumkinmi? Attraktsion zarralarni birga ushlab turadi. I variant Tabiiy aralashmalar tarkibiga kirmaydi: a) gil; b) sement; c) tuproq. gazsimon moddalar. II Variant Sun'iy aralashma: a) gil; b) sement; c) tuproq. Gaz molekulalari orasidagi masofa ko'proq o'lchamlar molekulalarning o'zlari.
Mavzu bo'yicha jami 23 ta taqdimot
Suyuqlikdagi molekulalar gazga qaraganda bir-biriga yaqinroqdir. Bu 1300 hajm bug'ning kondensatsiyasi natijasida 1 hajm suv hosil bo'lishidan kelib chiqadi. Gazdan suyuqlik hosil bo'lishi molekulalar orasidagi tortishish kuchlarining paydo bo'lishining natijasidir. Molekulalarning kinetik energiyasini yengish uchun ular muhim bo'lishi kerak. Gazning sovishi molekulalar tomonidan kinetik energiyaning yo'qolishi bilan birga bo'lib, ular haroratga yetguncha ularning kinetik energiyasi molekulalararo tortishish kuchlarini to'sib qo'ymaydi va natijada gaz suyuqlana boshlaydi.
Suyuq holat gazsimon holatga qaraganda qattiq jismga yaqinroqdir. Suyuq holatdagi zarralar qattiq holatga qaraganda bir-biridan uzoqroq va kamroq tartibli. Qattiq jismning erishi odatda hajmning 10% ortishi bilan birga kechadi (Ushbu bayonot suv, vismut, quyma temir kabi moddalarga taalluqli emas, ularning erishi hajmi kamayishi bilan birga keladi).
1 atm haroratda 1 mol suyuqlikni bug'ga aylantirish uchun zarur bo'lgan issiqlik miqdori deyiladi bug'lanishning standart entalpiyasi:∆H° ilovasi. 1 atm haroratda 1 mol bug'ning kondensatsiyasi paytida bir xil miqdorda issiqlik chiqariladi. 1 atm haroratda 1 mol qattiq jismni suyuqlikka aylantirish uchun sarflangan issiqlik miqdori deyiladi standart sintez entalpiyasi:∆H° kvadrat 1 mol suyuqlik 1 atm haroratda qattiqlashganda bir xil miqdorda issiqlik chiqariladi. Standart termoyadroviy entalpiyalar bug'lanishning standart entalpiyalariga qaraganda ancha kichikdir. qattiq holat suyuqlikka o'tish suyuqlikdan gazsimon holatga o'tishga qaraganda molekulalararo tortishishning kamroq buzilishi bilan birga keladi.
Guruch. 8.1 Suyuqlik molekulalari orasidagi masofa:
a- suyuqlik molekulalari orasidagi masofa; b- suyuqlikning xayoliy siqilishi, uning molekulalarining ko'proq yaqinlashishiga olib keladi;
1 - molekulalar orasidagi tortishish kuchlari; 2 - molekulalarning itarishiga olib keladigan elektron bulutlarning o'zaro qoplanishi.
Suyuqliklar ma'lum hajmga ega va ularning siqilishi ahamiyatsiz.
Suyuqlikda molekulalar orasidagi masofa ularning tortish kuchlari va qo'shni elektron bulutlarning itaruvchi kuchlari o'rtasidagi muvozanat tufayli yuzaga keladi (8.1-rasm). Suyuqlikdagi molekulalararo tortishish kuchlari qattiq jismlarga qaraganda kichikroq, lekin suyuqlikka ma'lum bir shakl berish uchun etarlicha kuchli emas. Shuning uchun suyuqlik oqadi va uni o'z ichiga olgan idish shaklini oladi.
Gazlar orqali tarqalishi mumkin yuqori tezlik ularning molekulalarining harakati. Suyuqliklarning diffuziya tezligi gazlarnikidan ancha past; qattiq jismlar uchun undan ham kichikroq. Suyuqlik molekulalari tez harakat qilsa ham, ular suyuqlikning bir qismidan ikkinchisiga erkin o'ta olmaydi, chunki ular molekulalarni qo'shni molekulalarga bo'shashmasdan o'ralgan tarmoqqa bog'laydigan jozibali kuchlar tomonidan ushlab turiladi. Biroq, ba'zida molekula bu tarmoqdan "buziladi" va suyuqlikning boshqa hududiga o'tadi, ya'ni tarqaladi. Suyuqlik molekulalari doimo harakatda bo'lganligi sababli, ularning ba'zilari suyuqlikdan bug'ga chiqish uchun etarli energiyaga ega. (Tushuncha bug ' kritik haroratdan past haroratdagi gazni nazarda tutadi.).
Qochib ketayotgan molekulalarning energiyasi o'rtacha energiyadan ancha katta va boshqa molekulalarning jozibador kuchlarini engish uchun etarli. Suyuqlikda qolgan molekulalarning energiyasi chiqib ketadigan molekulalarning energiyasidan kamroq bo'ladi, shuning uchun suyuqlikning harorati pasayadi.

Guruch. 8.2 Suyuqlik va uning bug'i yopiq idishda muvozanatga erishadi: bug'lanish va kondensatsiya tezligi tenglashadi.
Yuqori energiyali molekulalarning ulushi harorat oshishi bilan ortib borayotganligi sababli, bug'lanish tezligi ham ortadi. Suyuqlik bor ekan, bug'lanish davom etadi. Biroq, agar suyuqlik yopiq idishda bo'lsa, bug 'molekulalari idishning devorlari bilan to'qnashadi; ularning ba'zilari suyuqlik tomon harakat qiladi, ba'zilari esa unga qaytadi, ya'ni keladi kondensatsiya(8.2-rasm). Muvozanat suyuqlik bug'lanishi va bug'ning kondensatsiyasi tezligi tenglashganda erishiladi.






