Fizikte eriyen nedir. Petrol ve gazın büyük ansiklopedisi. Kimyasal bileşiklerin türüne göre erir
Hepimiz biliyoruz okul kursu fizik, bir madde değiştiğinde toplama durumu bir faz geçişi meydana gelir. içindeki madde katı hal doğrudan gaza geçebilir. Örneğin kuru buzun (katı karbon dioksit, CO 2 ) sıcaklığı yükseldiğinde gaza dönüşür. Bu işleme süblimasyon veya süblimasyon denir.
Çoğu insan kendi şekerlerini alır ve yer. satın alındıktan sonra birkaç gün veya saat içinde. Daha ilginç yöntemlerden biri, erimiş kakao yağının düşük seviyeli X-ışınları ile ışınlanmasını içerir. Bu, doktor gibi bir röntgen resmi almak için değil, girişimin resmini çekmek için yapılır. Bu tekniğe X-ışını kırınımı denir ve başka bir bölümde tartışılacaktır. Uzman bir teknisyen, resmi yorumlayabilir ve katı bir kafes içindeki atomların veya moleküllerin konfigürasyonunu çıkarabilir.
Ancak daha sık başka süreçler meydana gelir. Örneğin, su donduğunda, sıvı hal katı hale gelir (kristalleşme). Taşlar lav içinde eritildiğinde katıdan sıvıya dönüşürler (ergime). Bir su ısıtıcısında su kaynadığında sıvıdan gaza dönüşür (buharlaşma ve kaynama). Söz konusu madde, ilave ısı eklerken veya çıkarırken yeni bir duruma geçerken - sıvı, katı veya gaz halinde, sıcaklık değişmez. Bu neden oluyor?
Optimum proses elde edilene kadar çeşitli ısıtma, soğutma ve karıştırma modları test edilir. Çikolatanın ağzınızda bu kadar iyi erimesinin nedenlerinden biri de budur. Bu özellik aynı zamanda ilaç firmaları tarafından fitillerin hazırlanmasında da kullanılmaktadır. Bir fitil, bir ilaçla karıştırılmış kakao yağından oluşan ve daha sonra ağızdan başka bir açıklığa sokulan kurşun şeklinde bir ilaç verme sistemidir. Kakao yağı eridikçe, ilaç yavaş yavaş salınır.
İlaçlar yüzeye yakın kalabilir veya kılcal damarlara yayılabilir ve dolaşım sistemi yoluyla vücudun geri kalanına yayılabilir. Üç aşama, küçük Yunan harfleri, gama ve delta ile tanımlanır. Alfa ve delta fazları ayrıca ferrit veya ferritik demir olarak adlandırılır ve bunlardan elde edilir. Latince kelime demir demir için. Gama fazı, İngiliz metalürjist William Chandler Roberts-Austin'den sonra östenit veya östenitik demir olarak da adlandırılır. Östenitik demir, ikisinin daha karmaşık olanıdır.
Erime sırasında sıcaklığın neden değişmediğine dair ayrıntılı bir açıklama
Sakin bir şekilde limonata içtiğinizi (sıradan su ile yaklaşık olarak aynı ısı kapasitesine sahip) hayal edin. Bu limonatada buz parçaları yüzer. Bu yarım limonata, yarım buz karışımının sıcaklığı sıfır santigrat dereceye yakındır. Bir bardağı avuçlarınızda tutarken ve içindeki süreci gözlemlerken, buz erimeye başlar, ancak kabın içindekiler, içindeki tüm buzlar eriyene kadar ısınmaz.
Demir, katı olduğu sıcaklık aralığında manyetik özelliklerini değiştirdiğinden, alfa fazı başlangıçta bir alfa manyetik fazı ve bir manyetik olmayan beta fazına bölünmüştür. Bu manyetik geçişin polimorfizm ile ilgisi olmadığı için beta fazı bu şekilde sahnelendi.
Kristal yapı iki ferritik fazdan biri merkezde olmak üzere kübiktir ve y-östenitik fazı daha yoğun paketlenmiş tane merkezli kübiktir. Bu yoğun şekilde paketlenmiş fazın kristal yapısı, adı geçen altıgen yakın pakete karşılık gelir. Dünyanın çekirdeğinin, bir demir-nikel alaşımı olan çok büyük tek bir epsilon faz kristalinden oluştuğuna inanılmaktadır.
Soru. Erime sırasında sıcaklık neden değişmez? gelen termal enerji çevre, karışımı bir bütün olarak ısıtmadan buzu eritir. Isı miktarını hesaplamak için bu denklem (ısı miktarı nerede, numunenin kütlesi, sıcaklıktaki değişim) işe yaramaz mı? Hiç değil - sadece faz geçişi için geçerli olmadığı anlamına gelir.
Çelik bir demir alaşımıdır - bir metal matrisindeki diğer elementlerle demir karışımı. İlk çelikler muhtemelen bir demir kılıcın boşlukları kömür ocaklarında ısıtıldığında ve bazı karbon parçacıkları demir matrisine girdiğinde tesadüfen yaratıldı. Karbon ile çelik daha serttir ve demirden daha yüksek çekme mukavemetine sahiptir, ancak aynı zamanda daha kırılgandır. Çelik, demiri büken gerilimler altında bükülür, ancak çeliğin kırılarak demire dönüşmesi daha olasıdır.
Her iki isim de bu bileşiğin sert, kırılgan ve son derece metalik olmayan doğasını andırıyor. Tüm çözücüler gibi, demirin de karbonu çözme yeteneği sınırlıdır. Yüksek ila çok yüksek konsantrasyonda, α-ferrit matrisinde sementit kristalleri oluşmaya başlayacaktır. Yuvarlak kristallerle benzer bir karışıma sferoidit denir. Daha fazla bilgi için metalurji uzmanıyla iletişime geçin. Klasik çelikler, az miktarda karbon ile yüksek miktarda demir karışımıdır, ancak modern çelikler ayrıca krom, nikel, manganez, molibden veya vanadyum gibi diğer metalleri de içerebilir.
Bir maddenin sıcaklığının aktarılan ısı miktarına bağımlılığının bir grafiğini oluşturmak mümkündür. Örneğin, Şekil. Şekil 1, dondurucudan alınan buzun faz geçişlerinin bir grafiğini göstermektedir. Bölüm buzun ısınmasına, bölüm buzun erimesine, bölüm ortaya çıkan suyun ısınmasına, bölüm suyun kaynamasına, bölüm ise ortaya çıkan buharın ısınmasına tekabül ediyor.
Paslanmaz çelik üretmek için krom eklenir. Ortaya çıkan alaşım oksidasyona ve korozyona direnir. Demiri olmaması gereken bir fazda tutarak sertliğini artırmak için nikel ve manganez eklenir. Oda sıcaklığında, demirin doğal hali nispeten yumuşak, merkez merkezli, kübik α-ferrit fazıdır. ile birlikte demire ortalama miktarda karbon eklenmesi sağlıklı bir doz nikel ve molibden çizgi bize özel özelliklere sahip bir karışım verir. Sıcaklık geçiş sıcaklığının üzerine ısıtıldığında ve normal olarak soğumaya bırakıldığında, merkez merkezli γ-östenitik kübik yapı kilitli kalır.

Pirinç. bir. Faz geçişlerinin grafiği H 2 0.
Gördüğünüz gibi, eğri genellikle artar, yani ısıdaki bir artış, sıcaklıkta bir artışa yol açar. Bununla birlikte, maddenin durumunu değiştirmek enerji gerektirdiğinden, faz geçişleri sırasında ( ve sıcaklıklarında) eğri yatay olarak çalışır. Geçiş tamamlandıktan sonra sıcaklık tekrar yükselmeye başlar.
Bir anlamda nikel ve molibden atomları koruma görevi görür. Kübik bir kafes merkezli merkezde demir atomlarının amaçlarına ulaşmasını engellerler. Korozyon direnci için krom ekleyin ve dünyanın en yaygın kullanılan paslanmaz çelik grubuna sahip olursunuz.
Östenitik paslanmaz çelikler tencere, çatal bıçak takımı, mutfak lavaboları, gıda işleme ekipmanları, delici takılar, cerrahi ekipmanlar ve disket kepenklerinde bulunabilir. Östenitik paslanmaz çelikler genellikle demire eklenen krom ve nikel oranlarıyla anılır.
Bir buz torbası alıp ocağa koyduğunuzu düşünelim. Bundan önce buzun sıcaklığı suyun donma noktasının altındaydı, diyelim ki -5 °C. Ama ocakta değişmeye başladı. Faz geçişi olmadığı sürece, verilen ısı miktarındaki artışla buzun sıcaklığı lineer olarak artar. c= 2100 J/(kg⋅°C) — özısı buz.
Östenitik çelikler sertlikleri ile dikkat çekicidir, ancak en karmaşık çelik ailesi değildirler. Bu fark, Alman metalurji uzmanı Adolf Martens'in adını taşıyan martensitik çeliğe aittir. Martensitik çelik çatal bıçak takımlarında, neşterlerde, anahtarlarda, türbinlerde ve sertliğin önemli olduğu diğer uygulamalarda kullanılır.
Martensit hazırlama tarifi, ana demir, karbon, krom karışımının, demir y-östenitik faza girene kadar ısıtılmasıyla başlar. Bunu, sıcak çeliğin suya, tuzlu suya veya yağa daldırıldığı su verme adı verilen hızlı bir soğutma işlemi takip eder. Sıcaklık düşüşü o kadar diktir ki kristal, merkezi merkezli kübik bir gövdeden dörtgen bir merkeze geçer. Normal basınçlardaki bir katıdaki karbon atomları, iki düzenlemeden birinde var olmak ister: kübik veya kübik merkezli kübik.
Buz bir sıcaklığa ulaştığında t 1 = 0 °C, katı halde kalamayacak kadar ısınır ve bir faz geçişi yaşayarak erimeye başlar (eğri grafikte düzleşir). Bu süreç - buzun kristal kafesinin yok edilmesi - bir ısı kaynağı tarafından üretilen enerjiye ihtiyaç duyar. Bu nedenle erime sırasında sıcaklık değişmez.
Dörtgen düzenleme doğal değildir ve yalnızca malzemenin atomların "doğru" konumlarına hareket etmesine izin vermek için çok hızlı soğuduğu için var olur. Ortaya çıkan cihaz kararsız ancak dayanıklıdır - yarı kararlıdır. Martensitik yapı, ısı eklenerek kolayca yok edilebilir. Bu kontrol edildiğinde, işleme sertleştirme denir. Kontrolsüz ısı ilavesi felaket olabilir.
Çeliği çeşitli aşamalardan geçirerek gerekli özelliklere sahip olana ulaşmak, büyük ölçüde uygun miktarlarda ısıtma ve soğutma ile sağlanır. Benzer değişiklikler çelikte de meydana gelir. Her bir uçağın etkisi, ciddi ancak felaket olmayan ciddi yapısal hasara neden oldu. Her jet, bir bankadan diğerine uçmaya yetecek kadar jet yakıtı ile doluydu. Ateşlendiğinde sıcaktı ama içindeki çelik kirişleri eritecek kadar sıcak değildi.
Torbayı ocakta bir süre izledikten sonra, sonunda tüm buzların eridiğini fark ediyorsunuz. Soba üretmeye devam ederken Termal enerji, su sıcaklığı yükselir. Son olarak, içinde kabarcıklar belirir. "Evet," diye düşünüyorsunuz, "başka bir aşama geçişi." Evet öyle. Su ısınır ve bir sıcaklıkta t 2 = 100 °C kaynar. Çanta şişmeye başlar.
Kuleler geliştirildikçe varlığını sürdürmeye devam etmiştir. Her iki uçak da o kadar ağır hasar gördü ki itfaiyeciler yangını söndüremedi hatta azaltamadı. Yatay çelik kirişler daha sıcak, daha sıcak ve daha sıcaktı, ama erimediler. Bunun yerine plastiğe döndüler ve sarktılar. Bu, onları dikey destek kirişlerinden uzaklaştırarak zeminin çökmesine neden oldu. Tüm bu kirişler bölündükten sonra, feci bir çöküş oldu, tüm kule çökene kadar bir kat diğerine tırmandı.
Bu, yaklaşık bir saat yanan jet yakıtına maruz kaldıktan sonra, 110 katlı kulelerin her biri için bir kez olmak üzere iki kez tekrarlandı. Yangın daha sonra ortak bir bodrumdan 40 katlı bir binaya sıçradı. Bu, birkaç dahili dikey sütunu zayıflattı. Biri başarısız olduğunda, yakındaki diğerleri telafi edemedi ve üçüncü felaket kazası yaklaşık 7 saat sonra başladı.
Suyun sıcaklığını ölçüyorsunuz. Şaşırtıcı bir şekilde, su kaynarken sıcaklığı da değişmez. Yine, sıvıdan gaza geçişi tamamlamak için belirli bir miktarda ısı gereklidir.
Ayrıntılar Kategori: Moleküler-kinetik teori Yayınlanma tarihi 06.11.2014 13:52 İzlenme: 8274Aynı madde belirli koşullar altında farklı kümelenme durumlarında olabilir - katı, sıvı veya gaz halinde. Bir durumdan diğerine geçiş sırasında, bu maddenin moleküllerinin bileşimi değişmez. Sadece konumları, termal hareketin doğası ve moleküller arası hareket kuvvetleri değişir.
Çelik kirişlerin yapısal yangınlarda yumuşaması yaygındır. Aşağıdaki fotoğraf, Manhattan'ın Yukarı Batı Yakası'ndaki eski NYC Merkez Tren İstasyonlarının terk edilmiş kargo iskelesini göstermektedir. Kalaylı metal teneke, kalaylı teneke kutular, "kalay hastalığı" veya "kalay cüzzamı". Kırmızı fosfor polimerik bir katıdır Beyaz Fosfor kristalli bir katıdır Siyah fosfor grafite benzer bir yarı iletkendir.
- Saf titanyumda, alfa fazı oda sıcaklığından 882 ℃'ye kadar bulunur.
- 400 km'de: Olivin, spinel polimorfizmine dönüşüyor.
- 700 km'de: Spinel, daha da yoğun bir perovskit yapı ile değiştirilir.
- Kalsit aragonit, yumuşakça kabukları.
İtibaren katı hal madde sıvı hale gelir ve sıvıdan gaza geçer. Böyle bir geçiş denir faz geçişi .
Erime

Düşük sıcaklıklarda, tüm maddeler donar ve atomları ve molekülleri o kadar sıkı bir şekilde paketlenir ki, karşılıklı çekim kuvvetleri sadece performans göstermelerine izin veren katılara dönüşür. salınım hareketleri denge konumu etrafında. Bu nedenle, normal koşullar altında katılar hacmini ve şeklini korur.
Uydu, iniş sırasında birkaç dakika boyunca o kadar yoğun bir şekilde ısınır ki, uzay kapsülünü çevreleyen her molekül iyonize olur ve astronotları hiçbir iletişim sinyalimizin geçemeyeceği bir plazma zaman bariyerinde saklar. Sıcaklık azaldıkça hava daha yoğun hale gelir ve plazma durumu artık kararlı olamaz.
- Yıldırım ve diğer kıvılcımlar.
- Gemi atmosferde ilerlerken yavaşlamaya devam ediyor.
Yıldızlar Plazmanın bu evliliği ve manyetik alan yıllık güneş aktivitesi döngüsünün önemli bir özelliğidir. Güneş'in ekvatorunun yakınındaki plazma, kutuplarının yakınındaki plazmadan biraz daha hızlı döner. Güneş'in manyetik alanı plazmasında donduğunda, alan gerilir ve bükülür. Güneş lekeleri, parlamalar, çıkıntılar ve diğer güneş lekeleri, gnar manyetik alanı Güneş'in yüzeyinden geçerken, güneş plazmasını da beraberinde taşırken gelir ve gider. bulutsu. Neon tüpleri "plazma küreleri" tokamak ve diğer kuark-gluon plazma füzyon jeneratörleri. Nispeten yumuşaktır ve kırılma indisi ona kesimde kullanılabilecek bir parlaklık verir. Soda-kireç camından biraz daha pahalıdır ve mükemmel olması nedeniyle elektrik uygulamalarında tercih edilir. elektriksel özellikler izolasyon. Termometre tüpleri ve sanat camı da genellikle kurşun cam olarak adlandırılan kurşun-alkali camdan yapılır. Bulaşıklar için ve prizma olarak optik aletler için kullanılır, yoğunluğu yüksek derecede saçılma gücü verir; - sözde, çünkü daha önce silika toz haline getirilmiş çakmaktaşından elde edildi. Sıcaklık değişimine ve kimyasal korozyona karşı yüksek dirence sahiptir. Kireç veya kurşun cam kadar uygun olmayan ve kireç kadar ucuz olmayan borosilikat maliyeti, kullanışlılığı açısından orta düzeydedir. Boru hatları, ampuller, fotokromik camlar, sızdırmaz huzmeli farlar, laboratuvar ürünleri ve fırınlanmış ürünler borosilikat ürünlerine örnektir. Boraks ayrıca pentahidrat ve susuz formlara sahiptir. Oksijen içeren bor bileşikleri için genel terim. Silikon dioksit ve bor oksit içeren bir dizi cama atıfta bulunan genel bir terim. Çoğu uygulamada iki özel cam kullanılır: yüksek seviye cam geçiş ve yüksek mukavemetli "nötr" cam. Borosilikat ile karşılaştırıldığında, alüminosilikat üretimi daha zordur. Elektriksel olarak iletken bir film ile kaplandığında, direnç olarak alüminosilikat cam kullanılır. elektronik devreler. İngiliz camına göre: Tekstiller için, iyi kimyasal direnci ve yüksek yumuşama noktası nedeniyle çok düşük sodyum oksit içeriğine sahip alümino-borosilikat cam tercih edilir. aynı zamanda, kask, tekne, boru hattı, araba şasisi, halat, araba egzozu ve diğer birçok öğeyi yapmak için güçlendirilmiş plastiklerde kullanılan bir tür fiberglastır. Küçük ama önemli bir cam türü olan alüminosilikat, nispeten küçük miktarlarda kalsiyum oksit, magnezyum oksit ve bor oksit de dahil olmak üzere %20 alüminyum oksit içerir, ancak çok az soda veya potasyum içerir. Bu cam 900℃'ye kadar termal şoka dayanıklıdır. Yapması çok zordur, bu nedenle tüm gözlüklerin en pahalısıdır. Televizyon, absorbe edilmesi gereken X-ışınları üretir veya bunlar sonunda sağlık sorunlarına neden olabilir. röntgen minimum miktarda ağır oksit içeren cam tarafından emilir. Bu diferansiyel kötü haber güneşin rengi için. . Saf kristal katılar, bir katının eriyerek sıvı hale geldiği sıcaklık olan karakteristik bir erime noktasına sahiptir.
Bir maddenin katı halden sıvı hale geçmesi olayına ne denir erime . Bu süreç, sıcaklık yükseldiğinde gerçekleşir.
İlkbaharda, güneş ısındığında kar yığınları erimeye başlar. Karı oluşturan minik buz kristalleri suya dönüşür. Ancak havanın ısınmasına ve sıcaklığının sıfırın üzerine çıkmasına rağmen, eriyen karın sıcaklığı ile eriyen suyun sıcaklığı, kar tamamen eriyene kadar 0 0 C'de kalır. Mesele şu ki, erime yavaş yavaş gerçekleşir. Erime sırasında madde dışarıdan aldığı ısıyı emer ve bir süre hem katı hem de sıvı haldedir. Ve sıcaklığı tamamen eriyene ve sıvı hale gelene kadar değişmez.
Bir katı ısıtıldığında ne olur? Sıcaklık arttıkça maddenin içindeki parçacıkların salınım hızı artar. Bu nedenle de artar içsel enerji. denilen belirli bir sıcaklıkta erime noktası , kristal hücre sağlam vücut bozulmaya başlar. Moleküller daha fazla özgürlük kazanır. Zıplayabilir ve başka pozisyonlar alabilirler. Madde sıvı hale dönüşür.
İle sağlam erimeye başlar, erime noktasına kadar ısıtılmalıdır. Dışarıdan ısı almaya başladığında, bir süre ısınma süresi ile doğru orantılı olarak sıcaklığı yükselecektir. Erimeye başlayana kadar bu şekilde kalır. Ancak sıcaklığı erime noktasına eşitlenir ulaşmaz değişmeyi bırakacak ve tüm madde sıvı hale gelene kadar sabit kalacaktır. Bundan sonra, sıvının sıcaklığı tekrar yükselmeye başlayacaktır.
Ancak sıvı ısı almayı bırakırsa soğumaya başlayacaktır. Ve sıcaklığı bir değere düşer düşmez, sıcaklığa eşit erime, kristalleşme süreci başlar.
Her maddenin kendi erime noktası vardır. Normal basınçta (760 mm Hg), buz 0 o C'de erimeye başlar. Yüksek sıcaklık metaller arasında erime tungstene sahiptir - 3422°C. Basit bir madde karbon 3500 - 4500 ° C sıcaklıkta erir. Ve alkolün erime noktası eksi 114 o C'dir.
kristalizasyon
Bir sıvının sıcaklığı azaldıkça molekülleri daha az hareketli hale gelir. Ve katı bir cismin karakteristiği olan molekülleri belirli bir katı düzende tutan çekici kuvvetler artar.
Eğer bir sıvı madde belli bir sıcaklığa soğutun, sertleşecektir. İşlem faz geçişi sıvıdan katıya denir kristalleşme . Erimenin aksine, bir madde ısı aldığında, kristalleşme sırasında onu verir ve sıcaklığı düşer.
Bu işlemin gerçekleştiği sıcaklığa denir. kristalleşme sıcaklığı . Saf bir madde için erime noktası kristalleşme sıcaklığına eşittir.
Erime gibi, kristalleşme de yavaş yavaş gerçekleşir. Benzer şekilde, bir sıvı ve bir katı, tüm madde katılaşana kadar aynı sıcaklığa sahip olacaktır.
Havya ile eritilen sıvı kalay, havyayı çıkardığımızda katılaşır ve katı hale gelir. Kalıplara dökülen erimiş sıvı metal, sıcaklık düştükçe katılaşır.
Her yıl doğada kristalleşme gözlemliyoruz, rezervuarlardaki su düşük sıcaklıklarda donduğunda, yağmur damlaları yerine kar taneleri düşüyor.
Maddenin kümelenme durumundaki değişikliklerin grafiği
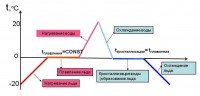
Erime ve kristalleşme süreçleri, bir maddenin kümelenme durumunun sıcaklığa bağlı olarak nasıl değiştiğini gösteren bir grafikte açıkça görülebilir.
Bir buz parçasının sıcaklığını ölçelim. Termometre -20 oC gösteriyor. Buzu bir kovaya koyun ve odaya getirin. Yavaş yavaş erimeye başlayacak ve sıcaklığı artacaktır. Termometre 0 o C gösterdiğinde, tüm buz eriyene kadar sıcaklıkta daha fazla artış olmayacaktır. Hepsi suya dönüştüğünde kovadaki su oda sıcaklığına gelene kadar ısınmaya başlayacaktır.
Bir kova suyu soğuğa çıkaralım. Su soğumaya devam edecek. Sıcaklığı 0 o C'ye düştüğünde buza dönüşmeye başlayacaktır. Ve tüm su katılaşana kadar sıcaklık değişmeyecek. Ve ancak bundan sonra tekrar yavaş yavaş hava sıcaklığına eşit bir değere düşmeye başlayacaktır.
Böyle bir grafik yardımıyla, herhangi bir maddenin kümelenme durumundaki değişiklikleri görüntüleyebilirsiniz.






