kristalizasyon formülü. Kristal cisimlerin katılaşması
Bir maddenin katı halden sıvı hale geçmesine erime, bir maddenin katı halden sıvı hale geçmesine erime denir. sıvı hal bir katıya - katılaştırma veya kristalleştirme yoluyla.
Eridiğinde sağlam kristal kafesi oluşturan parçacıklar arasındaki mesafeler artar ve kafesin kendisi yok olur. Bu, erime işlemi sırasında moleküler potansiyel enerji maddeler. Bu nedenle, bir maddenin erimesi kendiliğinden gerçekleşemez, çünkü bu işlem için enerji harcanması gerekir.
Kristalleşme sırasında tanecikler birbirine yaklaşarak bir kafes oluşturur ve potansiyel enerjileri azalır. Bu nedenle, kristalleşme ancak sıvı, enerjisini bazı dış cisimlere verdiğinde meydana gelebilir.
Yani kütle birimi sıvı madde daha fazla var içsel enerji sıcaklıkları aynı olsa bile, aynı maddenin katı haldeki birim kütlesinden daha fazladır.
Maddenin tüm fiziksel ve yapısal olarak homojen olduğu bölge. kimyasal özellikler, bu maddenin halinin fazı olarak adlandırılır. Aynı sıcaklıktaki bir maddenin katı ve sıvı fazları, eğer katı faz enerji alamıyorsa ve sıvı faz onu veremiyorsa, keyfi olarak uzun bir süre dengede kalabilir. Örneğin, çevredeki tüm cisimlerin sıcaklığı aynı ve 0°C'ye eşitse, buz suda uzun süre yüzebilir.
Diğer cisimlerden enerji alan maddenin yalnızca katı bir fazı olsun. Daha sonra, kristal kafes içindeki parçacıklar arasındaki mesafeler ve hareket hızları artacağından, önce bu maddenin hem moleküler potansiyeli hem de moleküler kinetik enerjileri artacaktır. Ardından, belirli bir sıcaklıkta kristal kafesin yıkımı başlayacaktır. Tüm madde eriyene kadar sıcaklığı değişmeden kalır ve madde tarafından alınan tüm enerji yalnızca moleküler kohezyon kuvvetlerinin üstesinden gelmek için çalışır. Sadece sıvı faz kaldığında, enerji almaya devam ederse, zaten ısınacaktır, yani moleküler kinetik enerjisi artmaya başlayacaktır.
Sıvı faz enerjisini çevreleyen cisimlere bırakırsa, açıklanan tüm işlemler ters sırada tekrarlanacaktır.
Şek. 12.1, erime ve katılaşma sırasında bir maddenin sıcaklığındaki değişikliklerin grafiklerini gösterir. Segment (Şekil 12.1, a), katı halde ısıtıldığında (erime sırasında T'den segmente ve segment - sıvı halde ısıtıldığında) madde tarafından alınan ısı miktarını ifade eder. b) Maddenin sıvı halde soğutulduğunda ('den -'ye), kes - katılaşırken ve kes - katı halde soğutulduğunda verdiği ısı miktarını ifade eder. maddenin katı ve sıvı fazları bir arada olduğu sürece değişmeyen aynı sıcaklıktır.Bu sıcaklığa erime noktası denir.
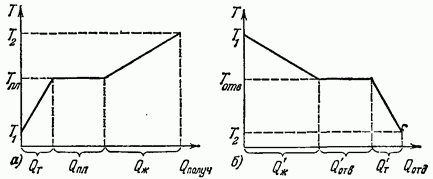
Bir maddenin erimesi ve katılaşması sırasında katı ve sıvı fazlar arasında her zaman keskin bir sınır olduğuna dikkat edin.
Tecrübelerin gösterdiği gibi, amorf maddelerde erime ve katılaşma süreçleri gözlenmez. Isıtıldıklarında yavaş yavaş yumuşarlar ve soğuduklarında yavaş yavaş kalınlaşırlar. Bu durumlarda amorf maddelerin sıcaklığı sürekli değişir ve tüm kütleleri tek tip bir görünüme sahip olduğundan katı ve sıvı fazlar arasında sınır yoktur.
Bu nedenle erime ve kristalleşme sadece kristal cisimler.
Kristal halde ve bir kristal halden diğerine (yeniden kristalleşme veya ikincil kristalleşme); ilk tür. Sıvı veya gaz fazından kristalizasyon, ısının serbest bırakıldığı ekzotermik bir işlemdir. faz geçişi, veya kristalizasyon ısısı; çoğu durumda değişiklik [J / (mol. K) cinsinden] iken: için basit maddeler 5-12, inorganik bileşikler için 20-30, organik bileşikler için 40-60. Yeniden kristalleşme, ısının serbest bırakılması veya emilmesi ile devam edebilir. Endüstride ve laboratuvarda. Uygulamada, belirli bir bileşim, kirlilik içeriği, boyut, şekil ve kusurlu (bkz. ... Kristaller) ürünler elde etmek için ve ayrıca karışımların fraksiyonel olarak ayrılması, büyüyen tek kristaller vb. için kristalizasyon kullanılır.
Prosesin fiziksel ve kimyasal temelleri. Kristalleşmenin mümkün olduğu koşullar, türe göre belirlenir. Kristalleşmenin sonlu bir hızda ilerlemesi için, ilk fazın aşırı soğutulması (aşırı ısıtılması), kristalleşen bir madde ile aşırı doyması veya bir dış faza katılması gerekir. kristalleşme fazının çözünürlüğünü azaltan alan. Aşırı soğutulmuş (aşırı ısıtılmış) veya aşırı doymuş fazda, kristallere dönüşen ve kural olarak şekli, safsızlıkların içeriğini ve kusuru değiştirerek büyüyen kristalleşme merkezleri oluşur. Kristalleşme merkezleri, ilk fazın hacminde homojen olarak ve yabancı katı parçacıkların yüzeylerinde (birincil çekirdeklenme) ve daha önce oluşturulmuş yeni fazın yüzeyinin yakınında (ikincil çekirdeklenme) heterojen olarak görünür. Toplam sayısı Bir çözeltinin birim hacminde veya 1 s'de veya birincil ve ikincil oluşumlarının toplam yoğunluğunda ortaya çıkan kristalleşme merkezleri, aşağıdaki formülle bulunur:
a, çerçeve içinde kabul edilen birincil çekirdeklenmenin kinetik katsayısıdır. Kinetik teori yeni bir aşamanın oluşumu; R -
. T, kristalleşme sıcaklığıdır; y - özel yüzey bedava enerji kristaller; V t - yeni fazın molar hacmi; Erimeler için Dm \u003d DHS ve S \u003d (T 0 -7) / T 0, çözümler için am \u003d RT1n (S + 1) ve S \u003d (c-c 0) / c 0; DH-kristalizasyon entalpisi; c - kristalleşen madde; T 0 ve c 0 - sırasıyla. maddenin sıcaklığı ve doymuş çözelti; E eylemi - çevreden kristalleşme merkezlerine geçiş; ben - ilk fazın hacmindeki ikincil çekirdeklenmenin yoğunluğu. a, E act ve IW'yi ölçmek için kristalleşme merkezlerinin oluşum yoğunluğunun sıcaklığa, aşırı doygunluğa ve yabancı katı parçacıkların konsantrasyonuna bağımlılığı bulunur.
I ve değeri, artan aşırı soğutma (aşırı doygunluk) ile bir veya kristalleşmeyen maksimumlardan (Şekil 1) geçer ve mekanik ile artar. etkiler (karıştırma,
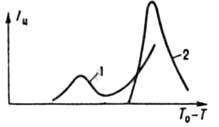
Pirinç. I Çekirdeklenme hızının InSb'nin aşırı soğumasına bağlılığı: I 16 g ağırlığındaki bir eriyik bir kuvars potada 9 dakika boyunca sıcaklığın 15 K üzerinde aşırı ısıtıldı ve ardından 1 derece/dakika hızında soğutuldu; 2 aynı, 55 K'de 20 s'nin etkisi altında . Büyüme sırasında, kristalleşen madde önce oluşan kristalin yüzeyinde adsorbe edilir ve daha sonra kristal kafesine gömülür: güçlü aşırı soğutma ile, yüzeyin herhangi bir yerinde (normal büyüme), zayıf aşırı soğutma ile, katmanlar halinde teğetsel olarak eşit olabilir. sarmal veya iki boyutlu çekirdekler tarafından oluşturulan adımlar üzerinde (katman katman büyüme). Aşırı soğutma belirli bir değerin altındaysa, buna morfolojik kararlılık sınırı denir, normal olarak büyüyen bir kristal, etrafındaki termal veya konsantrasyon alanının şeklini (genellikle yuvarlak) tekrarlar ve katman katman büyüyen bir kristalin şekline sahiptir. bir polihedron. Bu sınır aşıldığında ağaç benzeri kristaller (dendritler) büyür. Nicel olarak, büyüme, yüzeylerinin normal yönde hareket hızına eşit doğrusal bir hız ile karakterize edilir. Endüstride, etkili doğrusal büyüme oranı kullanılır (hacmi kristalin hacmine eşit olan topun yarıçapında 1 s'lik bir artış): I eff \u003d bS n exp (E p / RT) , burada b kinetik büyüme katsayısıdır (10 -5 -10 -14 m/s), n-büyüme parametresi (genellikle 1-3), E p - büyüme (10-150 kJ/mol). b, n ve E p parametreleri, I eff'de ölçülerek bulunur. farklı sıcaklıklar ve çözeltinin aşırı doygunluğu veya eriyiğin aşırı soğutulması. Aşırı soğutmadaki artışla, I m m'ye benzer bir maksimumdan geçer. .
Büyüme hızı, kütle ve çevre (sırasıyla, dış difüzyon ve ısı alışverişi büyüme modları) ile sınırlanabilir. kimyasal etkileşim ortamın diğer bileşenleri ile kristalleşen bileşen (dış kinetik rejim) veya yüzeydeki işlemler (adsorpsiyon-kinetik rejim). Harici kinetik modda, artan reaktif konsantrasyonları ile I eff artar ve . dış difüzyon ve ısı değişim modlarında - karıştırma yoğunluğunda bir artışla, adsorpsiyon-kinetik modda - yüzey kusurlarında bir artış ve yüzey aktif maddelerin konsantrasyonunda bir azalma ile.
Yüksek büyüme oranlarında, kristaller önemli sayıda dengesizlik kusuru (boşluklar, dislokasyonlar, vb.) kazanır. Morfolojik stabilite sınırı aşıldığında, dendritlerin dalları (tıkanma) arasına gömülen ortamın üç boyutlu inklüzyonları hacme girer. Tıkanma nedeniyle, bileşim ortamın bileşimine ne kadar çok yaklaşırsa, I eff o kadar yüksek olur. Büyümeleri sırasında, kristaller ortamdaki herhangi bir safsızlığı yakalar ve yakalanan safsızlık, büyüme hızına bağlıdır. Çözeltide kristalleşme meydana gelirse ve büyüme tamamlandıktan sonra kristaller ortamla temas etmeye devam ederse, dengede olmayan yakalanmış safsızlık ortamdan çıkarılır ve yapıları iyileştirilir (yapısal yeniden kristalleşme). Aynı zamanda, birbirleriyle ve kalıbın duvarlarıyla çarpışmalar sırasında karışık ortamda ek yapısal kusurlar ortaya çıkar. Bu nedenle, sistemde karıştırma yoğunluğuna bağlı olarak kademeli olarak kristallerin sabit bir kusuru kurulur. Naib'de. Kristalizasyon (kütle kristalizasyonu) sırasında bir çoğulluğun oluşumunun yaygın durumunda, çökelmiş faz, çekirdeklenmenin eşzamanlı olmamasından ve büyümelerindeki dalgalanmalardan dolayı polidisperstir. Küçük kristaller büyük kristallerden daha fazla çözünür; bu nedenle, azalan aşırı doygunlukla, ikincisine göre aşırı doygun kalan ortamın bir an gelir.

Pirinç. 2. Boyut dağılım fonksiyonu (olağan r ve en olası r A) izotermal (298 K) sırasında bir karıştırıcılı bir kristalleştiricideki sulu bir çözeltiden periyodik kristalizasyon (Re=104 sayısı): 1 BaSO 4 , ilk aşırı doygunluk S 0 =500 . rA =7.6 um; 2 - K2S04, metanol (1.1) ile tuzlama rA = 1 um; t işlem süresi.
Bu andan itibaren, büyük olanların çözünmesi ve büyümesi (Oswald olgunlaşması) başlar, bunun sonucunda ortalama büyüklük artar ve sayıları azalır. Aynı zamanda, karıştırılan bir ortamda, kristaller çarpışmalar sırasında parçalanır ve bir süre sonra mekanik hareketin yoğunluğu ile belirlenen sabit bir dağılım elde eder. Ana miktarlar, kütle kristalleşme karakteristiği - boyut dağılım fonksiyonu f(r,t)=dN/dr , burada N, t zamanında birim hacim başına boyutu mevcut r boyutundan daha küçük olan kristallerin sayısıdır. Bu fonksiyon genellikle çan şeklinde bir görünüme sahiptir (Şekil 2); yükselen dalı esas olarak kristallerin çekirdeklenmesine, büyümesine, bölünmesine ve çözünmesine (olgunlaşma sırasında) duyarlıdır, inen dal ise agregatlarının büyümesine ve oluşumuna duyarlıdır. Boyutun ortalamadan standart sapması yarıyı geçmezse, ikincisi, belirtilen fonksiyon çağrılır. dar, aşıyorsa - geniş. fonksiyon değişikliği f(r,t) kristalizasyonda aşağıdaki denklemle tanımlanır:

a, kristal büyüme hızının dalgalanma katsayısıdır; D'ye ve v için - cevap. ortamdaki difüzyon katsayısı ve hareket hızı; I ar ve ben p - sırasıyla. daha küçük parçacıkların yapışması ve kristallerin ayrılması nedeniyle belirli bir boyutun oluşum yoğunluğu.
Malzeme ve ısı dengeleri denklemleri sistemi, denklemler (2) ve boyut ve büyüme oranını şekilleri, kusurları ve safsızlık içeriği ile ilişkilendiren denklemler, kütle kristalleşmesini modellemek ve hesaplamak ve bunun için en uygun koşulları seçmek için temel oluşturur. uygulama. Kütle kristalizasyonu periyodik veya sürekli olarak gerçekleştirilir. Periyodik kristalizasyon sırasında, eriyik veya doymuş çözelti (buhar) soğutulur, solvent buharlaştırılır, tuzlayıcı maddeler eklenir (aşağıya bakınız) veya üretim kristallerini oluşturan reaktiflerin kısımları karıştırılır. Sürekli kristalizasyonda, eriyik akışları, aşırı doymuş çözelti veya reaktifler kristalleştiriciye verilir ve kristalli ürün sürekli olarak geri çekilir.
Periyodik ile işlem, aşağıdaki formülle belirlenen kristalleşme hızı:
![]() ,
,
nerede r ve V - resp. katı fazın yoğunluğu ve sistemin hacmi, önce yavaşça artar (indüksiyon periyodu), ardından r'deki eşzamanlı artışın bir sonucu olarak keskin bir şekilde artar ve f ve bir maksimumu geçtikten sonra, I eff'deki azalma nedeniyle azalır (Şekil 3). İndüksiyon periyotları ve kristalleşme hızındaki bir artış sırasında, sistemde kristallerin çekirdeklenmesi ve büyümesi, hız, büyüme, kümelenme ve ayrılmada bir azalma ve ardından Oswald olgunlaşması ve yapısal yeniden kristalleşme döneminde baskındır. İndüksiyon periyodu, kristallerin çekirdeklenmesini ve büyümesini hızlandıran faktörlerin etkisi altında kısalır. Dolayısıyla soğutma eridiğinde, bu süre artan soğutma şiddeti ile önce azalır, daha sonra
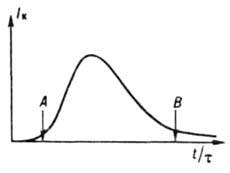
Pirinç. 3. Periyodik kristalleşme oranındaki tipik değişiklik: t - işlem süresi; t, indüksiyon döneminin süresidir; A, yeni bir aşamanın ortaya çıkış anıdır; B - yapısal yeniden kristalleşme aşamasının başlangıcı ve çekirdeklenme ve büyüme oranlarının aşırı soğumaya aşırı bağımlılığı nedeniyle Oswald olgunlaşması artar; soğutma hızı yeterince yüksekse, eriyik şekilsiz kalırken katılaşır (bkz. camsı hal). İndüksiyon süresini azaltmak için, sisteme ürün (tohum) kristalleri eklenir, bu da kristalleşme hızında bir artışa yol açar. Düşük aşırı soğumalarda (süper doygunluklar), çekirdekler hiç görünmez ve sisteme tek kristaller şeklinde verilen tohum, tek bir kristal halinde ve bir toz şeklinde, sözde monodispers ürüne büyüyebilir. dar bir fonksiyon f(r, t).
Sürekli kristalizasyon ile fonksiyon f(r, t) karşılaştırılabilir koşullar altında, sürekli kristalleştiricilerde kalma sürelerinin yayılmasıyla açıklanan periyodik kristalleşmeden daha geniştir. Bu işlevi daraltmak için, kristalleştirme modu, ideal moda genişletmek için ideal yer değiştirme moduna yaklaştırılır (bkz. iplik yapısı). Sistemin düşük bir aşırı doygunluğunda, sürekli kristalleşme dıştaki dalgalanmalara karşı stabildir. koşullar; yüksek aşırı doygunlukta, kristalizasyon sırasında değeri ve boyutu dalgalanır.
Kimyada. ve ilgili endüstrilerin yanı sıra laboratuvarlarda, eriyiklerden ve çözeltilerden kristalizasyon esas olarak daha az sıklıkla kullanılır - buhar ve katı fazlardan kristalizasyon. Eriyiklerden kristalizasyon, esas olarak erimiş maddelerin katılaştırılması ve ayrıca bunların fraksiyonel olarak ayrılması için kullanılır. Döküm (blok) şeklindeki maddelerin katılaştırılması özel formlarda gerçekleştirilir. Küçük ölçekli üretimde (örneğin reaktifler), genellikle eriyiğin doğal ısı değişimi ile soğutulduğu belirli bir boyut veya konfigürasyonda ayrı kalıplar kullanılır. çevre; büyük kapasiteli endüstrilerde (naftalin, vb.), kristalizasyon, su, sıvı NH3, freonlar vb. ile zorla soğutulmuş, yerleşik kalıplara sahip kesitli, boru şeklinde, konveyör ve diğer kristalleştiricilerde gerçekleştirilir.
İnce plakalar veya pullar şeklinde ürünler elde etmek için, kürlemenin kalıplara göre çok daha yoğun gerçekleştiği, sürekli çalışan bant, rulo ve disk kalıpları kullanılır. Bir şerit kalıpta (Şekil 4), ilk eriyik
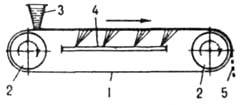
Pirinç. 4. Bant kalıbı: 1 bant; 2 tahrik tamburu; 3 besleme hunisi; 4 soğutma cihazı; Şekil 5'te, kürlenmiş ürün, tamamen katılaşana kadar üzerinde soğutulduğu hareketli bir metal kayış üzerine ince bir tabaka halinde beslenir. Silindir aparatında (Şekil 5) ürün, içeriden soğutulmuş, kısmen bir eriyik banyosuna daldırılmış, dönen içi boş bir tamburun (merdane) dış yüzeyinde kristalleşir; kristaller sabit bir bıçakla tamburdan çıkarılır. Disk cihazlarında ürünler içeriden soğutulan dönen disklerin yüzeyinde kürlenir.

Pirinç. 5. Silindir kalıbı: 1 tambur; 2 banyo; 3 bıçak; 4 soğutucu besleme borusu; 5 meme; 6 erime; 7 kürlenmiş ürün.
Ürünleri granülasyon için hazırlarken, eriyik doğrudan, esas olarak hava (amonyum nitrat, üre, vb. üretimi) veya sıvı, örneğin su veya yağ (plastik, kükürt üretimi, vb.) olmak üzere gaz halindeki bir soğutucu akışına içi boş kulelerde dağıtılır. veya küçük damlacıkların kristalleştiği akışkan tabakalı aparatlar
Çözeltilerden kristalizasyon, esas olarak değerli bileşenleri çözeltilerden izole etmek, ayrıca bunları konsantre etmek ve maddeleri safsızlıklardan arındırmak için kullanılır. Çözünürlüğü büyük ölçüde sıcaklığa bağlı olan maddeler (örneğin, sudaki KNO3) sıcak çözeltilerin soğutulmasıyla kristalleşirken, ana sıvıda bulunan ilk çözücü miktarı sistemde değişmez (izohidrik kristalleşme). Küçük ölçekli üretimde, soğutulmuş ceketlerle donatılmış kapasitif toplu kalıplar kullanılır. Bu tür cihazlarda çözelti belirli bir programa göre sürekli karıştırılarak soğutulur. Soğutma yüzeylerinin yoğun kabuklanmasını önlemek için, çözelti ile soğutucu arasındaki sıcaklık farkı 8-10°C'den fazla olmamalıdır. Büyük ölçekli üretimde, kural olarak, sıyırıcı, vida, disk, tambur ve döner sürekli hareketli kalıplar kullanılır. Sıyırıcılar genellikle, her biri sıyırıcılı bir şafta sahip olan ve ortak veya ayrı bir soğutma ceketi ile donatılmış, seri bağlı kristalleşmeyen boru biçimli bölümlerden oluşur. Mil döndüğünde sıyırıcılar içini temizler. Soğutulmuş boruların yüzeyleri üzerlerine yerleşir ve sonuçta oluşan kalınlaşmış süspansiyonun kesitten kesite taşınmasına katkıda bulunur. Vidalı kalıplarda solüsyon yekpare veya kayış vida kullanılarak karıştırılır ve hareket ettirilir.
Disk kalıpları sabit veya döner disklerle donatılmıştır. İlk durumda (Şekil 6), disklerin yüzeylerini biriken kristallerden temizlemek için aparatın ekseni boyunca kazıyıcılı bir tahrik mili bulunur; ilk çözelti kalıba yukarıdan beslenir ve ortaya çıkan süspansiyon sırayla soğutulmuş diskler arasındaki boşluktan geçer ve alt bağlantıdan boşaltılır. İkinci durumda, diskli şaft bir oluk veya yatay silindirik bir kabın içine yerleştirilir; kristaller sabit sıyırıcılar ile disklerin yüzeyinden uzaklaştırılır.

Tambur kalıbının ana elemanı, yatay eksene 15°'lik bir açıyla yerleştirilmiş ve 5-20 dak-1 frekansında dönen destek bandajlı içi boş bir tamburdur. Bir su ceketi veya hava (bir fan tarafından tamburun iç boşluğundan pompalanan) ile soğutulan çözelti, bir ucundan girer ve süspansiyon diğerinden boşaltılır.
Viskoz çözeltiler (örneğin yağ asitleri) genellikle döner kristalleştiricilerde - içinde silindirik aparatta soğutulur. yüksek hız bıçaklı rotor döner. İkincisi, merkezkaç kuvvetinin etkisi altında, kalıbın iç yüzeyine bastırılır ve onu çökelmiş kristallerden temizler. Çözelti genellikle pozitif basınç altında cihaza beslenecektir. Çözeltinin kristalleştiricisinde kalma süresini ve daha fazla aşırı soğumasını artırmak için birkaç cihaz seri olarak bağlanır.
Sıyırıcı, vidalı, döner ve bazen diskli kalıplar kullanıldığında, genellikle küçük kristaller (0,1-0,15 mm) oluşur, bu da ürünün kekleşme ve adsorpsiyon kontaminasyonunun artmasına neden olur ve ayrıca filtrelenebilirliğini kötüleştirir. Bu nedenle, ürünü büyütmek için, bahsedilen aparatlardan sonra, konsantre süspansiyonun yavaş soğutma altında tutulduğu ve 2-3 mm'ye kadar büyümeye yol açan kristal çözücüler denir.
İri taneli homojen ürünler elde etmek için genellikle akışkan yataklı kristalleştiriciler kullanılır (Şekil 7). İlk çözelti, dolaşımdaki berraklaştırılmış ana likör ile birlikte, ısı eşanjörüne pompalanır, burada soğutma sonucunda çözelti aşırı doygun hale gelir ve sirkülasyon borusundan kristallerin içinde bulunduğu kristal çözücünün alt kısmına girer. Çözeltinin yukarı doğru akışı ile süspansiyon halinde tutulur. Kristalizasyon, esas olarak hazır kristalizasyon merkezlerinde meydana gelirken, büyük kristaller, kalınlaştırılmış bir süspansiyon şeklinde çıkarıldıkları aparatın alt kısmında biriktirilir. Arıtılmış ana likör iki kısma ayrılır: biri aparatın üst kısmından çıkarılır, diğeri devridaim için beslenir.

Pirinç. 7. Akışkan yataklı kristalleştirici: I pompa: 2 ısı eşanjörü: 3 sirkülasyon borusu; 4 kristal çözücü.
Bazı durumlarda, çözeltilerin kristalizasyonu, karıştırma, köpürme, püskürtme ve diğer aparatlarda sıvı, gaz halinde ve buharlaşan soğutucularla doğrudan karıştırılarak gerçekleştirilir. Bir maddenin çözünürlüğü sıcaklıkla çok az değişiyorsa (örneğin, sudaki NaCl), kristalizasyon, doymuş bir çözeltinin hemen hemen Sabit sıcaklık(izotermal kristalizasyon). Tasarım gereği, evaporatör kristalleştiriciler büyük ölçüde evaporatörlere benzer ve dahili veya harici ısıtma odalarına sahip olabilir (Şekil 8). Böyle bir kristalleştiricide, hazneden geçen ilk ve dolaşımdaki çözeltiler kaynama noktasına kadar ısıtılır. Elde edilen buhar-sıvı karışımı, buharın çözeltiden ayrıldığı ayırıcıya girer. Ayırıcıda biriken kristaller, ana likör ile birlikte, ondan ayrıldıkları ve konsantre bir süspansiyon şeklinde çıkarıldığı özel bir aparata gönderilir;
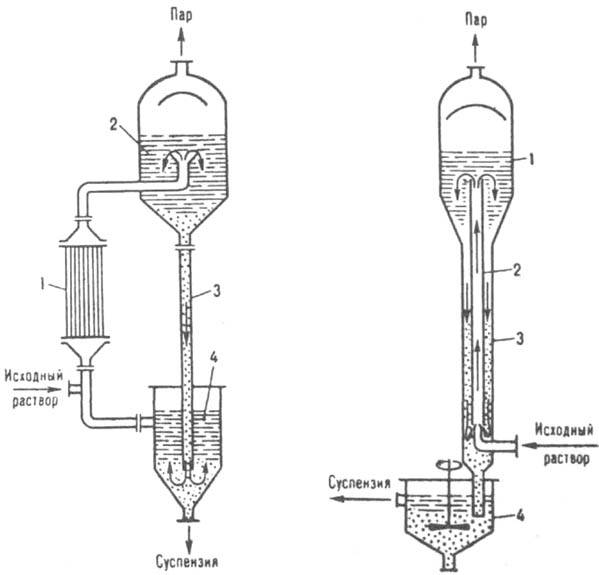
Pirinç. 8. Buharlaşan kristal dağlar: 1 uzak ısıtma odası: 2 ayırıcı: 3 sirkülasyon borusu; 4 kristal ayırıcı.
Pirinç. 9. Vakum kristalleştirici: 1 - ayırıcı: 2 - sirkülasyon borusu: 3 barometrik boru; 4 su contası
arıtılmış ana likör odaya geri döndürülür. Isıtma yüzeylerinin kabuklanmasını (kirlenmesini) önlemek için, çözelti, genellikle eksenel pompalar kullanılarak elde edilen, yeterince yüksek bir hızda (3 m/s'ye kadar) kalıp içinde dolaşmalıdır.
Çözücünün aynı anda soğutulması ve buharlaştırılmasıyla, çözeltinin zorunlu veya doğal sirkülasyonu ile kesikli veya sürekli vakumlu kristalleştiricilerde kristalizasyon gerçekleştirilir. Çözelti, böyle bir aparatta belirli bir vakum oluşturulduğunda çözücünün bir kısmının adyabatik buharlaşması nedeniyle soğutulur. Buharlaşan çözücü miktarı genellikle çözeltinin toplam kütlesinin %8-10'u kadardır. Doğal sirkülasyonlu bir kristalleştiricide (Şekil 9) ilk çözelti, sirkülasyon borusunun alt kısmına beslenir ve sirkülasyon süspansiyonu ile birlikte yükselir, burada basınç düşüşü sonucu kaynar. Ortaya çıkan buharlar ayırıcıdan geçer ve barometrik kondansatöre girer. Aşırı doymuş çözelti ve çökeltilmiş kristaller, kristallerin ana sıvının bir kısmı ile birlikte hidrolik contaya boşaltıldığı barometrik tüpten aşağı doğru hareket eder. Vakumu korumak için vakum pompaları veya buhar püskürtmeli enjektörler kullanılır. Büyük ölçekli üretimde, 4-24 muhafazalı çok damarlı vakum kristalizasyon tesisleri yaygın olarak kullanılmaktadır ve bu tesislerde nadirlik derinliği ilk muhafazadan son muhafazaya kademeli olarak artmaktadır. Vakumlu kristalleştiriciler, evaporatörlü kristalleştiricilerden daha verimli ve ekonomiktir.
Bazı maddeler tuzlanarak kristalleştirilebilir. İnorganik bileşikler izole edilirken, organik maddeler kullanılır (örneğin, sulu çözeltisine metanol, etanol veya NH3 eklenerek Na2S04 kristalleştirilir) veya izole edilen bileşikle aynı iyonu içerir (örneğin, FeS04 kristalleştirilir) konsantre H2S04 ekleyerek dağlama çözeltilerinden); org seçerken bileşikler - su, inorganik tuzların sulu çözeltileri, vb. Çözeltiye tuzlama ajanları olarak organik maddelerin katılması, rejenerasyonlarının karmaşıklığı nedeniyle genellikle işlemin maliyetini artırır. Buhar fazı kristalizasyonu, yüksek orandaki maddelerin kristalleştirilmesine izin verir. kısmi basıncı katı fazın üzerindeki buharlar ve doğrudan gaz halinden kristal hale geçebilen (örneğin, iyot, ftalik anhidrit). Bu tür kristalizasyon, değerli bileşenleri buhar-gaz karışımlarından izole etmek, aerosoller elde etmek, çeşitli cisimlerin yüzeyinde ince kristal tabakalar biriktirmek (örneğin, yarı iletken malzemelerin üretiminde) vb. için kullanılır. Amorf katı fazın kristalizasyonu ve yeniden kristalleştirme, kural olarak, kristalize maddelerin sıcaklıklarına yakın sıcaklıklarda gerçekleştirilir. Bu durumda termal difüzyon süreçleri sonucunda maddenin birincil kristal yapısı değişir veya amorf fazdan çekirdeklenme ve büyüme meydana gelir. Bu tür kristalizasyon, belirli bir kristal yapıya veya kristallik derecesine (termoplastik polimerler, cam, vb.) sahip maddeler ve malzemeler elde etmek için kullanılır. Aydınlatılmış.: Mullin, J.W. Crystallization, çev. İngilizce'den, M., 1965; Magusevich LN.Kimya endüstrisindeki çözeltilerden kristalizasyon, M., 1968; Bamfort A V, Endüstriyel kristalizasyon, per. İngilizce'den, M., 1969; Ponomarenko VG Tkachenko kristalizasyon P., Kurlyand Yu. A., Akışkan yatakta kristalizasyon. kristalizasyon, 1972; Melikhov I.V., Merkulova M.S. Kokristalizasyon, M.. 1975; Gelperin N.I., Nosov G.A., Eriyiklerin kristalizasyon teknolojisinin temelleri, M., 1975; Kidyarov B.I., Eğitim Kinetiği
KRİSTAL VÜCUTLARIN KATILANMASI
Sıcaklık azaldıkça, bir madde sıvı halden katı hale geçebilir.
Bu işleme kürleme veya kristalizasyon.
Bir maddenin katılaşması sırasında, erimesi sırasında emilen aynı miktarda ısı açığa çıkar.

Erime ve kristalleşme sırasındaki ısı miktarı için hesaplama formülleri aynıdır.

Aynı maddenin basınç değişmiyorsa erime ve katılaşma sıcaklıkları aynıdır.
Kristalleşme süreci boyunca bir maddenin sıcaklığı değişmez ve aynı anda hem sıvı hem de katı halde bulunabilir.
KİTAP RAFINA BAKIN!
VAY, İLGİNÇ OLGU!
Renkli buz?
Plastik bir bardağa su ile biraz boya veya çay yaprağı eklerseniz, karıştırın ve alın renk çözümü, bardağı üstüne sarın ve soğuğa koyun, ardından alttan yüzeye bir buz tabakası oluşmaya başlayacaktır. Ancak, renkli buz almayı beklemeyin!

Suyun donmasının başladığı yerde, kesinlikle şeffaf bir buz tabakası olacaktır. Üst kısmı renkli olacak ve orijinal çözümden bile daha güçlü olacak. Boya konsantrasyonu çok yüksekse, buzun yüzeyinde çözeltisinin bir su birikintisi kalabilir.
Gerçek şu ki, boya ve tuz çözeltilerinde şeffaf taze buz oluşur. büyüyen kristaller, yabancı atomları ve safsızlık moleküllerini yer değiştirir ,
mümkün olduğunca uzun süre mükemmel ızgara oluşturmaya çalışmak. Ancak safsızlıkların gidecek hiçbir yeri olmadığında, buz onları kendi yapısında oluşturmaya veya konsantre bir sıvı ile kapsüller şeklinde bırakmaya başlar. Bu nedenle deniz buzu tazedir ve en kirli su birikintileri bile şeffaf ve temiz buzla kaplıdır.
Su hangi sıcaklıkta donar?
Her zaman sıfır derecede mi?
Ancak kaynamış su kesinlikle temiz ve kuru bir bardağa dökülürse ve eksi 2-5 derece C sıcaklıkta pencerenin dışına yerleştirilirse, temiz camla kaplanır ve doğrudan güneş ışığından korunursa, birkaç saat içinde içindekiler. cam sıfırın altına soğuyacak, ancak sıvı kalacaktır.
Daha sonra bir bardak açar ve suya bir parça buz veya kar, hatta sadece toz atarsanız, o zaman kelimenin tam anlamıyla gözlerinizin önünde su anında donacak ve hacim boyunca uzun kristallerle filizlenecektir.
Neden? Niye? Bir sıvının bir kristale dönüşmesi, öncelikle safsızlıklar ve homojen olmayanlar - toz parçacıkları, hava kabarcıkları, kabın duvarlarındaki düzensizlikler üzerinde gerçekleşir. Saf
suyun kristalleşme merkezleri yoktur ve Süper havalı, sıvı kalmak. Bu şekilde su sıcaklığını eksi 70°C'ye getirmek mümkün oldu.
Doğada nasıl olur?
Sonbaharın sonlarında, çok temiz nehirler ve akarsular alttan donmaya başlar. Bir berrak su tabakası sayesinde, alt kısımdaki alglerin ve dalgaların karaya attığı odunların gevşek bir buz tabakasıyla büyüdüğü açıkça görülebilir. Bir noktada, bu alt buz ortaya çıkar ve suyun yüzeyi anında bir buz kabuğu ile bağlı hale gelir.
Suyun üst katmanlarının sıcaklığı derin olanlardan daha düşüktür ve donma yüzeyden başlar gibi görünmektedir. Bununla birlikte, saf su isteksizce donar ve her şeyden önce buz, bir silt süspansiyonunun ve katı bir yüzeyin olduğu yerde - dibe yakın.
Süngerimsi kütleler genellikle şelalelerin ve baraj dolusavaklarının akış aşağısında görülür. iç buz, köpüklü suda büyüyen. Yüzeye yükseldiğinde, bazen tüm kanalı tıkar ve nehre bile baraj yapabilen sözde zazhory'yi oluşturur.
Buz neden sudan daha hafiftir?
Buzun içinde havayla dolu çok sayıda gözenek ve boşluk var, ancak nedeni bu değil,
Bu, buzun sudan daha hafif olduğu gerçeğini açıklayabilir. Buz ve mikroskobik gözenekler olmadan
yine de sudan daha az yoğunluğa sahiptir. Her şey özelliklerle ilgili iç yapı buz. Bir buz kristalinde, su molekülleri kristal kafesin düğümlerinde bulunur, böylece her biri dört "komşu" olur.
su yok kristal yapı ve sıvıdaki moleküller birbirine daha yakındır,
bir kristalden daha, yani su buzdan daha yoğundur.
İlk olarak, buz eridiğinde, salınan moleküller hala kristal kafesin yapısını korur ve suyun yoğunluğu düşük kalır, ancak yavaş yavaş kristal kafes yok edilir ve suyun yoğunluğu artar.
+ 4°C sıcaklıkta suyun yoğunluğu maksimuma ulaşır ve daha sonra sıcaklıktaki artışla moleküllerin termal hareket hızındaki artış nedeniyle azalmaya başlar.
Bir su birikintisi nasıl donar?
Soğutulduğunda, suyun üst katmanları daha yoğun hale gelir ve batar. Onların yerini daha yoğun su alır. Bu karıştırma, suyun sıcaklığı düşene kadar devam eder.
+4 santigrat dereceye kadar. Bu sıcaklıkta suyun yoğunluğu maksimumdur.
Sıcaklığın daha da düşmesiyle, suyun üst katmanları zaten daha fazla sıkıştırılabilir,
ve yavaş yavaş 0 dereceye soğuyunca su donmaya başlar.

Sonbaharda, gece ve gündüz hava sıcaklığı çok farklıdır, bu nedenle buz katmanlar halinde donar.
Dondurucu bir su birikintisi üzerindeki buzun alt yüzeyi, enine şekle çok benzer. ağaç gövdesi kesimi:
gözle görülür eş merkezli yüzükler. Buz halkalarının genişliği, hava durumunu değerlendirmek için kullanılabilir. Genellikle bir su birikintisi
kenarlardan donmaya başlar, tk. daha az derinlik var. Merkeze yaklaştıkça oluşan halkaların alanı azalır.
İLGİNÇ!
Binaların yeraltı kısmının borularında, su genellikle donmada değil, çözülmede donar!
Bu, toprağın zayıf termal iletkenliğinden kaynaklanmaktadır. Isı dünyada çok yavaş hareket eder
topraktaki minimum sıcaklığın, dünya yüzeyinden daha sonra meydana geldiği. daha derin
daha geç. Çoğu zaman, donlar sırasında toprağın soğumaya zamanı yoktur,
ve ancak yeryüzünde bir çözülme meydana geldiğinde, donlar dünyaya ulaşır.
Bu, mantarlı bir şişede donma, su onu kırar. İçindeki suyu dondurursanız bardağa ne olur? Su, donma, sadece yukarı doğru değil, aynı zamanda yanlara doğru da genişler ve cam küçülür. Bu yine de camın yok olmasına yol açacaktır!
BİLİYOR MUSUN?
Sıcak bir yaz gününde dondurucuda iyice soğutulmuş bir narzan şişesinin içeriğinin bir anda buza dönüştüğü bilinen bir vaka var.
Metal "dökme demir", kristalizasyon sırasında genişleyen ilginç bir şekilde davranır. Bu, ince dantel kafeslerin ve küçük masa heykellerinin sanatsal dökümü için bir malzeme olarak kullanılmasına izin verir. Sonuçta, katılaşırken, genişlerken, dökme demir, formun en ince ayrıntılarını bile doldurur.
Kuban'da kışın güçlü içecekler hazırlanır - “donar”. Bunu yapmak için şarap dona maruz kalır. Her şeyden önce, su donar ve konsantre bir alkol çözeltisi kalır. Drenaj yapılır ve istenilen mukavemet elde edilene kadar işlem tekrarlanır. Alkol konsantrasyonu ne kadar yüksek olursa, donma noktası o kadar düşük olur.
en dolu tanesi, insanlar tarafından düzeltildi, Kansas, ABD'de düştü.
Ağırlığı neredeyse 700 gramdı.
oksijen gaz hali eksi 183 derece C sıcaklıkta sıvıya dönüşür,
ve eksi 218.6 derece C sıcaklıkta sıvı oksijenden katı oksijen elde edilir.

Eski günlerde insanlar yiyecek depolamak için buz kullanırlardı. Carl von Linde, freon gazını borulardan pompalayan bir buhar motoruyla çalışan ilk ev buzdolabını yarattı. Buzdolabının arkasında borulardaki gaz yoğunlaşarak sıvı hale geldi. Buzdolabının içinde sıvı freon buharlaştı ve sıcaklığı keskin bir şekilde düşerek buzdolabı bölmesini soğuttu. 1923'e kadar İsveçli mucitler Balzen von Platen ve Carl Muntens, freonun sıvıdan gaza dönüştüğü ve buzdolabındaki havadan ısı aldığı ilk elektrikli buzdolabını yaratmadı.
BU EVET!
Birkaç parça kuru buz, terk edilmiş yanan benzine, ateşi söndür.
Dokunulduğunda parmakları yakacak buz var. Suyun içine girdiği çok yüksek basınç altında elde edilir. katı hal 0 santigrat derecenin çok üzerindeki sıcaklıklarda.
Sıcaklık azaldıkça, bir madde sıvı halden katı hale geçebilir.
Bu işleme katılaşma veya kristalleşme denir.
Bir maddenin katılaşması sırasında, erimesi sırasında emilen aynı miktarda ısı açığa çıkar.

Erime ve kristalleşme sırasındaki ısı miktarı için hesaplama formülleri aynıdır.

Aynı maddenin basınç değişmiyorsa erime ve katılaşma sıcaklıkları aynıdır.
Kristalleşme süreci boyunca bir maddenin sıcaklığı değişmez ve aynı anda hem sıvı hem de katı halde bulunabilir.
KİTAP RAFINA BAKIN
KRİSTALİZASYON HAKKINDA İLGİNÇ
Renkli buz?
Plastik bir bardağa su ile biraz boya veya çay yaprağı eklerseniz, karıştırın ve renkli bir çözelti aldıktan sonra bardağı üstüne sarın ve donmaya maruz bırakın, alttan bir buz tabakası oluşmaya başlayacaktır. yüzey. Ancak, renkli buz almayı beklemeyin!

Suyun donmasının başladığı yerde, kesinlikle şeffaf bir buz tabakası olacaktır. Üst kısmı renkli olacak ve orijinal çözümden bile daha güçlü olacak. Boya konsantrasyonu çok yüksekse, buzun yüzeyinde çözeltisinin bir su birikintisi kalabilir.
Gerçek şu ki, boya ve tuz çözeltilerinde şeffaf taze buz oluşur. Büyüyen kristaller, mümkün olduğu kadar mükemmel bir kafes oluşturmaya çalışarak, yabancı atomları ve safsızlık moleküllerini yer değiştirir. Ancak safsızlıkların gidecek hiçbir yeri olmadığında, buz onları kendi yapısında oluşturmaya veya konsantre bir sıvı ile kapsüller şeklinde bırakmaya başlar. Bu nedenle deniz buzu tazedir ve en kirli su birikintileri bile şeffaf ve temiz buzla kaplıdır.
Su hangi sıcaklıkta donar?
Her zaman sıfır derecede mi?
Ancak, kaynamış su kesinlikle temiz ve kuru bir bardağa dökülür ve eksi 2-5 derece C sıcaklıkta pencerenin dışına yerleştirilirse, temiz camla kaplanır ve doğrudan güneş ışığından korunursa, birkaç saat içinde içindekiler. cam sıfırın altına soğur, ancak sıvı kalır.
Daha sonra bir bardak açar ve suya bir parça buz veya kar, hatta sadece toz atarsanız, o zaman kelimenin tam anlamıyla gözlerinizin önünde su anında donacak ve hacim boyunca uzun kristallerle filizlenecektir.
Neden? Niye?
Bir sıvının bir kristale dönüşmesi, öncelikle safsızlıklar ve homojen olmayanlar - toz parçacıkları, hava kabarcıkları, kabın duvarlarındaki düzensizlikler üzerinde gerçekleşir. Saf suyun kristalleşme merkezi yoktur ve sıvı kalırken aşırı soğutulabilir. Bu şekilde su sıcaklığını eksi 70°C'ye getirmek mümkün oldu.
Doğada nasıl olur?
Sonbaharın sonlarında, çok temiz nehirler ve akarsular alttan donmaya başlar. Bir berrak su tabakası sayesinde, alt kısımdaki alglerin ve dalgaların karaya attığı odunların gevşek bir buz tabakasıyla büyüdüğü açıkça görülebilir. Bir noktada, bu alt buz ortaya çıkar ve suyun yüzeyi anında bir buz kabuğu ile bağlı hale gelir.
Suyun üst katmanlarının sıcaklığı derin olanlardan daha düşüktür ve donma yüzeyden başlar gibi görünmektedir. Bununla birlikte, saf su isteksizce donar ve her şeyden önce buz, bir silt süspansiyonunun ve katı bir yüzeyin olduğu yerde - dibe yakın.
Şelalelerin ve baraj dolusavaklarının akış aşağısında, genellikle çalkantılı suda büyüyen süngerimsi bir su içi buz kütlesi vardır. Yüzeye yükseldiğinde, bazen tüm kanalı tıkar ve nehre bile baraj yapabilen sözde zazhory'yi oluşturur.
Buz neden sudan daha hafiftir?
Buzun içinde havayla dolu birçok gözenek ve boşluk vardır, ancak bu, buzun sudan daha hafif olduğu gerçeğini açıklayabilecek sebep değildir. Buz ve mikroskobik gözenekler olmadan
yine de sudan daha az yoğunluğa sahiptir. Her şey buzun iç yapısının özellikleri ile ilgili. Bir buz kristalinde, su molekülleri kristal kafesin düğümlerinde bulunur, böylece her biri dört "komşu" olur.
Su ise kristal bir yapıya sahip değildir ve bir sıvıdaki moleküller bir kristalden daha yakın bulunur, yani. su buzdan daha yoğundur.
İlk olarak, buz eridiğinde, salınan moleküller hala kristal kafesin yapısını korur ve suyun yoğunluğu düşük kalır, ancak yavaş yavaş kristal kafes yok edilir ve suyun yoğunluğu artar.
+ 4°C sıcaklıkta suyun yoğunluğu maksimuma ulaşır ve daha sonra sıcaklıktaki artışla moleküllerin termal hareket hızındaki artış nedeniyle azalmaya başlar.
Bir su birikintisi nasıl donar?
Soğutulduğunda, suyun üst katmanları daha yoğun hale gelir ve batar. Onların yerini daha yoğun su alır. Bu karıştırma, su sıcaklığı +4 santigrat dereceye düşene kadar gerçekleşir. Bu sıcaklıkta suyun yoğunluğu maksimumdur.
Sıcaklığın daha da düşmesiyle, suyun üst katmanları zaten daha fazla büzülebilir ve yavaş yavaş 0 dereceye kadar soğuyarak su donmaya başlar.

Sonbaharda, gece ve gündüz hava sıcaklığı çok farklıdır, bu nedenle buz katmanlar halinde donar.
Dondurucu bir su birikintisi üzerindeki buzun alt yüzeyi, bir ağaç gövdesinin enine kesitine çok benzer:
eşmerkezli halkalar görülebilir. Buz halkalarının genişliği, hava durumunu değerlendirmek için kullanılabilir. Genellikle su birikintisi kenarlardan donmaya başlar, çünkü. daha az derinlik var. Merkeze yaklaştıkça oluşan halkaların alanı azalır.
İLGİNÇ
Binaların yeraltı kısmının borularında, su genellikle donmada değil, çözülmede donar!
Bu, toprağın zayıf termal iletkenliğinden kaynaklanmaktadır. Isı, yeryüzünden o kadar yavaş geçer ki, topraktaki minimum sıcaklık, dünyanın yüzeyinden daha sonra meydana gelir. Ne kadar derin, o kadar geç. Çoğu zaman, donlar sırasında, toprağın soğumaya zamanı yoktur ve yalnızca zeminde bir çözülme meydana geldiğinde don yere ulaşır.
Bu, mantarlı bir şişede donma, su onu kırar. İçindeki suyu dondurursanız bardağa ne olur? Su, donma, sadece yukarı doğru değil, aynı zamanda yanlara doğru da genişler ve cam küçülür. Bu yine de camın yok olmasına yol açacaktır!
BİLİYOR MUSUN
Sıcak bir yaz gününde dondurucuda iyice soğutulmuş bir narzan şişesinin içeriğinin bir anda buza dönüştüğü bilinen bir vaka var.
Metal "dökme demir", kristalizasyon sırasında genişleyen ilginç bir şekilde davranır. Bu, ince dantel kafeslerin ve küçük masa heykellerinin sanatsal dökümü için bir malzeme olarak kullanılmasına izin verir. Gerçekten de, katılaşırken, genişlerken, dökme demir her şeyi, hatta formun en hassas ayrıntılarını bile doldurur.
Kuban'da kışın güçlü içecekler hazırlanır - “donar”. Bunu yapmak için şarap dona maruz kalır. Her şeyden önce, su donar ve konsantre bir alkol çözeltisi kalır. Drenaj yapılır ve istenilen mukavemet elde edilene kadar işlem tekrarlanır. Alkol konsantrasyonu ne kadar yüksek olursa, donma noktası o kadar düşük olur.
İnsanlar tarafından kaydedilen en büyük dolu tanesi ABD'nin Kansas eyaletine düştü. Ağırlığı neredeyse 700 gramdı.
Eksi 183 derece C sıcaklıkta gaz halindeki oksijen sıvıya dönüşür ve eksi 218.6 derece C sıcaklıkta sıvıdan katı oksijen elde edilir.






