Kompresija i razrjeđivanje plinova
Ideal Machines in pravi zivot ne postoji, to je samo mentalni konstrukt. Svaka od ovih hipotetičkih mašina, među kojima carnot engine zauzima važno mjesto, ilustruje neki važan teorijski zaključak. (Čak i zamak u vazduhu koji se zove večna mašina služi, zapravo, samo da pokaže da ne možete dobiti energiju ni iz čega.) Carnotov motor, koji je u osnovi rada idealnog toplotnog motora, izumeo je francuski inženjer Sadi Carnot dvadeset godina prije kako su formulirani temelji termodinamike, međutim, ilustruje važnu posljedicu drugog zakona termodinamike.
Radni dio Carnot motora može se zamisliti kao klip u cilindru ispunjenom plinom. Budući da je Carnot motor čisto teoretska, odnosno idealna mašina, sile trenja između klipa i cilindra i toplinski gubici se smatraju nula. Klip se može slobodno kretati između dva termalni rezervoari- Sa visoke temperature i sa niskom temperaturom. (Radi praktičnosti, zamislite da se vrući rezervoar toplote zagreva sagorevanjem mešavine benzina sa vazduhom, a hladan se hladi vodom ili vazduhom na sobnoj temperaturi.) U ovom toplotnom motoru dolazi do sledećeg idealnog četvorofaznog ciklusa:
1. Prvo, cilindar dolazi u kontakt sa vrelim rezervoarom, a idealni gas se širi na konstantna temperatura. Tokom ove faze, gas prima neku toplotu iz vrućeg rezervoara.
2. Cilindar je tada okružen savršenom toplotnom izolacijom, pri čemu se količina toplote koja je dostupna gasu čuva i gas nastavlja da se širi sve dok njegova temperatura ne padne na temperaturu hladnog termalnog rezervoara.
3. U trećoj fazi se uklanja toplotna izolacija, a gas u cilindru koji je u kontaktu sa hladnim rezervoarom se komprimira, a deo toplote odaje hladnom rezervoaru.
4. Kada kompresija dostigne određenu tačku, cilindar je ponovo okružen toplotnom izolacijom, a gas se kompresuje podizanjem klipa dok se njegova temperatura ne izjednači sa temperaturom vrućeg rezervoara. Nakon toga se uklanja toplinska izolacija i ciklus se ponavlja od prve faze.
Carnotov motor ima mnogo zajedničkog sa stvarnim motorima: radi u zatvorenoj petlji (tzv. Carnot ciklus); prima energiju izvana zbog procesa visoke temperature (na primjer, prilikom sagorijevanja goriva); dio energije se raspršuje u okruženje. U ovom slučaju se obavlja određeni rad (u slučaju Carnot motora, zbog kretanje napred klip). efikasnost, ili efikasnost Carnotov motor se definira kao omjer rada koji proizvodi i energije (u obliku topline) uzete iz vrućeg rezervoara. Lako je dokazati da je efikasnost ( E) izražava se formulom:
E = 1 - (T c/ T h),
gdje T c i T h - temperatura hladnog i toplog rezervoara (u kelvinima). Očigledno, efikasnost Carnot motora je manja od 1 (ili 100%).
Carnotov veliki uvid je da je pokazao da nijedan toplotni motor koji radi na dvije date temperature ne može biti efikasniji od idealnog Carnot motora (ova izjava se zove Carnotova teorema). U suprotnom, naišli bismo na kršenje drugog zakona termodinamike, jer bi takav motor uzimao toplinu iz manje zagrijanog rezervoara i prenosio je na topliji. (Zapravo, drugi zakon termodinamike je posledica Carnotove teoreme.) Dakle, relacija koju je Carnot dobio uspostavlja granica efikasnosti stvarni motori koji rade u stvarnom svijetu. Njemu se može pristupiti, ali inženjeri ga neće moći postići i, štoviše, nadmašiti. Dakle, čisto hipotetički Carnotov motor igra važnu ulogu u svijetu stvarne, bučne i smrdljive tehnologije zagrijanog motornog ulja, a ovo je još jedan primjer primijenjene vrijednosti čisto teorijskih, na prvi pogled, istraživanja.
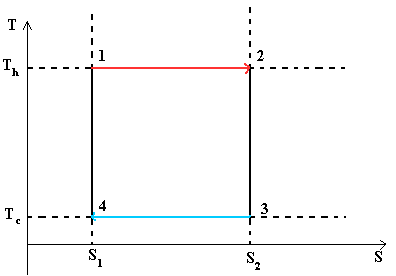
Slika 1 – Carnotov ciklus je idealan termodinamički ciklus.
Ovaj dijagram prikazuje zatvorenu petlju. Sistem uzastopno prelazi od tačke 1 do 2, zatim 3, 4 i ponovo do 1. Grafikon pokazuje da je proces 1® 2 izotermičan (javlja se na T 1), a proces 3® 4 je također izotermičan (javlja se na T 2)
Procesi 2® 3 i 4® 1 su adijabatski. Pošto u njima nema promjene entropije, onda je dS = 0, dakle dQ = 0 ili Q = const.
Količina toplote koja se isporučuje sistemu:
Q 1 \u003d T 1 ´ (S 2 -S 1) ili površina pravokutnika 1-2-S 2 -S 1 -1
Količina toplote koju odaje sistem:
Q 2 \u003d T 2 ´ (S 2 -S 1) ili površina pravokutnika 3-S 2 -S 1 -4-3
Rad ciklusa L = Q 1 - Q 2
Efikasnost ciklusa h \u003d (Q 1 - Q 2) / Q1.
Važna posljedica formule za efikasnost ciklusa Carnot je da je za povećanje efikasnosti potrebno povećati temperaturu dovoda topline T 1 i smanjiti temperaturu odvođenja topline T 2 .
AT toplotni motor, plin se (reverzibilno) zagrijava (reverzibilno zagrijava), a zatim hladi. Model ciklusa je sljedeći: Pozicija 1 ---(izotermna ekspanzija) --> Položaj 2 ---(adijabatska ekspanzija) --> Pozicija 3 ---(izotermna kompresija) --> Pozicija 4 ---(adijabatska kompresija) -- > Pozicija 1
Pozicija 1 - Položaj 2: Izotermno širenje
Izotermna ekspanzija. Na početku procesa radni fluid ima temperaturu Th, odnosno temperaturu grijača. Tada se tijelo dovodi u kontakt sa grijačem koji mu izotermno (pri konstantnoj temperaturi) prenosi količinu topline Q H . Istovremeno se povećava volumen radnog fluida. Q H \u003d∫Tds \u003d T h (S 2 -S 1) \u003d T h ΔS
Pozicija 2 - Pozicija 3: Adijabatsko širenje
Adijabatsko (izentropsko) širenje. Radni fluid se odvaja od grejača i nastavlja da se širi bez razmene toplote sa okolinom. Istovremeno se njegova temperatura smanjuje na temperaturu hladnjaka.
Položaj 3 - Položaj 4: Izotermna kompresija
Izotermna kompresija. Radni fluid, koji do tog vremena ima temperaturu T c , dolazi u kontakt sa hladnjakom i počinje izotermno da se skuplja, dajući hladnjaku količinu toplote Q c . Q c \u003d T c (S 2 -S 1) \u003d T c ΔS
Položaj 4 - Položaj 1: Adijabatska kompresija
Adijabatska (izentropska) kompresija. Radni fluid se odvaja od frižidera i komprimuje bez razmene toplote sa okolinom. Istovremeno, njegova temperatura raste do temperature grijača.
U izotermnim procesima temperatura ostaje konstantna, u adijabatskim procesima nema prijenosa topline, što znači da je entropija očuvana.
Stoga je zgodno predstaviti Carnotov ciklus u koordinatama T i S (temperatura i entropija).
3. Radni ciklus rashladna mašina(do lekcije br. 16)
Mašina za hlađenje Ovo je mašina za reverzni karno ciklus.. Odnosno, ako prođete kroz ciklus obrnuti smjer, toplina će se uzimati iz hladnjaka i prenositi na grijač (zbog rada vanjskih sila).
U rashladnim sistemima, prenos toplote iz sredine sa nižom temperaturom u sredinu sa višom temperaturom vrši se pomoću radnog fluida tzv. rashladna tečnost.
Do prehlade dolazi kružni proces, ili ciklus u kojem je proces odvođenja topline iz ohlađenog medija praćen kompenzacijskim procesom - opskrbom energijom (na primjer, pri komprimiranju pare rashladnog sredstva u kompresoru).
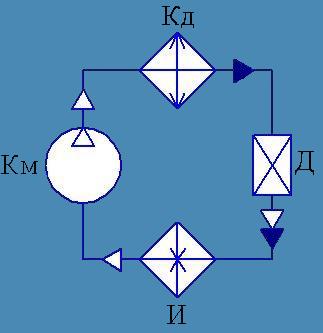
Proces prenosa toplote sa manje zagrejanog tela na više zagrejano po ceni mehanički rad naziva se obrnuti Carnotov ciklus. Ciklus se sastoji od sljedećih procesa:
1-2 - adijabatska kompresija pare rashladnog sredstva (konačna temperatura kompresije T);
2-3 - izotermna kondenzacija pare rashladnog sredstva na temperaturi T sa povratkom kondenzacione toplote Q u okolinu (npr. vodu);
3-4 - adijabatsko širenje tečnog rashladnog sredstva (konačna temperatura ekspanzije T o);
4-1 - izotermno isparavanje tečnog rashladnog sredstva na temperaturi T o sa odvođenjem toplote isparavanja Q o iz ohlađenog medija.
![]()
Takav ciklus je izvodljiv samo ako je entropija sistema konstantna. Stoga, ako se tokom isparavanja rashladnog sredstva, entropija ohlađenog medija smanji za Q o /T o , tada bi entropija zagrejanijeg medijuma (vode) trebalo da poraste za istu vrednost, na koju se prenosi toplota Q o, preuzeta iz ohlađenog medija, i toplota ekvivalentna radu Lk utrošenom na kompresiju rashladnog sredstva. Kao rezultat, povećanje entropije zagrejanijeg medija je (Q o + L c)/T.
Prema energetskom bilansu
Q o /T o \u003d (Q o + L do) / T
Otuda i rad koji mora biti utrošen u rashladnoj jedinici koja radi na obrnutim Carnot ciklusom
L k \u003d Q o (T - T o) / T o
Toplota Q o koju oduzima rashladno sredstvo ohlađenog medija na temperaturi T o< Т, определяет kapacitet hlađenja b ciklus, ili rashladna jedinica.
Dakle, koristeći primjer obrnutog Carnotovog ciklusa, energetski bilans bilo koje rashladne mašine:
gdje je L rad realnog ciklusa.
Termodinamička efikasnost rashladnih ciklusa izražava se kao omjer rashladnog kapaciteta Q o i utrošenog rada, L i ova relacija se zove koeficijent performansi i označava se sa ε. Koeficijent ε izražava se zavisnošću
ε \u003d Q o / L \u003d Q / (Q - Q o) \u003d T o (S 1 - S 2) / [ T (S 1 - S 2) - T o (S 1 - S 2)] \ u003d T o / T - T o
Koeficijent učinka pokazuje koliko topline percipira rashladno sredstvo iz ohlađenog medija po jedinici utrošenog rada.
Koeficijent performansi koji karakteriše stepen upotrebe mehaničkog rada za dobijanje veštačke hladnoće, kao što se može videti iz izraza, ne zavisi od svojstava rashladnog sredstva ili šeme rada rashladne jedinice, već je samo u funkciji temperature T o i T. U ovom slučaju, stepen upotrebe mehaničkog rada će biti veći što je manja razlika između temperatura rashladnog sredstva pri odavanju T i primanju T o toploti.
Proces izotermnog širenja 1 - 2 pregrijana para u koordinatama je prikazano na sl. 12.8. Definicija početne / i krajnje 2 tačke procesa je jasna iz prethodno navedenog.
Izotermički proces ekspanzije ili kontrakcije također se može izvesti reverzibilno u uvjetima brze izmjene topline sa spoljašnje okruženje potrebno za održavanje konstantne temperature.
AT izotermni proces ekspanzija vode, prijavljuje se količina topline, jednaka toploti isparavanje / h i na dijagramu s - T grafički definisano područje.
U procesu izotermnog širenja n, unos topline se u potpunosti pretvara u rad, a promjena unutrašnje energije je nula.
Izuzetak je idealni proces izotermne ekspanzije, kada sva toplina ide u rad, ali je kapacitet hlađenja takvog procesa nula.
Dakle, u izotermnom procesu ekspanzije sva dovedena toplina troši se na vanjski rad, a u izotermnom procesu kompresije vanjski rad se u potpunosti pretvara u toplinu.
Dakle, u izotermnom procesu ekspanzije gasa unutrašnja energija sistem, pretvoren u rad protiv vanjskog pritiska, dopunjava se zbog priliva topline. U slučaju reverzibilnog procesa koji se ovdje razmatra, obavljeni rad je identičan maksimalnom korisnom radu, koji je, kao što je prikazano u nastavku, jednak promjeni funkcije stanja. Kada je proces nepovratan (gubitak trenjem, Ap0), dio korisnog rada se gubi, pretvarajući se u toplinu.
Na sl. 4 - 3 prikazuje proces izotermnog širenja idealan gas u ri sistemu.
Treba napomenuti da je mjerenje entropije AS Q/T dobiveno za konkretan slučaj procesa izotermnog širenja isto kao i ranije dobiveno analizom Carnotovog ciklusa. Na ovaj način, statistička fizika potkrepljuje postojanje funkcije stanja - entropije, čiji je prirast u reverzibilnim procesima jednak reduciranoj toplini, te poziciju da entropija zatvorenog sistema teži maksimumu. Ova funkcija stanja omogućava određivanje smjera procesa i ravnotežnih uslova pomoću mjerenja toplinskih veličina. Sa principom povećanja entropije u zatvoreni sistemi srodne ideje o toplotnoj mešavini Univerzuma, koje je izneo Klauzijus, koji je tvrdio: Energija sveta je konstantna, entropija sveta teži maksimumu. Otuda - zaključak o postizanju kao rezultat jednostranih procesa koji se dešavaju u prirodi, konačnog stanja ravnoteže, u kojem je entropija svijeta maksimalna, a Univerzum umire od toplotne smrti.
Upoređujući (15.16) i (15.4), primjećujemo da je specifičan rad teoretskog pneumatskog motora tokom procesa potpunog izotermnog širenja jednak istoj vrijednosti specifične energije zraka. To vrijedi i za adijabatske i politropske procese.
Upoređujući (288) i (272), primjećujemo da je specifičan rad teoretskog pneumatskog motora tokom procesa potpunog izotermnog širenja jednak istoj vrijednosti specifične energije zraka. To vrijedi i za procese adijabatskog i politropskog širenja.
Od sl. 23 može se vidjeti da segment SW jednak Asp - As0 istovremeno predstavlja prirast entropije u izotermnom procesu širenja SW.
Skup radnih procesa u ekspanderu, kao iu kompresoru, nije zatvoren sistem. termodinamički procesni ciklus. Međutim, proces izotermnog širenja teško je implementirati, a procesi u ekspanderima su bliski adijabatskim.
Na sl. 15.7 prikazuje teorijske dijagrame indikatora za različite procese ekspanzije zraka u motorima. Za implementaciju procesa izotermnog širenja (kriva 2-3, politropni indeks n 1) potrebno je dovođenje topline tako da se temperatura zraka održava konstantnom, a za adijabatski proces (kriva 2-3, n K) razmjena topline sa okolinom treba isključiti. Politropni proces će biti u tom slučaju (kriva 2 - 3, 1 p k), ako je dovod topline manji nego u izotermnom procesu.
Reverzibilni ciklus se može izvesti pod sledećim uslovima. Prvo, u procesu izotermnog širenja, toplina se reverzibilno dovodi do radnog fluida iz izmjenjivača topline s konstantnom temperaturom.
Unutrašnja energija (vidi tabelu 1.1) sastoji se od Helmholtzove energije F i pridružene energije TS. Gubitak energije F tokom procesa izotermnog širenja (S const) jednak je radu RT In (VVK2) - Apsorpcija toplote od strane sistema (na V const) dovodi do povećanja pridružene energije za T (S2 - Sx), budući da je dS 8Q / T. Ako nema promjene volumena pri konstantnoj temperaturi, onda nam smanjenje Helmholtzove energije omogućava da dobijemo koristan rad.
Direktni Carnotov ciklus sastoji se od šest procesa (sl. Kriva A-B prikazuje izotermni proces ekspanzije gasa pri konstantnoj temperaturi 7; kriva 3-C prikazuje adijabatski proces ekspanzije gasa u odsustvu razmene toplote sa spoljnim okruženjem - 50H; C-D kriva prikazuje izotermni proces kompresije plina pri konstantnoj temperaturi Tz; Linija D-A prikazuje adijabatski proces kompresije gasa u odsustvu razmene toplote sa okolinom. U pro-lesovima A-B i B-C, plin, šireći se, obavlja vanjski rad, 1 in C-D procesi i D-A gas se komprimira i na njegovu kompresiju se primenjuje spoljni rad. Primjenjujući jednačinu prvog zakona termodinamike na cijeli ciklus, dobijamo Qt - Q2A (L. Dakle, u direktnom Carnotovom ciklusu, dovedena toplota Qi se djelimično troši na koristan rad, numerički jednak Kvadrat A-B-C-D-A(Sl. Efikasnost dikle Carnot u principu ne može biti jednaka jedinici.
Općenito, vrijednost a ovisi o temperaturi i pritisku. Istovremeno, u izotermnom procesu ekspanzije plina, vrijednost a se javlja kao proizvod ap.
Image reg - proces proširenja 4 - / - poruka njemu. Uprkos ovom svojstvu Carnotovog ciklusa, drugi ciklusi se koriste kao osnova za rad stvarnih motora, kao što će slijediti iz onoga što slijedi. To je uglavnom zbog nemogućnosti provođenja izotermnih procesa širenja i skupljanja u realnim uvjetima.
Rad komprimovanog vazduha pri punjenju i širenju je pozitivan, dok je rad komprimovanog vazduha negativan. Kao što se vidi na sl. 93, a, maksimalni rad će biti s procesom izotermnog širenja, a minimalni - s adijabatskim.
Stranica 2
Na prvi pogled može izgledati da je takvoj formulaciji u suprotnosti, na primjer, proces izotermnog širenja idealnog plina. Zaista, sva toplina koju idealni plin primi od nekog tijela u potpunosti se pretvara u rad. Međutim, dobijanje toplote i njeno pretvaranje u rad nije jedini krajnji rezultat procesa; osim toga, kao rezultat procesa dolazi do promjene volumena plina.
Na prvi pogled može izgledati da je Thomsonova formulacija u suprotnosti, na primjer, s procesom izotermnog širenja idealnog plina. Zaista, tokom ovog procesa, sva količina toplote koju dobije idealni gas iz određenog tela u potpunosti se pretvara u rad. Međutim, dobijanje toplote i njeno pretvaranje u rad nije jedino krajnji rezultat proces; osim toga, dolazi do promjene u zapremini gasa.
Znajući koliko je izotermno i adijabatski procesi u Ts-dijagramu se u njemu može konstruisati Carnotov ciklus. Ovde je 1 - 2 proces izotermnog širenja, tokom kojeg se dovodi količina toplote qv, merena površinom 1 - 2 - 5 - 6 - 1; 2 - 3 - adijabatsko širenje; 3 - 4 - izotermna kompresija, pri kojoj se odvodi količina toplote d% mjereno površinom 4 - 3 - 5 - 6 - 4; 4 - 1 - adijabatska kompresija. Količina toplote 70, pretvorena u koristan rad w0, biće predstavljena kvadratom.
PRITISAK KRITIČAN - vidi stanje materije je kritično. PRITISAK ZASIĆENJA - maksimalni pritisak pri kojem, u procesu izotermnog širenja nafte ili formacijske vode, počinje oslobađanje plina koji su oni sorbirani. Međutim, pouzdanost ove metode još nije potvrđena. Ulje u prisustvu gasne kapice je obično zasićeno.
Kao što se vidi iz jednačine (VI, 5), entropija raste u procesu izotermnog širenja. Kao iu prethodnom primjeru topljenja kristalne žive, u procesu izotermnog širenja, određena količina topline (koja se uzima iz izvora topline - termostata) pri konstantnoj temperaturi se reverzibilno prenosi plinu koji se širi.
Razmotrite karakteristike fazni prelaz od tečno stanje u gasovito - prelazak tečnosti u paru. Ako kao rezultat nesreće dođe do smanjenja pritiska, a temperatura inercijom zadrži svoju vrijednost, tada se razvija proces izotermnog širenja dabe. Iskustvo pokazuje da se pri prelasku na izoterme sa višim temperaturama dužina ab presjeka smanjuje, za niže temperature povećava dužina ab presjeka.
Obrnuti Carnotov ciklus je također prikazan na s - G - dijagramu kao pravougaonik / - 2 - 3 - 4 (slika 7.6, b), ali su svi procesi u njemu usmjereni suprotno od kazaljke na satu. Ciklus se također sastoji od dvije izoterme i dvije adijabate: / - 2 - proces adijabatske ekspanzije, 2 - 3 - proces izotermnog širenja, 3 - 4 - proces adijabatske kompresije, 4 - / - proces izotermne kompresije.
Pošto je ovaj gas izolovan od okoline (Q O, A 0), njegova unutrašnja energija U, kao što sledi iz prvog zakona termodinamike, mora ostati konstantna. Dakle, kao reverzibilni proces koji gas prenosi u isto konačno stanje kao i ovaj proces, možemo smatrati proces reverzibilnog izotermnog širenja, tokom kojeg se zapremina gasa udvostručuje.
U praksi su procesi izotermnog širenja obično prilično teški za implementaciju zbog nedovoljne toplotne provodljivosti; ipak, zanimljivo je uporediti termodinamička svojstva takvog strujanja sa uobičajenijim adijabatskim tokom. Pod ovim uslovima, izotermno širenje daje gornju granicu koeficijentu korisna akcija proces ekspanzije. Teoretski su razmatrani procesi izotermnog širenja u raketnim mlaznicama, ali zbog kratkog vremena zadržavanja čestica gasa u mlaznici, praktična upotreba ovih procesa, po svemu sudeći, nije izvodljiva.
Iz tačke / sa parametrima p1; uh, 7 radni fluid se adijabatski širi do stanja 2 (proces / - 2) i povezuje se na izvor sa niskom temperaturom. Daljnje širenje (proces 2 - 3) događa se dovodom topline c / 2 u radni fluid. Događa se proces izotermnog širenja.
Carnot se može zamisliti na sljedeći način. U procesu izotermnog širenja 1 - G, gas je u toplotnom kontaktu i ravnoteži sa telom koje ima temperaturu TV. Ovo tijelo se zove grijač. Jasno je da toplinski kapacitet grijača mora biti, strogo govoreći, beskonačno velik. U suprotnom bi otpuštanje topline Q4 u plin izazvalo smanjenje temperature grijača, a samim tim i kršenje izotermnog procesa ekspanzije plina. U procesu I - - 2, plin je potpuno toplinski izoliran i njegovo širenje se nastavlja adijabatski.
Isti rezultat se lako može dobiti direktno iz jednačine (3 - 177), budući da smo se složili da izvor rada razmatran u ovom primjeru ima svojstva idealnog plina, i budući da je temperatura izvora u stanjima 1 i 2 isti i jednak T0, tada je unutrašnja energija rada izvora u stanjima 1 i 2 također ista i prvi član jednačine (3 - 177) jednak je nuli. Drugi član jednadžbe je količina topline dovedena izvoru rada u izotermnom procesu na temperaturi T0, jednaka radu u ovom procesu (unutrašnja energija ostaje nepromijenjena. Entropija izvora rada u procesu izotermnog širenja raste (dovodi se toplina. Slt i stoga će drugi član jednačine (3 - 177) biti pozitivan. Zadnji član jednadžba će biti negativna (F2 Fj), a njena numerička vrijednost je ekvivalentna površini a-c-2 - b - a. Dakle, L ts (površina l - 2 - b - a - l) - (površina a-c-2 - b - a) (područje l - 2 - c - l ), što se, očekivano, poklapa sa prethodno dobijenim rezultatom.
Glavni načini prijenosa energije iz jednog dijela sistema u drugi su toplota i rad. Na primjer, izotermna ekspanzija idealnih gasova nije praćeno oslobađanjem ili apsorpcijom topline, ako se proces odvija bez vršenja rada plina. Ako je proces izotermnog širenja plina praćen radom, tada se toplina apsorbira.
Procesi u GCM-u se odvijaju sljedećim redoslijedom. Toplota kompresije u ovom procesu odvodi se u okolinu. Zatim se komprimirani plin, dok se klipovi kreću ulijevo, gura kroz ohlađeni regenerator 2 (izohorni proces), pri čemu se temperatura i pritisak gasa smanjuju. U sljedećem trenutku dolazi do procesa izotermnog širenja plina, u kojem desni klip miruje, a ekspanderski klip ide ulijevo.






