Temperaturni pritisak pregrijane pare. Velika enciklopedija nafte i gasa
Stranica 1
Svojstva pregrijane pare kao rastvarača mijenjaju se promjenom njenih parametara - temperature i pritiska. Za razliku od zasićena para, čija je temperatura jedinstveno određena pritiskom, pregrijana para at konstantan pritisak može imati razne temperature. Kao što je poznato, pri konstantnom pritisku, s povećanjem temperature pregrijavanja, gustina pare opada. Takođe se smanjuje sa smanjenjem pritiska na konstantnoj temperaturi. Kako se gustina pare smanjuje, dielektrična konstanta O i polaritet njegovih molekula.
Svojstva pregrijane pare, kao što smo već primijetili, u blizini krivulje pare primjetno se razlikuju od svojstava idealan gas i stoga ne prate pv RT jednačinu. Jednačina stanja za pregrijanu paru ima složeniji oblik. Postoje takve jednačine veliki broj. Međutim, zbog svoje složenosti, rijetko se koriste u praksi. Potrebne projektne vrijednosti za pregrijanu paru mogu se pronaći na sljedeći način.
Svojstva pregrijane pare (tačka d, slika 1.16) značajno se razlikuju od svojstava zasićene pare.
Svojstva pregrijane pare oštro se razlikuju od zasićene pare. Što je viša temperatura pregrijavanja pare, to su njena svojstva bliža idealnom plinu. Stanje pregrijane pare, za razliku od zasićene pare, određeno je ne jednim, već dva parametra - temperaturom i tlakom.
Osobine pregrijane pare su vrlo različite od onih zasićene pare.
Svojstva pregrijane pare oštro se razlikuju od svojstava zasićene pare i približavaju se svojstvima plinova.
Svojstva pregrijane pare oštro se razlikuju od osobina zasićene pare i približavaju se svojstvima plinova; kao što pokazuje iskustvo, pregrijane pare su po svojim svojstvima bliže plinovima, što je veće njihovo pregrijavanje, što se podrazumijeva kao temperaturna razlika između pregrijane pare i zasićene pare istog pritiska; kao što smo ranije vidjeli, jako pregrijane pare vode i ugljičnog dioksida se praktično mogu smatrati plinovima.
Svojstva pregrijane pare značajno se razlikuju od svojstava zasićene pare. Što je veća kriva pregrijavanja, to su svojstva pregrijane pare bliža svojstvima idealnog plina.Odstupanje ovih svojstava objašnjava se konačnim volumenima molekula pare i prisustvom interakcijskih sila koje se od njih očekuju.
Svojstva pregrijanih para približavaju se svojstvima plinova.
Stepen korištenja svojstava pregrijane pare ogleda se u gubitku ulja sa otpadom, trajanju obrade sirovina i, posljedično, performansama aparata.
Poteškoće u analizi svojstava pregrijane i prezasićene pare nastaju zbog nedostatka dovoljno precizne jednačine stanja za metastabilno područje materije. Van der Waalsova jednačina, koja kvalitativno opisuje metastabilna stanja, nije uvijek pogodan za kvantitativne proračune.
Sljedeći paragrafi govore o svojstvima pregrijane pare. Ovdje je data Zeinerova jednadžba stanja i formule za toplinu, rad, promjenu unutrašnja energija i entropija. Sljedeća dva paragrafa bave se svojstvima ugljičnog dioksida i para amonijaka. U posljednjem pasusu, Stacionarno kretanje pare ili plina kroz cijev, izvedena je samo jedna formula - formula brzine. Ovaj dio u Zernovljevom udžbeniku predstavljen je na mnogo primitivniji način nego u prethodnim udžbenicima.
Nakon toga se razmatraju svojstva pregrijane pare i daju se jednadžbe stanja Girn i Linde. Nadalje, dati su odnosi koji se odnose na zasićenu vodenu paru, izvedena je Clapeyron-Clausiusova formula i analitičkom metodom izračunati osnovni procesi pare. Kada se razmatra p - v dijagram vodene pare, govori se o graničnim krivuljama i kritičnom stanju.
U § 8, koji je posvećen svojstvima pregrijane pare, prije svega se izvodi konstrukcija kompletnog dijagrama p - v za tečnost, paru i gas sa graničnim krivuljama, kritičnom tačkom i površinama pojedinačnih stanja materija koja se na njemu razlikuje. Također se govori o izotermama i vrijednosti izoterme kritične temperature. Mercalov se odnosi na područje dijagrama koje se nalazi ispod kritične izoterme i iznad gornje granične krive kao pregrijane pare, a područje koje se nalazi iznad kritične izoterme kao gasove. Nakon toga se raspravlja o karakterističnoj jednadžbi pregrijane pare i daju se Zeinerove i Girn-ove jednačine.
Pregrijana para je kroz ventile ušla u hladnjak, gdje je njena temperatura smanjena na vrijednost nešto veću od temperature zasićenja pri datom pritisku.
Shema (a, ciklus (b) i procesi u turbinama (u PTU. Pregrijana para (stanje 1)) iz pregrijača P kotla K dovodi se u turbinu visokog pritiska HPT-a, gdje se adijabatski širi do tlaka pd.
Pregrijana para nakon pregrijača 7 šalje se kroz parovod 14 do parne turbine 15, gdje se značajan dio njene toplotne energije pretvara u mehanički rad. C i uklanjanje kisika iz njega, što uzrokuje koroziju metala. Iz deaeratora se napojna pumpa 21 preko visokotlačnog grijača (HPV) 22 i kondenzat ekonomajzera vode ponovo dovodi u parni kotao.
Pregrijana para nakon pregrijača 7 kroz parovod 14 šalje se u parnu turbinu 15, gdje se značajan dio njene toplinske energije pretvara u mehanički rad. Nakon rada u turbini, para sa temperaturom od 35 - 40 C ulazi u razrijeđeni prostor kondenzatora 16, gdje na svom putu nailazi na veliki broj cijevi unutar kojih cirkulaciona pumpa 17 neprekidno pumpa rashladnu vodu.
Šema (a, ciklus (b) i proces u turbini (u PTU sa regeneracijom. Pregrijana para (stanje /), nastala kao rezultat dovoda topline radnog fluida u kotlu K i pregrijaču P, ulazi u turbinu T, gde se adijabatski širi.
Pregrijana para se pretvara u zasićenu paru dovodeći je u direktan kontakt sa hladnom vodom u aparatima koji se nazivaju parni umformeri. U parnom umformeru sa direktnim ubrizgavanjem atomizirane vode (Sl. 291), pregrijana para se dovodi odozgo kroz priključak /, prolazi kroz vijčanu mlaznicu 2 i prima vrtložno kretanje.
Pregrijana para u HPC, baš kao i u HPC, ulazi kroz parne razvodne kutije i ventile koji regulišu pristup pare od pregrijača do turbine u slučajevima rasterećenja i režima malog protoka.
Pregrijana para se dovodi u dvije nepovratne ventilske kutije kroz četiri cijevi 720X X25 mm i iz njih kroz četiri cijevi do kutija zapornih ventila smještenih na cilindru.
Pregrijana para po svojim svojstvima odgovara idealnom plinu u smislu da je njegovo stanje određeno ako su data bilo koja dva parametra, na primjer, tlak i temperatura.
Pregrijana para na istom pritisku može imati različite temperature, u svim slučajevima ove temperature će biti veće od tačke ključanja koja odgovara datom pritisku. Ovo svojstvo pregrijane pare razlikuje se od zasićene pare, koja ima strogo definiranu temperaturu pri datom tlaku. U skladu s tim, specifična zapremina pregrijane pare za isti pritisak ima različitu vrijednost.
Pregrijana para kondenzira se na isti način kao i zasićena para ako je njena temperatura zasićenja t viša od temperature zida tcm. Jezgro struje pare tokom kondenzacije može ostati pregrijano.
Pregrijana para prolazi kroz cijevi hlađene izvana vodom. Hlađenje parom, ovisno o izvedbi odgovarajućih uređaja, vrši se u posebnim daljinskim odzračivačima ili u cijevima smještenim unutar bubnja kotla ili jednog od kolektora pregrijača.
Horizontalni pregrijač bez obloge. Pregrijana para iz cijevi pregrijača usmjerava se u izlaznu komoru-kolektor, a odatle do potrošača.
Kotlovi sa vatrom bez obloge. Pregrijana para iz pregrijača ulazi u izlazni razvodnik 11, odakle se usmjerava do potrošača.
Kondenzacija filma na tri cijevi u rasporedu hodnika.| Kondenzacija filma na cijevima kada se nalaze prema Zhinabo shemi. | Kapljična kondenzacija [L. 375]. Pregrijanu paru karakterizira gotovo isti koeficijent prijenosa topline kao i zasićena para.
Pregrijana para iz izvlačenja turbine se odozdo dovodi u kućište grijača kroz parni spoj i kroz uspon u središnjem dijelu kućišta ulazi u OP zonu, gdje u nekoliko prolaza ispire cijevni snop, odaje toplinu pregrijavanje i već na temperaturi blizu temperature zasićenja ulazi u CP zonu. Kondenzat pare se ispušta van cevnog sistema i struji duž zidova kućišta u donji deo kućišta, u OK zonu.
Pregrijana para nije zasićena, jer je pri datom pritisku specifična zapremina pregrijane pare veća od specifične zapremine suhe zasićene pare, a gustina je manja. On je na svoj način fizička svojstva približava se gasu i što je bliže, to je veći stepen pregrevanja.
Pregrijana para i, u još većoj mjeri, zasićena para se značajno razlikuju po svojim svojstvima idealnih gasova.
Pregrijana para se dobiva iz suhe zasićene pare u posebnim pregrijačima.
Pregrijana para ima višu temperaturu t u odnosu na temperaturu/suhu zasićenu paru istog pritiska. Stoga, za razliku od zasićene pare, pregrijana para određenog tlaka može imati različite temperature. Za karakterizaciju stanja pregrijane pare potrebno je poznavati dva njena parametra, na primjer, tlak i temperaturu. Temperaturna razlika između pregrijane i zasićene pare istog tlaka t - ta naziva se pregrijavanje pare.
Pregrijanu paru je teško očistiti od ulja. Što se tiče vlažne pare, pri konstantnom sadržaju ulja, efikasnost njenog odvajanja raste sa povećanjem vlažnosti. Stoga, prije nego što se unese u separator, temperatura pregrijane pare mora se sniziti propuštanjem kroz neizolovani cevovod, a sadržaj vlage u mokra para- povećava se puhanjem kroz vodeno kupatilo ili ubrizgavanjem kondenzata.
Pregrijana para se dobija na posebnim instalacijama - pregrijačima zbog dodatnog zagrijavanja zasićene pare. Pregrijana para se izuzetno rijetko koristi kao nosač topline, jer je njen koeficijent prijenosa topline nizak. Toplotni sadržaj pregrijane pare također se neznatno povećava u odnosu na zasićenu paru, pa se trošak njenog pregrijavanja ne može opravdati. Ponekad se malo pregrijavanje koristi za smanjenje gubitaka topline u dovodnim parnim vodovima.
Pregrijana para ima temperaturu podešenu u skladu sa stanjem primjera.
Pregrijana para ulazi u fabričku mrežu. Treća ćelija služi vakuum koloni postrojenja. Para za pregrijavanje se u ovu peć dovodi iz fabričke mreže i nakon pregrijavanja se vraća nazad u fabričku mrežu.
Pregrijana para ima temperaturu od 400 C, a kotlovska voda 238 C na 32 ati. Oštećenje metala nastaje na vanjskoj površini cijevi za dovod pare, na granici između kotlovske vode i pare. Teška korozija metala u blizini nivoa vode uočena je i na glavnoj cijevi i na segmentu koji je zamijenio oštećeni dio.
Steam umformer. Pregrijana para se pretvara u zasićenu paru direktnim kontaktom sa hladnom vodom u aparatima koji se nazivaju parni umformeri. U parnom umformeru sa direktnim ubrizgavanjem atomizirane vode (Sl. 264), pregrijana para se dovodi odozgo kroz priključak 1, prolazi kroz vijčanu mlaznicu 2 i prima vrtložno kretanje.
Steam umformer. Pregrijana para se pretvara u zasićenu paru direktnim kontaktom sa hladnom vodom u aparatima koji se nazivaju parni umformeri.
Steam Umformer Seifert. Pregrijana para ulazi u mlaznicu A, prolazi do dna aparata, miješajući se s vodom na putu i izlazi kroz centralnu cijev do mlaznice B. Prisilno okretanje parnog mlaza odozdo prema gore i hidraulički udar koji se javlja na prekretnice značajno doprinose izdvajanju neisparenih kapljica vode, koje se na dno ispuštaju kroz mašinu D.
Pregrijana para se dovodi do svijeće.
Pregrijana para ima temperaturu iznad temperature zasićenja.
Pregrijanu paru kompresori 12 usisavaju kroz separator tekućine 8, komprimiraju i ubrizgavaju kroz separatore ulja 13 i povratne klapne ventile 14 ugrađene na svakom kompresoru u kondenzator 15, gdje se para kondenzira kao rezultat izmjene topline sa vode.
Pregrijana para, čija je temperatura čak mnogo veća od tačke ključanja, i dalje nosi male kapljice tečnosti koje nemaju vremena da ispare na putu od isparivača do kompresora. U cilindru kompresora pretvaraju se u paru, dok smanjuju količinu usisne pare i povećavaju rad kompresije.
Pregrijana para nastaje kada se zagrije zasićena para koja ne sadrži tekućinu.
Šematski dijagram kondenzacijskog parnoturbinskog postrojenja.| Rankineov ciklus u ra-dijagramu.
Pregrijana para ulazi u parnu turbinu 3, gdje se širi, stvarajući rad.
Pregrijana para se dobija na posebnim instalacijama - pregrijačima - dodatnim zagrijavanjem zasićene pare. Pregrijana para se izuzetno rijetko koristi kao nosač topline, jer je njen koeficijent prijenosa topline nizak.
Pregrijana para se koristi u turbini za pogon turbopunjača, koji komprimira zrak do željenog tlaka.
Za zadatak.| Na zadatak. Pregrijana para, koja je odrađena u turbini visokog pritiska HPT-a (stanje 6), ponovo se pregrijava zbog topline dimnih plinova HPG-a (stanje 7), zatim radi u turbini nizak pritisak LPT (stanje 8) i kondenzuje u kondenzatoru Kr. Vodeni ciklus je tako zatvoren.
Pregrijana para, odrađena u turbini visokog pritiska HPT-a (stanje o), ponovo se pregrijava zbog topline dimnih plinova HPG-a (stanje 7), zatim radi u turbini niskog pritiska u LPT (stanje 8) i kondenzuje u kondenzatoru Kr. Vodeni ciklus je tako zatvoren.
Propisi za sigurnosne ventile. Pregrijana para je po svojstvima slična plinu, mlaz je nevidljiv kada teče u atmosferu.
Pregrijana para ima prednost u odnosu na zasićenu paru u tome što kada dođe u dodir sa hladnijim zidovima cjevovoda i druge opreme, ne kondenzira, već samo neznatno snižava svoju temperaturu.
Pregrijana para s temperaturom od 145 °C i tlakom od 0,23 MPa (2 3 kgf/cma) ulazi u aparat kroz priključak / i, prošavši regulacijsku iglu i dvostepenu parnu mlaznicu, stvara vakuum u usisna vazdušna komora 2, gde se vazduh usisava iz atmosfere i meša sa parom.
Pregrijana para koristi se uglavnom za tehnološke potrebe industrijskih preduzeća i elektrane. Domaći korisnici pare obično koriste zasićenu paru.
Pregrijana para se uglavnom koristi za tehnološke potrebe proizvodnje, kao i ako je potrebno prenijeti je do mjesta potrošnje na velike udaljenosti. U zavisnosti od tehnološke potrebe, temperatura pregrijavanja pare može biti od 250 do 450 C.
Pregrijana para se koristi u industrijske svrhe, zasićena para - u sistemima grijanja.
Ovisnost viskoznosti boje o temperaturi. Pregrijana para, koja se koristi umjesto komprimovanog zraka za raspršivanje boje, zagrijava je dok prolazi kroz pištolj, kao i tokom početne faze prskanja.
Pregrijana para se može proizvesti na povišenim temperaturama bez pribjegavanja visokim pritiscima, ali se rijetko koristi kao medij za prijenos topline jer nema dvije velike prednosti zasićene pare, a to su ujednačenost temperature i visoka brzina prijenosa topline. Takođe treba imati na umu da na temperaturi od 480 C i više, hemijska reakcija između vodene pare i željeznih površina.
Pregrijana para, koja ima visoku entalpiju i nizak prijenos topline, dobro je sredstvo protiv kondenzacije. Imajući visoku pregrijanost i nizak prijenos topline, pregrijana para možda uopće neće imati početnu kondenzaciju. U modernim termoelektranama, temperatura pregrijane pare se dovodi do 600 C, a pritisak - do 100 - f - 150 atm.
Zasićena para je para koja je u ravnoteži sa tečnošću.. Temperatura takve pare zavisi od pritiska, tj. Određena temperatura odgovara određenom pritisku pare zasićenja.
Zasićena para može biti suho i mokro.suva para ne sadrži tečnost . Vlažna zasićena para je mješavina pare i tekućine ravnomjerno raspoređena po svojoj masi. .
Država suva zasićena para samo utvrđeno jedan parametar - pritisak ili temperatura.
Država vlažna zasićena para odlučan dva parametra: pritisak ili temperatura i stepen suvoće.
Stepen suhoće (X)- je maseni udio suve pare u sastavu vodene pare.
U \u003d sv (tK - tN) + r [kJ / kg oko s].
Toplota isparavanjar, karakterizira količina topline potrebna za pretvaranje 1 kg vode u suva zasićena para .
Na temperaturi od 374°C i pritisku od 2,25 MPa, cijela masa vode trenutno se pretvara u paru bez dodatne potrošnje topline, tj. formirana pregrijana para, čija je temperatura viša od temperature zasićene pare istog pritiska. Ova para nema definitivnu vezu između temperature i pritiska. .
Temperaturna razlika između pregrijane i zasićene pare pri istom tlaku naziva se stepen pregrijavanja .
Ip \u003d in + cn (tP - tN) [kJ / kg oko s],
gdje OD P je toplotni kapacitet pregrijane pare; (t P - t H ) – temperatura pregrijavanja (stepen pregrijavanja); t H je temperatura zasićene pare.
Za termičku obradu teškog betona preporučuje se mokra ili suha zasićena para. Takva para stvara parno-vazdušno okruženje u komori sa 100% relativnom vlažnošću ( φ , %), u kojem praktično nema isparavanja vlage iz betona, jer para se lako kondenzira na površini proizvoda i zagrijava ga.
Do kondenzacije pregrijane pare dolazi nakon što ona izgubi toplotu pregrijane, tj. kada njegova temperatura padne na temperaturu zasićenja . Kao rezultat prijelaza pregrijane pare u stanje zasićene pare, uklanjanje vlage iz betona, tj. – sušenje , a to nije dozvoljeno. Istovremeno, beton gubi dio vlage koja je uključena u fizičko-hemijske procese hidratacije minerala klinkera (C 3 S, C 2 S, C 3 A, C 4 AF), što značajno smanjuje čvrstoću betona. proizvodi.
Parametri vlažnog vazduha
Toplinska obrada betona se obično izvodi u vlažnom vazduhu, koji se sastoji od mešavine suvog vazduha i vodene pare, koji formiraju mešavina pare i vazduha, poštujući Daltonov zakon: ako su dva različita gasa sadržana u istoj zapremini, tada svaki gas ispunjava celu zapreminu, kao da ne postoji drugi gas.
Pritisak bilo kog od ovih gasova se naziva parcijalni pritisak, a ukupni pritisak mešavine gasova jednak je zbiru njihovih parcijalnih pritisaka
P = P AT + P P ,
gdje R AT i R P – parcijalni pritisak vazduha i pare, respektivno.
U termičkoj obradi betona važan je stepen zasićenosti vazduha parom, koji se određuje relativna vlažnost φ(%), jer intenzitet isparavanja vlage iz betona ovisi o ovom pokazatelju.
relativna vlažnost je omjer mase vodene pare sadržane u 1m 3 zraka ρ P, do njegovog ograničavajućeg sadržaja ρ H pri istoj zapremini, temperaturi i pritisku
φ = ρ P / ρ H × 100%.
Maksimalna količina vodene pare u vazduhu se naziva stanje zasićenja ρ H i temperaturu na kojoj dolazi do zasićenja tačka rose, ili temperatura zasićenjat H .
Najznačajnija razlika između stvarnih plinova i zamišljenog idealnog plina je u tome što je svaki stvarni plin pregrijana para, odnosno, svaki pravi plin kondenzira se uz odgovarajuće smanjenje temperature - pretvara se u tekućinu ili kristal. Razmotrite proces isparavanja.
Pretpostavimo da imamo čistu vodu bez vazduha sipanu na dno ogromnog cilindra (napravljenog od supstance koja dobro provodi toplotu) i prekrivenu klipom koji je čvrsto uz vodu. Neka početna temperatura vode bude jednaka a i pritisku.Ubuduće ćemo pritisak držati nepromenjenim, tako da će proces koji razmatramo biti izobaričan, odnosno odvijati se pri konstantnom pritisku. Na sl. 214, gdje su zapremine iscrtane duž apscise, a pritisci duž ordinate, početno stanje razmatranog kilograma vode prikazano je točkom a.
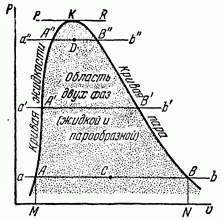
Rice. 214. Na analizu procesa isparavanja.
Daćemo toplinu vodi; temperatura vode će porasti; njegov volumen će se prvo malo smanjiti, a zatim povećati, tako da će se tačka koja predstavlja stanje vode kretati duž "izobare" (dakle, horizontalno) udesno. Na kraju će temperatura vode rasti sve dok u ovom trenutku zapremina uzete vode ne bude oko 4% veća od prvobitne zapremine. Ovo stanje vode je uvjetno prikazano točkom A (toplina koju apsorbira voda u procesu koji se razmatra približno je jednaka kcal).
Obavijestit ćemo vodu o novim količinama topline; voda će se pretvoriti u paru; zapremina koju zauzimaju voda i para će se brzo povećati. Steam in pravi smisao ima plina; ali u cilindru iznad vode bit će mješavina gasovita voda sa najmanjim kapljicama tekuće vode zahvaćene tokom isparavanja (u tehnologiji se takva mješavina naziva mokra para, ili „mokra para“, za razliku od suhe pare koja ne sadrži kapljice vode). Jedno od ovih stanja je na dijagramu predstavljeno tačkom C. Kako se sve više i više procenta tečnosti pretvara u paru, zapremina sistema će nastaviti da raste, a tačka C će se pomerati udesno. Temperatura sistema će tada ostati ista.
Konačno će doći trenutak kada će sva tečnost ispariti do poslednje kapi. U ovom trenutku ćemo imati suhi cilindar zasićena temperatura i dalje je 100°C. Stanje sistema će sada biti predstavljeno tačkom B (ova tačka B se zove tačka kondenzacije pare, ili tačka zasićene pare, tačka je takođe tačka ključanja tečnosti).
Važno je napomenuti da proces isparavanja nije samo izobaričan, već i izotermičan: sve dok se u cilindru nalaze dvije faze iste tvari - tekućina i para, temperatura obje faze ostaje konstantna i jednaka " prelazna temperatura" iz jedne faze u drugu; u stvari, pod pritiskom i na temperaturi C, voda takođe može da ispari (ako joj se prenese toplota), a para se takođe može kondenzovati u tečnost (ako joj se toplota ukloni).
Količina toplote koja se prenosi tečnosti tokom isparavanja naziva se specifična toplota. latentna toplota isparavanje i označeno slovom Kada (za vodu) je jednako 539 kcal. Od ove količine troši se 41 kcal van rada, povezano sa širenjem sistema, dok preostalih 498 kcal čini povećanje unutrašnje energije suve zasićene pare u u poređenju sa tečnom vodom.
Deo latentne toplote isparavanja, koji ide na povećanje unutrašnje energije sistema, naziva se unutrašnja latentna toplota isparavanja i označava se slovom; deo koji ide na spoljašnji rad naziva se spoljašnja latentna toplota isparavanja; to je ekvivalentno radu ekspanzije pritiska zasićene pare, zapremine pare i zapremine tečnosti.
Pratili smo proces isparavanja pod pritiskom. Ali ovaj proces bi se odvijao na sličan način pri drugačijem pritisku, manjem ili višem nego na sl. 214 prikazuje još dvije izobare koje odgovaraju višim pritiscima.
Gledajući ove izobare, odmah uočavamo sledeće promene u toku procesa u zavisnosti od pritiska (Sl. 213):
1. Što se izobara nalazi više, to je veća apscisa tačke ključanja tečnosti. To znači šta veći pritisak na sistemu, tečnost se više širi pre nego što počne da ključa. Razlog za to je jasan: na kraju krajeva, da bi tekućina ključala pod povećanim pritiskom, potrebno je zagrijati na više visoke temperature ključanja i stoga se više širi.
2. Što je izobara veća, apscisa je manja tačka zasićene pare.To znači da zasićena para sa povećanjem pritiska (a samim tim i sa povećanjem temperature) zauzima sve manji volumen (drugim rečima, njena gustina raste) .
Iz rečenog se vidi da kako se pritisak (i temperatura) povećava, tačka ključanja tečnosti i tačka zasićene pare se približavaju jedna drugoj i izoterma-izobara postaje sve kraća i kraća. Iskustvo pokazuje da se sa povećanjem pritiska i temperature ove tačke na kraju spajaju jedna s drugom; takvo spajanje se odvija u tzv kritična tačka Temperatura supstance u kritičnoj tački naziva se kritična temperatura, a pritisak i zapremina koji odgovaraju ovoj tački nazivaju se kritični pritisak i kritična zapremina. Svaka tvar ima svoje posebne vrijednosti kritičnih količina: za vodu, kritična temperatura je 374,2°C, kritični pritisak je jednak kritičnoj zapremini
U kritičnoj tački, razlika između tečnog i parnog stanja materije nestaje.
Sve tačke ključanja tečnosti do i uključujući tačku K definišu određenu krivu, koja se naziva granična kriva tečnosti. Na isti način, sve točke zasićene pare definiraju graničnu krivulju pare. U području omeđenom ovim krivuljama (na primjer, u tačkama imamo mješavinu dvije faze - tečne i pare). Lijevo od ove oblasti supstanca je u tečnom stanju, desno - u stanju pare.
Prijelaz tekućine u paru (ili obrnuto), praćen oštrom promjenom volumena i apsorpcijom ili oslobađanjem topline, može se odvijati samo u području između graničnih krivulja. Ali čak i iznad granične krivulje, možemo zamisliti proces koji počinje malim volumenom i završava se velikom zapreminom - počevši u regiji tečno stanje i završava u gasovitom stanju. Jasno je da u toku ovog procesa nikada ne nailazimo na nagli prelaz iz tečnosti u gas; otuda slijedi da se ovdje ova tranzicija odvija kontinuirano.
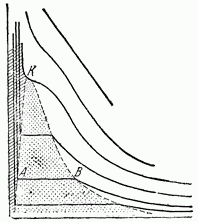
Rice. 215. Stvarni tok izotermi (Andrewsov dijagram).
Kontinuitet tečnosti i gasovitim stanjima eksperimentalno je ustanovio engleski fizičar Andrews 1866. godine; u takvom procesu, supstanca prolazi kroz takva stanja u kojima se ne može nazvati ni tečnom ni gasovitom.
U području ravnoteže tekućine i pare, izoterme su segmenti izobara. Na sl. 215 pokazuje kakav oblik imaju ove izoterme u području pregrijane pare (ili stvarnog plina) iu području tečnog stanja. U području pregrijane pare oni liče na hiperboličke izoterme idealnog plina; izoterme tečnosti se dižu skoro okomito (jer je za blago smanjenje zapremine tečnosti potrebno veoma veliko povećanje pritiska). Na sl. 215 također prikazuje dvije izoterme koje odgovaraju temperaturama iznad kritične, i izotermu koja prolazi kroz kritičnu tačku (za ovu izotermu, kritična tačka K je tačka pregiba).
Andrewsov dijagram koji smo mi razmatrali, koji prikazuje izoterme tekućine, pare i njihove mješavine prema eksperimentalnim podacima, objasnio je Van der Waals 1873. na osnovu molekularno-kinetičkih koncepata (ovo je opisano u § 110; Andrewsov dijagram je u poređenju sa teorijskim dijagramom Van der Walsa, slika 218).
Postojanje kritične temperature prvi je predvidio D. I. Mendeljejev 1860. godine. Istražujući promjenu površinske napetosti tečnosti u zavisnosti od temperature, Mendeljejev je došao do zaključka da mora postojati temperatura na kojoj za datu tečnost površinski napon je nula, a time i meniskus tečnosti i razlika između tečnosti i njenog zasićena para. Ova temperatura, nazvana Mendeljejevljeva "apsolutna tačka ključanja", jeste
ništa više od kritične temperature. Mendeljejevljeve ideje su u potpunosti potvrđene Andrewsovim eksperimentima nekoliko godina kasnije.
Prve najopsežnije i sistematičnije studije kritičnih parametara niza supstanci izveli su Mihail Petrovič Avenarius i njegovi studenti u fizičkoj laboratoriji Kijevskog univerziteta 1873-1895.
Svojstva materije u kritičnom stanju takođe je sveobuhvatno proučavao istaknuti ruski fizičar, profesor Moskovskog univerziteta Aleksandar Grigorijevič Stoletov. Stoletov je rastavio i sažeo veliki broj teorijskih tvrdnji i eksperimentalnih podataka, odvojivši pouzdane od sumnjivih, i uneo potpunu jasnoću u pitanje kritičnog stanja, odobravajući zaključke Andrewsa i Van der Waalsa.
U novije vrijeme (1947-1950) razumijevanje kritično stanje supstancu su doradili i proširili profesor Moskovskog univerziteta V.K. i njen trajekt, ali može biti nešto viši od nje. Stoga, blizu kritične temperature, nakon nestanka meniskusa, ali prije nego što se postigne identitet tečnosti i njene pare, nastaje neobična dispergirana mješavina tekućine i plina. To se ogleda u zamućenosti supstance, u opalescenciji - u pojavama koje su opisali Avenarius, Nadezhdin i drugi.
Kritično stanje karakterizira anomalno visoka vrijednost toplinskog kapaciteta i koeficijenta toplinskog širenja.
Transformacije - tečnost u paru, čvrsto telo u tečnost itd. - nazivaju se faznim prelazima prvog reda. Ove transformacije karakterizira promjena volumena i promjena energije - toplina transformacije.
Transformacije u kojima se ne uočava ni promjena volumena ni promjena energije, ali u isto vrijeme postoje kvalitativne promjene latentne prirode, što se ogleda, na primjer, u oštrom porastu toplotnog kapaciteta u blizini prelazne tačke, su koji se nazivaju prelazima drugog reda. V. K. Semenchenko smatra prijelaz tekućine u plin u kritičnoj tački faznom tranzicijom druge vrste i otkriva analogiju kritičnog stanja s nizom drugih slučajeva fazni prelazi druga vrsta (za mješavine tekućina, za transformacije u kristalima).
Andrewsov dijagram pokazuje da svakoj ravnotežnoj temperaturi tekućine i pare odgovara određeni pritisak, koji je veći što je temperatura viša, a što je manja, to je niža temperatura. Drugim riječima, za zasićenu paru, tlak i temperatura se povećavaju ili smanjuju zajedno. kriva,
Drugim riječima, toplina isparavanja jednaka je prirastu vezane energije (§ 107):
![]()
S druge strane, toplota isparavanja, prema jednačini prvog zakona, jednaka je zbiru prirasta unutrašnje energije i rada izobarnog širenja iz zapremine tečnosti u zapreminu pare:
Izjednačavajući prave dijelove dva dobijena izraza za i (3), nalazimo:
Ova jednadžba znači da u termodinamičkoj ravnoteži tekućine i njene zasićene pare ukupni termodinamički potencijali za jedinicu mase materije u obe faze su jednake.






