fotoni roșii. Fotonii. Proprietățile cuantice ale radiației electromagnetice
Mai puțin de un atom
Un foton este un micro-obiect subnuclear care nu poate fi împărțit în părțile sale componente. Nu are automasă și este neutru din punct de vedere electric. Este cea mai mică particulă indivizibilă radiatie electromagnetica. Un foton călătorește cu viteza luminii și există doar în mișcare. Este imposibil să-l oprești. Masa sa în repaus este zero, deci fie se mișcă cu viteza luminii, fie nu există deloc. Nu poate fi în mișcare. Potrivit unor oameni de știință, un foton nu este o particulă, ci o undă electromagnetică. Cu toate acestea, această opinie este controversată.
Despre natura luminii
Primul om de știință care a venit cu ideea că lumina constă din cele mai mici particule invizibile a fost oficialul arab Abu al-Haytham. El a exprimat această idee în 1021 în Cartea sa de optică. Sute de ani mai târziu, în 1873, Maxwell, un om de știință britanic, a revoluționat domeniul. A ajuns la concluzia că lumina sunt unde electromagnetice. Adevărat, la acea vreme teoria lui în unele aspecte  nu corespundea cu realitatea. Mai departe, studiind diferite fenomene electromagnetice, a ajuns la o altă concluzie logică. Cea mai importantă descoperire a sa a fost că lumina pune inevitabil presiune asupra unui obstacol. Acest fenomen se bazează pe faptul că fotonii în mișcare își transferă impulsul către moleculele sau atomii pe care îi întâlnesc pe drum. Această afirmație a lui Maxwell a fost confirmată de N.P. Lebedev. Momentul unui foton este egal cu raportul dintre constanta lui Planck și lungimea de undă a luminii. Aceasta poate fi exprimată prin formula p=h/λ.
nu corespundea cu realitatea. Mai departe, studiind diferite fenomene electromagnetice, a ajuns la o altă concluzie logică. Cea mai importantă descoperire a sa a fost că lumina pune inevitabil presiune asupra unui obstacol. Acest fenomen se bazează pe faptul că fotonii în mișcare își transferă impulsul către moleculele sau atomii pe care îi întâlnesc pe drum. Această afirmație a lui Maxwell a fost confirmată de N.P. Lebedev. Momentul unui foton este egal cu raportul dintre constanta lui Planck și lungimea de undă a luminii. Aceasta poate fi exprimată prin formula p=h/λ.
Folosind... fotoni
Poate că, după ceva timp, omenirea va trece complet la un nou tip de sursă de energie, care va fi mult mai ieftină și mai eficientă decât gazul, petrolul sau cărbunele. Este suficient să spunem că este deja aproape peste tot. Printre altele, va fi imposibil de monopolizat această sursă de energie, care va oferi o mulțime de avantaje față de utilizarea gazului, a energiei electrice etc. Ce este? Aceasta este energia unui foton. Deja acum este folosit cu ajutorul solarului  baterii. Energia unui foton este produsul constantei lui Planck și frecvența radiației. Prin formula aceasta se poate exprima astfel: e=hv. Litera v în acest caz indică frecvența fotonului. Densitatea radiației solare la nivelul suprafeței pământului este de aproximativ o mie de wați pe metru pătrat. Acest flux puternic și continuu de fotoni care vin de la steaua cea mai apropiată de planeta noastră poate fi transformat în energie electrica. In ce fel? Imaginați-vă un pătrat plat cu colțuri teșite, din silicon, al cărui diametru este de obicei de 12,5 cm.Acesta este convertorul fotovoltaic. Poate fi mono- sau multi-cristalin. Aceste piese sunt folosite pentru a face panouri solare. Energia fotonului este transformată în electricitate. Eficiența convertorului poate varia de la 5 la 17 la sută, în funcție de tipul și structura acestuia. În ciuda acestui fapt, lumina soarelui (citește - energie fotonică) este o sursă promițătoare de electricitate gratuită. Panouri speciale care îl reciclează sunt instalate în multe case din Europa. Un exemplu mai impresionant poate fi dat - în vremea noastră au apărut deja mașini cu baterii încărcate de lumina soarelui.
baterii. Energia unui foton este produsul constantei lui Planck și frecvența radiației. Prin formula aceasta se poate exprima astfel: e=hv. Litera v în acest caz indică frecvența fotonului. Densitatea radiației solare la nivelul suprafeței pământului este de aproximativ o mie de wați pe metru pătrat. Acest flux puternic și continuu de fotoni care vin de la steaua cea mai apropiată de planeta noastră poate fi transformat în energie electrica. In ce fel? Imaginați-vă un pătrat plat cu colțuri teșite, din silicon, al cărui diametru este de obicei de 12,5 cm.Acesta este convertorul fotovoltaic. Poate fi mono- sau multi-cristalin. Aceste piese sunt folosite pentru a face panouri solare. Energia fotonului este transformată în electricitate. Eficiența convertorului poate varia de la 5 la 17 la sută, în funcție de tipul și structura acestuia. În ciuda acestui fapt, lumina soarelui (citește - energie fotonică) este o sursă promițătoare de electricitate gratuită. Panouri speciale care îl reciclează sunt instalate în multe case din Europa. Un exemplu mai impresionant poate fi dat - în vremea noastră au apărut deja mașini cu baterii încărcate de lumina soarelui.
Dualitatea luminii unde corpusculare
Lumina este emisă, propagată și absorbită sub formă de corpusculi - fotoni, care sunt particule din câmpul electromagnetic și purtători de cuante (porțiuni) de energie. Valoarea cuantumului de energie este determinată de formula lui Planck: Caracteristicile corpusculare ale unui foton () sunt completate de caracteristicile undei (), ceea ce confirmă Principiul de complementaritate al lui Bohr.

Experiența lui Bothe (1924). În acest experiment, o folie metalică subțire F a fost iluminată de raze X de intensitate scăzută, ceea ce a cauzat o fluorescență slabă a razelor X (lucire ulterioară) în folie. Radiația de raze X de la folie a căzut pe două contoare de radiații ionizante, Cch1 și Cch2 (contoare Geiger). Sensibilitatea unor astfel de contoare este atât de mare încât pot înregistra cuante individuale de raze X. La declanșare, contoarele au acționat mecanismele înregistratoarelor M1 și M2, care fac semne pe banda în mișcare L. Ca urmare, s-a constatat că semnele de pe bandă de la două reportofoare, asociate cu momentele cuantelor de raze X. lovind ghișeele, sunt absolut aleatorii. Acest fapt ar putea fi explicat doar prin lovirea aleatorie a cuantelor de raze X împrăștiate de folie într-una sau în cealaltă direcție, în timp ce, conform conceptelor de undă, radiația de la sursă ar trebui să se propage uniform în toate direcțiile.
Energia, masa și impulsul unui foton.
Lumina este emisă, absorbită și propagată în porțiuni discrete (cuante) numite fotoni. Energia fotonică. Masa sa se găsește din legea relației dintre masă și energie:
. Un foton este o particulă elementară care întotdeauna (în orice mediu) se mișcă cu o viteză c și are o masă în repaus egală cu zero. În consecință, masa fotonului diferă de masa particulelor el-tar precum electronul, protonul și neutronul, care au o masă în repaus diferită de zero și pot fi în repaus. Momentul unui foton se obține dacă forma generala teoria relativitatii ![]() (E - energie totală) pune masa în repaus a fotonului:
(E - energie totală) pune masa în repaus a fotonului: ![]() . Prin urmare, un foton, ca orice altă particulă, este caracterizat de energie, masă și impuls.
. Prin urmare, un foton, ca orice altă particulă, este caracterizat de energie, masă și impuls.
Efect fotoelectric.
Ipoteza lui Planck, care a rezolvat problema radiației termice a unui corp negru, a fost confirmată și dezvoltată în continuare în explicarea efectului fotoelectric - un fenomen a cărui descoperire a jucat o teorie importantă în dezvoltarea teoriei cuantice. Există efecte fotoelectrice externe, interne și de supapă. efect fotoelectric extern se numeste emisie de electroni in-tion sub influenta radiatiei electromagnetice (lumina). Se observă în solide(metale, semiconductori, dielectrici), precum și în gaze pe atomii și moleculele individuale. Efect fotoelectric intern- Acestea sunt tranzițiile electronilor în interiorul unui semiconductor sau dielectric cauzate de radiația electromagnetică de la stările legate la cele libere fără a scăpa în exterior. În p-tate, concentrația purtătorilor de curent în interiorul corpului crește, ceea ce duce la apariția fotoconductivității (o creștere a conductibilității electrice a unui semiconductor sau dielectric atunci când este iluminat) sau la apariția unui EMF. efect fotoelectric al supapei- apariția EMF (foto-EMF) la iluminarea contactului a doi semiconductori diferiți sau a unui semiconductor și a unui metal (în absența unui câmp electric extern). Cu ajutorul efectului fotoelectric al supapei, este posibilă transformarea directă a energiei solare în energie electrică. Ecuația lui Einstein pentru efectul fotoelectric extern: Energia fotonului incident este cheltuită pentru a efectua munca de ieșire din metal și pentru a comunica energie cinetică către fotoelectron. Conform legii conservării energiei, ![]() .
.
Efectul Compton și teoria lui.
În efectul Compton, proprietățile corpusculare ale luminii se manifestă cel mai pe deplin. Cercetând împrăștierea radiațiilor monocromatice de raze X de către substanțe cu atomi de lumină, Compton a constatat că în compoziția radiației împrăștiate, împreună cu radiația lungimii de undă inițiale, se observă și radiații cu lungimi de undă mai mari. Experimentele au arătat că diferența Δλ \u003d λ '-λ nu depinde de lungimea de undă λ a radiației incidente și de natura substanței de împrăștiere, ci este determinată numai de mărimea unghiului de împrăștiere. ![]() , unde este lungimea de undă a radiației împrăștiate, este lungimea de undă Compton (când un foton este împrăștiat de un electron
=
2,426nm). Efectul Compton se numește împrăștiere elastică a radiațiilor cu undă scurtă (raze X și radiații γ) pe electronii liberi (sau slab legați) din insule, însoțită de o creștere a lungimii de undă. Dacă socoti cum se întâmplă teoria cuantica că radiația are o natură corpusculară, adică reprezintă un flux de fotoni, atunci efectul Compton este p-tat al coliziunii elastice a fotonilor de raze X cu electronii liberi din insule (pentru atomii de lumină, electronii sunt legați slab de nucleele atomilor, deci pot fi considerați gratuit). În timpul acestei coliziuni, fotonul transferă o parte din energia și impulsul său în conformitate cu legile conservării lor.
, unde este lungimea de undă a radiației împrăștiate, este lungimea de undă Compton (când un foton este împrăștiat de un electron
=
2,426nm). Efectul Compton se numește împrăștiere elastică a radiațiilor cu undă scurtă (raze X și radiații γ) pe electronii liberi (sau slab legați) din insule, însoțită de o creștere a lungimii de undă. Dacă socoti cum se întâmplă teoria cuantica că radiația are o natură corpusculară, adică reprezintă un flux de fotoni, atunci efectul Compton este p-tat al coliziunii elastice a fotonilor de raze X cu electronii liberi din insule (pentru atomii de lumină, electronii sunt legați slab de nucleele atomilor, deci pot fi considerați gratuit). În timpul acestei coliziuni, fotonul transferă o parte din energia și impulsul său în conformitate cu legile conservării lor.
Efectul Compton nu poate fi observat în regiunea vizibilă a spectrului, deoarece energia fotonului lumina vizibila este comparabilă cu energia de legare a unui electron cu un atom și nici măcar electronul exterior nu poate fi considerat liber. Efes. K. se observă nu numai în electroni, ci și pe particulele încărcate, cum ar fi protonii, totuși, datorită masei mari a protonului, recul acestuia este „vizibil” doar atunci când fotonii de energii foarte mari sunt împrăștiați. Ca ef. K. iar efectul fotoelectric bazat pe concepte cuantice se datorează interacţiunii fotonilor cu electronii. În primul caz, fotonul este împrăștiat, în al doilea, este absorbit. Difuzarea are loc atunci când un foton interacționează cu un electron liber, iar efectul fotoelectric cu electronii legați. Când un foton se ciocnește, deoarece acesta este în conflict cu legile conservării impulsului și energiei. Prin urmare, atunci când fotonii interacționează cu electronii liberi, se poate observa doar împrăștierea lor, adică. Efectul Compton.
Radiația Bremsstrahlung.
Un electron care se mișcă într-un mediu își pierde viteza. Acest lucru creează o accelerație negativă. Conform teoriei lui Maxwell, orice accelerat mișcarea unei particule încărcate este însoțită de radiații electromagnetice. Se numește radiația care apare atunci când un electron decelerează în materialul anodic bremsstrahlung raze X.
Presiune ușoară.
Dacă fotonul are impuls, atunci lumina care cade asupra corpului trebuie să exercite presiune asupra acestuia. Din punctul de vedere al teoriei cuantice, presiunea luminii asupra repetiției se datorează faptului că fiecare foton, atunci când se ciocnește cu repetiția, își transferă impulsul acestuia. Să calculăm, din punctul de vedere al teoriei cuantice, presiunea uşoară exercitată pe suprafaţa corpului de un flux de radiaţii monocromatice (frecvenţa ν) incidentă perpendicular pe suprafaţă. Dacă N fotoni cad pe unitatea de timp pe unitatea de suprafață a corpului, atunci cu un coeficient de reflexie ρ al luminii, ρ va fi reflectat de suprafața corpului N fotoni și (1− ρ )N- vor fi absorbite. Fiecare foton absorbit transmite un al doilea impuls , și fiecare reflectat - 2 =2 hν / c(când este reflectat, impulsul unui foton se schimbă în ). Presiunea luminii pe buclă este egală cu impulsul care este transmis de bucle în 1 s de N fotoni:
este energia tuturor fotonilor care cad pe unitate rep per unitate de timp, adică iluminarea energetică a zonei, a/ c=ω - densitatea volumică a energiei radiației. Prin urmare, presiunea produsă de lumină în timpul incidenței normale la suprafață, ![]() .
.
6. Spectre atomice. formule seriale. experiența lui Rutherford. postulatele lui Bohr. Experimentul Frank-Hertz. Teoria elementară a atomului de hidrogen. Semnificația teoriei lui Bohr. Spectre caracteristice de raze X. legea lui Moseley.
Spectrele atomice.formule seriale.
Studiile spectrelor de emisie ale gazelor rarefiate (adică spectrele de emisie ale atomilor individuali) au arătat că fiecare gaz are un spectru de linii bine definit, constând din linii spectrale individuale sau grupuri de linii strâns distanțate. Cel mai studiat este spectrul celui mai simplu atom - atomul de hidrogen. Balmer (1825-1898) a preluat o formulă empirică care descrie toate cele cunoscute la acea vreme linii spectrale atomul de hidrogen și regiunea vizibilă a spectrului ![]() ,(n = 3, 4, …) unde R„este constanta Rydberg. Deoarece ν = Cu/λ , atunci f-la poate fi rescris pentru frecvențe:
,(n = 3, 4, …) unde R„este constanta Rydberg. Deoarece ν = Cu/λ , atunci f-la poate fi rescris pentru frecvențe: ![]() , Unde R=
R"c este, de asemenea, constanta Rydberg. Din expresiile obținute rezultă că liniile spectrale care diferă în diferite valori ale lui n formează un grup sau o serie de linii, numită seria Balmer. Pe măsură ce n crește, liniile seriei se apropie între ele; valoarea n = ∞ determină limita seriei, la care se învecinează spectrul continuu din partea frecvenţelor înalte. Ulterior, mai multe serii au fost descoperite în spectrul atomului de hidrogen.
, Unde R=
R"c este, de asemenea, constanta Rydberg. Din expresiile obținute rezultă că liniile spectrale care diferă în diferite valori ale lui n formează un grup sau o serie de linii, numită seria Balmer. Pe măsură ce n crește, liniile seriei se apropie între ele; valoarea n = ∞ determină limita seriei, la care se învecinează spectrul continuu din partea frecvenţelor înalte. Ulterior, mai multe serii au fost descoperite în spectrul atomului de hidrogen.
În regiunea ultravioletă a spectrului este
Seria Lyman: ![]()
În regiunea infraroșu s-au găsit:
Seria Paschen: ![]()
seria bracket: ![]()
Seria Pfund: ![]()
Seria Humphy: ![]()
Toate seriile de mai sus din spectrul atomului de hidrogen pot fi descrise printr-o buclă f, numită bucla f generalizată Balmer: , unde m are o valoare constantă în fiecare serie dată, m = 1, 2, 3, 4, 5, 6 (definește seria), n - preia valori întregi, începând de la m + 1 (definește liniile individuale ale acestei serii).
experiența lui Rutherford.
În dezvoltarea ideilor despre structura atomului, importanța experimentelor lui Rutherford privind împrăștierea particulelor α în materie. Particulele alfa apar din transformări radioactive; sunt particule încărcate pozitive cu o sarcină de 2e și o masă de aproximativ 7300 de ori mai mare decât masa unui electron. Fasciculele de particule α sunt foarte monocromatice (pentru o transformare dată au practic aceeași viteză (de ordinul a 10^7 m/s)). Rutherford, investigând trecerea particulelor α în v-ve (prin folie de aur de aproximativ 1 μm grosime), a arătat că majoritatea dintre ele experimentează abateri minore, dar unele particule α (aproximativ una din 20.000) se abat brusc de la direcția lor inițială ( unghiurile de deviere au ajuns chiar la 180°). pentru că electronii nu pot schimba în mod semnificativ mișcarea unor particule atât de grele și rapide precum particulele α, apoi Rutherford a concluzionat că abaterea semnificativă a particulelor α se datorează interacțiunii lor cu o sarcină pozitivă a unei mase mari. Cu toate acestea, doar câteva particule α experimentează o deviație semnificativă; prin urmare, doar unele dintre ele trec în apropierea unei sarcini pozitive date. Aceasta, la rândul său, înseamnă că sarcină pozitivă a unui atom este concentrat într-un volum foarte mic în comparație cu volumul unui atom. Pe baza experimentelor sale, Rutherford a propus un model nuclear al atomului. Conform acestui model, pus în jurul numărului de serie al el-ta în sistemul Mendeleev, e este o sarcină elementară), dimensiunea este 10^(−15) −10^(−14) m și o masă practic egală cu masa unui atom, într-o regiune cu dimensiuni liniare de ordinul 10^(−10) m electroni se mișcă pe orbite închise, formând învelișul de electroni atom. Deoarece atomii sunt neutri, atunci sarcina nucleului este egală cu sarcina totală a electronilor, adică. Electronii Z trebuie să se rotească în jurul nucleului.
postulatele lui Bohr.
Prima încercare de a construi o nouă teorie calitativ - cuantică - a atomului a fost întreprinsă de Bohr. El și-a propus scopul de a lega într-un singur întreg modelele empirice ale spectrelor de linii, modelul nuclear al lui Rutherford al atomului (Conform acestui model, în jurul unui nucleu pozitiv cu sarcina Ze (Z este numărul de serie al elementului din Mendeleev). sistem, e este sarcina elementară), dimensiunea 10 ^(−15) −10^(−14) m și o masă practic egală cu masa unui atom, electronii se mișcă pe orbite închise într-o regiune cu dimensiuni liniare de ordin de 10^(−10 m), formând învelișul de electroni a unui atom. Deoarece atomii sunt neutri, atunci sarcina nucleului este egală cu sarcina totală a electronilor, adică electronii Z trebuie să se rotească în jurul nucleului) și cuantica natura emisiei și absorbției luminii. Două postulate:
Primul postulat al lui Bohr(postulat al stărilor staţionare): există stări staţionare în atom în care acesta nu radiază energie. Stările staționare ale unui atom corespund orbitelor staționare de-a lungul cărora se mișcă electronii. Mișcarea electronilor pe orbite staționare nu este însoțită de emisia de unde electromagnetice. În starea staționară a unui atom, un electron care se mișcă de-a lungul unei orbite circulare trebuie să aibă valori cuantice discrete ale momentului unghiular care să îndeplinească condiția (n=1,2,3,...), unde - masa electronului, v - viteza acestuia de-a lungul orbitei a n-a a razei , = h/ 2π .
Al doilea postulat(regula frecvenței): când un electron se mișcă de pe o orbită staționară pe alta, un foton cu energie este emis (absorbit) egal cu diferența de energie a stărilor staționare corespunzătoare ( și -- respectiv, energia stărilor staționare ale atomului înainte și după radiație (absorbție)). La< este emis un foton (trecerea unui atom dintr-o stare cu o energie mai mare la o stare cu una inferioară, adică trecerea unui electron de pe o orbită mai îndepărtată de nucleu la una apropiată), la > - absorbția acestuia (trecerea unui atom la o stare cu o energie mai mare, adică trecerea unui electron pe o orbită mai îndepărtată de nucleu). Mulțimea tuturor frecvențelor discrete posibile ν=( −)/h tranziții cuantice și determină spectrul de linie al atomului.
Experimentul Frank-Hertz.
Prin studierea metodei de întârziere a potențialelor coliziuni ale electronilor cu atomii de gaze, s-a dovedit experimental că valorile energiei atomilor sunt discrete. O diagramă schematică a instalării acestora este prezentată în fig. Un tub vid umplut cu vapori de mercur (presiune aproximativ egală cu 13 Pa) conținea un catod (K), două grile (i) și un anod (A). Electronii emiși de catod au fost accelerați de diferența de potențial aplicată între catod și rețea. Între rețea și anod se aplică un potențial de întârziere mic (aproximativ 0,5 V). Electronii accelerați în regiunea 1 intră în regiunea 2 dintre grile, unde experimentează coliziuni cu atomii de vapori de mercur. Electronii care, după ciocniri, au suficientă energie pentru a depăși potențialul de întârziere din regiunea 3 ajung la anod. În ciocnirile neelastice ale electronilor cu atomii de mercur, aceștia din urmă pot fi excitați. Conform teoriei lui Bohr, fiecare dintre atomii de mercur poate primi doar o energie foarte definită, trecând în același timp într-una dintre stările excitate. Din experiență rezultă că, odată cu creșterea potențialului de accelerare până la 5 V, curentul anodului crește monoton, valoarea lui trece printr-un maxim, apoi scade brusc și crește din nou. 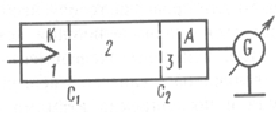
legea lui Moseley.
În 1913 Fizicianul englez Moseley a măsurat lungimile de undă raze X emis de diferite metale în tubul catodic și a reprezentat grafic inversul rădăcinii pătrate a lungimii de undă a razelor X în funcție de numărul atomic al elementului. Acest grafic (Fig. 1) arată că numărul de serie reflectă unele caracteristici importante ale elementului. Moseley a sugerat că această caracteristică este sarcina nucleului unui atom și că aceasta crește cu unu atunci când se trece de la un element la altul în ordine. El a numit numărul de serie număr atomic - Z. 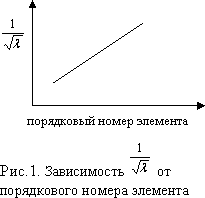
Legea lui Moseley:
Rădăcina pătrată a inversei lungimii de undă a razelor X emise de atomi diverse elemente, este in dependență liniară din numărul de serie al elementului unde este lungimea de undă, este o valoare constantă, Z este numărul ordinal al elementului (sarcină nucleară).
Mai târziu a devenit cunoscut faptul că numărul de serie este egal cu numărul de protoni din nucleu. Astfel, numărul ordinal (atomic) este egal cu sarcina nucleului și, de asemenea, determină prezența protonilor (particule pozitive) în acesta. Și deoarece atomii sunt neutri, numărul de electroni dintr-un atom trebuie să fie egal cu numărul de protoni. Dar masele atomilor s-au dovedit a fi mai mari decât masa totală a protonilor. Pentru a explica excesul de masă, a fost sugerată existența neutronilor.
7. lungime de undă De Broglie. Fundamentarea experimentală a dualismului undelor. Relația de incertitudine Heisenberg. Funcția de undă și semnificația ei statistică. Ecuația Schrödinger. Funcții proprii și valori proprii. Ecuația Schrödinger staționară. Reprezentarea mecanică cuantică a unei particule care se mișcă liber. Descriere mecanică cuantică a unei particule într-un puț de potențial dreptunghiular infinit de adâncime.
lungime de undă De Broglie.
Omul de știință francez Louis de Broglie (1892-1987), realizând simetria existentă în natură și dezvoltând idei despre natura corpusculară duală a luminii, a înaintat în 1923 o ipoteză despre universalitatea dualismului corpuscular-undă. De Broglie a susținut că nu numai fotonii, ci și electronii și orice alte particule de materie, împreună cu cele corpusculare, au și proprietăți de undă. Deci, potrivit lui de Broglie, fiecare micro-obiect conectat, pe de o parte, corpuscular caracteristici – energie Eși impulsul p și, pe de altă parte, caracteristicile undei- frecvența v și lungimea de undă LA. Rapoarte cantitative care leagă corpusculare și proprietățile valurilor particulele sunt aceleași ca și pentru fotoni: Astfel, orice particulă cu impuls este asociată cu un proces de undă cu o lungime de undă determinată de conform formulei de Broglie: Această relație este valabilă pentru orice particulă cu impuls R.
Fundamentarea experimentală a dualismului undelor.
Curând, ipoteza lui de Broglie a fost confirmată experimental. În 1927, fizicianul american și K. Davisson (1881 - 1958) și L. Germer (1896 - 1971) au descoperit că un fascicul de electroni împrăștiat dintr-o rețea de difracție naturală - un cristal de nichel - dă un model de difracție distinct. Maximele de difracție corespundeau formulei Wulff-Braggs (182.1), iar lungimea de undă Bragg s-a dovedit a fi exact egal cu lungimea val, calculat prin formula. Mai târziu, formula lui de Broglie a fost confirmată de experimentele lui P. S. Tartakovsky și G. Thomson, care au observat modelul de difracție în timpul trecerii unui fascicul de electroni rapizi (energie „50 keV) printr-o folie metalică (grosime x 1 micron). Deoarece modelul de difracție a fost studiat pentru fluxul de electroni, a fost necesar să se demonstreze că proprietățile undei sunt inerente nu numai fluxului unui set mare de electroni, ci și fiecărui electron separat. Acest lucru a fost confirmat experimental în 1948 de către fizicianul sovietic V. A. Fabrikant (n. 1907). El a arătat că chiar și în cazul unui fascicul de electroni atât de slab, atunci când fiecare electron trece prin dispozitiv independent de ceilalți (intervalul de timp dintre doi electroni este de 10^4 ori mai mare decât timpul în care electronul trece prin dispozitiv), modelul de difracție care apare în timpul expunerii lungi nu diferă de modelele de difracție obținute cu o expunere scurtă pentru fluxuri de electroni de zeci de milioane de ori mai intense. În consecință, proprietățile de undă ale particulelor nu sunt o proprietate a colectivului lor, ci sunt inerente fiecărei particule separat. Ulterior, au fost descoperite fenomene de difracție și pentru neutroni, protoni, fascicule atomice și moleculare. Aceasta a servit în cele din urmă ca o dovadă a prezenței proprietăților de undă ale microparticulelor și a făcut posibilă descrierea mișcării microparticulelor sub forma unui proces de undă caracterizat printr-o anumită lungime de undă calculată prin formula de Broglie. Descoperirea proprietăților de undă ale microparticulelor a condus la apariția și dezvoltarea de noi metode de studiere a structurii substanțelor, cum ar fi difracția electronilor și difracția neutronilor, precum și la apariția unei noi ramuri a științei - optica electronică.
Relația de incertitudine Heisenberg.
Conform naturii cu undă corpusculară duală a particulelor de materie, pentru a descrie microparticulele sunt folosite fie reprezentări de undă, fie corpusculare. Prin urmare, este imposibil să le atribuim toate proprietățile particulelor și toate proprietățile undelor. W. Heisenberg, ținând cont de proprietățile de undă ale microparticulelor și de limitările comportamentului lor asociate cu proprietățile undelor, a ajuns la concluzia în 1927 că este imposibil să se caracterizeze un obiect al microparticulelor simultan cu o precizie predeterminată atât prin coordonate, cât și prin impuls. . Conform relația de incertitudine Heisenberg, o microparticulă (microobiect) nu poate avea simultan o anumită coordonată (x, y, z) și o anumită proiecție a impulsului corespunzătoare (px, ru, rg),în plus, incertitudinile acestor cantități îndeplinesc condițiile, i.e. produsul unei coordonate și proiecția impulsului corespunzătoare nu poate fi mai mic decât o valoare a ordinului h. Din relația de incertitudine rezultă că, de exemplu, dacă o microparticulă se află într-o stare cu o valoare exactă a coordonatei (), atunci în această stare proiecția corespunzătoare a impulsului său se dovedește a fi complet incertă și invers. Astfel, pentru o microparticulă nu există stări în care coordonatele și impulsul ei să aibă ambele valori exacte. Aceasta implică imposibilitatea reală de a măsura simultan coordonatele și impulsul unui micro-obiect cu orice precizie predeterminată. Deoarece în mecanica clasică se presupune că măsurarea poziției și a impulsului poate fi făcută cu orice precizie, atunci relația de incertitudine este, prin urmare, limitarea cuantică a aplicabilității mecanicii clasice la micro-obiecte.
Funcția de undă și semnificația ei statistică.
Fizicianul german M. Born în 1926 a sugerat că, conform legii undelor, nu probabilitatea în sine se modifică, ci cantitatea numită amplitudinea probabilitățiişi notat Această valoare se mai numeşte funcția de undă(sau -funcţie). Amplitudinea probabilității poate fi complexă, iar probabilitatea W proporțional cu pătratul modulului său: ![]() este un complex de funcții conjugat la ).
Astfel, descrierea stării unui microobiect cu ajutorul funcției de undă are caracter statistic, probabilistic: pătratul modulului funcției de undă (pătratul modulului amplitudinii undelor de Broglie) determină probabilitatea de a găsi o particulă la un moment dat în regiunea cu coordonate
este un complex de funcții conjugat la ).
Astfel, descrierea stării unui microobiect cu ajutorul funcției de undă are caracter statistic, probabilistic: pătratul modulului funcției de undă (pătratul modulului amplitudinii undelor de Broglie) determină probabilitatea de a găsi o particulă la un moment dat în regiunea cu coordonate
Ecuația Schrödinger.
Ecuația de bază mecanica cuantică non-relativista formulată în 1926 de E. Schrödinger. Ecuația Schrödinger, ca toate ecuațiile de bază ale fizicii (de exemplu, ecuațiile lui Newton în mecanica clasică și ecuațiile lui Maxwell pentru câmpul electromagnetic), nu este derivată, ci postulată. Corectitudinea acestei ecuații este confirmată de acordul cu experiența rezultatelor obținute cu ajutorul ei, care, la rândul său, îi conferă caracterul unei legi a naturii. Ecuația Schrödinger are forma: ![]() , Unde m este masa particulei, este operatorul Laplace, i- unitate imaginară, U(X,
y,
z,
t)
-funcția potențială a unei particule în câmpul de forță în care se mișcă Ψ (X y,
z,
t)
este funcția de undă dorită a particulei.
, Unde m este masa particulei, este operatorul Laplace, i- unitate imaginară, U(X,
y,
z,
t)
-funcția potențială a unei particule în câmpul de forță în care se mișcă Ψ (X y,
z,
t)
este funcția de undă dorită a particulei.
Funcții proprii și valori proprii. Ecuația Schrödinger staționară.
Ecuația ![]() numit Ecuația Schrödinger pentru staționar state. Această ecuație include energia totală ca parametru E particule. În teoria ecuațiilor diferențiale, se demonstrează că astfel de ecuații au o mulțime infinită de soluții, din care, prin impunerea condițiilor la limită, se selectează soluții care au sens fizic. Pentru ecuația Schrödinger, astfel de condiții sunt condițiile de regularitate ale funcțiilor de undă: funcțiile de undă trebuie să fie finite, cu o singură valoare și continue împreună cu derivatele lor primare. Astfel, numai soluțiile care sunt exprimate prin funcții regulate au o semnificație fizică reală y. Dar soluțiile obișnuite nu au loc pentru nicio valoare a parametrului E, dar numai pentru un anumit set de ele, caracteristice unei sarcini date. Aceste valori energetice se numesc proprii. Soluții care se potrivesc proprii se numesc valorile energetice funcții proprii. Valori proprii E poate forma atât serii continue, cât și discrete. În primul caz, se vorbește despre continuu, sau continuu, spectru, in secunda - despre spectrul discret.
numit Ecuația Schrödinger pentru staționar state. Această ecuație include energia totală ca parametru E particule. În teoria ecuațiilor diferențiale, se demonstrează că astfel de ecuații au o mulțime infinită de soluții, din care, prin impunerea condițiilor la limită, se selectează soluții care au sens fizic. Pentru ecuația Schrödinger, astfel de condiții sunt condițiile de regularitate ale funcțiilor de undă: funcțiile de undă trebuie să fie finite, cu o singură valoare și continue împreună cu derivatele lor primare. Astfel, numai soluțiile care sunt exprimate prin funcții regulate au o semnificație fizică reală y. Dar soluțiile obișnuite nu au loc pentru nicio valoare a parametrului E, dar numai pentru un anumit set de ele, caracteristice unei sarcini date. Aceste valori energetice se numesc proprii. Soluții care se potrivesc proprii se numesc valorile energetice funcții proprii. Valori proprii E poate forma atât serii continue, cât și discrete. În primul caz, se vorbește despre continuu, sau continuu, spectru, in secunda - despre spectrul discret.
Reprezentarea mecanică cuantică a unei particule care se mișcă liber.
Când o particulă liberă se mișcă (U(x) = 0) energia sa totală coincide cu cea cinetică. Pentru o particulă liberă care se mișcă de-a lungul axei X, ecuația Schrödinger pentru stările staționare ia forma ![]() .Sustituția directă poate asigura că o anumită soluție a ecuației i este o funcție, unde A=const și k = const, cu valoare proprie de energie Funcția este doar partea de coordonate a funcției de undă. Prin urmare, funcția de undă dependentă de timp, conform
.Sustituția directă poate asigura că o anumită soluție a ecuației i este o funcție, unde A=const și k = const, cu valoare proprie de energie Funcția este doar partea de coordonate a funcției de undă. Prin urmare, funcția de undă dependentă de timp, conform ![]() , (219.3) (aici
, (219.3) (aici ![]() Funcția este o undă de Broglie monocromatică plană). Din expresia rezultă că dependența energiei de impuls
Funcția este o undă de Broglie monocromatică plană). Din expresia rezultă că dependența energiei de impuls ![]() se dovedește a fi obișnuit pentru particulele nonrelativiste. În consecință, energia unei particule libere poate lua orice valoare (de la numărul de undă k poate lua orice valoare pozitivă), adică spectrul său de energie este continuu. Astfel, o particulă cuantică liberă este descrisă de o undă de Broglie monocromatică plană. Aceasta corespunde unei densități de probabilitate independentă de timp pentru detectarea unei particule într-un punct dat din spațiu.
se dovedește a fi obișnuit pentru particulele nonrelativiste. În consecință, energia unei particule libere poate lua orice valoare (de la numărul de undă k poate lua orice valoare pozitivă), adică spectrul său de energie este continuu. Astfel, o particulă cuantică liberă este descrisă de o undă de Broglie monocromatică plană. Aceasta corespunde unei densități de probabilitate independentă de timp pentru detectarea unei particule într-un punct dat din spațiu.
Descriere mecanică cuantică a unei particule într-un puț de potențial dreptunghiular infinit de adâncime.
Să efectuăm o analiză calitativă a soluțiilor ecuației Schrödinger, așa cum sunt aplicate unei particule dintr-un „puț de potențial” dreptunghiular unidimensional cu „pereți” infinit de înalți. O astfel de „groapă” este descrisă de o energie potențială a formei (pentru simplitate, presupunem că particula se mișcă de-a lungul axei X) 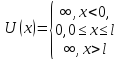 Unde l- lățimea „gropii”, iar energia se măsoară din fundul acesteia.
Unde l- lățimea „gropii”, iar energia se măsoară din fundul acesteia.
Ecuația Schrödinger pentru stările staționare în cazul unei probleme unidimensionale poate fi scrisă ca 
![]() . La limitele „gropii” (pentru x = 0 și x = l) trebuie să dispară și funcția de undă continuă. Prin urmare, condițiile la limită în acest caz au forma
. La limitele „gropii” (pentru x = 0 și x = l) trebuie să dispară și funcția de undă continuă. Prin urmare, condițiile la limită în acest caz au forma ![]()
Soluția generală a ecuației diferențiale: Deoarece ![]() . Apoi
. Apoi ![]() Condiție
Condiție ![]() efectuat numai atunci când P- numere întregi, adică este necesar ca . Rezultă că
efectuat numai atunci când P- numere întregi, adică este necesar ca . Rezultă că ![]() adică, ecuația staționară Schrödinger care descrie mișcarea unei particule într-un „puț de potențial” cu „pereți” infinit înalți este satisfăcută numai pentru valorile proprii ,
„în funcție de un număr întreg P.În consecință, energia £n a unei particule dintr-un „puț de potențial” cu „pereți” infinit de înalți ia doar anumite valori discrete, adică cuantizate. Valori energetice cuantizate
numit niveluri de energie, si numarul P, care determină nivelurile de energie ale unei particule se numește număr cuantic principal. Astfel, o microparticulă într-un „puț de potențial” cu „pereți” infinit de înalți poate fi doar la un anumit nivel de energie £n sau, după cum se spune, particula este într-o stare cuantică. P.
adică, ecuația staționară Schrödinger care descrie mișcarea unei particule într-un „puț de potențial” cu „pereți” infinit înalți este satisfăcută numai pentru valorile proprii ,
„în funcție de un număr întreg P.În consecință, energia £n a unei particule dintr-un „puț de potențial” cu „pereți” infinit de înalți ia doar anumite valori discrete, adică cuantizate. Valori energetice cuantizate
numit niveluri de energie, si numarul P, care determină nivelurile de energie ale unei particule se numește număr cuantic principal. Astfel, o microparticulă într-un „puț de potențial” cu „pereți” infinit de înalți poate fi doar la un anumit nivel de energie £n sau, după cum se spune, particula este într-o stare cuantică. P.
Pirometria optică este un set de metode optice (fără contact) pentru măsurarea temperaturii. Se folosește de legile Radiație termala.
Proprietățile cuantice ale radiației electromagnetice
Pentru a explica distribuția energiei în spectrul radiațiilor termice, Planck a presupus că undele electromagnetice sunt emise în porțiuni (cuante). Einstein în 1905 a ajuns la concluzia că radiația nu este doar emisă, ci și propagată și absorbită sub formă de cuante. Această concluzie a făcut posibilă explicarea tuturor faptelor experimentale (efect fotoelectric, efect Compton etc.) care nu au putut fi explicate prin electrodinamica clasică, care a pornit de la ideile ondulatorii despre proprietățile radiației.
Astfel, propagarea luminii ar trebui considerată nu ca un proces continuu de undă, ci ca un flux de particule discrete localizate în spațiu, care se deplasează cu o viteză. Cu propagarea luminii în vid. Ulterior (în 1926) aceste particule au fost numite fotoni. Fotonii au toate proprietățile unei particule (corpuscul).
1. Energia fotonului
e=hv= , (1)
Unde h = 6,6×10-34 J × s- constanta lui Planck, = h/2p= 1.055×10-34 J × s de asemenea constanta lui Planck , w = 2pv- frecventa circulara.
În mecanică, există o mărime având dimensiunea „energie×timp”, care se numește acțiune. Prin urmare, constanta lui Planck este uneori numită cuantumul acțiunii. Dimensiunea , coincide, de exemplu, cu dimensiunea momentului unghiular ( L = rmv).
După cum rezultă din (1), energia fotonului crește odată cu creșterea frecvenței (sau cu descreșterea lungimii de undă) și, de exemplu, un foton de lumină violetă ( l = 0.38 micron) are mai multă energie decât un foton de lumină roșie ( l = 0,77 um).
2. Masa fotonului.
Un foton este o particulă fără masă, adică pentru el
3. Momentul unui foton.
Pentru orice particulă relativistă, energia sa ![]() De când fotonul m= 0, apoi impulsul fotonului
De când fotonul m= 0, apoi impulsul fotonului
acestea. lungimea de undă este invers proporțională cu impulsul.
Pagina 3
Prin emiterea unui foton, electronul își pierde o parte din energie, care este transportată de lumină. În acest caz, masa corpului, conform formulei Einstein, scade. Se pare că un foton este o particulă uimitoare care are propria sa energie, impuls, dar nu are propria sa masă. După cum spun fizicienii, este o particulă fără masă (m=0).
Datorită lui Einstein, fotonul a stat în linie cu alții particule elementare, doar ca spre deosebire de ei, nu are masa si este „condamnat” sa zboare mereu cu viteza luminii.
3. Dezvoltarea unui algoritm de rezolvare a problemei
Energia unui foton poate fi exprimată în termeni de lungime de undă:
Când un foton interacționează „unu la unu” cu un electron, electronul preia toată energia fotonului, care din acel moment nu mai există. În acest caz, se spune că electronul a absorbit fotonul.
Energia unui foton după o coliziune cu un electron liber în repaus poate fi exprimată în termeni de lungime de undă
din (1) urmează , de unde  .
.
Pe baza acestei formule, după efectuarea calculelor, obținem valoarea energie fotonică împrăștiată
![]()
este impulsul fotonului incident
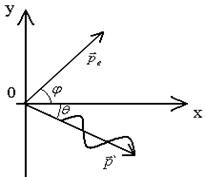 este impulsul fotonului împrăștiat
este impulsul fotonului împrăștiat
este impulsul electronului de recul.
Din legea conservării impulsului rezultă:
Oi: ![]() ;
; ![]() ;
;
Împărțind a doua expresie la prima, obținem:
![]() ;
; 
este impulsul fotonului incident,
este impulsul fotonului împrăștiat.
, ![]()

Cosinusul unghiului de împrăștiere este determinat folosind formula Compton.
5. Lista de programe
const n=1,6E-13; (1 MeV=1,6*10 până la -13 J)
nm=1E-9; (1 nanometru = 10 până la -9 metri)
var E,dl,c,h,e0,Temp:real;
(E - energia fotonului, dl - lungimea de undă, Temp - variabilă timp)
(c - viteza luminii, h - constanta lui Planck, e0 - energia de repaus a electronilor)
lc,E1,f,Ek:real;
(E1 este energia fotonului împrăștiat, f este unghiul de emisie de electroni
Ek - energia cinetică a unui foton, lc - lungimea de undă în vid)
cod:car; (cod cheie)
clrscr; (ecran curat)
textcolor(2); (setează culoarea caracterului)
gotoxy(33,9); (deplasați la poziția cu coordonatele 33.9)
Writeln("LUCRARE DE CURS "); (afișează mesajul pe ecran)
Writeln("Calculul energiei fotonilor împrăștiați,");
Writeln(„unghiul de plecare a electronului de recul”);
Writeln ("și energie kinetică electron de recul");
Write("Apăsați tasta pentru a continua.<ПРОБЕЛ>");
în timp ce codul<>#32 do (până când tasta cu codul 32 (SPAȚIU) este apăsată)






