1 atom yadrosi uning tarkibi. Atom yadrosi. Elektr to'rt kutupli moment
Klaster parchalanishi
Atom yadrosi- atomning asosiy massasi to'plangan markaziy qismi (99,9% dan ortiq). Yadro musbat zaryadlangan, yadro zaryadi atom tayinlangan kimyoviy elementni aniqlaydi. Turli atomlarning yadrolarining o'lchamlari bir necha femtometrdir, bu atomning o'zidan 10 ming marta kichikdir.
Yana bitta qiziq fakt kattaroq elementlar uchun neytronlarning protonlarga nisbati odatda 5 ga teng, lekin undan yuqori emas. Bu shuni ko'rsatadiki, agar ularning protonlari va neytronlari zanjir bo'ylab teng taqsimlangan bo'lsa, u holda bir juft proton o'rtasida bir yoki ikkita neytron bo'lar edi, lekin hech qachon ketma-ket uchta neytron bo'lmaydi.
Ikki va uchta neytronlar protonlar orasiga o'ralgan holda shunday ko'rinadi. Ko'rinib turibdiki, ikkita neytron mavjud bo'lganda, protonlar o'zlarining tashqi manfiy zaryadlariga qo'shilib, ularni barqaror ushlab turadiganga o'xshaydi. Uchta neytron bo'lsa, o'rtacha neytronni ta'minlash qiyin, shuningdek, bir-biriga yaqin bo'lgan ko'p miqdordagi manfiy zaryadlar mavjud. Shuning uchun uchta neytron bilan vaziyat barqaror bo'lishi dargumon.
Ma'lum miqdordagi proton va neytronlarga ega bo'lgan zarralar sinfi sifatida qaraladigan atom yadrosi odatda deyiladi. nuklid.
Yadrodagi protonlar soni uning zaryad raqami deb ataladi - bu raqam davriy jadvaldagi atom tegishli bo'lgan elementning tartib raqamiga teng. Yadrodagi protonlar soni neytral atomning elektron qobig'ining tuzilishini va shuning uchun tegishli elementning kimyoviy xususiyatlarini aniqlaydi. Yadrodagi neytronlar soni uning deyiladi izotopik raqam. Protonlar soni bir xil va neytronlari har xil bo'lgan yadrolar izotoplar deyiladi. Neytronlar soni bir xil, lekin protonlari har xil bo'lgan yadrolar izotonlar deyiladi. Izotop va izoton atamalari ko'rsatilgan yadrolarni o'z ichiga olgan atomlarga nisbatan, shuningdek, bitta kimyoviy elementning kimyoviy bo'lmagan navlarini tavsiflash uchun ham qo'llaniladi. Yadrodagi nuklonlarning umumiy soni uning massa soni () deb ataladi va davriy jadvalda ko'rsatilgan atomning o'rtacha massasiga taxminan tengdir. Xuddi shunday nuklidlar massa raqami, lekin har xil proton-neytron kompozitsiyalari izobarlar deb ataladi.
Barqaror izotoplarning hosil bo'lishini ma'lum qoidalar boshqaradiganga o'xshaydi.
- Protonni zanjirning oxiridagi boshqa protonga to'g'ridan-to'g'ri bog'lab bo'lmaydi.
- Neytron zanjirning oxirida bo'la olmaydi.
- Ketma-ketlikda ikkitadan ortiq neytron bo'lishi mumkin emas.
- Katta buyumlar talab qilinadi ko'proq neytronlar va qoidaga rioya qiling.
Har qanday kvant tizimi singari, yadrolar ham metastabil qo'zg'aluvchan holatda bo'lishi mumkin va ba'zi hollarda bunday holatning umri yillar bilan hisoblanadi. Yadrolarning bunday qo'zg'aluvchan holatlari yadro izomerlari deyiladi.
Qisqacha kashfiyot tarixi
Zaryadlangan zarrachalarning tarqalishini bir nuqtada to'plangan va qarama-qarshi elektrning bir xil sferik taqsimoti bilan o'ralgan markaziy elektr zaryadidan tashkil topgan atomni faraz qilish bilan izohlash mumkin. teng o'lchamda. Atomning bunday tuzilishi bilan a- va b-zarralar, ular orqali o'tayotganda yaqin masofa atom markazidan katta og'ishlarni boshdan kechiradi, garchi bunday og'ish ehtimoli kichik bo'lsa ham.
Yadro kuchlarining xossalari, ularning tavsifi va kelib chiqishi
Vodorod-3 2-qoidani buzadi, chunki u asosan barqaror. Bu barqarorlik mumkin, chunki geliy-3 ning proton kengayishi elektron uchun etarli. 1-qoidaga kelsak, bu zanjirga emas, faqat zanjirning oxiridagi protonlarga taalluqlidir, chunki bir juft proton atrofdagi neytronlar bilan himoyalanishi mumkin.
3-qoidaga qo'shimcha ravishda, ketma-ketlikdagi bu ikki neytron zanjirning oxiriga yaqin bo'lmasligi kerak, chunki ularni ushlab turish uchun protonlarning protonlari etarli emas. Ya'ni, ketma-ket neytronlar zanjirga o'rnatilishi kerak. Bu nima uchun kichikroq elementlarning ketma-ket neytronlarga ega bo'lishiga yo'l qo'yilmasligini ko'rsatadi, chunki ularning zanjiri etarlicha uzun emas.
Shunday qilib, Rezerford atom yadrosini kashf etdi, shu paytdan boshlab yadro fizikasi atom yadrolarining tuzilishi va xususiyatlarini o'rgana boshladi.
Elementlarning barqaror izotoplari kashf etilgandan so'ng, eng engil atomning yadrosiga barcha yadrolarning strukturaviy zarrasi roli berildi. 1920 yildan beri vodorod atomining yadrosi rasmiy atama - protonga ega. Ko'pgina aniq kamchiliklarga ega bo'lgan yadro tuzilishining oraliq proton-elektron nazariyasi, birinchi navbatda, yadrolarning spinlari va magnit momentlarini o'lchashning eksperimental natijalariga zid bo'lganidan so'ng, 1932 yilda Jeyms Chedvik yangi elektr neytral zarrachani kashf etdi. , neytron deb ataladi. Xuddi shu yili Ivanenko va mustaqil ravishda Geyzenberg yadroning proton-neytron tuzilishi haqida gipotezani ilgari surdilar. Ushbu gipoteza yadro fizikasining keyingi rivojlanishi va uning qo'llanilishi bilan to'liq tasdiqlandi.
Oldingi kuzatishlar barcha izotoplarni to'liq tushuntirib bera olmaydi. Masalan, geliy-8 geliy-7 dan, litiy-11 esa litiydan barqarorroq. Ikkala holatda ham kattaroq izotop ko'proq neytronlarga ega va biz kamroq barqarorlikni kutamiz. Litiy holatida qiziqarli tadqiqot shuni ko'rsatdiki, litiy-11 va litiy-12 yadrolari litiydan ancha katta. Qo'shimcha neytronlar zanjirning qolgan qismidan qandaydir tarzda ajralib turishi va ma'lum masofada suzib yurishi mumkin. Masalan, litiy-11 litiy-9 va bir oz masofada joylashgan ikkita neytrondan tayyorlanishi mumkin.
Yadro fizikasi
Birinchi marta atom yadrolarining zaryadlarini Genri Mozili 1913 yilda aniqlagan. Ularning eksperimental kuzatishlar olim rentgen to'lqin uzunligining elementdan elementga o'zgarib turadigan va vodorod uchun bittaga teng bo'lgan ma'lum bir konstantaga bog'liqligini izohladi:
Bu qanday sodir bo'lishi aniq emas. nazariyalar atom modellari: Jon Dalton Materiya bo'linmas atomlardan iborat, ular buzilmaydi. Berilgan elementning barcha atomlari fizik va kimyoviy xossalarida bir xil. Turli elementlarning atomlari fizik va jihatidan farqlanadi kimyoviy xossalari. Turli elementlarning atomlari butun sonlar orasidagi oddiy nisbatlarga birlashtiriladi va molekulalarni hosil qiladi. kimyoviy reaksiyalar atomlarni ajratish yoki qayta joylashtirish birikmasidan iborat. Cheklovlar: U atomlarning nima uchun va qanday qilib murakkab atomlarni hosil qilish uchun birlashishini tushuntira olmadi. Murakkablar atomlarida atomlarni tutib turuvchi kuchlarning tabiati. Nima uchun atomlar erkin holatda bo'lolmaydi va nima uchun birikmalar atomlari erkin mavjud bo'lishi mumkin. Shokoladli muzqaymoq keyinchalik noto'g'ri bo'lib chiqdi. Cheklovlar: U Ruterford tajribasi bilan izohlangan sochilish tajribasining natijasini tushuntira olmadi. Uning qo'llab-quvvatlashida eksperimental dalillar yo'q edi. Shu asosda termion nurlanish, fotoelektrik nurlanish va ionlanish tushuntirildi. Bu folga atomlari tomonidan a-zarrachalarning tarqalishi bilan bog'liq. Atomning barqarorligiga kelsak, yadro atrofida aylanadigan elektronlar markazga yo'naltirilgan tezlanishga ega. Elektrodinamikaga ko'ra, tezlashtirilgan zaryadlangan zarralar energiyani elektromagnit to'lqinlar shaklida chiqaradi. Shuning uchun elektromagnit to'lqinlar doimiy ravishda aylanadigan elektronlar tomonidan chiqarilishi kerak. Elektron energiyasining bunday uzluksiz yo'qolishi tufayli ularning orbitalarining radiuslari doimiy ravishda kamayishi va oxir-oqibat elektron yadroga tushishi kerak. Shunday qilib, atom barqaror qola olmaydi. Ruterford modeli ham chiziq spektrini tushuntirib bermadi. Rezerford Niels modelining kamchiliklari Devid Bor atom modeli nazariyalari: Bor nazariyasi Ruxsat etilgan aylana orbitalari: Elektronlar yadro atrofida konsentrik aylana orbitalarda harakatlanadi. Barqaror orbitalarda aylanayotganda, elektronlar orbita markaziga qarab tezlashishiga qaramay, energiya chiqarmaydi. Ruxsat etilgan orbitalarning har biri statsionar energiya deb ataladigan ma'lum miqdordagi energiya bilan bog'liq. Elektronning bir energiya darajasidan ikkinchisiga sakrashi. Zeeman va Stark effekti uchun hech qanday izoh yo'q: elektr va magnit maydonlarning ta'siri spektral atomlar. Atomga magnit maydon qo'llanilganda uning keng tarqalgan spektral chiziqlari bo'linadi. Ushbu ta'sir Zeeman effekti sifatida tanilgan. Spektral chiziqlar elektr maydoni mavjudligida ham bo'linadi. Ushbu effekt Stark effekti deb nomlanadi. Atomlarning tasnifi: Izomerlar molekulyar formulalari bir xil, ammo kimyoviy tuzilmalari har xil bo‘lgan molekulalardir. Bu qoida kattaroq yadrolar uchun aniqroq. Tabiiy elementlarning barcha ma'lum izotoplari uchun faqat 250 tasi barqaror . Bu barqaror izotoplarning barchasi mavjud atom raqami 1 va orasida. Yadroning massasi uni tashkil etuvchi barcha proton va neytronlarning massasidan kichik bo'ladi. Farq massa nuqsoni deb ataladi, agar yadro vayron bo'lsa, energiyaga aylanadi. Nuklonlarni tutib turuvchi energiya miqdori bog’lanish energiyasi deyiladi. Bu energiya miqdori barqaror bo'lmagan yadrolarga qaraganda barqaror yadrolar uchun yuqori. Atom massasi va energiya birliklari. Elektronlarning orbitallarda joylashishi.
- Har bir materiya elementlar deb ataladigan asosiy ob'ektlardan iborat.
- Yadro proton va neytronlardan iborat bo'lib, ular nuklonlar deb ataladi.
- Atom massasining katta qismi yadroga tegishli.
Va - doimiy.
Bundan Mozeli o'z tajribalarida topilgan, xarakterli rentgen nurlanishining to'lqin uzunligini aniqlaydigan va elementning seriya raqamiga to'g'ri keladigan atom konstantasi faqat zaryad bo'lishi mumkin degan xulosaga keldi. atom yadrosi nomi bilan tanilgan Moseley qonuni .
Og'irligi
Neytronlar sonining farqi tufayli elementning izotoplari har xil massaga ega, bu yadroning muhim xarakteristikasi hisoblanadi. DA yadro fizikasi yadrolarning massasi odatda atom massa birliklarida o'lchanadi ( a. yemoq.), biri uchun a. e. m. 12 C nuklid massasining 1/12 qismini oling. Shuni ta'kidlash kerakki, odatda nuklid uchun berilgan standart massa neytral atomning massasi hisoblanadi. Yadroning massasini aniqlash uchun atom massasidan barcha elektronlar massalarining yig'indisini ayirish kerak (agar biz elektronlarning yadro bilan bog'lanish energiyasini ham hisobga olsak, aniqroq qiymat olinadi) .
Ammo atomlarda elektronlar o'sha erda, yadrodagi protonlar yonida. Nega elektronlar yadro ichiga yashirinib, protonlarga yopishmaydi? Elektronlar yadroga tushishi kerak. To'rtinchi sinfda o'tirgan har bir kishi biladiki, siz balonni sochingiz yoki kozokingizga surtsangiz, uni devorga yopishtirishingiz mumkin. Buni qilishingiz mumkin, chunki ishqalanish balonda juda ko'p elektron to'planishiga olib keldi. Elektronlar protonlarga tortiladi va boshqa elektronlar tomonidan qaytariladi, shuning uchun shar devorga yaqin surilganda devordagi elektronlar shoshilib ichkariga kirib, ochiq protonlarni qoldiradi.
Bundan tashqari, massaning energiya ekvivalenti ko'pincha yadro fizikasida qo'llaniladi. Eynshteyn munosabatlariga ko'ra, har bir massa qiymati mos keladi umumiy energiya:
, bu erda yorug'likning vakuumdagi tezligi.a orasidagi nisbat. e.m va uning jouldagi energiya ekvivalenti:
Bu yarim yalang'och protonlar shardagi elektronlar uchun chidab bo'lmas edi va elektronlar protonlar tomon yugurib, sharni o'zlari bilan olib ketishdi. Savol shundaki, nima uchun bu elektronlar birinchi navbatda sizning sochingizdan sharga o'tdi? Agar ular protonlarni hayratda qoldirganlarida edi, ular sochlaringizda juda ko'p bo'lar edi. Juftning zaryadsiz atomlari elektronlar va protonlar soniga teng. Elektronlar atom yadrosiga yaqinlashishi kerak.
Klassik fizikada elektronlar proton zaryadi bilan tortilmasa ham, yadroga tushishi kerak. Atomlarning dastlabki modellarida xuddi sayyora quyosh atrofida aylanayotgani kabi, yadro atrofida elektronlar aylanardi. Aylana bo'ylab aylanish juda ko'p yo'nalish o'zgarishini yaratishni anglatadi, bu tezlashtirishni anglatadi. Qachon elektr zaryadi tezlashuvga duchor bo'lib, u elektromagnit nurlanish chiqaradi. Elektromagnit nurlanish energiya bo'lib, elektron ikki turdagi energiyadan birini yo'qotishi mumkin: kinetik energiya yoki potentsial energiya.
Radius
Og'ir yadrolarning parchalanishini tahlil qilish Ruterfordning taxminini aniqladi va yadro radiusini massa soniga oddiy munosabat bilan bog'ladi:
,konstanta qayerda.
Yadro radiusi sof geometrik xarakteristika emasligi va birinchi navbatda yadro kuchlarining ta'sir radiusi bilan bog'liq bo'lganligi sababli, qiymat tahlil qilish jarayonida qiymat olingan jarayonga bog'liq, o'rtacha qiymat m, shuning uchun radius. yadroning metrda:
Qanday bo'lmasin, u yadroga qulab tushadi. Kinetik va potensial energiya yechimi. Keling, kosmosda suzuvchi bitta elektronni ko'rib chiqaylik. Uning kinetik va potentsial energiyasini qanday o'lchaymiz? Bir protonni uzoqda tasavvur qilishdan boshlang. Ular birgalikda birlashib, vodorod atomini hosil qilishlari mumkin. Ularning bir-biriga bo'lgan taraqqiyotini energiya nuqtai nazaridan o'lchaganimizda, biz klassik fizikada ko'rgan narsalarning ko'pini ko'ramiz.
Protonga yaqinlashayotgan elektron kinetik va potentsial energiyaga ega bo'ladi. Uzoqda bo'lsa, u nisbatan katta miqdorga ega bo'ladi potentsial energiya, xuddi yerdan baland ko'tarilgan jismlar juda katta miqdordagi potentsial energiyaga ega. Proton tomon harakatlanar ekan, u potentsial energiyaning bir qismini yo'qotadi. Ulardan ba'zilari elektromagnit energiya sifatida tarqaladi. Ulardan ba'zilari kinetik energiyaga aylanadi. Kinetik energiya elektronning sakrashini ushlab turadi va uning yadroda qolishi va proton bilan birlashishiga yo'l qo'ymaydi.
Yadro lahzalari
Uni tashkil etuvchi nuklonlar singari, yadroning ham o'z momentlari bor.
Spin
Nuklonlarning o'z mexanik momenti yoki spini ga teng bo'lganligi sababli, yadrolar ham mexanik momentlarga ega bo'lishi kerak. Bundan tashqari, nuklonlar yadroda orbital harakatda ishtirok etadilar, bu ham har bir nuklonning ma'lum bir burchak impulsi bilan tavsiflanadi. Orbital momentlar faqat butun son qiymatlarni oladi (Dirak doimiysi). Nuklonlarning barcha mexanik momentlari, spinlari ham, orbitallari ham algebraik tarzda yig'iladi va yadro spinini tashkil qiladi.
Bu erda, pastki protonlar bilan birlashtirilmagan elektronlar foydasiga bir oz buklangan. Agar elektron yadroda bo'lsa, kinetik energiya cheksizdir. Potensial energiya, agar elektron yadroda bo'lsa, manfiy cheksizlikdir. agar siz istalgan nuqtada kinetik energiyani hisoblamoqchi bo'lsangiz, bu potentsial energiyaning yarmi. Boshqacha qilib aytganda, kinetik energiya ko'proq og'irlikka ega va elektron yadrodan tashqarida qoladi.
Elektronlarni materiyaning katta qismi atrofida aylanadigan kichik materiya bo'laklari deb hisoblash muammosi mavjud. Aslida, ular o'zlarini bunday tutmaydilar. Elektronni sayyora deb hisoblash mumkin emas va buning o'rniga bir xil ehtimollik buluti sifatida qarash kerak. Va bu bu haqda o'ylashning eng foydali usuli degan ma'noda emas - elektron haqiqatan ham shunday. Elektronning xatti-harakatini tushunish uchun biz bu bulut qayerda yoki qayerda eng zich bo'lishi haqida o'ylashimiz kerak katta ehtimol bilan elektron yoki maksimal manfiy zaryad bo'lgan joyda.
Yadrodagi nuklonlar soni juda ko'p bo'lishi mumkinligiga qaramasdan, yadrolarning spinlari odatda kichik bo'lib, bir nechtadan ko'p bo'lmaydi, bu bir xil nomdagi nuklonlarning o'zaro ta'sirining o'ziga xosligi bilan izohlanadi. Barcha juftlashgan protonlar va neytronlar faqat spinlari bir-birini bekor qiladigan tarzda o'zaro ta'sir qiladi, ya'ni juftlar doimo antiparallel spinlar bilan o'zaro ta'sir qiladi. Juftlikning umumiy orbital momentumi ham har doim nolga teng. Natijada, juft sonli proton va juft sonli neytronlardan tashkil topgan yadrolar mexanik impulsga ega emas. Nolga teng bo'lmagan spinlar faqat tarkibida juftlanmagan nuklonlarga ega bo'lgan yadrolar uchun mavjud bo'lib, bunday nuklonning spini o'z orbital impulsiga qo'shiladi va qandaydir yarim butun qiymatga ega: 1/2, 3/2, 5/2. Toq-toq tarkibli yadrolar butun spinga ega: 1, 2, 3 va boshqalar.
atom yadrolarining bo'linishi
Keling, proton-vodorod yadrosiga bo'lgan sayohatni yana bir bor ko'rib chiqaylik, agar siz fazoning har bir kichik hajmini ehtimollik o'lchagich bilan o'lchasangiz, buni qilgan bo'lar edingiz. Yadrodan uzoqda, ehtimollik o'lchagich manfiy zaryad ehtimolini deyarli qayd etmaydi. Sekin-asta yaqinlashganda, hisoblagich yuqoriga va yuqoriga ko'tarilib, u yadrodagi eng yuqori ehtimollikni qayd etadi. Bu biz yuqorida tushungan narsaga va haqiqatga zid ko'rinadi.
Bu erda hiyla-nayrang, yadrodan ma'lum masofada joylashgan chiziqda kichik bo'sh joy emasligini tushunishdir eng yaxshi yo'l elektronning har qanday ma'lum hajmdagi fazoda bo'lish ehtimolini o'lchash. Elektron yadroning tepasida, pastida, chap yoki o'ng tomonida bo'ladimi, bizni qiziqtirmaydi. Biz faqat bir oz masofada bo'lishini xohlaymiz. Bu shuni anglatadiki, u yadro atrofidagi sharsimon "qobiq" ning istalgan joyida bo'lishi mumkin. Biz xohlagan narsa - bu qobiqning hajmi.
Magnit moment
Spin o'lchovlari to'g'ridan-to'g'ri bog'liq bo'lgan magnit momentlar mavjudligi tufayli mumkin bo'ldi. Ular magnetonlarda o'lchanadi va turli yadrolar uchun ular -2 dan +5 gacha yadro magnetonlari. Nuklonlarning nisbatan katta massasi tufayli yadrolarning magnit momentlari elektronlarnikiga nisbatan juda kichik, shuning uchun ularni o'lchash ancha qiyin. Spinlar singari, magnit momentlar spektroskopik usullar bilan o'lchanadi, eng aniqi yadro magnit-rezonans usulidir.
Spin kabi juft-juft juftlarning magnit momenti nolga teng. Juftlanmagan nuklonli yadrolarning magnit momentlari bu nuklonlarning ichki momentlari va juftlanmagan protonning orbital harakati bilan bog'liq bo'lgan moment orqali hosil bo'ladi.
Elektr to'rt kutupli moment
Spin birlikdan katta yoki teng bo'lgan atom yadrolari nolga teng bo'lmagan to'rt kutupli momentlarga ega bo'lib, ular aniq sharsimon emasligini ko'rsatadi. Agar yadro spin o'qi bo'ylab cho'zilgan bo'lsa (fusiform tana) to'rt kutupli moment plyus belgisiga ega, agar yadro spin o'qiga perpendikulyar tekislikda cho'zilgan bo'lsa (lentikulyar jism). Ijobiy va manfiy kvadrupol momentli yadrolar ma'lum. Nolga teng bo'lmagan to'rt kutupli momentga ega yadro tomonidan yaratilgan elektr maydonida sferik simmetriyaning yo'qligi atom elektronlarining qo'shimcha energiya darajalarining shakllanishiga va atomlar spektrlarida o'ta nozik tuzilish chiziqlarining paydo bo'lishiga olib keladi, ularning orasidagi masofalar to'rt kutupli momentga bog'liq. .
Bog'lanish energiyasi
Asosiy barqarorlik
Massa soni 50-60 dan katta yoki undan kam bo'lgan nuklidlar uchun o'rtacha bog'lanish energiyasining kamayishidan kelib chiqadiki, kichik yadrolarga ega bo'lgan yadrolar uchun termoyadroviy sintez energetik jihatdan qulay bo'lib, massa sonining ko'payishiga olib keladi. va katta bo'lgan yadrolar uchun - bo'linish jarayoni. Hozirgi vaqtda energiya chiqishiga olib keladigan bu ikkala jarayon ham amalga oshirildi, ikkinchisi zamonaviy atom energiyasining asosi bo'lib, birinchisi ishlab chiqilmoqda.
Batafsil tadqiqotlar shuni ko'rsatdiki, yadrolarning barqarorligi ham sezilarli darajada parametrga - neytronlar va protonlar sonining nisbatiga bog'liq. O'rtacha, eng barqaror yadrolar uchun, shuning uchun engil nuklidlarning yadrolari eng barqaror bo'ladi va massa soni ortishi bilan protonlar orasidagi elektrostatik itarilish tobora sezilarli bo'ladi va barqarorlik mintaqasi () tomon siljiydi. izohli rasmga qarang).
Tabiatda uchraydigan barqaror nuklidlar jadvalini ko'rib chiqsak, ularning juft va toq qiymatlari bo'yicha taqsimlanishiga e'tibor qaratishimiz mumkin. Bu miqdorlarning teng qiymatlariga ega bo'lgan barcha yadrolar engil nuklidlarning yadrolari , , , . Toq A bo'lgan izobarlar orasida, qoida tariqasida, faqat bittasi barqaror. Juft bo'lgan taqdirda, ko'pincha ikki, uch yoki undan ko'p barqaror izobarlar mavjud, shuning uchun juft-juftlar eng barqaror, eng kami - toq-toq. Bu hodisa neytronlar ham, protonlar ham antiparallel juftlikda to'planishga moyilligini ko'rsatadi.
20-asrning 20-yillariga kelib fiziklar 1911-yilda E.Rezerford tomonidan kashf etilgan atom yadrolari hamda atomlarning oʻzlari murakkab tuzilishga ega ekanligiga shubha qilmay qoʻydilar. Ular bunga o'sha paytda to'plangan ko'plab eksperimental faktlar bilan amin bo'lishdi: radioaktivlikning kashf etilishi, yadroning yadro modelining eksperimental isboti, elektron, a-zarracha va boshqalar uchun e / m nisbatini o'lchash. H-zarracha deb ataladigan - vodorod atomining yadrosi, sun'iy radioaktivlikning kashf etilishi va yadro reaksiyalari, atom yadrolarining zaryadlarini o'lchash va hokazo. Hozirda bu qat'iy tasdiqlangan bu atom yadrolari turli elementlar Ular ikkita zarracha, proton va neytrondan iborat.
Bu zarralarning birinchisi vodorod atomi bo'lib, undan bitta elektron chiqarilgan. Bu zarracha J. Tomson (1907) tajribalarida allaqachon kuzatilgan, u undagi e / m nisbatini o'lchashga muvaffaq bo'lgan. 1919-yilda E.Rezerford koʻpgina elementlar atomlari yadrolarining boʻlinish mahsulotida vodorod atomining yadrolarini topdi. Rezerford bu zarrachani proton deb atadi. U protonlar barcha atom yadrolarining bir qismi ekanligini taklif qildi. Ruterford tajribalarining sxemasi shaklda ko'rsatilgan. o'n bir.
Rezerford qurilmasi evakuatsiya qilingan kameradan iborat bo'lib, uning ichiga a-zarrachalar manbai bo'lgan K idish qo'yilgan. Kamera oynasi metall folga F bilan qoplangan bo'lib, uning qalinligi a-zarralar u orqali o'tmasligi uchun tanlangan. Deraza tashqarisida sink sulfid bilan qoplangan E ekrani bor edi. M mikroskop yordamida og'ir zaryadlangan zarrachalar ekranga urilgan nuqtalarda ssintilatsiyani kuzatish mumkin edi. Kamera past bosimda azot bilan to'ldirilganda, ekranda yorug'lik miltillashlari paydo bo'ldi, bu F folga orqali o'tishga qodir bo'lgan ba'zi zarrachalar oqimining ko'rinishini ko'rsatib, a-zarrachalar oqimini deyarli butunlay to'sib qo'ydi.
Rezerford E ekranini kamera oynasidan uzoqlashtirgan holda o'lchadi erkin yo'l degan ma'noni anglatadi havodagi zarralar kuzatildi. Taxminan 28 sm ga teng bo'lib chiqdi, bu J. Tomson tomonidan ilgari kuzatilgan H-zarrachalarining yo'l uzunligini baholashga to'g'ri keldi. Elektr va magnit maydonlarining azot yadrolaridan chiqib ketgan zarrachalarga ta'sirini o'rganish shuni ko'rsatdiki, bu zarralar ijobiy elementar zaryadga ega va ularning massasi vodorod atomi yadrosi massasiga teng. Keyinchalik, bir qator boshqa gazsimon moddalar bilan tajriba o'tkazildi. Barcha holatlarda a-zarralar H-zarrachalarni yoki bu moddalar yadrolaridan protonlarni chiqarib yuborishi aniqlandi. Zamonaviy o'lchovlarga ko'ra, musbat zaryad proton elementar zaryadga to'liq teng e = 1,60217733 10 –19 C, ya'ni moduli bo'yicha teng. manfiy zaryad elektron. Hozirgi vaqtda proton va elektron zaryadlarining tengligi 10-22 aniqlik bilan tasdiqlangan. Ikki o'xshash bo'lmagan zarrachalar zaryadlarining bunday mos kelishi hayratlanarli va zamonaviy fizikaning asosiy sirlaridan biri bo'lib qolmoqda.
11-rasm. Yadro parchalanish mahsulotlarida protonlarni aniqlash bo'yicha Rezerford tajribalarining sxemasi. K - a-zarrachalarning radioaktiv manbai bo'lgan qo'rg'oshin idishi, F - metall folga, E - rux sulfid bilan qoplangan ekran, M - mikroskop.
proton massasi, zamonaviy o'lchovlarga ko'ra, mp = 1,67262 10 -27 kg ga teng. Yadro fizikasida zarrachaning massasi koʻpincha massa soni 12:1 a.u boʻlgan uglerod atomi massasining 1/12 qismiga teng atom massa birliklarida (a.m.u.) ifodalanadi. e.m = 1,66057 10 -27 kg.
Shuning uchun, m p \u003d 1.007276 a. e. m. Ko'p hollarda zarrachaning massasini E = mc 2 formulasiga muvofiq ekvivalent energiya qiymatlarida ifodalash qulay. 1 eV = 1,60218 10 -19 J bo'lgani uchun energiya birliklarida proton massasi 938,272331 MeV ga teng. Shunday qilib, Rezerford tajribasida tez a-zarrachalar ta'sirida azot va boshqa elementlar yadrolarining bo'linish hodisasi aniqlandi va protonlar atomlar yadrolarining bir qismi ekanligi ko'rsatildi. Proton kashf etilgandan so'ng, atomlarning yadrolari faqat protonlardan iborat degan fikr paydo bo'ldi. Biroq, bu taxmin asossiz bo'lib chiqdi, chunki yadro zaryadining uning massasiga nisbati turli yadrolar uchun doimiy bo'lib qolmaydi, chunki yadrolar tarkibiga faqat protonlar kiritilganda bo'ladi. Og'irroq yadrolar uchun bu nisbat engil bo'lganlarga qaraganda kichikroq bo'lib chiqadi, ya'ni og'irroq yadrolarga o'tganda yadro massasi zaryaddan tezroq o'sadi. 1920 yilda Rezerford yadrolar tarkibida qattiq bog'langan ixcham proton-elektron juftligi mavjudligini faraz qildi, bu elektr neytral shakllanish - massasi taxminan proton massasiga teng bo'lgan zarracha. U hatto bu faraziy zarrachaning nomini ham o'ylab topdi - neytron.
Bu juda chiroyli, ammo keyinchalik ma'lum bo'lishicha, noto'g'ri fikr edi. Elektron yadroning bir qismi bo'lishi mumkin emas. Noaniqlik munosabatiga asoslangan kvant-mexanik hisoblash shuni ko'rsatadiki, yadroda lokalizatsiya qilingan elektron, ya'ni o'lchami R ≈ 10-13 sm bo'lgan hududda ulkan bo'lishi kerak. kinetik energiya dan kattaroq bo'lgan ko'plab buyurtmalar yadroviy bog'lanish energiyasi zarracha uchun. Og'ir neytral zarraning mavjudligi haqidagi g'oya Ruterfordga shu qadar jozibali tuyuldiki, u darhol Jeyms Chadvik boshchiligidagi bir guruh shogirdlarini shunday zarrachani qidirishga taklif qildi. 12 yil o'tgach, 1932 yilda Chadwick berilliyni a-zarrachalar bilan nurlantirganda paydo bo'ladigan nurlanishni eksperimental ravishda o'rganib chiqdi va bu nurlanish massasi taxminan protonnikiga teng bo'lgan neytral zarralar oqimi ekanligini aniqladi. Neytron aynan shunday kashf etilgan. Shaklda. 12 neytronlarni aniqlash uchun sozlashning soddalashtirilgan diagrammasini ko'rsatadi.
Beriliyni radioaktiv poloniy chiqaradigan a-zarrachalar bilan bombardimon qilganda, 10-20 sm qalinlikdagi qo'rg'oshin qatlami kabi to'siqni yengib o'ta oladigan kuchli penetratsion nurlanish paydo bo'ladi.Bu nurlanish deyarli bir vaqtning o'zida Chadvik bilan Joliot-Kyuri turmush o'rtoqlari Iren va Iren tomonidan kuzatilgan. Frederik (Iren va Per Kyurining qizi), lekin ular bu yuqori energiyali g-nurlari deb taxmin qilishgan. Ular agar berilliy nurlanish yo'liga kerosin plitasi qo'yilsa, bu nurlanishning ionlashtiruvchi kuchi keskin ortadi. Ular berilliy nurlanishi ushbu vodorod o'z ichiga olgan moddada ko'p miqdorda mavjud bo'lgan protonlarni kerosindan chiqarib tashlashini isbotladilar. Protonlarning havodagi erkin yo'liga asoslanib, ular to'qnashuvda protonlarga kerakli tezlikni berishga qodir bo'lgan g-kvantalarning energiyasini hisobladilar.
Bu juda katta bo'lib chiqdi - taxminan 50 MeV. J.Chedvik 1932-yilda berilliyning a-zarrachalar bilan nurlanishidan kelib chiqadigan nurlanish xossalarini har tomonlama oʻrganish boʻyicha bir qator tajribalar oʻtkazdi. Chadvik o'z tajribalarida ionlashtiruvchi nurlanishni o'rganish uchun turli usullardan foydalangan. Shaklda. 12-rasmda zaryadlangan zarralarni aniqlash uchun mo'ljallangan Geiger hisoblagichi ko'rsatilgan. U ichki tomondan metall qatlam (katod) bilan qoplangan shisha naychadan va trubaning (anod) o'qi bo'ylab o'tadigan ingichka ipdan iborat. Quvur past bosimda inert gaz (odatda argon) bilan to'ldiriladi. Gaz orqali uchadigan zaryadlangan zarracha molekulalarning ionlanishiga olib keladi. Ionlanish natijasida hosil bo'lgan erkin elektronlar tezlashadi elektr maydoni anod va katod o'rtasida ta'sir ionlashuvi boshlanadigan energiyaga. Ionlarning ko'chkisi paydo bo'ladi va hisoblagich orqali qisqa oqim pulsi o'tadi. Zarrachalarni o'rganish uchun yana bir muhim vosita bu bulut kamerasi bo'lib, unda tez zaryadlangan zarracha iz (iz) qoldiradi. Zarrachalar traektoriyasini bevosita kuzatish yoki suratga olish mumkin.
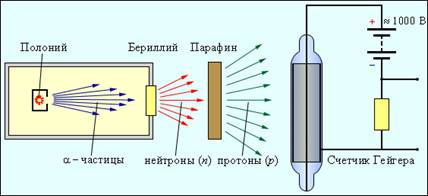
Shakl 12. Neytronlarni aniqlash uchun sozlash sxemasi.
1912 yilda yaratilgan bulutli kameraning harakati zaryadlangan zarrachaning traektoriyasi bo'ylab kameraning ish hajmida hosil bo'lgan ionlarda o'ta to'yingan bug'ning kondensatsiyasiga asoslangan. Bulutli kameradan foydalanib, elektr va zaryadlangan zarrachaning traektoriyasining egriligini kuzatish mumkin. magnit maydonlar. J.Chedvik o'z tajribalarida bulut kamerasida berilliy nurlanishi bilan to'qnashuvni boshdan kechirgan azot yadrolarining izlarini kuzatdi. Ushbu tajribalar asosida u azot yadrolariga tajribada kuzatilgan tezlikni bildirishga qodir bo'lgan g-kvant energiyasiga baho berdi. 100-150 MeV ga teng bo'lib chiqdi. Bunday ulkan energiya berilliy chiqaradigan g-kvantaga ega bo'lishi mumkin emas. Shu asosda Chedvik berilliydan a-zarralar taʼsirida massasiz g-kvantlar emas, balki ogʻir zarrachalar uchib chiqadi, degan xulosaga keldi.
Bu zarralar yuqori darajada kirib borgani va Geiger hisoblagichidagi gazni bevosita ionlashtirmagani uchun ular elektr neytral edi. Mavjudligi shu tarzda isbotlangan. neytron- Chadwick tajribalaridan 10 yil oldin Rezerford tomonidan bashorat qilingan zarralar. Neytron bu elementar zarracha. Dastlab Ruterford taklif qilganidek, uni ixcham proton-elektron juftligi sifatida ko'rsatmaslik kerak. Zamonaviy o'lchovlarga ko'ra, neytron massasi m n \u003d 1,67493 10 -27 kg \u003d 1,008665 a.u. e. m. Energiya birliklarida neytron massasi 939,56563 MeV ni tashkil qiladi. Neytronning massasi protonning massasidan taxminan ikki elektron massasi kattaroqdir. Neytron kashf etilgandan so'ng darhol rus olimi D. D. Ivanenko va nemis fizigi V. Geyzenberglar atom yadrolarining proton-neytron tuzilishi haqidagi farazni ilgari surdilar va bu keyingi tadqiqotlarda to'liq tasdiqlandi.
Protonlar va neytronlar deyiladi nuklonlar. Atom yadrolarini xarakterlash uchun bir qancha belgilar kiritiladi. Atom yadrosini tashkil etuvchi protonlar soni Z belgisi bilan belgilanadi va deyiladi zaryad raqami yoki atom raqami (bu Mendeleyev davriy sistemasidagi seriya raqami). Yadro zaryadi Ze, bu yerda e elementar zaryad. Neytronlar soni N belgisi bilan belgilanadi. Umumiy soni nuklonlar (ya'ni proton va neytronlar) deyiladi massa raqami A: A=Z+N.
Kimyoviy elementlarning yadrolari belgisi bilan belgilanadi, bu erda X elementning kimyoviy belgisidir. Masalan, - vodorod, - geliy, - kislorod, - uglerod, - uran. Xuddi shu kimyoviy elementning yadrolari neytronlar soni bo'yicha farq qilishi mumkin. Bunday yadrolar deyiladi izotoplar. Ko'pgina kimyoviy elementlarning bir nechta izotoplari mavjud. Masalan, vodorod uchta izotopga ega: - oddiy vodorod, - deyteriy va - tritiy. Uglerodda 6 ta, kislorodda 3 ta izotop mavjud. Kimyoviy elementlar ichida tabiiy sharoitlar odatda izotoplar aralashmasi. Izotoplarning mavjudligi Mendeleyev davriy sistemasidagi tabiiy elementning atom massasining qiymatini aniqlaydi. Shunday qilib, masalan, nisbiy atom massasi tabiiy uglerod - 12,011.






