Neytronning massa soni bir xil. Neft va gaz katta ensiklopediya
Fizika 9-sinf
Mavzu: Atomning tuzilishi va atom yadrosi. Atom yadrolari energiyasidan foydalanish
56-dars Massa raqami. Zaryadlash
raqam. yadro kuchlari
Yeryutkin Evgeniy Sergeevich
Fizika o'qituvchisi eng yuqori toifa GOU SOSH №1360
Moskva
Salom! Bugungi darsimiz atom yadrosining tuzilishi, zaryad soni, massa raqamini muhokama qilish bilan bog'liq savolga bag'ishlangan bo'lib, biz nima haqida gaplashamiz. yadro kuchlari. Bizning darsimiz ilgari o'rganilgan barcha masalalar bo'yicha ba'zi bir oraliq natijalarning xulosasidir. Aytmoqchimanki, biz atom tuzilishi va yadro tuzilishi bilan bog'liq savollarni o'rgandik. Shuning uchun, bugun biz bu haqda gaplashamiz. Oldingi mavzularning qisqacha mazmuni, oldingi savollar. Birinchi savolga o'tishdan oldin, biz bu haqda gaplashamiz. Oldingi darsda biz Rezerford o'z tajribalarida proton kabi zarracha borligini aniqlaganligini aytdik. Biroz vaqt o'tgach, 1932 yilda Chadvik neytron deb nomlangan yana bir zarracha borligini aniqladi. Ushbu kashfiyotdan keyin bir-biridan mustaqil ravishda ikki kishi, rus olimi Ivanenko va nemis olimi Geyzenberg atom yadrosining tuzilishi uchun proton-neytron modelini taklif qilishdi. Ushbu Ivanenko-Geyzenberg nazariyasiga ko'ra, har qanday atomning yadrosida proton va neytronlar mavjud. Bu protonlar va neytronlar birgalikda atom yadrosida bo'lganlarni nuklon deb atashga qaror qilindi. Shunday qilib, "nuklon" (lotincha "yadro" dan) - proton va neytronlarning umumiy nomi. Zaryadga ega bo'lgan zarralar va zaryadga ega bo'lmagan zarralar, neytronlar, bu zarralarning barchasi birgalikda nuklonlar deb ataladi. Keling, boshqa narsa haqida gapiraylik. Yadro zaryadi g'oyasini birinchi marta 1913 yilda ingliz olimi Genri Mozili ilgari surgan. U atom elektr neytral bo'lganligi sababli tartibli, deb taklif qildi element raqami, elementar bilan ko'paytiriladi elektr zaryadi, bu yadroning zaryadidir. Mozeli qanday qilib bu xulosaga keldi? Gap shundaki, atomdagi elektronlar soni seriya raqamiga mos keladi. Bu shuni anglatadiki, barcha elektronlarning zaryadi seriya raqami va bitta elektronning zaryadi mahsulotidir. Chunki yadro konsentratsiyalangan musbat zaryad, shuning uchun yadro haqida ham shunday deyish mumkin. Keling, bu qanday kelganini ko'rib chiqaylik Moseley aynan biz to'lov raqami deb ataydigan narsaga. Qarang:
qI = Z . | e|
qI- yadro zaryadi
e - elektron zaryad
Zyadrodagi protonlar soni, zaryad soni
Raqamning zaryadi, ushbu bayonotga ko'ra, seriya raqami va elementar elektr zaryadining mahsuloti sifatida aniqlanadi. Ushbu holatda e - bu elektronning zaryadidir, u elementar elektr zaryadi deb ataladi va u modulli qabul qilinadi, chunki yadro zaryadi musbat ekanligi aniq. Bunday holda, seriya raqami zaryad raqami deb atala boshlandi, seriya raqami yadrodagi protonlar soniga mos keladigan raqamdir. Shunday qilib, seriya raqami haqida gapirganda, yadrodagi protonlar soni haqida gapirish mumkin. So'zlash kerak bo'lgan keyingi raqam - bu ommaviy raqam. U, bu raqam A harfi bilan belgilanadi va xuddi shu raqam davriy jadvaldan olinadi va butun sonlarga yaxlitlanadi. Keyin biz butun dunyoda Ivanenko-Gayzenberg tenglamasi deb ataladigan tenglama haqida gapirishimiz mumkin. Bu tenglama uchta raqamdan iborat: massa soni, zaryad soni va neytronlar soni. Keling, qanday yozilganligini va bu miqdorlar qanday belgilanishini ko'rib chiqaylik.
Ivanenko-Gayzenberg tenglamasi
A =Z + N
A - massa soni
Zelement raqami,
Nyadrodagi neytronlar soni
Qarang: A massa raqami qancha ekanligini bildiradi nuklonlar yadroga kiradi. Ma'lum bo'lishicha, davriy jadvalga ko'ra, massa sonini aniqlash kimyoviy element, atom yadrosidagi nuklonlar sonini aniqlaymiz.
Z, aytganimizdek, yadrodagi seriya raqami va protonlar soni bo'ladi. Bu holda N - neytronlar soni. Shunday qilib, biz massa raqami va seriya raqamini bilib, bu tenglamadan neytronlar sonini, protonlar sonini aniqlashimiz mumkin. Shu o'rinda bir muhim jihatga e'tibor qaratish lozim. Gap shundaki, 1913 yilda yana bir olim Soddi (siz bu odam Ruterford bilan ishlaganini eslaysiz) qiziq bir narsani aniqlagan. Aynan bir xil kimyoviy xossalarga ega, ammo massa raqamlari har xil bo'lgan kimyoviy elementlar mavjudligi aniqlandi. Bir xil bo'lgan elementlar Kimyoviy xossalari, lekin turli xil massa raqamlari bilan izotoplar sifatida ma'lum bo'ldi. Izotoplar - Bu kimyoviy elementlar bir xil kimyoviy xususiyatlarga ega, ammo ular bilan turli vazn atom yadrolari.
Shuni ham qo'shimcha qilish kerakki, izotoplar turli xil radioaktivlikka ega. Bularning barchasi birgalikda ushbu masalani o'rganishga olib keldi. Unda engil va og'ir kimyoviy elementlarning izotoplari ko'rsatilgan. Ko'raylikchi. Deyarli barcha kimyoviy elementlarning izotoplari borligini ko'rsatish uchun biz davriy jadvalning alohida sohalarini tanladik.
Izotoplar:
H - protiumU
H - deyteriyU
H - tritiy
Vodorodda bu izotoplardan uchtasi bor. Birinchi H izotopi protiy deb ataladi. E'tibor bering, seriya raqami quyida joylashgan, bu Z raqami va massa raqami tepada - bu raqam A. A dan yuqori, Z dan pastda va agar biz bu yadro yadrosida ekanligini anglatsak. protium atomi eng oddiy kimyoviy element, koinotda eng keng tarqalgan. Faqat 1 proton bor va bu yadroda umuman neytronlar yo'q. Vodorodning ikkinchi turi mavjud - bu deyteriy. Bu so'zni ko'pchilik eshitgan bo'lsa kerak. Iltimos, diqqat qiling: seriya raqami 1, massa raqami esa 2. Deyteriy yadrosi allaqachon 1 proton va bitta neytrondan iborat. Va vodorodning yana bir izotopi bor. U tritiy deb ataladi. Tritiy shunchaki (birinchi seriya) va massa soni bu izotop yadrosida 2 ta neytron borligini ko'rsatadi. Va yana bir element - uran. Davriy jadvalning boshqa tomoni. Bu allaqachon og'ir elementlardir. Uran ikkita umumiy izotopga ega. Bu uran 235. Seriya raqami 92, massa raqami esa 235. Bir elementning yadrosi boshqasidan qanday farq qilishi haqida darhol gapirishingiz mumkin. Ikkinchi izotop: shuningdek seriya raqami 92 va massa raqami 238. Juda tez-tez, qachon savol ostida izotoplar, xususan uran haqida hech qachon seriya raqamini aytmang. Ular shunchaki “uran” deyishadi, kimyoviy elementning nomini aytib, uning massa raqami 238. Yoki uran 235. Biz bu masalani oddiy sababga ko‘ra muhokama qilmoqdamiz, chunki bu kimyoviy element bugungi kunda mamlakatimiz energetikasi uchun qanchalik muhim ekanini bilamiz. butun dunyo energiyasi uchun umumiy.
Biz to'xtashimiz kerak bo'lgan keyingi savol aytilganlardan kelib chiqadi. Bu zarralar, nuklonlar yadro ichida qanday saqlanadi? Biz turli xil kimyoviy elementlarni, turli izotoplarni, ayniqsa og'ir elementlar uchun nom berdik, bu erda nuklonlar, ya'ni. protonlar va neytronlar, juda ko'p. Qanday qilib, ular yadro ichida saqlanadi? Biz bilamizki, kichik masofadagi yadroda yadroning o'lchami juda va juda kichik, juda ko'p miqdordagi nuklon zarralari to'planishi mumkin. Qanday qilib bu nuklonlar u erda juda zich, qanday kuchlar tomonidan chambarchas bog'langan? Darhaqiqat, elektrostatik itarilish tufayli bu zarralar juda tez parchalanishi, tarqalishi kerak. Biz bilamizki, faqat qarama-qarshi zaryadlar, qarama-qarshi zaryadlangan zarralar o'ziga tortadi. Agar zarralar bir xil nom bilan zaryadlangan bo'lsa, ular qaytarilishi kerakligi aniq. Yadroning ichida protonlar mavjud. Ular musbat zaryadlangan. Yadro hajmi juda kichik. Xuddi shu yadroda neytronlar ham mavjud, ya'ni u va boshqa zarralarni ushlab turadigan kuchlar bo'lishi kerak. Aynan shu kuchlar yadro kuchlari deb ataladi. Yadro kuchlari nuklonlar orasida harakat qiluvchi jozibador kuchlardir. Aytishimiz mumkinki, bu kuchlar o'ziga xos xususiyatlarga ega.
Biz gapirishimiz kerak bo'lgan birinchi mulk - bu yadro kuchlari elektrostatik itarilish kuchlaridan oshib ketishi kerak. Va bu shunday, ularni aniqlash mumkin bo'lganda, ular elektrostatik itarilish kuchlaridan 100 baravar ko'p ekanligi ma'lum bo'ldi. Yana bir muhim eslatma shu yadro kuchlari qisqa masofada ishlaydi. Masalan, 10 -15 m - bu yadroning diametri, bu kuchlar harakat qiladi. Ammo yadro kattaligi 10-14 ga oshishi bilanoq, bu biroz bo'lib tuyuldi, bu yadroning albatta parchalanishiga olib keladi. Bu masofada yadro kuchlari endi faol emas. Va elektrostatik itarilish kuchlari harakat qilishda davom etadi va yadro parchalanishiga aynan ular javobgardir.
Yadroviy kuchlar haqida yana bir narsani aytish kerak ular markaziy emas, ya'ni. ular bu zarralarni tutashtiruvchi to'g'ri chiziq bo'ylab harakat qilmaydi. Yadro kuchlari esa zarrachaning zaryadga ega yoki yo'qligiga bog'liq emas, chunki yadroga proton ham, neytron ham kiradi. Bu zarralar birga. Shunday qilib, xulosa: bu zarralar, nuklonlar yadro kuchlari tufayli yadroda ushlab turiladi va bu kuchlar faqat yadroda harakat qiladi. Yana shuni ta'kidlash mumkinki, yadroviy kuchlar yadro barqarorligi nuqtai nazaridan muhim ahamiyatga ega. Ushbu elementning mavjudligi uzoq umr ko'rish uchun javobgardir. Xulosa qilib aytganda, yana bir narsani ta'kidlashimiz mumkin: energiya haqida gapirganda, aynan shu erda yadro kuchlari asosiy rol o'ynaydi. Bu haqda keyingi darslarda gaplashamiz. Xayr.
Dars uchun vazifa.
1. Temir yadrolarining nuklon tarkibini aniqlang(nuklonlar, protonlar, neytronlar soni).
2. Kimyoviy element atomining yadrosida 22 ta proton va 26 ta neytron mavjud. Ushbu kimyoviy elementni nomlang.
3. Yadrodagi ikkita neytron o‘rtasidagi tortishish o‘zaro ta’sirining kuchini hisoblang. Neytronning massasi taxminan 1,7 * 10 ga teng -27 kg, neytronlar orasidagi masofani 10 ga teng oling -15 m, tortishish doimiysining qiymati 6,67 * 10 ga teng-11 (N * m 2) / kg 2.
Massa raqami
Massa sonini bilish yadro va atomning massasini taxmin qilish imkonini beradi. Agar massa soni ma'lum bo'lsa, u holda massa M Atom va uning yadrosi quyidagi munosabat asosida baholanadi M ≈ A m N, qayerda m N ≈ 1,67 10 −27 kg - nuklon, ya'ni proton yoki neytronning massasi. Masalan, alyuminiy-27 atomi va uning yadrosida 27 ta nuklon (13 proton va 14 neytron) mavjud. Uning massasi taxminan 27 1,67 10 −27 kg ≈ 4,5 10 −26 kg ga teng. Agar yadro massasini kattaroq aniqlik bilan olish zarur bo'lsa, yadrodagi nuklonlar yadro tortishish kuchlari bilan bog'langanligini va shuning uchun munosabatlarga muvofiqligini hisobga olish kerak. E=mc 2 yadroning massasi kamayadi. Yadro atrofidagi orbitalardagi elektronlarning umumiy massasi ham atom massasiga qo'shilishi kerak. Biroq, bu tuzatishlarning barchasi 1% dan oshmaydi.
| 238 92 U | → | 234 90 Th | + | 4 2 U |
chap tomonda boshlang'ich yadroning massa soni 238, reaksiyaning o'ng tomonida esa massa raqamlari 234 va 4 bo'lgan ikkita yadro mavjud bo'lib, u jami 238 tani beradi. Alfa zarrachaning massa soni (geliy-4 yadrosi) 4, alfa -parchalanish parchalanuvchi yadroning massa sonini 4 birlikka kamaytiradi. Beta-yemirilishning har qanday turlari (beta-minus yemirilishi, pozitron parchalanishi, elektronni tutib olish, qoʻshaloq beta-yemirilishning barcha turlari) massa sonini oʻzgartirmaydi, chunki bu jarayonda faqat yadroning baʼzi nuklonlarining bir turdan ikkinchisiga (protonlar) aylanishi sodir boʻladi. neytronlarga yoki orqaga). Izomerik o'tish ham massani o'zgartirmaydi asosiy raqam.
Eslatmalar
Shuningdek qarang
Wikimedia fondi. 2010 yil.
Boshqa lug'atlarda "Ommaviy raqam" nima ekanligini ko'ring:
- (nuklonlar soni, A belgisi), ATOM Yadrosidagi NUKLEONLAR (NEYTRON va PROTONLAR) umumiy soni. Odatda elementning kimyoviy belgisidan oldin ustun belgisi sifatida yoziladi. Shunday qilib, eng yengil element vodorod yadrosida faqat bitta proton bor va ... ... Ilmiy-texnik entsiklopedik lug'at
Nuklonlarning umumiy soni (neytronlar va protonlar) at. yadro. Xuddi shu kimyoning izotoplari uchun har xil. element. Jismoniy ensiklopedik lug'at. M.: Sovet entsiklopediyasi. Bosh muharrir A. M. Proxorov. 1983. MASS RANGAR ... Jismoniy entsiklopediya
Atom yadrosidagi nuklonlar soni. Odatda kimyoviy element belgisining yuqori chap qismida ko'rsatilgan (masalan, 10V) ... Katta ensiklopedik lug'at
MASS NUMBER- atom yadrosidagi nuklonlarning (proton va neytronlarning) umumiy soni, masalan, A bilan belgilangan va tegishli element belgisining yuqori chap tomonidagi indeks bilan ko'rsatilgan. 32S massa soni 32 (A = 32) bo'lgan oltingugurt izotopi degan ma'noni anglatadi. Izotopning massasi butun ...... ga teng. Katta politexnika entsiklopediyasi
massa raqami- — [Ya.N.Luginskiy, M.S.Fezi Jilinskaya, Yu.S.Kabirov. Inglizcha ruscha elektrotexnika va energetika lug'ati, Moskva] Elektrotexnika mavzulari, asosiy tushunchalar EN massa soni ... Texnik tarjimon uchun qo'llanma
Atom yadrosidagi nuklonlar soni. Odatda kimyoviy element belgisining yuqori chap qismida ko'rsatilgan (masalan, 10V). * * * MASSA SONI MASS SONI, atom yadrosidagi nuklonlar soni. Odatda kimyoviy element belgisining yuqori chap qismida ko'rsatilgan ... ... ensiklopedik lug'at
massa raqami- masės skaičius statusas T sritis Standartizacija ir metrologija apibrėžtis Atomo branduolio nukleonų skaičius. attikmenys: ingliz. massa raqami; yadro raqami; nuklon soni vok. Massenzahl, f; Nukleonenzahl, f rus. massa soni, n; raqam…… Penkiakalbis aiskinamasis metrologijos terminų žodynas
massa raqami- masės skaičius statusas T sritis chemija apibrėžtis Atomo branduolio nukleonų skaičius. attikmenys: ingliz. massa raqami; yadro raqami; nuklon raqami eng. ommaviy raqam ... Chemijos terminų aiskinamasis žodynas
massa raqami- masės skaičius statusas T sritis fizika atitikmenys: angl. massa raqami; yadro raqami; nuklon soni vok. Massenzahl, f; Massezahl, f; Nukleonenzahl, f rus. massa soni, n pranc. nombre de masse, m; nombre de nucléons, m … Fizikos terminų žodynas
Atom yadrosidagi nuklonlar (proton va neytronlar) soni; A harfi bilan belgilanadi va odatda element belgisining yuqori chap qismida ko'rsatiladi, masalan, 32S oltingugurt izotopini bildiradi A \u003d 32. M. h. Va elementar birliklarda ifodalangan yadroviy zaryad Z Z. ... Buyuk Sovet Entsiklopediyasi
Atom markazi uning massasining katta qismini va barcha musbat zaryadini o'z ichiga oladi. Atomning bu hududi yadro deb ataladi.
Atomning o'lchamlari m, yadroning o'lchamlari 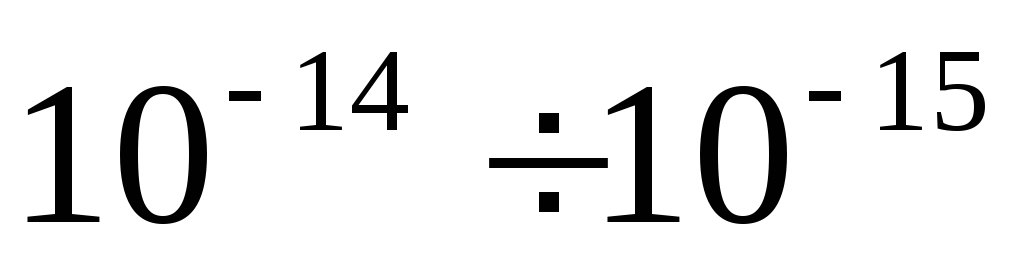 m yadro massasi atom massasining 99,95% ni tashkil qiladi. Neytral atomda Z elektronlar. Yadro zaryadi musbat va elementar zaryadga karrali
m yadro massasi atom massasining 99,95% ni tashkil qiladi. Neytral atomda Z elektronlar. Yadro zaryadi musbat va elementar zaryadga karrali 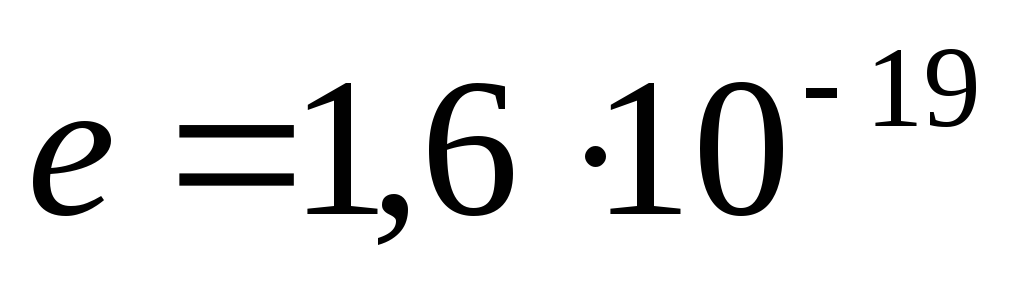 Cl. Yadro zaryadini quyidagicha ifodalash mumkin
Cl. Yadro zaryadini quyidagicha ifodalash mumkin 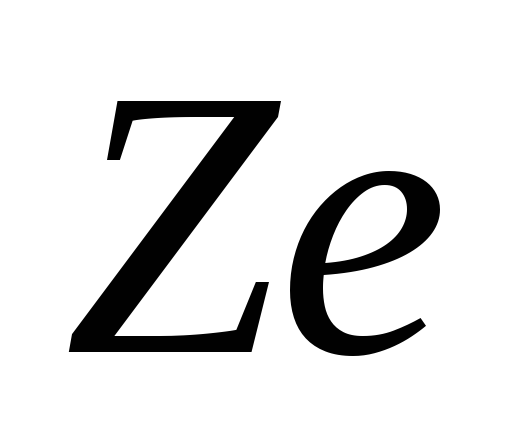 , qayerda Z- zaryad raqami, u davriy jadvalning kimyoviy soniga to'g'ri keladi va yadroga kiradigan protonlar soniga teng.
, qayerda Z- zaryad raqami, u davriy jadvalning kimyoviy soniga to'g'ri keladi va yadroga kiradigan protonlar soniga teng.
Yadroning ikkinchi muhim xususiyati uning massasidir. Yadroning massasi yadroga kirgan protonlar massalari yig'indisidan kattaroq bo'lib chiqdi.
Yadro tarkibida neytral zarralar borligi taxmin qilingan. 1932 yilda Chadvig neytronlarni kashf etdi. Ivanenko va Geyzenberg yadroning proton-neytron nazariyasini taklif qildilar. Yadro proton va neytronlarga bo'linadi. Ular nuklonlar deb ataladi. Umumiy soni yadrodagi nuklonlar massa raqami deb ataladiA
.
Neytronlarning umumiy soni N=A-Z ga teng. Protonning qolgan massasi 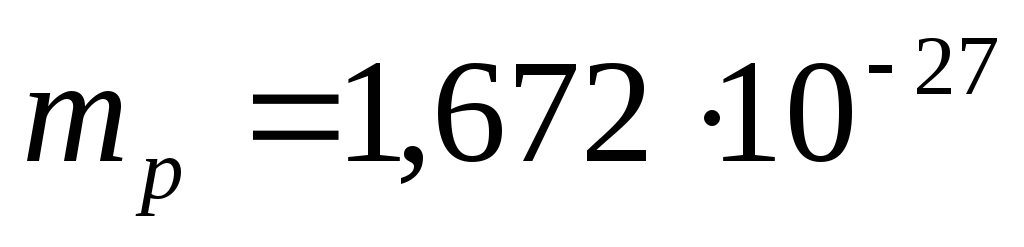 kg, neytron massasi
kg, neytron massasi 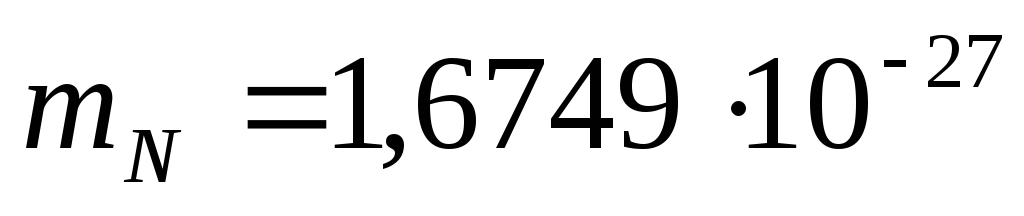 kg.
kg.
Kimyoviy elementning yadrosi neytral atom bilan bir xil belgi bilan belgilanadi. 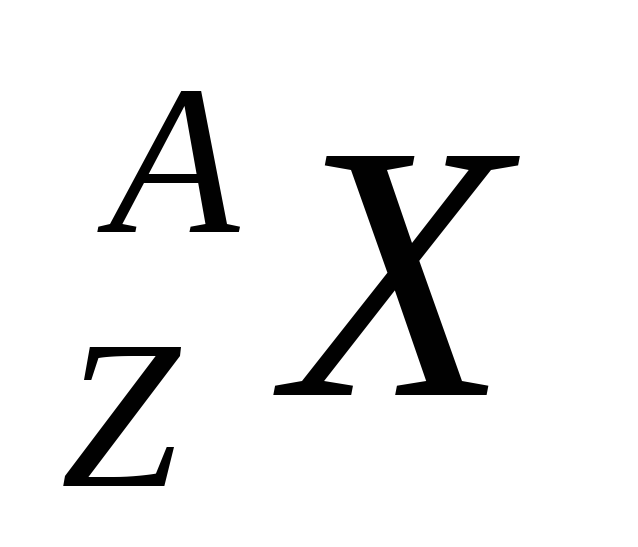 , qayerda Z- atom raqami (yadro zaryadi), A- massa soni (yadrodagi nuklonlar soni). Zaryad soni bir xil, ammo massalari har xil bo'lgan yadrolar izotoplar deb ataladi (izotoplar neytronlar soni bilan farqlanadi). Massa soni bir xil, lekin zaryadlari har xil bo'lgan yadrolar izobarlar deyiladi.
, qayerda Z- atom raqami (yadro zaryadi), A- massa soni (yadrodagi nuklonlar soni). Zaryad soni bir xil, ammo massalari har xil bo'lgan yadrolar izotoplar deb ataladi (izotoplar neytronlar soni bilan farqlanadi). Massa soni bir xil, lekin zaryadlari har xil bo'lgan yadrolar izobarlar deyiladi.
28. Yadro kuchlarining xossalari.
Yadro kuchlarining xususiyatlari:
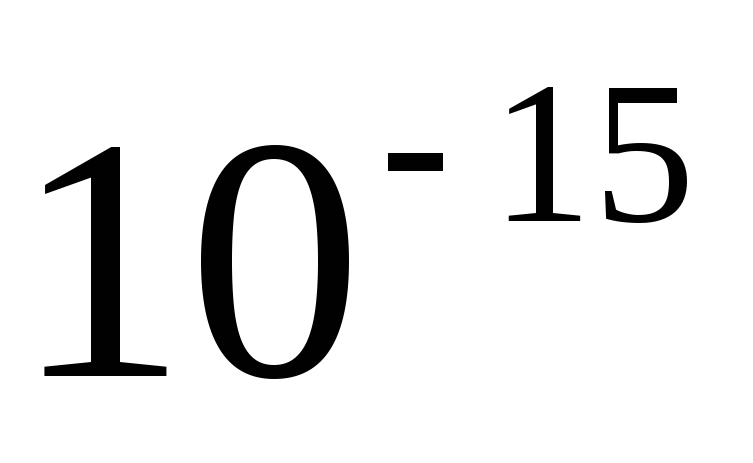
29. Radioaktivlik. Alfa va beta parchalanishi. O'zgartirish qoidalari.
Radioaktivlik deyiladi bir kimyoviy elementning beqaror izotoplarining boshqa elementning izotoplariga aylanishi, ma'lum zarrachalarning emissiyasi. Tabiiy radioaktivlik deganda tabiiy ravishda yuzaga keladigan beqaror izotoplarda kuzatilgan radioaktivlik tushuniladi. Sun'iy radioaktivlik yadro reaksiyalari natijasida olingan izotoplarning radioaktivligi deyiladi.
Radioaktiv nurlanish murakkab tarkibga ega. Magnit maydonda radioaktiv nurlanishning tor nurlari uch qismga bo'linadi:

 -zarralar -
geliy yadrolarining zaryad bilan oqimi Z=2
e va massa soni A=4
(
-zarralar -
geliy yadrolarining zaryad bilan oqimi Z=2
e va massa soni A=4
(![]() ). Tezlik
). Tezlik  -zarralar ga teng
-zarralar ga teng 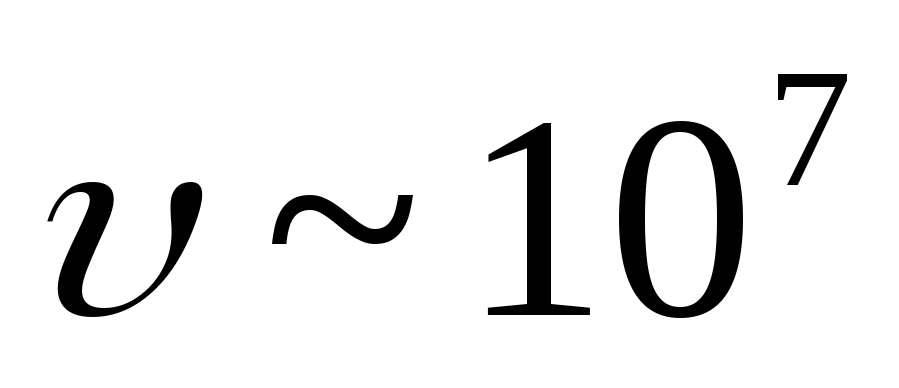 Xonim. Moddaga kirish
Xonim. Moddaga kirish  -zarralar atomlar va molekulalar bilan faol ta'sir o'tkazadi, uni ionlashtiradi va qo'zg'atadi. Qachon energiya
-zarralar atomlar va molekulalar bilan faol ta'sir o'tkazadi, uni ionlashtiradi va qo'zg'atadi. Qachon energiya  -zarra termal harakatga tushadi, u ikkita elektronni ushlaydi va geliy atomiga aylanadi ( U). Undan oldin u yugurish deb ataladigan yo'ldan o'tadi. Materiya bilan kuchli o'zaro ta'sir tufayli diapazon qisqa. Bir varaq qog'oz yoki kiyim ko'tariladi
-zarra termal harakatga tushadi, u ikkita elektronni ushlaydi va geliy atomiga aylanadi ( U). Undan oldin u yugurish deb ataladigan yo'ldan o'tadi. Materiya bilan kuchli o'zaro ta'sir tufayli diapazon qisqa. Bir varaq qog'oz yoki kiyim ko'tariladi  -zarralar. 0,05 mm qalinlikdagi alyuminiy qatlam ham kechiktiradi
-zarralar. 0,05 mm qalinlikdagi alyuminiy qatlam ham kechiktiradi  -zarralar. Ionlash qobiliyati
-zarralar. Ionlash qobiliyati  -zarralar katta va teng
-zarralar katta va teng 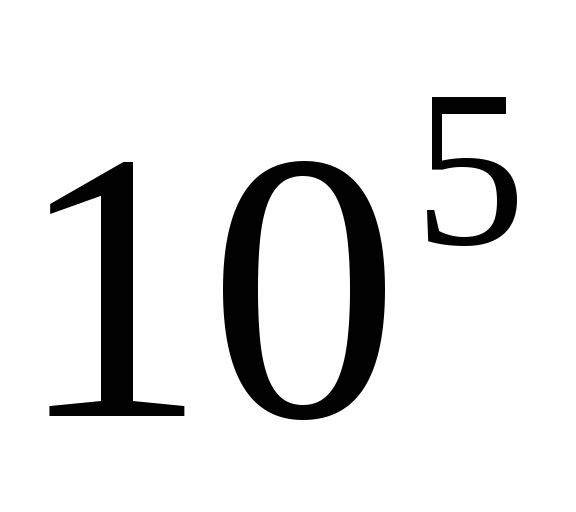 yugurish ustida bug '.
yugurish ustida bug '.
 -zarralar
tezlikda yadrolardan chiqadigan elektronlar oqimidir
-zarralar
tezlikda yadrolardan chiqadigan elektronlar oqimidir 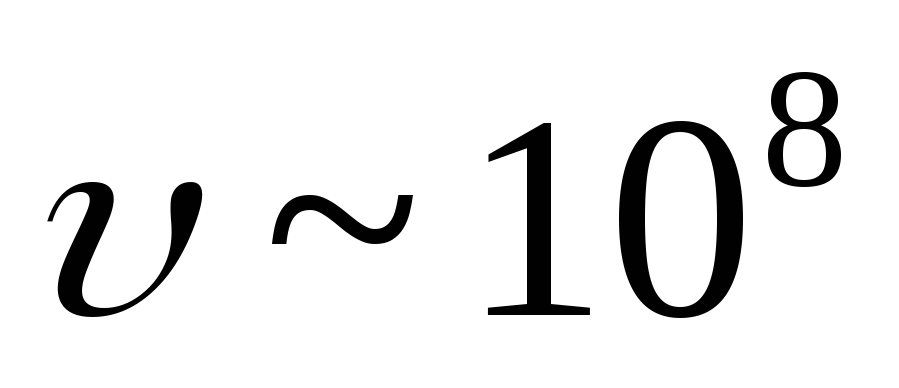 Xonim. Neytron protonga aylanganda yadro elektron chiqaradi:
Xonim. Neytron protonga aylanganda yadro elektron chiqaradi:
qayerda  - elektron belgisi,
- elektron belgisi, 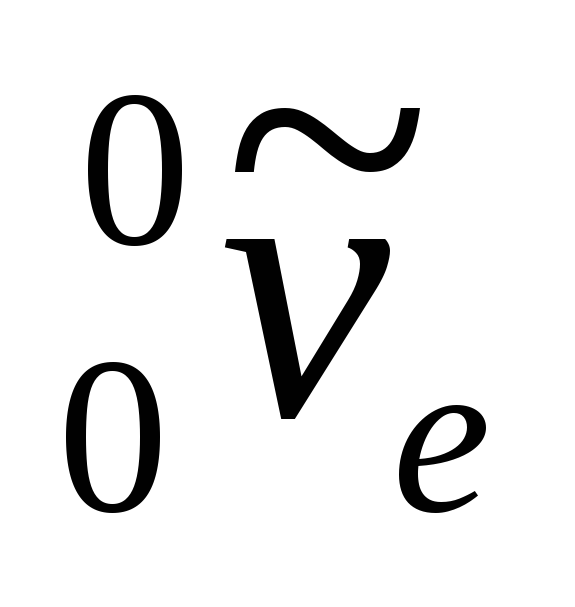 - elektron antineytrino.
- elektron antineytrino.
Ionlash qobiliyati  dan yuzlab marta kichik zarralar
dan yuzlab marta kichik zarralar  -zarralar va penetratsion quvvat kattaroqdir.
-zarralar va penetratsion quvvat kattaroqdir.  - radiatsiya 2 mm qalinlikdagi alyuminiy qatlami bilan kechiktiriladi.
- radiatsiya 2 mm qalinlikdagi alyuminiy qatlami bilan kechiktiriladi.
Atom yadrolarini o'rganish quyidagi eksperimental faktlar aniqlangandan so'ng boshlandi: 1) 1896 yilda frantsuz olimi Anri Bekkerel tomonidan tabiiy radioaktivlikni kashf etishi; 2) 1910-yilda ingliz olimi Soddi tomonidan kimyoviy elementlarning izotopiyasining kashf etilishi; 3) 1911 yilda buyuk ingliz fizigi Ernest Rezerford tomonidan taklif qilingan atomning yadro modeli.
Rezerford 1908 yilda radioaktivlikni tadqiq qilib, radioaktiv parchalanish paytida ba'zi kimyoviy elementlar atomlarining boshqa elementlar atomlariga aylanishi sodir bo'ladi, degan xulosaga keldi. Keyinchalik, bir necha megaelektron-volt energiyaga ega bo'lgan a-zarrachalarning yupqa oltin plyonkalari orqali o'tishini o'rganar ekan, Rezerford atomning yadro modelini ochdi, shundan so'ng radioaktivlik paytida ba'zi elementlarning yadrolari zarrachalarga aylanadi. boshqa elementlarning yadrolari.
Izotopiyaning kashf etilishi qo'shimcha rol o'ynadi. Atom og'irliklari, ya'ni. kimyoviy toza elementlar atomlarining massalari, qoida tariqasida, a.m.u.da ifodalanadi. butun sonlarga unchalik yaqin bo'lmagan raqamlar. Masalan, borning atom og'irligi (B) 10,82; Yo'q - 20,183; Cl - 35,457; Fe -56,85;… . Izotopiyaning kashf etilishi bilan kimyoviy sof element atom og'irliklari bo'yicha bir-biridan farq qiluvchi izotoplar aralashmasi degan fikr o'rnatildi. Izotoplarning atom og'irliklari elementlarning atom og'irliklariga qaraganda butun sonlarga yaqinroq bo'lib chiqdi va qanchalik yaqin bo'lsa, izotop engilroq bo'ladi, ya'ni. uning atom og'irligi qanchalik past bo'lsa. Bu olimlarni yadro atom og'irliklari birlikka yaqin bo'lgan zarralardan iborat degan fikrga olib keldi. Bu holat vodorod atomining yadrosi - atom og'irligi birlikka yaqin bo'lgan proton tomonidan yaxshi qondiriladi (1,008). Bundan tashqari, protonning zaryadi ijobiy bo'lganligi sababli, yadro tarkibiga protonlar ham kirishi kerak degan fikr paydo bo'ldi. Yadroning boshqa tarkibiy zarralarini aniqlash uchun uzoq vaqt kerak bo'ldi. Tabiiy b-faollik hodisasi elektronlar yadro tarkibiga kiritilganligini ko'rsatgandek tuyuldi. Shuning uchun yadroning proton-elektron modeli taklif qilindi. Biroq, proton-elektron modeli asossiz bo'lib chiqdi. Bu modelga ko'ra, juft sonli proton va elektronlardan tashkil topgan yadroning spini butun son bo'lishi kerak (protonning spini, xuddi elektronning spini kabi, ½ ħ), amalda esa yarim butun sonlar bo'lishi kerak. ham kuzatiladi. Model nega yadroning magnit momenti elektronning magnit momentidan 2000 marta kam ekanligini tushuntirib bermadi. Nihoyat, proton-elektron modeli Geyzenberg printsipiga zid bo'lib chiqdi. Yadroning o'lchamini bilgan holda, yadroning bir qismi bo'lgan elektron impulsining kattaligini va demak, uning energiyasining kattaligini taxmin qilish mumkin. Bunday hisob-kitoblar shuni ko'rsatadiki, yadrodagi elektronning energiyasi taxminan 200 MeV ni tashkil qiladi. Tajribaga ko'ra, yadrodagi bir zarrachaning bog'lanish energiyasi 7 - 8 MeV ni tashkil qiladi. Bundan tashqari, 200 MeV energiyasi yadroning b-emirilish vaqtida chiqaradigan elektronlar energiyasidan ko'p marta katta.
Qiyinchilikdan chiqish yo'li 1932 yilda Ruterfordning xodimi Chadvik yangi kashfiyotdan so'ng topildi. elementar zarracha- neytron. Neytronning massasi protonning massasiga taxminan teng, undan biroz kattaroq, elektr zaryadi esa 0 ga teng.Neytron kashf etilgandan ko'p o'tmay, 1934 yilda sovet fizigi D.D.Ivanenko proton haqida gipotezani ilgari surdi. yadroning neytron tuzilishi. Xuddi shu faraz Geyzenberg tomonidan mustaqil ravishda taklif qilingan.
Hozirda yadroning proton-neytron tuzilishi umume'tirof etilgan va yadro va barcha yadro fizikasi haqidagi zamonaviy g'oyalar asosida yotadi.
Zamonaviy ma'lumotlarga ko'ra, proton (p) musbat zaryadga ega, zaryadga teng elektrod qp= 1.6. 10 -19 C va dam olish massasi m p= (1,0075957 ±0,000001) amu = (1836,09±0,01) men.
Neytron (n) - tinch massaga ega neytral zarracha m n= (1,008982 ±0,000003)a.m.u. = (1838,63 ± 0,01) men, Bu erda 1amu = 1,667. 10 -27 kg - C 12 atomi massasining 1/12 qismi;
men= 9.106. 10-31 kg – elektronning qolgan massasi.
Zamonaviy fizikada proton va neytron bir xil zarrachaning ikkita zaryad holatidir, deb ishoniladi. nuklon(lot. yadro — yadrodan). Demak, proton nuklonning proton holati, neytron nuklonning neytron holatidir. Atom yadrosidagi nuklonlarning umumiy soni deyiladi massa raqami A.
Atom yadrosi Ze zaryadi bilan tavsiflanadi , qayerda Z - yadroning zaryad raqami, yadrodagi protonlar soniga teng va Mendeleyev davriy elementlar tizimidagi kimyoviy elementning seriya raqamiga to'g'ri keladi. Davriy sistemaning hozirgi vaqtda ma'lum bo'lgan 107 ta elementi yadrolarining zaryad raqamlari Z = 1 dan Z = 107 gacha. Z yadrodagi protonlar soniga teng bo'lganligi sababli yadrodagi neytronlar soni: N = A - Z In yadro fizikasi Yadroni neytral atom bilan bir xil belgi bilan belgilash odatiy holdir: , bu erda X- belgi
kimyoviy element, Z- atom raqami (yadrodagi protonlar soni), LEKIN- massa soni (yadrodagi nuklonlar soni).
Atom neytral bo'lgani uchun yadro zaryadi atomdagi elektronlar sonini aniqlaydi. Elektronlar soni ularning atomdagi holatlar bo'yicha taqsimlanishini belgilaydi, bu esa o'z navbatida atomning kimyoviy xususiyatlarini belgilaydi. Binobarin, yadro zaryadi berilgan kimyoviy elementning o'ziga xos xususiyatlarini aniqlaydi, ya'ni atomdagi elektronlar sonini, ularning konfiguratsiyasini aniqlaydi. elektron qobiqlar, atom ichidagi elektr maydonining kattaligi va tabiati.
Yadrolar bir xil Z, lekin boshqacha LEKIN(ya'ni, neytronlarning soni har xil bo'lgan) izotoplar va bir xil yadrolar deb ataladi. LEKIN, lekin har xil Z izobarlari. Masalan, vodorod ( Z= 1) uchta izotopga ega; - protiy ( Z =1, N= 0); - deyteriy, ( Z =1, N= 1); - tritiy ( Z =1, N= 2).Ko'p hollarda bir xil kimyoviy elementning izotoplari bir xil kimyoviy va deyarli bir xil bo'ladi. jismoniy xususiyatlar(istisno vodorod izotoplaridir), ular asosan elektron qobiqlarning tuzilishi bilan belgilanadi, bu ma'lum bir elementning barcha izotoplari uchun bir xil.
Quyidagi yadrolar izobar yadrolarga misol bo'la oladi: , , . Hozirgi vaqtda bir-biridan farq qiladigan 2500 dan ortiq yadrolar ma'lum Z, yoki A, yoki ikkalasi ham.
Ruterford buni ko'rsatdi atom yadrolari taxminan 10 -14 - 10 -15 m o'lchamlarga ega (taqqoslash uchun atomning chiziqli o'lchamlari taxminan 10-10 m). Yadro radiusi - empirik formula bilan berilgan R = R 0 A 1/3 qaerda R0= (1,3 ÷ 1,7) 10 -15 m Biroq, bu kontseptsiyadan foydalanganda, uning noaniqligi, masalan, yadro chegarasining xiralashganligi sababli ehtiyot bo'lish kerak. Yadro hajmi yadrodagi nuklonlar soniga proporsionaldir. Demak, yadro moddasining zichligi barcha yadrolar uchun taxminan bir xil: ρ » 10 17 kg/m 3 .
Massa raqami
Massa sonini bilish yadro va atomning massasini taxmin qilish imkonini beradi. Agar massa soni ma'lum bo'lsa, u holda massa M Atom va uning yadrosi quyidagi munosabat asosida baholanadi M ≈ A m N, qayerda m N ≈ 1,67 10 −27 kg - nuklon, ya'ni proton yoki neytronning massasi. Masalan, alyuminiy-27 atomi va uning yadrosida 27 ta nuklon (13 proton va 14 neytron) mavjud. Uning massasi taxminan 27 1,67 10 −27 kg ≈ 4,5 10 −26 kg ga teng. Agar yadro massasini kattaroq aniqlik bilan olish zarur bo'lsa, yadrodagi nuklonlar yadro tortishish kuchlari bilan bog'langanligini va shuning uchun munosabatlarga muvofiqligini hisobga olish kerak. E=mc 2 yadroning massasi kamayadi. Yadro atrofidagi orbitalardagi elektronlarning umumiy massasi ham atom massasiga qo'shilishi kerak. Biroq, bu tuzatishlarning barchasi 1% dan oshmaydi.
92 238 U → 90 234 T h + 2 4 H e (\displaystyle (\mathsf (_(92)^(238)U\o‘ng ko‘rsatkich _(90)^(234)Th+_(2)^(4)He )))Chap tomonda boshlang'ich yadroning massa soni 238, reaksiyaning o'ng tomonida massa raqamlari 234 va 4 bo'lgan ikkita yadro joylashgan bo'lib, ular jami 238 tani beradi. alfa zarracha (geliy-4 yadrosi) 4, alfa -parchalanish parchalanadigan yadroning massa sonini 4 birlikka kamaytiradi. Har qanday turlar






