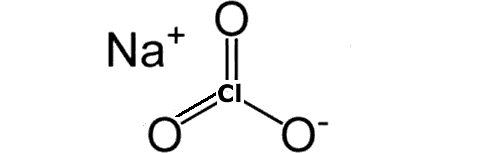
Sodyum klorat: ekotoksisite. Elektrokimyasal yöntemle sodyum ve potasyum klorat üretimi Taşıma ve depolama
Vikipedi, özgür ansiklopedi
| Sodyum klorat | |
| Sodyum-klorat-bileşen-iyonları-2D.png | |
| Genel | |
|---|---|
| Sistematik İsim |
Sodyum klorat |
| Geleneksel isimler | sodyum klorit |
| Kimya formül | NaClO3 |
| Fiziksel özellikler | |
| Durum | renksiz kristaller |
| Molar kütle | 106.44 g/mol |
| Yoğunluk | 2.490; 2.493 g/cm³ |
| termal özellikler | |
| T. eriyik. | 255; 261; 263°C |
| T. kip. | aralık 390°C |
| Mol. ısı kapasitesi | 100,1 J/(mol K) |
| oluşum entalpisi | -358 kJ/mol |
| Kimyasal özellikler | |
| sudaki çözünürlük | 100,5 25; 204 100 gr/100 ml |
| etilendiamin içinde çözünürlük | 52,8 g/100 ml |
| Dimetilformamidde çözünürlük | 23.4 g/100 ml |
| Monoetanolamin içinde çözünürlük | 19,7 gr/100 ml |
| asetonda çözünürlük | 0.094 gr/100 ml |
| sınıflandırma | |
| Kayıt CAS numarası | 7775-09-9 |
| gülümser | Cl(=O)=O] |
| Kayıt EC numarası | 231-887-4 |
| RTEC'ler | FO0525000 |
| Veriler, aksi belirtilmedikçe standart koşullara (25 °C, 100 kPa) dayanmaktadır. | |
Sodyum klorat- NaClO 3 formülüne sahip inorganik bileşik, sodyum metal tuzu ve klorik asit, renksiz kristaller, suda yüksek oranda çözünür.
Fiş
- Sodyum klorat, klorik asidin sodyum karbonat üzerindeki etkisiyle hazırlanır:
- veya ısıtıldığında kloru konsantre bir sodyum hidroksit çözeltisinden geçirerek:
- Sulu sodyum klorür çözeltilerinin elektrolizi:
Fiziksel özellikler
Sodyum klorat - renksiz kübik kristaller, uzay grubu P 2 1 3 , hücre parametreleri a= 0.6568 nm, Z = 4.
230-255°C'de başka bir faza, 255-260°C'de monoklinik faza geçer.
Kimyasal özellikler
- Isıtıldığında orantısız:
- Sodyum klorat güçlü bir oksitleyici ajandır katı hal karbon, kükürt ve diğer indirgeyici maddelerle karıştırıldığında, ısıtıldığında veya çarpıldığında patlar.
Başvuru
- Sodyum klorat piroteknikte uygulama bulmuştur.
"Sodyum Klorat" makalesi hakkında bir inceleme yazın
Edebiyat
- Kimya Ansiklopedisi / Ed.: Knunyants I.L. vb. - M.: Sovyet Ansiklopedisi, 1992. - T. 3. - 639 s. - ISBN 5-82270-039-8.
- Bir kimyagerin el kitabı / Yayın kurulu: Nikolsky B.P. ve diğerleri - 2. baskı, düzeltildi. - M.-L.: Kimya, 1966. - T. 1. - 1072 s.
- Bir kimyagerin el kitabı / Yayın kurulu: Nikolsky B.P. ve diğerleri - 3. baskı, düzeltildi. - L.: Kimya, 1971. - T. 2. - 1168 s.
- Ripan R., Chetyanu I. İnorganik kimya. Metallerin kimyası. - M.: Mir, 1971. - T. 1. - 561 s.
| İnorganik madde ile ilgili bu madde bir taslaktır. Projeye ekleyerek yardımcı olabilirsiniz. |
Sodyum kloratı açıklayan bir alıntı
Sabah saat on birdi. Güneş Pierre'in biraz solunda ve arkasında duruyordu ve önünde yükselen arazi boyunca bir amfitiyatro gibi açılan devasa panoramayı temiz, nadir havayla parlak bir şekilde aydınlattı.Bu amfitiyatro boyunca yukarı ve sola doğru, onu kesen büyük Smolenskaya yolu, beyaz kiliseli bir köyden geçerek höyüğün önünde ve altında beş yüz adım uzanıyordu (bu Borodino'ydu). Köyün altından köprünün üzerinden geçen yol ve inişler ve çıkışlar boyunca, altı mil ötede görülebilen Valuev köyüne doğru gittikçe daha yükseğe kıvrılıyordu (Napolyon şimdi içinde duruyordu). Valuev'in arkasındaki yol, ufukta sararmış bir ormanda gizlenmişti. Bu ormanda, huş ve ladin, yolun sağında, uzak bir haç ve Kolotsky Manastırı'nın çan kulesi güneşte parlıyordu. Bu mavi mesafe boyunca, ormanın ve yolun sağında ve solunda, farklı yerlerde duman tüten ateşler ve bizim ve düşman birliklerinin belirsiz kitleleri görülüyordu. Sağda, Kolocha ve Moskva nehirleri boyunca uzanan bölge, vadi ve dağlıktı. Boğazları arasında, Bezzubovo ve Zakharyino köyleri uzaktan görülebiliyordu. Solda, arazi daha düzdü, tahıllı tarlalar vardı ve biri sigara içen, yanmış bir köy görebiliyordu - Semenovskaya.
Pierre'in sağda ve solda gördüğü her şey o kadar belirsizdi ki, alanın ne solu ne de sağı fikrini tam olarak tatmin etti. Her yerde görmeyi umduğu savaştan bir pay değil, tarlalar, açıklıklar, birlikler, ormanlar, yangınlardan çıkan dumanlar, köyler, höyükler, dereler; ve Pierre ne kadar demonte olursa olsun, bu yaşam alanında mevzi bulamadı ve birliklerinizi düşmandan bile ayırt edemedi.
"Bilen birine sormalıyız," diye düşündü ve askeri olmayan devasa figürüne merakla bakan subaya döndü.
"Sorayım," Pierre subaya döndü, "hangi köy ileride?"
- Burdino ya da ne? - dedi memur, arkadaşına bir soru ile hitap ederek.
- Borodino, - düzelterek, diğerine cevap verdi.
Memur, görünüşe göre konuşma fırsatından memnun, Pierre'e doğru hareket etti.
Bizimkiler orada mı? diye sordu.
"Evet ve Fransızlar daha uzakta," dedi subay. "İşte oradalar, görünüyorlar.
- Neresi? nerede? diye sordu.
- Çıplak gözle görebilirsiniz. Evet, burada, burada! Subay, eliyle nehrin solunda görünen dumanı işaret etti ve yüzünde Pierre'in tanıştığı birçok yüzde gördüğü sert ve ciddi ifade ortaya çıktı.
Ah, bu Fransız! Ve orada? .. - Pierre, birliklerin göründüğü höyüğün soluna işaret etti.
- Bunlar bizim.
- Ah, bizimki! Ve orada? .. - Pierre, köyün yakınında, vadide görülebilen, yakınında yangınların da içtiği ve kararmış bir şeyin olduğu büyük bir ağaçla uzak bir höyüğü işaret etti.
"Yine o," dedi memur. (Shevardinsky tabyasıydı.) - Dün bizimdi ve şimdi onun.
Peki bizim pozisyonumuz nedir?
- Durum? dedi memur memnuniyetle gülümseyerek. - Bunu size net bir şekilde söyleyebilirim çünkü neredeyse tüm tahkimatlarımızı ben yaptım. Burada, görüyorsunuz, merkezimiz Borodino'da, tam burada. Önünde beyaz bir kilise olan bir köyü işaret etti. - Kolocha üzerinde bir geçit var. İşte, görüyorsunuz, ovalarda sıra sıra biçilmiş samanların uzandığı yerde, işte köprü. Burası bizim merkezimiz. Sağ kanadımız (dik bir şekilde sağı, geçidin içini işaret etti), Moskova Nehri'nin olduğu yer ve orada çok güçlü üç tabya inşa ettik. Sol kanat ... - ve sonra memur durdu. - Görüyorsun ya, sana açıklamak zor... Dün sol kanadımız tam oradaydı, Şevardin'de, şurada, meşenin nerede olduğunu görüyorsun; ve şimdi sol kanadı geri aldık, şimdi dışarı, dışarı - köyü ve dumanı görüyor musun? - Bu Semenovskoye, evet burada, - Raevsky höyüğüne işaret etti. “Ama burada bir savaş olması pek olası değil. Askerleri buraya taşıması bir aldatmacadır; o, doğru, Moskova'nın sağına gidecek. Evet, nerede olursa olsun, yarını pek saymayacağız! dedi memur.
Hikâyesi sırasında memura yanaşan yaşlı astsubay, sessizce amirinin konuşmasının sonunu bekledi; ama bu noktada memurun sözlerinden memnun olmadığı belliydi ve sözünü kesti.
"Turlara gitmek zorundasın," dedi sertçe.
Memur utanmış gibiydi, sanki yarın kaç kişinin kaybolacağını düşünebileceğini ama bunun hakkında konuşmaması gerektiğini anlamış gibiydi.
"Eh, evet, üçüncü şirketi tekrar gönder," dedi memur aceleyle.
"Peki sen nesin, doktorlardan biri değil misin?"
Buluş, yaygın olarak kullanılan sodyum klorat üretimi ile ilgilidir. çeşitli alanlar sanayi. Sodyum klorür çözeltisinin elektrolizi, önce klor diyafram hücrelerinde gerçekleştirilir. Elde edilen klorür-alkali çözeltileri ve elektrolitik klor gazı, bir klorür-klorat çözeltisi oluşturmak üzere karıştırılır. Nihai çözelti, kristalizasyon aşamasının ana likörü ile karıştırılır ve diyaframsız elektrolize gönderilir, ardından klorür-klorat çözeltilerinin buharlaştırılması ve sodyum kloratın kristalleştirilmesi yapılır. Diyafram elektrolizinin ürünleri, klorat elektrolizinin asitleştirilmesi için klor gazından hidroklorik asit elde etmek ve sıhhi kolonların sulanması için klorür-alkali çözeltilerinin kullanımı için kısmen yönlendirilebilir. Teknik sonuç, güç tüketiminde bir azalma ve özerk üretim düzenleme olasılığıdır. 1 z.p.f.
Buluş, çeşitli endüstrilerde yaygın olarak kullanılan sodyum kloratın üretimi ile ilgilidir. Dünya sodyum klorat üretimi yılda birkaç yüz bin tona ulaşıyor. Sodyum klorat, uranyum cevherinin işlenmesi sırasında metalurjide klor dioksit (ağartıcı), potasyum klorat (Bertolet tuzu), kalsiyum ve magnezyum kloratlar (yaprak dökücüler), sodyum perklorat (katı roket yakıtı üretimi için bir ara madde) üretmek için kullanılır, vb. Sodyum hidroksit çözeltilerinin sodyum klorat elde etmek için klorlamaya tabi tutulduğu, kimyasal bir yöntemle sodyum klorat üretmek için bilinen bir yöntem. Teknik ve ekonomik göstergelerine göre, kimyasal yöntem elektrokimyasal yöntemle rekabet edemez, bu nedenle şu anda pratik olarak kullanılmamaktadır (L.M. Yakimenko "Klor, kostik soda ve inorganik klor ürünleri üretimi", Moskova, "Kimya" dan, 1974, s. .366). Kristalli sodyum kloratın buharlaştırma ve kristalizasyon yoluyla izole edildiği klorür-klorat çözeltileri elde etmek için diyaframsız elektrolizörlerin bir kademesinde bir sodyum klorür çözeltisinin elektrolizi yoluyla sodyum klorat üretmek için bilinen bir yöntem (K. Wihner, L. Kuchler "Chemische Technologie", Bd.1, "Anorganische Technologie", s.729, München, 1970; L.M. Yakimenko, T.A. Seryshev "İnorganik bileşiklerin elektrokimyasal sentezi, Moskova, "Kimya", 1984, s. 35-70. Bu yöntem, en yakın Ana teknolojik aşama, sodyum klorür çözeltilerinin diyaframsız elektrolizi, % 85-87'lik bir akım çıkışı ile ilerler. g/l aşındırıcı sodyum hipokloriti yok etmek için indirgeyici ajan ilavesiyle, her zaman elektroliz ürünlerinde bulunur. Klorür çözeltilerinin elektrolizindeki bir yan anot işlemi, yalnızca mevcut verimliliği azaltmakla kalmayıp aynı zamanda bir alkali çözeltisi ile sulanan sıhhi kolonlardaki elektroliz gazlarının saflaştırılmasını gerektiren Cl2'nin salınmasıdır. Bu nedenle işlemin uygulanması önemli miktarda hidroklorik asit ve alkali tüketimi ile ilişkilidir: 1 ton sodyum klorat ~120 kg %31 hidroklorik asit ve 44 kg %100 NaOH tüketir. Aynı nedenden dolayı, klor elektrolizinin olduğu yerde klorat üretimi düzenlenir, bu da kostik soda ve elektrolitik klor ve hidroklorik asit sentezi için hidrojen sağlarken, genellikle klor üretiminden uzak noktalarda otonom sodyum klorat üretimine ihtiyaç vardır. Ancak klor üretimi ve klorat elektrolizi yakınlarda olsa bile, klor elektrolizi bir nedenden dolayı durdurulduğunda ve kapatıldığında, klorat elektrolizinin zorla kapatılması meydana gelir.Bu nedenle, bilinen yöntemin önemli dezavantajları vardır: yüksek enerji maliyetleri (çok yüksek değil) mevcut verimlilik ) ve özerk üretimi organize etmenin imkansızlığı. Buluşun amacı, azaltılmış enerji maliyetleri ile sodyum klorür çözeltilerinin elektrolizi yoluyla sodyum klorat üretmek için bir yöntem yaratmaktır. Sorun, sodyum klorürün önce klor diyaframlı elektrolizörlerde işlenerek gaz halinde klor gazı ve 120-140 g/l NaOH ve 160-180 g/l NaCl'den oluşan elektrolitik kostik bileşimleri üretmek üzere işlendiği, önerilen yöntemle çözülür. veya kısmen kendi aralarında 50-60 g/l NaClO3 ve 250-270 g/l NaCl klorür-klorat çözeltisi elde ederek, bezdiafram elektrolizine gönderilen etkileşime tabi tutulur. Diyaframsız klorat elektroliz işlemi, hidroklorik asit ile asitleştirme yoluyla gerçekleştirilir. Sodyum klorür de içeren nihai klorat çözeltisi, buharlaştırma aşamasına gönderilir ve daha sonra kloratın kristalizasyonu sağlanır. Diyafram elektrolizinden gelen alkali ve klor etkileşiminin ürünleri ile birlikte kristalizasyon aşamasından gelen ana likör, diyaframsız klorat elektrolizine gönderilir. Katı ürünün izolasyon aşamasına girmeden önce elektrolit, sodyum hipokloriti yok etmek için bir indirgeyici ajan ilavesiyle 1 g/l'lik bir alkali fazlalığına alkalileştirilir. Elektroliz ürünlerinin klor diyaframlı elektrolizörlerinden kısmen çekilmesiyle, klorat elektrolizini asitleştirmek için kullanılan hidroklorik asit üretmek için klor kullanılır ve elektroliz gazlarının saflaştırılması sırasında sıhhi kolonları sulamak için alkali kullanılır. Bu şema ile, ilk çözeltinin her litresinde bulunan 300-310 g'dan 30-35 g sodyum klorür, klor elektrolizi koşulları altında işlenir. Böyle bir şema, enerji maliyetlerinde bir azalmaya neden olur, çünkü. klor elektrolizinin mevcut verimliliği daha yüksektir ve elektrolizörlerdeki voltaj, klorat elektrolizinden daha düşüktür ve klor elektrolizi koşulları altında sodyum klorürün kısmen elektrokimyasal olarak oksitlenmesi durumunda, tüm sürecin performansı artar. Ek olarak, açıklanan şema kullanıldığında, klor elektrolizörlerinin soğutmaya ihtiyacı olmadığından elektroliz soğutmanın maliyeti azalır. Klor elektrolizi koşulları altında belirtilenden (yaklaşık %10) daha derin bir klorür aktivasyonunun, klorürler, kloratlar ve su için teknolojik şemayı dengelemenin imkansızlığına yol açtığına ve bu nedenle mantıklı olmadığına dikkat edin. Önerilen şema çerçevesinde, klor içeren inertlerin klorlama için, NaOH içinde diyafram lye'den daha konsantre alkali çözeltilerden elde edilen klorat elektrolizine artan NaClO3 konsantrasyonuna sahip çözeltiler uygularken ek bir etki elde etmek mümkündür. yararlanılabilir. Elektrolitik klor elektrolizi, klor gazı ile tamamen değil, kısmen karıştırılabilir. Aynı zamanda, diyafram elektrolizinden elde edilen ve klorlamaya yönelik olmayan elektrolitik çözeltinin bir kısmı, sıhhi kolonlarda kullanılmak üzere yönlendirilir ve elektrolitik klorun eşdeğer kısmı hidroklorik asit sentezi için kullanılabilir. Diyaframlı elektrolizörlerden sıhhi kolonlara elektrolitik alkalilerin yönü ve hidroklorik asit üretmek için elektrolitik klor gazının yönü, alkali ve asidin dışarıdan tedarik edilmesi artık gerekmeyeceğinden, otonom klorat üretimi sorununu çözmektedir. Klor elektrolizörlerinde işlenen sodyum klorür oranı, kristalizasyon aşamasından diyaframsız elektrolize kadar ana likörle karıştırıldıktan sonra, ortaya çıkan ürünlerin etkileşimlerinin bir sonucu olarak sadece klorür-klorat likörleri elde etmek için kullanılıp kullanılmayacağına göre belirlenir veya klor elektrolizörlerinin elektrolikörü sadece alkalizasyon için ve elektrolitik klor - klorat elektroliz devresinde asitleştirme için perklorik asit sentezi için kullanılacaktır veya ürünlerin bir kısmı bir yönde ve bir kısmı diğerinde kullanılacaktır. Önerilen yöntemin avantajları şunlardır: 1) konvansiyonel klorat elektrolizinden daha düşük bir voltajda ve yüksek akım çıkışı ile elektrolizin ilk aşaması nedeniyle enerji maliyetlerinin azaltılması: klor elektrolizinde akım çıkışı %92-94 ve voltaj 3,2 V kloratta sırasıyla %85-90 ve 3.4 V ve üstü; 2) sıhhi kolonların alkalizasyonu ve sulanması için teknolojik şemanın gerektirdiği ana ürün - sodyum klorat - alkali çözeltilerle aynı anda elde etme olasılığı; 3) klorat elektrolizinin asitleştirilmesi için yerinde hidroklorik asit üretmek için klor elektrolizörlerinde üretilen kloru kullanma olasılığı. Örnek Deneysel bir hücrede, 300 g/l konsantrasyonlu bir sodyum klorür çözeltisinin klor diyafram elektrolizi, 1000 A/m 2 akım yoğunluğunda ve 90 o C sıcaklıkta rutenyum oksit anotları üzerinde gerçekleştirilir. 140 g/l NaOH ve 175 g/l NaCl içeren, anot klor gazı ile karıştırılmış ve 270 g/l NaCl ve 50 g/l NaCl03'ten oluşan klorür-klorat çözeltisi bileşimini alır. Bu çözelti daha sonra aşağıdaki bileşimin nihai bir çözeltisini elde etmek için 1000 A/m2 akım yoğunluğunda ve 80 o C sıcaklıkta rutenyum oksit anotlu 4 elektrolizörden oluşan bir kademede gerçekleştirilen diyaframsız bir klorat elektrolizine beslenir. : 105 g/l NaCl ve 390 g/l NaClO3 . Böylece, su buharının elektroliz gazları ile sürüklenmesi ve 50 g olan 355 g sodyum kloratın buharlaşması nedeniyle çözeltinin hacminde% 10'luk bir azalma hesaba katılarak, 1 litre ilk klorür çözeltisinden ( Klor diyafram elektrolizi ürünlerinin karıştırılmasından sonra %14.1) elde edildi ve klorat elektrolizi işleminde 305 (%85.9) üretildi. Klor hücresindeki voltaj, %93'lük bir akım çıkışıyla 3,3 V idi. Klorat hücresindeki ortalama voltaj, %85'lik bir akım çıkışıyla 3.4 V idi. Spesifik güç tüketimi W (kWh/t) deneysel verilere göre W = 1000E/mBT formülü kullanılarak hesaplanmıştır, burada E hücre voltajıdır (B); m - elektrokimyasal eşdeğer (g/Ah); BT - bir birimin kesirlerinde akım çıkışı,
klor elektrolizi için 2517 kWh / t ve klor elektroliz ürünlerinin karıştırılması sonucu üretilen kloratın payı dikkate alındığında 5404.9 kWh / t veren klorat elektrolizi için 5996 kWh / t olarak gerçekleşti. Aynı tesiste klor elektrolizörü kullanılmadan elektrik tüketimi 6150 kWh/t idi. Böylece enerji maliyetlerindeki azalma %12,1 olarak gerçekleşti.
İddia
1. Bir sodyum klorür çözeltisinin elektrolizi, ardından klorür-klorat çözeltilerinin buharlaştırılması ve kristalizasyon aşamasının ana sıvısının işleme geri döndürülmesiyle sodyum kloratın kristalleştirilmesi yoluyla sodyum klorat üretmek için bir yöntem olup, karakterize edici özelliği, önce elektrolizin bir sodyum klorür çözeltisinin bir klorür-diyafram elektrolizörlerinde, bir klorür-klorat çözeltisi elde etmek için karıştırılan ve kristalizasyon aşamasının ana likörü ile karıştırıldıktan sonra diyaframsız ortama gönderilen alkali klorür çözeltileri ve elektrolitik klor gazı elde etmek için gerçekleştirilir. elektroliz. 2. Diyafram elektrolizinin ürünlerinin, klorat elektrolizinin asitleştirilmesi için klor gazından hidroklorik asit elde etmek ve sıhhi kolonların sulanması için klorür-alkali çözeltilerinin kullanılması için kısmen uzaklaştırılmasıyla karakterize edilen, istem l'e göre yöntem.
Sodyum perklorat kristal madde renksiz ve kokusuz. Higroskopiktir ve birkaç kristal hidrat oluşturur. İTİBAREN kimyasal nokta görme, perklorik asidin sodyum tuzudur. Yanıcı değildir, ancak toksik etkisi vardır. Kimyasal formül sodyum perklorat - NaClO 4 .
Fiş
Tarif edilen madde hem kimyasal hem de elektrokimyasal olarak elde edilebilir. İlk durumda, genellikle perklorik asit ile sodyum hidroksit veya karbonat arasındaki olağan değişim reaksiyonu kullanılır. Sodyum kloratın termal bozunması da mümkündür. 400-600 °C'de perklorat ve sodyum klorür oluşturur. Ancak bu yöntem oldukça tehlikelidir, çünkü reaksiyon sırasında patlama tehdidi vardır.
Teorik olarak, sodyum kloratın kimyasal oksidasyonunu gerçekleştirmek mümkündür. Bu durumda en etkili oksitleyici ajan, asidik bir ortamda kurşun (IV) oksit olacaktır. Tipik olarak, reaksiyon karışımına perklorik asit eklenir.
Çoğu zaman endüstride elektrokimyasal yöntem kullanılır. Daha temiz bir ürün verir ve genellikle daha etkilidir. Aynı sodyum klorat, bir platin anot üzerinde oksitlendiğinde perklorat veren bir hammadde olarak kullanılır. İşlemin ekonomisi için, grafit gibi daha ucuz elektrotlarda sodyum klorat elde edilir. Tek aşamada sodyum perklorat elde etmek için umut verici bir yöntem de vardır. Anot olarak kurşun peroksit kullanılır.
Elektrokimyasal üretim için mekanizmalar
Kloratın perklorata oksidasyon mekanizması henüz tam olarak çalışılmamıştır, bununla ilgili sadece varsayımlar vardır. Araştırma halen devam etmektedir.
En makul seçenek, klorat iyonunun (ClO3 -) anotunda elektron bağışı varsayımına dayanır, bu da ClO3 radikalinin oluşumuyla sonuçlanır. Sırasıyla su ile reaksiyona girerek perklorat oluşturur.

Bu varsayım, bir dizi yetkili bilimsel çalışmalar. Ayrıca, ağır oksijen izotopları 18 O ile etiketlenmiş sulu çözeltilerde kloratların perkloratlara oksidasyon süreçlerinin çalışmalarının sonuçlarıyla da doğrulanmıştır. 18 O'nun ilk önce kloratın bileşimine dahil olduğu ve ancak daha sonra, sırasında olduğu bulunmuştur. oksidasyon işlemi, perklorat iyonunun bileşimine geçer. Ancak anot malzemesinin değiştirilmesinin (örneğin platinden grafite) reaksiyon mekanizmasını da değiştirebileceği dikkate alınmalıdır.
Proses akışının ikinci çeşidi, elektronlar hidroksit iyonu tarafından bağışlandığında oluşan klorat iyonlarının oksijen ile oksidasyonundan oluşur.

Bu varyanta göre, reaksiyon hızı doğrudan elektrolitteki klorat konsantrasyonuna bağlıdır, yani konsantrasyonunda bir azalma ile hız artmalıdır.
Hem klorat iyonu hem de hidroksit iyonu tarafından eşzamanlı elektron bağışına dayanan bir varyant da vardır. Reaksiyonlar sonucunda oluşan radikaller oldukça aktiftir ve OH - 'den salınan oksijen tarafından oksitlenir.

Fiziksel özellikler
Sodyum perklorat suda çok çözünür. Çözünürlüğü diğer perkloratlardan çok daha güçlüdür. Bu nedenle perkloratların üretiminde önce sodyum perklorat elde edilir, daha sonra gerekirse diğer perklorik asit tuzlarına dönüştürülür. Ayrıca sıvı amonyak, aseton, hidrojen peroksit, etanol ve etilen glikolde yüksek oranda çözünür.

Yukarıda bahsedildiği gibi higroskopiktir ve hidroliz üzerine sodyum perklorat kristalli hidratlar (mono- ve dihidratlar) oluşturur. Ayrıca diğer bileşiklerle solvatlar oluşturabilir. 482 ° C sıcaklıkta, sodyum klorür ve oksijene ayrışma ile erir. Sodyum peroksit, manganez (IV) oksit, kobalt (II, III) oksit katkı maddeleri kullanıldığında, ayrışma sıcaklığı 150-200 °C'ye düşer.
Kimyasal özellikler
Perklorik asidin sodyum tuzu çok güçlü bir oksitleyici ajandır, öyle ki birçok organik maddeyi karbondioksit ve suya oksitler.
Perklorat iyonu, amonyum tuzları ile reaksiyona girerek tespit edilebilir. Karışım kalsine edildiğinde reaksiyon ilerler:
3NaClO4 + 8NH4NO3 → 3KCl + 4N 2 + 8HNO 3 + 12H 2 O.
Başka bir saptama yöntemi, potasyum ile bir değişim reaksiyonudur. Potasyum perklorat suda çok daha az çözünür, bu nedenle çökelecektir.
NaClO 4 + KCl → KClO 4 ↓ + NaCl.
Diğer perkloratlarla karmaşık bileşikler oluşturabilir: Na 2 , Na, Na.
Başvuru
Kristalli hidratların oluşumu nedeniyle sodyum perklorat kullanımı son derece zordur. Son zamanlarda giderek daha az olmasına rağmen, esas olarak bir herbisit olarak kullanılır. Hemen hemen tüm sodyum perklorat, diğer perkloratlara (örneğin potasyum veya amonyum) veya perklorik aside dönüştürülür ve güçlü oksitleyici özelliklerinden dolayı diğer birçok bileşiğin sentezinde kullanılır. Hem sulu hem de alkollü çözeltilerden potasyum, rubidyum ve sezyum katyonlarının belirlenmesi ve çökeltilmesi için analitik kimyada da kullanılabilir.
Tüm perkloratların termal ayrışması oksijeni serbest bırakır. Bu nedenle tuzlar oksijen kaynağı olarak kullanılabilir. roket motorları. Bazı perkloratlar patlayıcılarda kullanılabilir. Potasyum perklorat, tıpta hipertiroidizmi tedavi etmek için kullanılır. Bu hastalığa tiroid bezinin artan işlevi neden olur ve herhangi bir perklorat, vücudu normale döndürmek için gerekli olan bu bezin aktivitesini azaltma yeteneğine sahiptir.
Tehlike
Sodyum perkloratın kendisi yanıcı değildir, ancak diğer bazı maddelerle etkileşime girerse yangına veya patlamaya neden olabilir. Yangında zehirli gazlar veya buharlar (klor veya klor oksitler) açığa çıkarabilir. Söndürme su ile yapılabilir.
Sodyum perklorat oda sıcaklığında pratik olarak buharlaşmaz, ancak püskürtüldüğünde vücuda girebilir. Solunduğunda öksürüğe, mukoza zarının tahriş olmasına neden olur. Cilt ile temasında kızarıklık görülür. İlk yardım olarak, etkilenen bölgenin bol miktarda sabun ve su ile yıkanması ve kirlenmiş giysilerden kurtulması tavsiye edilir. Vücuda uzun süre maruz kaldığında kan dolaşımına girer ve methemoglobin oluşumuna yol açar.
Hayvanlara (özellikle kemirgenlere) 0.1 g sodyum perklorat enjekte edildiğinde, refleks uyarılabilirlikleri arttı, konvülsiyonlar ve tetanoz ortaya çıktı. 0.22 g uygulamadan sonra, sıçanlar 10 saat sonra öldü. Güvercinlere aynı doz verildiğinde, sadece hafif zehirlenme belirtileri geliştirdiler, ancak 18 saat sonra öldüler. Bu, sodyum perklorat uygulamasının çok yavaş geliştiğini göstermektedir.
Sodyum, kalsiyum ve magnezyum kloratlar hala seçici olmayan herbisitler olarak kullanılmaktadır - demiryolu raylarının, endüstriyel sitelerin vb. temizliği için; pamuk hasadında yaprak dökücü olarak. Kloratların asit ayrışması, yüksek mukavemetli hamuru ağartmak için "yerinde" (yerinde) klor dioksit üretiminde kullanılır.
K2 Ne yazık ki, bu yöntemin ciddi bir dezavantajı, ev tipi dezenfektanların ve ağartıcıların düşük kalitede olmasıdır. "Zorunlu standardizasyon" politikasını yumuşattıktan sonra, "beyazlık" ürünlerinin üreticileri, üründeki hipoklorit içeriğini standart ağırlıkça %5'ten düşürerek kendi özelliklerini kullanmaya başladılar. %3'e kadar veya daha az. Şimdi, aynı miktarda kloratı iyi bir verimle elde etmek için, yalnızca çok daha fazla "beyazlık" kullanmak değil, aynı zamanda suyun çoğunun çözeltiden çıkarılması gerekir. Belki de en uygun olanı, kısmi dondurma yoluyla "beyazlığı" önceden konsantre etmek olabilir.
Deniz atıkları için profesyonel sıvı nötrleştiriciler %40'a kadar sodyum hipoklorit içerir.
K3 Hipokloritin klorür ve klorata orantısızlığı pH'ta yüksek oranda ilerler
K4 Gerçekten de, elektroliz için önemli bir güce sahip yüksek verimli bir güç kaynağı, vakanın başarısının yarısıdır ve özel bir tartışma konusudur.
Burada elektrik güvenliği kurallarına uyulması gerektiğini hatırlatmak isterim.
Önemli ölçekte elektroliz ile ilgili işler, özellikle imha açısından tehlikeli olarak kabul edilir. Elektrik şoku. Bunun nedeni, deneycinin derisinin iletken elektrolit ile temasının neredeyse kaçınılmaz olmasıdır. Elektrotlarda gaz verilmesi, özellikle cebri hava soğutması kullanıldığında elektrikli ekipman bileşenleri üzerinde birikebilen aşındırıcı elektrolit aerosollerinin oluşumuna neden olur. Sonuçlar çok üzücü olabilir - metal parçaların korozyonundan ve güç kaynağının arızalanmasından hücre üzerindeki ana voltaj ile yalıtımın bozulmasına ve deneyci için tüm sonuçlara kadar.
Tesisin yüksek voltajlı parçaları hiçbir koşulda elektrolitik hücrenin yakın çevresine kurulmamalıdır. Güç kaynağının tüm bileşenleri, hücreden yeterli bir mesafeye ve bir hücre kazası durumunda üzerlerine elektrolit girmesini ve iletken aerosollerin birikmesini tamamen önleyecek şekilde yerleştirilmelidir. Bu durumda, kaynaktan elektrolizöre giden yüksek akım telleri, işlem akımına karşılık gelen yeterli bir kesite sahip olmalıdır. Doğrudan şebekeye bağlı tüm iletkenler (ve bağlantıları) neme dayanıklı yalıtımla hava geçirmez şekilde kapatılmalıdır.
Hücrenin şebekeden zorunlu galvanik izolasyonu. Geleneksel bir transformatör yeterli yalıtım sağlar, ancak elektrolizöre doğrudan LATR vb. gibi ototransformatörlerden güç verilmesi kesinlikle yasaktır, çünkü bu durumda elektrolizör ağın faz kablosuna doğrudan bağlanabilir. Ancak, ana transformatörün birincil sargısındaki voltajı düzenlemek için LATR (veya ev tipi ototransformatör) kullanılabilir. Sadece LATR'nin gücünün ana transformatörün gücünden daha az olmadığından emin olmanız gerekir.
Tesisatın uzun süreli çalışması için elektronik bileşenlerin aşırı ısınmadan ve kısa devrelerden korunması faydalı olacaktır. Başlangıç olarak, nominal gücüne karşılık gelen bir akım için transformatörün birincil sargısına bir sigorta takmakla kendinizi sınırlamak oldukça mümkündür. Hücrede bir kısa devrenin oldukça olası olduğu akılda tutularak, hücreye uygun bir sigorta (daha iyi - ayarlanabilir bir elektromanyetik serbest bırakma) aracılığıyla güç sağlanması da mantıklıdır.
Bu durumda kurulumu topraklama ihtiyacı sorusu o kadar basit değil. Gerçek şu ki, birçok yerleşim yerinde topraklama başlangıçta yoktur ve bunu kendi başınıza düzenlemek kolay değildir. Bazı durumlarda, topraklama yerine, kurnaz elektrikçiler "sıfırlama" düzenleyerek toprak veri yolunu ve ağı doğrudan tüketiciye nötr olarak bağlar. Bu durumda, "topraklanmış" cihaz doğrudan ağın akım taşıyan devresine bağlanır. Koşullarımız altında, elektrolizörün ağdan ve deneycinin tüm tesisattan yüksek kaliteli izolasyonuna öncelik verilmesi önerilebilir.
Amatör bir laboratuvarda yapılan uzun bir deney, deneycinin beceri ve davranışlarını kontrol edemediği diğer kişilerin her zaman dikkatini çekeceği için güvenlik kuralları ihmal edilmemelidir. Çevrenizdekilerin farkında olun ve güvenle çalışın.
Ayrıca kayıtlı: Amerika Birleşik Devletleri
Temel bilgiler:
| Otun tüm kısımlarına yayılan sistemik geniş spektrumlu. Tüm işletmeler için fitoksik. |
| Beyaz toz |
Serbest bırakmak:
sodyum klorat: çevredeki davranış
| dizin | Anlam | Açıklama | ||
| 20 o C'de suda çözünürlük (mg/l) | 650000 A5 Yüksek||||
| 20 o C'de organik çözücülerde çözünürlük (mg/l) | Çözünmeyen A5 - Çoğu organik Çözücü -||||
| Erime noktası (o C) | 255A5-||||
| Kaynama noktası (o C) | A4'ü kaynatmak için ayrışır -||||
| Bozunma sıcaklığı (o C) | 260A3-||||
| Parlama noktası (o C) | Yanıcılık yüksek değil A5 -||||
| pH 7, 20 o C'de oktanol/suda bölünme katsayısı | P: 1.26 X 10 -03 Hesaplanmış -||||
| Özgül ağırlık (g/ml) / Spesifik yer çekimi | 2.499 L3-||||
| 25 o C'de ayrışma sabiti (pKa) | -2 A4 -||||
| Not: Çok güçlü asit | ||||
| 25 o C'de buhar basıncı (MPa) | 5.2 X 10 -06 A2 Ara durum||||
| 25 o C'de Henry yasası sabiti (Pa * m 3 / mol) | 5.2 X 10 -09 A3 - Uçucu değil||||
| 20 o C'de Henry yasası sabiti (boyutsuz) | 3.50 X 10 -16 Hesaplanmış Uçucu değil||||
| Toprakta çürüme süresi (gün) | DT50 (tipik) 200 F3 Kararlı||||
| Avrupa Birliği laboratuvar çalışmalarına göre DT50 46.7-314.6 gündür. | ||||
| pH 7'de sulu fotoliz DT50 (günler) | Değer: Kararlı A5 Kararlı||||
| - | ||||
| DT50'nin 20 o C ve pH 7'de sulu hidrolizi (günler) | Değer: Kararlı A5 Çok kararlı||||
| pH'a duyarlı değil | ||||
| Su yağışı DT50 (gün) | - - -||||
| Sadece su fazı DT50 (gün) | - - -||||
| GUS arınma potansiyeli endeksi | 6.90 Hesaplanmış Yüksek Liç||||
| 1 kg/ha (l/ha) uygulama oranında yeraltı suyu SCI'sinde (µg/l) konsantrasyon büyüme indeksi | Değer: 4.51 X 10 +01 Hesaplanmış -||||
| - | ||||
| Partikül bağlı taşıma indeksi potansiyeli | - Ortalama hesaplanır||||
| Koc - organik karbon bölünme katsayısı (ml/g) | 10 F3 Çok hareketli||||
| pH direnci: | ||||
| Not: | ||||
| Freundlich adsorpsiyon izotermi | kf:-- | -|||
| - | ||||
| Maksimum UV absorbansı (l/(mol*cm)) | - - -||||
sodyum klorat: ekotoksisite
| dizin | Anlam | Kaynak / Niteliksel göstergeler / Diğer bilgiler | Açıklama | |
| Biyokonsantrasyon katsayısı | BCF:-- | -|||
| biyobirikim potansiyeli | - Hesaplanan Düşük||||
| LD50 (mg/kg) | > 5000 A5 Sıçan Düşük||||
| Memeliler - Kısa süreli gıda NOEL | (mg/kg): -- | -|||
| Kanatlı - Akut LD50 (mg/kg) | 2510 A5 Yeşilbaş Ördek Düşük||||
| Kuşlar - Akut toksisite (CK50 / LD50) | - - -||||
| Balık - Akut 96 saat CK50 (mg/l) | 10000 G2 Bilinmeyen türler Düşük||||
| Balık - Kronik 21 günlük NOEC (mg/L) | 500 A5 Danio yeniden -||||
| Suda Omurgasızlar - Akut 48 saat EC50 (mg/L) | 919.3 A5 Kısa||||
| Su Omurgasızları - Kronik 21 günlük NOEC (mg/L) | 500 A5 Daphnia magna (Daphnia büyük, Su piresi büyük) -||||
| Sucul kabuklular - Akut 96 saat CK50 (mg/l) | - - -||||
| Alt mikroorganizmalar - Akut 96 saat CK50 (mg/l) | - - -||||
| NOEC , statik, Su (mg/l) | - - -||||
| Alt mikroorganizmalar - Kronik 28 günlük NOEC , Sedimanter kaya (mg/kg) | - - -||||
| Su bitkileri - Akut 7 günlük EC50 , biyokütle (mg/l) | 134 A5 küçük su mercimeği Kısa||||
| Yosun - Akut 72 saatlik EC50 büyümesi (mg/L) | 1595 A5 Yeşil algler (Scenedesmus subspicatus) Kısa||||
| Yosun - Kronik 96 saatlik NOEC , büyüme (mg/l) | - - -||||
| Arılar - Akut 48 saat LD50 (mcg/bireysel) | > 75 A5 Oral Orta||||
| Solucanlar - Akut 14 günlük CK50 (mg/kg) | > 750 A5 Orta||||
| Toprak Solucanları - Kronik 14 Günlük Maksimum İnaktif Konsantrasyon, Üreme (mg/kg) | - - -||||
| Diğer Eklembacaklılar (1) | LR50 (g/ha): 84,4 A5 yırtıcı akar 1 kg/ha'da orta derecede tehlikeli||||
| Diğer Eklembacaklılar (2) | LR50 (g/ha): 250,6 A5 Binici 1 kg/ha'da orta derecede tehlikeli||||
| toprak mikroorganizmaları | Azotun mineralizasyonu: -47Aksiyon (%)||||
| Mesoworld (mezokozm) hakkında mevcut veriler | NOEAEC mg/l: - - -||||
sodyum klorat: insan sağlığı
Temel özellikleri:
| dizin | Anlam | Kaynak / Niteliksel göstergeler / Diğer bilgiler | Açıklama | |
| Memeliler - Akut oral LD50 (mg/kg) | > 5000 A5 Sıçan Düşük||||
| Memeliler - Dermal LD50 (mg/kg vücut ağırlığı) | > 2000 A5 Sıçan -||||
| Memeliler - Soluma CK50 (mg/l) | > 3.9 A5 Sıçan -||||
| ADI - kabul edilebilir günlük doz (günde mg / kg vücut ağırlığı) | Tanımlanmamış A5 -||||
| ARfD - ortalama günlük alım (günde mg/kg vücut ağırlığı) | Tanımlanmamış A5 -||||
| AOEL - bir operatör için tolere edilebilir sistemik maruziyet seviyesi | 0.35 A5 Sıçan, SF=200 -||||
| Cilt emilimi (%) | - - -||||
| Tehlikeli Maddeler Direktifi 76/464/EC | - - -||||
| kısıtlama türleri | - - -||||
| kategoriye göre | Genel:||||
| , | ||||
| Avrupa örnekleri | ||||