Tijela sa električnim nabojem istog znaka međusobno
DVIJE VRSTE NAPLATA
Postoje dvije vrste električnih naboja: pozitivni i negativni.
INTERAKCIJA NAPUNJENIH TIJELA
Naelektrisana tela međusobno deluju:
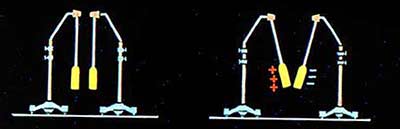
Tijela s električnim nabojem istog znaka se međusobno odbijaju. 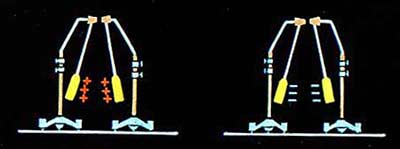 A tijela koja imaju naboje suprotnog predznaka privlače jedno drugo.
A tijela koja imaju naboje suprotnog predznaka privlače jedno drugo.
ELEKTROSKOP
Postoje dvije blisko povezane vrste instrumenata za detekciju električnih naboja: elektroskop ili elektrometar.
Elektroskop se sastoji od metalne šipke koja je provučena kroz dielektrični utikač i dvije latice od metalne folije obješene na nju. Kada se štap dotakne nabijenim tijelom, listovi su nabijeni istim imenom i odstupaju jedan od drugog.
U elektrometru je metalna igla spojena na metalnu šipku koja se može slobodno rotirati. Kada nabijeno tijelo dodirne štap, strelica prima naboj istog predznaka i pokušava se odbiti od slično nabijenog štapa, pokazujući veličinu naboja na mjernoj skali.
Po veličini ugla divergencije latica elektroskopa ili po kutu otklona igle elektrometra može se suditi o veličini električnog naboja.
Naelektrisani elektroskop vam omogućava da otkrijete naelektrisanje čiji znak je telo naelektrisano.
ZNAŠ LI
Da je naučnik Robert Bojl rođen u Irskoj 1627.
Nauka 17. veka poznavala je dve manifestacije električno polje električno privlačenje i odbijanje. Boyle je putem eksperimenata dokazao da električni eksperimenti rade u vakuumu na isti način kao i u običnim uvjetima. Odnosno, sa moderne tačke gledišta, zaključeno je da električno polje može postojati u vakuumu.
Boyle je napravio niz zapažanja o svojstvima naelektriziranih tijela. Na primjer, da dim privlače i naelektrizirana tijela, i da ne samo da naelektrizirano tijelo privlači neelektrificirano, već i obrnuto, prvo privlači drugo.
KAKO JE IZMIŠLJEN ELEKTROSKOP?
Kao što znate, prvi prihvatljiv dizajn elektroskopa predložio je G.V. Richman, koji je mjerio električni naboj odstupanjem od nabijenog postolja lanene niti.
Na donji kraj motke pričvršćeno je željezno ravnalo, na čiji je gornji dio bio zalijepljen svileni konac. Kada se grmljavina približila, metalni stup i ravnalo sa navojem bili su nabijeni, a nit je, odbijena od njega, odstupila za određeni ugao. Uz blisku i jaku grmljavinu, iskre su uklonjene sa lenjira.
Zatim, u iste svrhe, Abbé Nollet je predložio korištenje dvije međusobno odbojne niti.
Član Kraljevskog društva u Londonu, John Canton, 1753. godine razvio je dizajn u kojem niti više ne reagiraju tako osjetljivo na kretanje zraka ili na disanje eksperimentatora. Na krajeve konca kačio je kuglice plute ili bazge.
Ovako je raspoređen Kantonov elektroskop: "Okačite dvije kuglice od plute veličine graška svaka sa plafona na lanene niti tako da se dodiruju. Donesite staklenu cijev pobuđenu elektricitetom na kuglice odozdo - tada će kuglice raspršiti se."
Godine 1781. Volta je poboljšao elektroskop tako što je kuglice od bazge zamijenio s dvije lagane, suhe slamke koje su bile okačene na donji kraj metalne šipke. Kada je uređaj spojen na elektrificirano tijelo, slamke su se odbijale, pa se moglo procijeniti da li je tijelo napunjeno ili ne. Ovaj elektrometar je bio prilično osjetljiv instrument.
Godine 1799. engleski naučnik T. Cavallo predložio je izuzetno jednostavno i efikasno poboljšanje elektroskopa. Elektroskop od plute Kantona zatvorio je u prozirnu staklenu posudu. Sada ni protok vazduha ni vlaga nisu imali uticaja na očitavanja uređaja.
elektrifikacija tel.
2. Elektrifikacija tijela.
Ovi fenomeni su otkriveni u antičko doba. Drevni grčki naučnici su primijetili da ćilibar (okamenjena smola četinara koja je rasla na Zemlji prije mnogo stotina hiljada godina), kada se trlja vunom, počinje privlačiti različita tijela k sebi. Na grčkom, ćilibar je elektron, pa otuda i naziv "elektricitet".
Za tijelo koje nakon trljanja privlači druga tijela k sebi, kaže se da je naelektrizirano ili da mu je prenesen električni naboj.
Tijela napravljena od različitih tvari mogu se naelektrizirati. Lako je naelektrizirati štapove od gume, sumpora, ebonita, plastike, najlona trljanjem vune o vunu.
Elektrifikacija tijela nastaje kada tijela dođu u kontakt, a zatim se odvoje. Trljanje tijela jedno o drugo samo da bi se povećala površina njihovog kontakta.
Dva tijela su uvijek uključena u elektrifikaciju: u eksperimentima o kojima smo gore govorili, staklena šipka je došla u kontakt sa listom papira, komad ćilibara - s krznom ili vunom, štap od pleksiglasa - sa svilom. U ovom slučaju oba tijela su naelektrizirana. Na primjer, kada staklena šipka i komad gume dođu u kontakt, i staklo i guma se naelektriziraju. Guma, poput stakla, počinje privlačiti svjetlosna tijela.
Električno punjenje mogu se prenositi s jednog tijela na drugo. Da biste to učinili, trebate dodirnuti drugo tijelo s naelektriziranim tijelom, a zatim će dio električnog naboja proći na njega. Da biste bili sigurni da je i drugo tijelo naelektrizirano, potrebno je do njega donijeti male komadiće papira i vidjeti hoće li se privući.
3. Dvije vrste optužbi. Interakcija naelektrisanih tela.
Sva naelektrisana tela privlače druga tela, kao što su komadi papira, k sebi. Prema privlačenju tijela, nemoguće je razlikovati električni naboj staklenog štapića utrljanog o svilu od naboja dobivenog na ebonitnom štapu koji se trlja o njih. Uostalom, oba elektrificirana štapa privlače komadiće papira.
Da li to znači da su optužbe primljene na tijela napravljene od razne supstance, ne razlikuju se jedno od drugog?
Okrenimo se eksperimentima. Naelektriziramo štap od ebonita okačen na konac. Donesimo još jedan sličan štap, naelektrisan trenjem o istom komadu krzna. Štapovi se odbijaju Budući da su štapovi isti i naelektrisali su ih trljanjem o isto tijelo, možemo reći da su imali naboje iste vrste. To znači da se tijela koja imaju naelektrisanje iste vrste međusobno odbijaju.
Sada stavimo staklenu šipku natrljanu o svilu na elektrificiranu šipku od ebonita. Vidjet ćemo da se stakleni i ebonitni štapići međusobno privlače (slika br. 2). Posljedično, naboj dobiven na staklu utrljanom o svilu je drugačije vrste nego na ebonitu utrljanom o krzno. Dakle, postoji još jedna vrsta električnih naboja.
Budimo se kako bismo na ovjesni elektrificirani štapić od ebonita donijeli naelektrizirana tijela iz raznih tvari: guma, pleksiglas, plastika, najlon. Vidjet ćemo da se u nekim slučajevima štap od ebonita odbija od tijela koja su mu dovedena, au drugim se privlači. Ako se štap od ebonita odbije, tada tijelo koje mu je prineseno ima naboj iste vrste kao na njemu. A naboj tih tijela, kojima je privučen ebonitni štap, sličan je naboju dobivenom na staklu utrljanom o svilu. Stoga možemo pretpostaviti da postoje samo dvije vrste električnih naboja.
Naboj dobijen na staklu trljanom o svilu (i na svim tijelima gdje se dobije naboj iste vrste) nazivao se pozitivnim, a naboj dobiven na ćilibaru (kao i ebonit, sumpor, guma) trljanom o vunu nazivao se negativnim, odnosno optužbama su dodijeljeni znaci “+” i “-”.
I tako, eksperimenti su pokazali da postoje dvije vrste električnih naboja – pozitivni i negativni, te da naelektrizirana tijela međusobno djeluju na različite načine.
Tijela s električnim nabojem istog predznaka se međusobno odbijaju, a tijela sa naelektrisanjem suprotnog predznaka se međusobno privlače.
4. Elektroskop. Provodnici i neprovodnici električne energije.
Ako su tijela naelektrizirana, onda se privlače jedno drugo ili se odbijaju. Po privlačenju ili odbijanju može se procijeniti da li se tijelu prenosi električni naboj. Stoga se dizajn uređaja, uz pomoć kojeg se saznaje da li je tijelo naelektrizirano, temelji na interakciji nabijenih tijela. Ovaj uređaj se zove elektroskop (od grčkih riječi electron i scopeo - posmatrati, otkrivati).
U elektroskopu se metalna šipka provlači kroz plastični čep (sl. br. 3) umetnut u metalni okvir, na čijem su kraju pričvršćena dva lista tankog papira. Okvir je sa obje strane prekriven staklom.
Što je veći naboj elektroskopa, veća je odbojna sila listova i veći je ugao koji će se raspršiti. To znači da se promjenom ugla divergencije listova elektroskopa može procijeniti da li se njegov naboj povećao ili smanjio.
Ako rukom dodirnete nabijeno tijelo (na primjer, elektroskop), ono će se isprazniti. Električni naboji će proći do našeg tijela i kroz njega mogu otići do zemlje. Nabijeno tijelo će se također isprazniti ako je povezano sa zemljom metalnim predmetom, kao što je željezna ili bakarna žica. Ali ako je nabijeno tijelo povezano sa zemljom staklenom ili ebonitnom šipkom, tada električni naboji kroz njih neće ići u zemlju. U tom slučaju, napunjeno tijelo se neće isprazniti.
Prema sposobnosti provođenja električnih naboja, tvari se uvjetno dijele na provodnike i neprovodnike električne energije.
Svi metali, tlo, rastvori soli i kiselina u vodi su dobri provodnici struje.
Neprovodnici električne energije, ili dielektrici, uključuju porculan, ebonit, staklo, ćilibar, gumu, svilu, najlon, plastiku, kerozin, vazduh (gasovi).
Tijela napravljena od dielektrika nazivaju se izolatori (od grčke riječi isolaro - osamiti).
5. Deljivost električnog naboja. Elektron.
Napunimo metalnu kuglicu pričvršćenu za štap elektroskopa (slika br. 4a). Povežimo ovu kuglu sa metalnim provodnikom A, držeći je za dršku B, napravljenu od dielektrika, sa drugom potpuno istom, ali nenabijenom kuglom koja se nalazi na drugom elektroskopu. Polovina naboja će preći sa prve lopte na drugu (slika br. 4b). To znači da se početno punjenje prazni na dva jednaka dijela.
Sada odvojimo loptice i dodirnimo drugu loptu rukom. Od toga će izgubiti naboj - otpušten. Pričvrstimo ga ponovo na prvu kuglu, na kojoj ostaje polovina prvobitnog naboja. Preostali naboj će se ponovo podijeliti na dva jednaka dijela, a četvrti dio prvobitnog naboja će ostati na prvoj kugli.
Na isti način može se dobiti jedna osmina, jedna šesnaesta naboja, itd.
Dakle, iskustvo pokazuje da električni naboj može imati različitu vrijednost. Električni naboj je fizička veličina.
Jedan privjesak se uzima kao jedinica električnog naboja (označena kao 1 C). Jedinica je dobila ime po francuskom fizičaru C. Coulomb-u.
U eksperimentu prikazanom na slici 4, pokazano je da se električni naboj može podijeliti na dijelove.
Postoji li podjela naplate?
Da bi se odgovorilo na ovo pitanje, bilo je potrebno izvesti složenije i preciznije eksperimente od gore opisanih, jer vrlo brzo naboj koji ostaje na kugli elektroskopa postaje toliko mali da ga nije moguće detektirati pomoću elektroskopa.
Da biste naboj podijelili na vrlo male dijelove, potrebno ga je prenijeti ne na kuglice, već na mala zrna metala ili kapljice tekućine. Mjerenjem dobijenog naboja na tako malim tijelima, ustanovljeno je da je moguće dobiti dijelove naboja koji su milijarde milijardi puta manji nego u opisanom eksperimentu. Međutim, u svim eksperimentima nije bilo moguće odvojiti naboj iznad određene vrijednosti.
To nam je omogućilo da pretpostavimo da električni naboj ima granicu djeljivosti, ili, preciznije, da postoje nabijene čestice koje imaju najmanji naboj, koje više nisu djeljive.
Kako bi dokazali da postoji granica podjele električnog naboja i utvrdili koja je to granica, naučnici su sproveli posebne eksperimente. Na primjer, sovjetski naučnik A.F. Ioffe postavio je eksperiment u kojem su male čestice prašine cinka, vidljive samo pod mikroskopom, bile naelektrizirane. Naboj čestica prašine se mijenjao nekoliko puta, a svaki put se mjerilo koliko se naboj promijenio. Eksperimenti su pokazali da su sve promjene naboja zrna prašine cijeli broj puta (tj. 2, 3, 4, 5, itd.) veće od nekog određenog najmanjeg naboja, tj. naboja zrna prašine promijenjene, doduše vrlo male, ali cijele porcije. Budući da naboj iz zrna prašine izlazi s česticom materije, Ioffe je zaključio da u prirodi postoji takva čestica materije koja ima najmanji naboj, koja više nije djeljiva.
Ova čestica se zove elektron.
Vrijednost naboja elektrona prvi je odredio američki naučnik R. Milliken. U svojim eksperimentima, sličnim onima A. F. Ioffea, koristio je male kapi ulja.
Naboj elektrona je negativan, jednak je 1,610 C (0,000 000 000 000 000 000 16 C). Električni naboj je jedno od osnovnih svojstava elektrona. Ovaj naboj se ne može "ukloniti" sa elektrona.
Masa elektrona je 9,110 kg, to je 3700 puta manje od mase molekula vodonika, najmanjeg od svih molekula. Krilo muhe ima masu oko 510 puta veću od mase elektrona.
6. Nuklearni model strukture atoma
Proučavanje strukture atoma je praktično počelo 1897-1898, nakon što je konačno utvrđena priroda katodnih zraka kao struje elektrona i određena veličina naboja i masa elektrona. Činjenica da elektrone oslobađaju razne tvari dovela je do zaključka da su elektroni dio svih atoma. Ali atom kao cjelina je električno neutralan, stoga mora sadržavati još jedan dio, pozitivno naelektrisan, a njegov naboj mora uravnotežiti zbir negativnih naelektrisanja elektrona.
Ovaj pozitivno nabijeni dio atoma otkrio je 1911. Ernest Rutherford (1871-1937). Rutherford je predložio sljedeću shemu za strukturu atoma. U središtu atoma nalazi se pozitivno nabijeno jezgro, oko koje se elektroni vrte u različitim orbitama. Centrifugalna sila koja nastaje prilikom njihove rotacije uravnotežena je privlačenjem između jezgra i elektrona, zbog čega oni ostaju na određenim udaljenostima od jezgra. Ukupni negativni naboj elektrona numerički je jednak pozitivnom naboju jezgra, tako da je atom kao cjelina električno neutralan. Budući da je masa elektrona zanemarljiva, gotovo cijela masa atoma je koncentrisana u njegovom jezgru. Naprotiv, veličina jezgara je izuzetno mala čak iu poređenju sa veličinom samih atoma: prečnik atoma je oko 10 cm, a prečnik jezgra je oko 10 - 10 cm. samo neznatan deo celokupnog prostora koji zauzima atomski sistem (slika br. 5)
7. Sastav atomskih jezgara
Tako su Rutherfordova otkrića postavila temelje za nuklearnu teoriju atoma. Od vremena Rutherforda, fizičari su naučili mnogo više detalja o strukturi atomsko jezgro.
Najlakši atom je atom vodonika (H). Budući da je gotovo cijela masa atoma koncentrisana u jezgru, bilo bi prirodno pretpostaviti da je jezgro atoma vodika elementarna čestica pozitivnog elektriciteta, koja je nazvana proton od grčke riječi „protos“, što znači „ prvi”. Dakle, proton ima masu skoro jednaku masi atoma vodika (tačno 1,00728 ugljikovih jedinica) i električni naboj jednak +1 (ako uzmemo naboj elektrona jednak -1,602 * 10 C kao jedinicu negativnog elektriciteta ). Atomi drugih, težih elemenata sadrže jezgre koje imaju veći naboj i, očito, veću masu.
Mjerenja naboja jezgara atoma pokazala su da je naboj jezgra atoma u navedenim konvencionalnim jedinicama brojčano jednak atomskom, odnosno rednom broju elementa. Međutim, to je bilo nemoguće priznati, jer bi se potonji, budući da su nabijeni istim imenom, neminovno odbijali i, posljedično, takva jezgra bi se pokazala nestabilnima. Osim toga, ispostavilo se da je masa atomskih jezgara veća od ukupne mase protona, koji određuju naboj jezgara atoma odgovarajućih elemenata, dvaput ili više.
Tada se pretpostavljalo da jezgra atoma sadrže protone u broju većem od atomskog broja elementa, a višak pozitivnog naboja tako stvorenog jezgra kompenziraju elektroni koji čine jezgro. Ovi elektroni očigledno moraju držati protone koji se međusobno odbijaju u jezgru. Međutim, ova pretpostavka je morala biti odbačena, jer je bilo nemoguće priznati koegzistenciju teških (protona) i lakih (elektrona) čestica u kompaktnom jezgru.
Godine 1932. J. Chadwick je otkrio elementarnu česticu koja nema električni naboj, zbog čega je nazvana neutron (od latinska reč srednjeg roda, što znači "ni jedno ni drugo"). Neutron ima masu nešto veću od mase protona (tačno 1,008665 ugljikovih jedinica). Nakon ovog otkrića, D. D. Ivanenko, E. N. Gapon i V. Heisenberg, nezavisno jedan od drugog, predložili su teoriju sastava atomskih jezgara, koja je postala opšteprihvaćena.
Prema ovoj teoriji, jezgra atoma svih elemenata (osim vodonika) sastoje se od protona i neutrona. Broj protona u jezgru određuje njegovu vrijednost pozitivan naboj, a ukupan broj protona i neutrona je vrijednost njegove mase. Nuklearne čestice - protoni i neutroni - spajaju se ispod uobičajeno ime nukleoni (od latinske riječi nucleus, što znači "nukleus"). Dakle, broj protona u jezgru odgovara atomskom broju elementa, i ukupan broj nukleona, pošto je masa atoma uglavnom koncentrisana u jezgru, - njegov maseni broj, tj. njegova atomska masa A zaokružena na cijeli broj. Tada se broj neutrona u jezgru N može naći iz razlike između masenog i atomskog broja:
Tako je teorija proton-neutrona omogućila da se razriješe proturječnosti koje su se pojavile ranije u idejama o sastavu atomskih jezgri i njihovoj povezanosti s serijskim brojem i atomskom masom.
8. Izotopi
Teorija proton-neutrona omogućila je da se razriješi još jedna kontradikcija koja je nastala tokom formiranja teorije atoma. Ako prepoznamo da se jezgra atoma elemenata sastoje od određenog broja nukleona, onda atomske mase svi elementi moraju biti cijeli brojevi. Za mnoge elemente to je tačno, a manja odstupanja od celih brojeva mogu se objasniti nedovoljnom preciznošću merenja. Međutim, za neke elemente vrijednosti atomskih masa toliko su odstupale od cijelih brojeva da se to više ne može objasniti nepreciznošću mjerenja i drugim slučajnim razlozima. Na primjer, atomska masa hlora (CL) je 35,45. Utvrđeno je da otprilike tri četvrtine prirodnih atoma hlora ima masu 35, a jedna četvrtina - 37. Dakle, elementi koji postoje u prirodi sastoje se od mješavine atoma koji imaju različite mase, ali očigledno iste Hemijska svojstva, tj. postoje varijeteti atoma istog elementa s različitim i, osim toga, cjelobrojnim masama. F. Aston je uspio razdvojiti takve mješavine na sastavne dijelove, koji su nazvani izotopi (od grčkih riječi “isos” i “topos”, što znači “isto” i “mjesto” (ovdje to znači da različiti izotopi jednog elementa zauzimaju jedno mjesto u periodnom sistemu). Sa stanovišta proton-neutronske teorije, izotopi su varijeteti elemenata čija atomska jezgra sadrže različit broj neutrona, ali isti broj protona. Hemijska priroda elementa određena je brojem protona u atomskom jezgru, koji je jednak broju elektrona u ljusci atoma. Promjena broja neutrona (sa istim brojem protona) ne utiče na hemijska svojstva atoma.
Sve to omogućava formuliranje koncepta kemijskog elementa kao vrste atoma koju karakterizira određeni naboj jezgra. Među izotopima razni elementi nađeni su oni koji u jezgru sa različitim brojem protona sadrže isti ukupan broj nukleona, odnosno čiji atomi imaju istu masu. Takvi izotopi su nazvani izobari (od grčke riječi "baros", što znači "težina"). Različita kemijska priroda izobara uvjerljivo potvrđuje da priroda elementa nije određena masom njegovog atoma.
Za različite izotope koriste se nazivi i simboli samih elemenata, koji označavaju maseni broj, koji prati naziv elementa ili je naznačen kao indeks u gornjem lijevom dijelu simbola, na primjer: klor - 35 ili Cl.
Različiti izotopi se međusobno razlikuju po stabilnosti. 26 elemenata ima samo jedan stabilan izotop - takvi elementi se nazivaju monoizotopi, (odlikuju se uglavnom neparnim atomskim brojevima), a njihove atomske mase su približno jednake cijelim brojevima. 55 elemenata ima nekoliko stabilnih izotopa - nazivaju se poliizotopi (veliki broj izotopa je karakterističan uglavnom za parne elemente). Za preostale elemente poznati su samo nestabilni, radioaktivnih izotopa. To su sve teški elementi, počevši od elementa br. 84 (polonijum), pa od relativno lakih - br. 43 (tehnecijum) i br. 61 (prometijum). Međutim, radioaktivni izotopi nekih elemenata su relativno stabilni (obilježeni dugim poluživotom), pa se ovi elementi, poput torija, urana, nalaze u prirodi. U većini, međutim, radioaktivni izotopi se dobivaju umjetnim putem, uključujući brojne radioaktivne izotope stabilnih elemenata.
9. Elektronske ljuske atoma. Borova teorija.
Prema Rutherfordovoj teoriji, svaki elektron se okreće oko jezgra, a sila privlačenja jezgra je uravnotežena centrifugalnom silom koja proizlazi iz rotacije elektrona. Rotacija elektrona je prilično analogna njegovim brzim oscilacijama i trebala bi uzrokovati emisiju elektromagnetnih valova. Stoga se može pretpostaviti da rotirajući elektron emituje svjetlost određene valne dužine, ovisno o frekvenciji orbite elektrona. Ali, emitirajući svjetlost, elektron gubi dio svoje energije, zbog čega je poremećena ravnoteža između njega i jezgre. Da bi se uspostavila ravnoteža, elektron se mora postupno približavati jezgru, a učestalost okretanja elektrona i priroda svjetlosti koju emituje također će se postepeno mijenjati. Na kraju, nakon što je iscrpljena sva energija, elektron mora "pasti" na jezgro, a emisija svjetlosti će prestati. Da je zapravo došlo do takve kontinuirane promjene u kretanju elektrona, njegov "pad" na jezgro bi značio uništenje atoma i prestanak njegovog postojanja.
Dakle, Rutherfordov ilustrativni i jednostavan nuklearni model atoma jasno je u suprotnosti s klasičnom elektrodinamikom. Sistem elektrona koji rotiraju oko jezgra ne može biti stabilan, jer elektron tokom takve rotacije mora neprekidno zračiti energiju, što zauzvrat mora dovesti do njegovog pada na jezgro i uništenja atoma. U međuvremenu, atomi su stabilni sistemi.
Ove značajne kontradikcije djelimično je razriješio izvanredni danski fizičar Niels Bohr (1885. - 1962.), koji je 1913. razvio teoriju atoma vodika, koju je zasnovao na posebnim postulatima, povezujući ih, s jedne strane, sa zakonima klasične mehanike i, s druge strane, sa kvantna teorija energija zračenja njemačkog fizičara Maksa Planka (1858 - 1947).
Suština kvantne teorije se svodi na to da se energija emituje i apsorbuje ne neprekidno, kao što je ranije prihvaćeno, već u odvojenim malim, ali dobro definisanim delovima - energetskim kvantima. Rezerva energije zračećeg tijela mijenja se u skokovima, kvant po kvant; djelić broja kvanta koje tijelo ne može niti emitovati niti apsorbirati.
Veličina kvanta energije zavisi od frekvencije zračenja: što je frekvencija zračenja veća, to je veća veličina kvanta. Označavajući kvant energije kroz E, pišemo Planckovu jednačinu:
gdje h - konstantan, takozvana Plankova konstanta, jednaka 6,626 * 10 J * s., i - frekvencija Debroilovog vala.
Kvanti energije zračenja nazivaju se i fotoni. Primjenjujući kvantne koncepte na rotaciju elektrona oko jezgra, Bohr je svoju teoriju zasnovao na vrlo hrabrim pretpostavkama ili postulatima. Iako su ovi postulati u suprotnosti sa zakonima klasične elektrodinamike, svoje opravdanje nalaze u nevjerovatnim rezultatima do kojih dovode, te u potpunom slaganju između teorijskih rezultata i ogromnog broja eksperimentalnih činjenica. Borovi postulati su sljedeći:
Elektron se može kretati ne bilo kojim orbitama, već samo onim koje zadovoljavaju određene uslove koji proizilaze iz kvantne teorije. Ove orbite se nazivaju stabilne, stacionarne ili kvantne orbite. Kada se elektron kreće duž jedne od stabilnih orbita mogućih za njega, on ne zrači elektromagnetnu energiju. Prijelaz elektrona iz udaljene orbite u bližu je praćen gubitkom energije. Energija koju atom izgubi tokom svake tranzicije pretvara se u jedan kvant energije zračenja. Frekvencija svjetlosti koja se emituje u ovom slučaju određena je radijusima dvije orbite između kojih se odvija prijelaz elektrona. Označavajući energetsku rezervu atoma na poziciji elektrona u orbiti udaljenijoj od jezgra kroz En, i u bližoj orbiti kroz Ek, i podijelivši energiju izgubljenu atomom En - Ek sa Planckovom konstantom, dobivamo potrebna frekvencija:
= (En - Ek) / h
Što je veća udaljenost od orbite u kojoj se elektron nalazi do one u koju prolazi, to je veća frekvencija zračenja. Najjednostavniji od atoma je atom vodika, oko čijeg jezgra se okreće samo jedan elektron. Na osnovu gornjih postulata, Bohr je izračunao polumjere mogućih orbita za ovaj elektron i otkrio da su oni povezani kao kvadrati prirodnih brojeva: 1: 2: 3: ...: n. Vrijednost n se naziva glavni kvantni broj.
Nakon toga, Bohrova teorija je proširena na atomsku strukturu drugih elemenata, iako je to bilo povezano s određenim poteškoćama zbog svoje novosti. Dozvolila je da se vrlo riješi važno pitanje o rasporedu elektrona u atomima raznih elemenata i utvrditi zavisnost svojstava elemenata od strukture elektronske ljuske njihovih atoma. Trenutno su razvijene šeme za strukturu svih atoma hemijski elementi. Međutim, mora se imati na umu da su sve ove sheme samo manje-više pouzdana hipoteza koja omogućava objašnjenje mnogih fizičkih i kemijskih svojstava elemenata.
Kao što je ranije spomenuto, broj elektrona koji se okreću oko jezgra atoma odgovara rednom broju elementa u periodnom sistemu. Elektroni su raspoređeni u slojevima, tj. svaki sloj ima određeno punjenje ili, takoreći, zasićeni broj elektrona. Elektrone istog sloja karakteriše skoro ista količina energije, tj. su otprilike isti nivo energije. Čitava ljuska atoma se raspada na nekoliko energetskih nivoa. Elektroni svakog sljedećeg sloja su na višem energetskom nivou od elektrona prethodnog sloja. Najveći broj elektroni N, koji imaju mogućnost da budu na datom energetskom nivou, jednak je dvostrukom kvadratu broja sloja:
gdje je n broj sloja. Dakle, sa 1-2, sa 2-8, sa 3-18, itd. Osim toga, utvrđeno je da broj elektrona u vanjskom sloju za sve elemente, osim za paladij, ne prelazi osam, au pretposljednjem sloju - osamnaest.
Elektroni vanjskog sloja, kao najudaljeniji od jezgra i stoga najmanje čvrsto povezani s jezgrom, mogu se odvojiti od atoma i pridružiti drugim atomima, ulazeći u sastav vanjskog sloja potonjeg. Atomi koji su izgubili jedan ili više elektrona postaju pozitivno nabijeni, jer naboj atomskog jezgra premašuje zbir naboja preostalih elektrona. Suprotno tome, atomi koji su vezali elektrone postaju negativno nabijeni. Nabijene čestice formirane na ovaj način, kvalitativno različite od odgovarajućih atoma, nazivaju se ioni. Mnogi ioni, zauzvrat, mogu izgubiti ili dobiti elektrone, pretvarajući se ili u električno neutralne atome ili u nove ione s drugačijim nabojem.
10. Nuklearne snage.
Hipotezu da se atomska jezgra sastoje od protona i neutrona potvrdile su mnoge eksperimentalne činjenice. To je svjedočilo o valjanosti neutronsko-tonskog modela strukture jezgra.
No, postavilo se pitanje: zašto se jezgre ne raspadaju na pojedinačne nukleone pod djelovanjem sila elektrostatičkog odbijanja između pozitivno nabijenih protona?
Proračuni pokazuju da se nukleoni ne mogu držati zajedno zbog privlačnih sila gravitacijske ili magnetske prirode, jer su te sile mnogo manje od elektrostatičkih.
U potrazi za odgovorom na pitanje stabilnosti atomskih jezgara, naučnici su predložili da između svih nukleona u jezgrima djeluju neke posebne sile privlačenja, koje znatno premašuju elektrostatičke sile odbijanja između protona. Ove snage su nazvane nuklearnim.
Pokazalo se da je hipoteza o postojanju nuklearnih sila tačna. Također se pokazalo da su nuklearne sile kratkog dometa: na udaljenosti od 10-15 m one su oko 100 puta veće od sila elektrostatičke interakcije, ali se već na udaljenosti od 10-14 m pokazuju zanemarivim. Drugim riječima, nuklearne sile djeluju na udaljenostima usporedivim s veličinom samih jezgara.
11.Fisija jezgara uranijuma.
Fisiju jezgara uranijuma bombardiranjem neutronima otkrili su 1939. njemački naučnici Otto Gunn i Fritz Strassmann.
Razmotrimo mehanizam ovog fenomena. Na (sl. br. 7, a) uslovno je prikazano jezgro atoma uranijuma (23592U). Nakon što apsorbira dodatni neutron, jezgro se pobuđuje i deformira, poprima izduženi oblik (slika 7, b).
Već znamo da u jezgri djeluju dvije vrste sila: elektrostatičke sile odbijanja između protona, koje teže razbijanju jezgra, i nuklearne privlačne sile između svih nukleona, zbog kojih se jezgro ne raspada. Ali nuklearne sile su kratkog dometa, stoga u izduženom jezgru više ne mogu držati dijelove jezgra koji su jako udaljeni jedan od drugog. Pod dejstvom elektrostatičkih odbojnih sila, jezgro se cepa na dva dela (sl. br. 7, c), koji se velikom brzinom raspršuju u različitim pravcima i emituju 2-3 neutrona.
Ispostavilo se da je taj dio unutrašnja energija jezgro se pretvara u kinetičku energiju letećih fragmenata i čestica. Fragmenti se brzo usporavaju u okruženju, zbog čega se kinetička energija se pretvara u unutrašnju energiju medija (tj. u energiju interakcije toplotnog kretanja njegovih sastavnih čestica).
Uz istovremenu fisiju velikog broja jezgri uranijuma, unutrašnja energija medija koji okružuje uranijum i, shodno tome, njegova temperatura značajno raste (tj. medij se zagrijava).
Dakle, reakcija fisije jezgri urana teče oslobađanjem energije okruženje.
Energija sadržana u jezgrima atoma je kolosalna. Na primjer, potpunom fisijom svih jezgri prisutnih u 1 gramu uranijuma, oslobodila bi se ista količina energije koja se oslobađa prilikom sagorijevanja 2,5 tone nafte.
12. Nuklearne elektrane.
nuklearna elektrana (NPP) - elektrana u kojoj se atomska (nuklearna) energija pretvara u električnu energiju. Generator energije u nuklearnoj elektrani je nuklearni reaktor. Toplota koja se oslobađa u reaktoru kao rezultat lančana reakcija fisijom jezgara nekih teških elemenata, zatim se, kao i kod konvencionalnih termoelektrana (TE), pretvara u električnu energiju.1 g izotopa uranijuma ili plutonijuma oslobađa 22.500 kWh, što je ekvivalentno energiji sadržanoj u 2.800 kg standardno gorivo. Prva svjetska nuklearna elektrana za pilot industrijske svrhe snage 5 MW puštena je u rad u SSSR-u 27. juna 1954. godine u gradu Obninsku. Prije toga, energija atomskog jezgra korištena je u vojne svrhe. Puštanje u rad prve nuklearne elektrane označilo je otvaranje novog pravca u energetici, što je prepoznato na 1. međunarodnoj naučnoj i tehničkoj konferenciji o mirnoj upotrebi atomske energije (avgust 1955., Ženeva).
Šematski dijagram nuklearne elektrane s vodeno hlađenim nuklearnim reaktorom (sl. br. 6.). Toplota koja se oslobađa u jezgru reaktora uzima se kao rashladno sredstvo vodom (rashladnim sredstvom) 1. kruga, koja se pumpa kroz reaktor cirkulacijskom pumpom g Zagrijana voda iz reaktora ulazi u izmjenjivač topline (parogenerator) 3, gdje se prenosi toplinu primljenu u reaktoru na vodu 2. kruga. Voda 2. kruga isparava u generatoru pare, a para se formira i ulazi u turbinu 4.
U nuklearnim elektranama najčešće se koriste 4 vrste reaktora na termičkim neutronima: 1) reaktori sa hlađenjem vodom sa običnom vodom kao moderatorom i rashladnim sredstvom; 2) grafit-voda sa vodenim rashladnim sredstvom i grafitnim moderatorom; 3) teška voda sa vodenim rashladnim sredstvom i teška voda kao moderator 4) grafit-gas sa gasnim rashladnim sredstvom i grafitnim moderatorom.
Ovisno o vrsti i stanje agregacije rashladnog sredstva, stvara se jedan ili drugi termodinamički ciklus nuklearne elektrane. Izbor gornje granice temperature termodinamički ciklus određena je maksimalnom dozvoljenom temperaturom omotača gorivnih elemenata (TVEL) koji sadrže nuklearno gorivo, dozvoljenom temperaturom samog nuklearnog goriva, kao i svojstvima rashladnog sredstva usvojenog za ovaj tip reaktora. U nuklearnoj elektrani. termički reaktor koji se hladi vodom obično se koristi niskotemperaturni parni ciklusi. Reaktori hlađeni plinom omogućavaju korištenje relativno ekonomičnijih parnih ciklusa s povećanim početnim tlakom i temperaturom. Termička shema NPP-a u ova dva slučaja je izvedena kao 2-kružna: rashladna tečnost cirkuliše u 1. krugu, 2. krug je para-voda. U reaktorima s kipućom vodom ili rashladnim sredstvom na visokoj temperaturi moguća je termo NPP s jednom petljom. U reaktorima s kipućom vodom voda ključa u jezgru, dobivena mješavina vodene pare se odvaja i zasićena para se šalje ili direktno u turbinu, ili se prethodno vraća u jezgro radi pregrijavanja.
U visokotemperaturnim grafitno-gasnim reaktorima moguće je koristiti konvencionalni plinski turbinski ciklus. Reaktor u ovom slučaju djeluje kao komora za sagorijevanje.
Tokom rada reaktora, koncentracija fisionih izotopa u nuklearnom gorivu postepeno se smanjuje, a gorivo izgara. Stoga se s vremenom zamjenjuju svježim. Nuklearno gorivo se pretovaruje pomoću mehanizama i uređaja sa daljinski upravljač. Istrošeno gorivo se prenosi u bazen istrošenog goriva i zatim šalje na ponovnu obradu.
Reaktor i njegovi servisni sistemi uključuju: sam reaktor sa biološkom zaštitom, izmjenjivače topline, pumpe ili puhačke jedinice koje cirkulišu rashladno sredstvo; cjevovodi i armature cirkulacijskog kruga; Uređaji za ponovno punjenje nuklearnog goriva; specijalni sistemi ventilacija, hitno hlađenje itd.
U zavisnosti od konstrukcije, reaktori imaju sledeće karakteristike: u reaktorima pod pritiskom gorivo i moderator se nalaze unutar posude koja nosi ukupni pritisak rashladne tečnosti; u kanalnim reaktorima gorivo hlađeno rashladnom tečnošću se ugrađuje u specijalne cijevi-kanali koji prodiru u moderator zatvoreni u kućište tankih stijenki. Radi zaštite osoblja NEK od izlaganja radijaciji, reaktor je okružen biološkom zaštitom čiji su glavni materijal beton, voda, serpentinski pijesak. Oprema reaktorskog kruga mora biti potpuno zatvorena. Predviđen je sistem praćenja mesta mogućeg curenja rashladne tečnosti, preduzimaju se mere da pojava curenja i prekida u strujnom krugu ne dovede do radioaktivnih emisija i zagađivanja prostorija NEK i okoline. Oprema reaktorskog kola se obično ugrađuje u zatvorene kutije, koje su biološkom zaštitom odvojene od ostalih prostorija NE i ne servisiraju se tokom rada reaktora. ventilacijski sistem, u kojem su, kako bi se isključila mogućnost atmosferskog zagađenja, predviđeni filteri za čišćenje i držači plina. Služba dozimetrijske kontrole prati poštovanje pravila radijacione sigurnosti od strane osoblja NEK.
U slučaju havarija u sistemu za hlađenje reaktora, kako bi se spriječilo pregrijavanje i narušavanje nepropusnosti omotača gorive šipke, predviđeno je brzo (u roku od nekoliko sekundi) utišavanje. nuklearna reakcija; Sistem hlađenja u nuždi ima nezavisne izvore napajanja.
Prisustvo sistema biološke zaštite posebno. usluga ventilacije i hitnog hlađenja i dozimetrijske kontrole omogućava vam da u potpunosti zaštitite osoblje za održavanje NEK od štetnih efekata radioaktivnog izlaganja.
Oprema mašinske sale nuklearke je slična opremi mašinske sale TE. Razlikujemo, karakteristika većine nuklearnih elektrana je korištenje pare relativno niskih parametara, zasićene ili blago pregrijane.
Istovremeno, kako bi se isključila erozijska oštećenja lopatica posljednjih stupnjeva turbine česticama vlage sadržane u pari, u turbinu su ugrađeni separatori. Ponekad je potrebno koristiti daljinske separatore i grijače pare. Zbog činjenice da se rashladno sredstvo i nečistoće koje se u njemu nalaze aktiviraju pri prolasku kroz jezgro reaktora, projektno rješenje opreme turbinske hale i sistema hlađenja turbinskog kondenzatora NEK s jednom petljom trebalo bi u potpunosti isključiti mogućnost rashladnog sredstva. curenje. U nuklearnim elektranama s dva kruga sa visokim parametrima pare, takvi zahtjevi se ne postavljaju na opremu turbinske hale.
Dio toplotne snage reaktora ove nuklearne elektrane troši se na opskrbu toplinom. Osim za proizvodnju električne energije, nuklearne elektrane se koriste i za desalinizaciju morska voda. Nuklearne elektrane kojih je najviše moderan izgled elektrane imaju niz značajnih prednosti u odnosu na druge tipove elektrana: u normalnim radnim uvjetima, uopće ne zagađuju okoliš, ne zahtijevaju vezivanje za izvor sirovina i, shodno tome, mogu se postaviti gotovo svuda, nove elektrane imaju kapacitet gotovo jednak kapacitetu prosječne hidroelektrane, ali faktor iskorištenosti instalirane snage u nuklearnim elektranama (80%) značajno premašuje ovaj pokazatelj u hidroelektranama ili termoelektranama. Činjenica da 1 kg uranijuma može proizvesti istu količinu toplote kao pri sagorevanju oko 3000 tona uglja može govoriti o efikasnosti i efektivnosti nuklearnih elektrana.
Praktično nema značajnih nedostataka nuklearnih elektrana u normalnim uslovima rada. Međutim, ne može se ne primijetiti opasnost od nuklearnih elektrana pod mogućim okolnostima više sile: potresi, uragani itd. - ovdje stari modeli energetskih blokova predstavljaju potencijalnu opasnost od radijacijske kontaminacije teritorija zbog nekontrolisanog pregrijavanja reaktora.
13. Zaključak
Nakon što sam detaljno proučio fenomen naelektrisanja i strukturu atoma, saznao sam da se atom sastoji od jezgre i negativno nabijenih elektrona oko njega. Jezgro se sastoji od pozitivno nabijenih protona i nenabijenih neutrona. Kada je tijelo naelektrizirano, na naelektriziranom tijelu se javlja ili višak ili manjak elektrona. Ovo određuje naboj tijela. Postoje samo dvije vrste električnih naboja - pozitivni i negativni. Kao rezultat mog rada, duboko sam se upoznao sa fenomenima elektrostatike i shvatio kako i zašto nastaju ove pojave. Na primjer, munja. Fenomen elektrostatike usko je povezan sa strukturom atoma. Atomi supstanci kao što su uranijum, radijum itd. poseduju radioaktivnost.Energija atoma je od velike važnosti za život čitavog čovečanstva. Na primjer, energija sadržana u jednom gramu uranijuma jednaka je energiji koja se oslobađa pri sagorijevanju 2,5 tone nafte. Trenutno je radioaktivna energija atoma našla svoju primjenu u mnogim područjima života. Svake godine se gradi sve više nuklearnih elektrana (nuklearnih elektrana), razvija se proizvodnja ledolomaca i podmornica s nuklearnim reaktorom. Atomska energija se koristi u medicini za liječenje raznih bolesti, kao i u mnogim područjima. Nacionalna ekonomija. Nepravilna upotreba energije može predstavljati opasnost po zdravlje živih organizama. Energija atoma može koristiti ljudima ako nauče kako da je pravilno koriste.
"Fizika "Elektrostatika"" - Utjecaj okoline. Test kontrola. Rješenje ključnih zadataka. Zbroj pozitivnih i negativnih elementarne čestice. Da li je moguće dijeliti električni naboj na beskonačno vrijeme. Ispitivanje test zadataka. Faktor proporcionalnosti. Elektrifikacija. negativni naboj. ponavljanje znanja. Elektrostatika. Ponavljanje osnovnih pojmova.
"Elektrifikacija tijela u dodiru" - Dva tijela - naelektrizirana i neelektrificirana. Dvije vrste optužbi. U 18. vijeku organizovane su svjetovne zabave. Elektrifikacija telefona. Elektrifikacija tijela u kontaktu. Ćilibar je fosilizirana smola četinara. Pronađite naboje loptica. Pogledajte sliku sa desne strane. Tijela sa električnim nabojem istog znaka.
"Proces elektrifikacije tijela" - Crveni karton. Informacije o naučniku. Hajde da ponovimo. Zašto pričvršćuju lanac za zemlju na kamione za gorivo. Režim vlažnosti. Šta je elektrifikacija. Mehaničar povorke. Iz istorije. Priručni materijali. Koji je predznak naboja na kuglicama. Sh.Kulon. Daltonov zadatak. Laboratorij za fiziku. Elektrifikacija telefona. Interakcija naelektrisanih tela.
"Eksperimenti na elektrifikaciji" - Električna jegulja. Poreklo pojma "električna energija". Elektrifikacija. Philosopher Thales. električnih pojava. Formiranje početnih ideja. Komad ćilibara. Pronađite početak svega. Trenje tijela elektrificirana tijela. Tela sa naelektrisanjem istog znaka. Elektrifikacija telefona. Elektrometri. Elektrifikacija tečnosti.
"Elektrifikacija tijela" - Za čišćenje zraka koriste se elektrostatički filteri. Razvoj kognitivne aktivnosti učenika kroz nastavne oblike igre. Pušenje. Utjecaj elektrifikacije. Tinder je takođe ćilibar na ćilibaru, na dijamantu, na staklu i još mnogo toga. Pojave koje nastaju kao posljedica elektrifikacije. “Pronađi početak svega i mnogo ćeš razumjeti.
"Statički elektricitet" - Hiljadama godina naši su preci hodali zemljom bosi, uzemljujući se prirodno. Akumulacija statičkog elektriciteta. Ovlažite vazduh u prostoriji sa sprejom i jednom dnevno prebrišite vlažnom krpom. U toploj sezoni pokušajte što više hodati bosi, posebno po vlažnom tlu.
Ukupno ima 14 prezentacija u ovoj temi
sažetak ostalih prezentacija"Istorija razvoja električne rasvete"- Za rad na karbonskim lukovima visokog intenziteta N.A. Karyakin i njegovo osoblje nagrađeni su Državnom nagradom. Lampa Yablochkov našla je najširu primjenu u uličnoj rasvjeti glavni gradovi. Reflektori sa takvim izvorima svetlosti korišćeni su za vreme Velikog Otadžbinski rat, kao i na snimanju i za filmske projekcije. Neophodno je istaći doprinos N.A. Karyakin u razvoju lukova visokog intenziteta s ugljičnim elektrodama.
"Toplotna provodljivost i prijenos topline"- Zadatak broj 2. Zašto je podrum najhladnije mjesto u kući? Konvekcija. Koje tvari imaju najveću i najmanju toplinsku provodljivost? Hvala vam na pažnji! Kod provođenja toplote, nema prijenosa materije s jednog kraja tijela na drugi. U prostoru u kojem nema čestica ne može doći do provođenja toplote. Zračenje je tok talasa koji nosi energiju (prostiranje energetskih talasa). Toplotna provodljivost materijala.
"Lomonosov - veliki ruski naučnik"- Sećanje na Lomonosova. Domovina Lomonosova. Lomonosov je razvio sopstvenu naučnu metodologiju. Konačan cilj naučno istraživanje. Lomonosov je pjesnik i pedagog. Naučni radovi Lomonosov. Spomenik u domovini. M. V. Lomonosov. Kreativnost Lomonosova. Spomenici Lomonosovu. Metode kvantitativnog određivanja. Mihail Vasiljevič Lomonosov. Veliki ruski naučnik. Neprijateljski stav. Filozof. Mozaik djela Lomonosova.
"ruski naučnik Lomonosov"- M.V. Lomonosov je veliki ruski naučnik. Lomonosov Mihail Vasiljevič rođen je 8. novembra 1711. Zahvaljujući upornosti, uspeva da završi ceo 12-godišnji kurs za 5 godina. Lomonosov u nauci. Izreke, citati i aforizmi Lomonosova. Lomonosov i fizika. Nauka hrani mlade ljude, daje radost starijima. Lomonosov i matematika. Lomonosov u astronomiji. Lomonosov i hemija. U proleće 1765. Lomonosov se prehladio. Sjećanje na velikog ruskog naučnika-enciklopediste.
"Fizika u kuhinji"- Difuzija. Toplotna provodljivost. Iskustvo. Objašnjenje iskustva. Konvekcija. Fizika u kuhinji termičke pojave. Eksperimentirajte s prugastim staklom. Zašto se čaj kuva kipućom vodom. Prijenos topline.
"Eksperimenti prenosa toplote"- Proces promjene unutrašnje energije tijela. Metode prenosa toplote u praksi. Pomaknuto ulijevo. Vrijednosti. Kolona obojene tečnosti. Zagrevamo vodu u epruveti odozgo. Supstanca. Studenti. Koncept prijenosa topline u praksi. Toplotna provodljivost. Konvekcija. Komad leda. Sobni termometar. Zagrijavanje metalnog predmeta. Voda ključa u epruveti. Zagrijavamo epruvetu odozdo. zagrijani metalni predmet.






