Qattiq moddalarning erishi va qotib qolishi. Issiqlik hodisalarini moddaning tuzilishiga asoslangan holda o'rganish usullari
Erish - tananing kristallikdan o'tishi qattiq holat suyuqlikka. Erish sintezning o'ziga xos issiqligining yutilishi bilan sodir bo'ladi va bo'ladi fazali o'tish birinchi turdagi.
Erish qobiliyatiga ishora qiladi jismoniy xususiyatlar moddalar
Oddiy bosimda volfram metallar orasida eng yuqori erish nuqtasiga ega (3422 ° C), oddiy moddalar umuman olganda - uglerod (turli manbalarga ko'ra 3500 - 4500 ° C) va o'zboshimchalik bilan moddalar orasida - gafnium karbid HfC (3890 ° C). Biz geliyning eng past erish nuqtasiga ega deb taxmin qilishimiz mumkin: normal bosimda u o'zboshimchalik bilan past haroratlarda suyuqlik bo'lib qoladi.
Oddiy bosimdagi ko'p moddalar suyuq fazaga ega emas. Isitilganda ular darhol sublimatsiyadan o'tadi gazsimon holat.
9-rasm - Muzning erishi
Kristallanish - bu moddaning kristallar hosil bo'lishi bilan suyuq holatdan qattiq kristall holatga o'tish jarayonidir.
Faza - bu termodinamik tizimning boshqa qismlaridan (boshqa fazalardan) interfeys orqali ajratilgan bir hil qismi bo'lib, u orqali o'tganda Kimyoviy tarkibi, sakrashlarda materiyaning tuzilishi va xossalari o'zgaradi.
10-rasm - Muz hosil bo'lishi bilan suvning kristallanishi
Kristallanish - qattiq fazani kristallar shaklida eritmalar yoki eritmalardan ajratish jarayoni, kimyo sanoatida kristallanish jarayoni moddalarni sof shaklda olish uchun ishlatiladi.
Kristallanish ma'lum bir cheklash shartiga erishilganda boshlanadi, masalan, suyuqlikning o'ta sovishi yoki bug'ning o'ta to'yinganligi, ko'plab kichik kristallar deyarli bir zumda paydo bo'lganda - kristallanish markazlari. Kristallar suyuqlik yoki bug'dan atomlar yoki molekulalarni biriktirish orqali o'sadi. Kristal yuzlarning o'sishi qatlam-qatlam sodir bo'ladi, o'sish jarayonida to'liq bo'lmagan atom qatlamlarining qirralari (qadamlar) yuz bo'ylab harakatlanadi. O'sish tezligining kristallanish sharoitiga bog'liqligi o'sish shakllari va kristall tuzilmalarning xilma-xilligiga olib keladi (ko'p yuzli, qatlamli, o'tkir, skelet, dendritik va boshqa shakllar, qalam tuzilmalari va boshqalar). Kristallanish jarayonida muqarrar ravishda turli nuqsonlar paydo bo'ladi.
Kristallanish markazlarining soni va o'sish tezligi o'ta sovutish darajasidan sezilarli darajada ta'sirlanadi.
Supercooling darajasi - suyuq metallning kristalli (qattiq) modifikatsiyaga o'tish haroratidan past sovutish darajasi. Energiyani qoplash kerak yashirin issiqlik kristallanish. Birlamchi kristallanish - suyuqlikdan qattiq holatga o'tish jarayonida metallarda (va qotishmalarda) kristallarning hosil bo'lishi.
Maxsus issiqlik erish (shuningdek: termoyadroviy entalpiya; kristallanishning o'ziga xos issiqligining ekvivalent tushunchasi ham mavjud) - bir massa birligiga xabar qilinishi kerak bo'lgan issiqlik miqdori kristalli modda muvozanatli izobarik-izotermik jarayonda uni qattiq (kristalli) holatdan suyuq holatga o'tkazish uchun (moddaning kristallanishi paytida bir xil miqdordagi issiqlik chiqariladi).
Erish yoki kristallanish jarayonida issiqlik miqdori: Q=ml
> Bug'lanish va qaynatish. Bug'lanishning o'ziga xos issiqligi
Bug'lanish - bu moddaning suyuq holatdan gazsimon holatga (bug') o'tish jarayoni. Bug'lanish jarayoni kondensatsiya jarayonining teskari (bug'dan suyuq holatga o'tish. Bug'lanish (bug'lanish), moddaning kondensatsiyalangan (qattiq yoki suyuq) fazadan gazsimon (bug') holatiga o'tishi; birinchi tartibli faza. o'tish.
Oliy fizikada bug'lanish haqida batafsilroq tushuncha mavjud
Bug'lanish - suyuqlik yoki qattiq jism yuzasidan zarrachalar (molekulalar, atomlar) uchib chiqish (yirtib tashlash), Ek > Ep.
11-rasm - Bir stakan choy ustida bug'lanish
Bug'lanishning solishtirma issiqligi (bug'lanish) (L) -- jismoniy miqdor, qaynash nuqtasida olingan 1 kg moddani suyuq holatdan gazsimon holatga o'tkazish uchun unga berilishi kerak bo'lgan issiqlik miqdorini ko'rsatadi. Bug'lanishning solishtirma issiqligi J/kg da o'lchanadi.
Qaynatish - suyuqlikdagi bug'lanish jarayoni (moddaning suyuqlikdan gazsimon holatga o'tishi), fazalarni ajratish chegaralarining paydo bo'lishi. Qaynash nuqtasi atmosfera bosimi odatda kimyoviy toza moddaning asosiy fizik-kimyoviy xususiyatlaridan biri sifatida beriladi.
Qaynatish - bu birinchi darajali fazaga o'tish. Qaynatish bug'lanish o'choqlarining shakllanishi tufayli sirtdan bug'lanishdan ko'ra ko'proq intensiv ravishda sodir bo'ladi. haroratga yetdi qaynash va aralashmalarning mavjudligi.
Pufak hosil bo'lish jarayoniga bosim ta'sir qilishi mumkin, tovush to'lqinlari, ionlanish. Xususan, qabariq kamerasi zaryadlangan zarrachalarning o'tishi paytida ionlanishdan suyuqlikning mikro hajmlarini qaynatish printsipi asosida ishlaydi.
12-rasm - Qaynayotgan suv
Qaynatish, suyuqlikning bug'lanishi va bug'ning kondensatsiyasi paytidagi issiqlik miqdori: Q=mL
Suyuqlik va gazlarning o'zaro o'zgarishiga katta e'tibor berildi. Endi transformatsiyani ko'rib chiqing qattiq moddalar suyuqliklarda va suyuqliklarda qattiq moddalarda.
Kristal jismlarning erishi
Erish - bu moddaning qattiq holatdan suyuq holatga o'tishi.
Kristalli va amorf jismlarning erishi o'rtasida sezilarli farq bor. Kristal jism eriy boshlashi uchun uni erish nuqtasi deb ataladigan har bir moddaga xos bo'lgan haroratgacha qizdirish kerak.
Masalan, normal atmosfera bosimida muzning erish nuqtasi 0 ° S, naftalin 80 ° S, mis 1083 ° S, volfram 3380 ° S ga teng.
Tananing erishi uchun uni erish nuqtasiga qizdirish etarli emas; unga issiqlik etkazib berishni davom ettirish, ya'ni uning ichki energiyasini oshirish kerak. Erish vaqtida kristall jismning harorati o'zgarmaydi.
Agar tanani eritib bo'lgandan keyin qizdirish davom etsa, uning erishi harorati ko'tariladi. Yuqoridagilarni tana haroratining uning isishi vaqtiga bog'liqligi grafigi bilan ko'rsatish mumkin (8.27-rasm). Syujet AB qattiq jismni, gorizontal qismni isitishga to'g'ri keladi quyosh- eritish jarayoni va syujeti CD - eritmani isitish. Uchastka uchastkalarining egriligi va qiyaligi AB va CD jarayon sharoitlariga (isitilgan tananing massasi, isitgich quvvati va boshqalar) bog'liq.
O'tish kristall tanasi qattiq holatdan suyuqlikka to'satdan, to'satdan - suyuqlik yoki qattiq jismda sodir bo'ladi.
Amorf jismlarning erishi
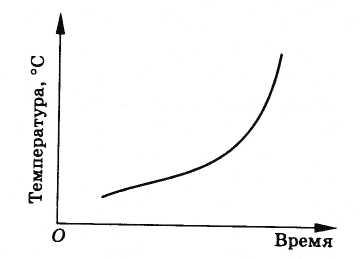
Amorf jismlar umuman boshqacha harakat qiladi. Qizdirilganda, ular asta-sekin, harorat ko'tarilib, yumshaydi va oxir-oqibat suyuqlikka aylanadi, isitishning butun vaqtida bir hil bo'lib qoladi. Qattiqdan suyuqlikka o'tishning aniq harorati yo'q. 8.28-rasmda amorf jismning qattiq holatdan suyuq holatga o'tish davridagi haroratning vaqtga nisbatan grafigi ko'rsatilgan.
Kristalli va amorf jismlarning qotib qolishi
Moddaning suyuqlikdan qattiq holatga o'tishi qattiqlashuv yoki kristallanish deyiladi.(kristal jismlar uchun).
Kristalli va amorf jismlarning qotib qolishi o'rtasida ham sezilarli farq mavjud. Eritilgan kristall tana (eritma) sovutilganda, u ichida qolishda davom etadi suyuqlik holati uning harorati ma'lum bir qiymatga tushmaguncha. Kristallanish harorati deb ataladigan bu haroratda tana kristallanishni boshlaydi. Qattiqlashuv jarayonida kristall jismning harorati o'zgarmaydi. Ko'p kuzatuvlar shuni ko'rsatdi kristall jismlar har bir modda uchun belgilangan bir xil haroratda eriydi va qotadi. Tananing yanada sovishi bilan, butun eritma qotib qolganda, tana harorati yana pasayadi. Yuqorida aytilganlar tana haroratining uning sovutish vaqtiga bog'liqligi grafigi bilan tasvirlangan (8.29-rasm). Syujet LEKIN 1 DA 1 suyuq sovutish, gorizontal qismga mos keladi DA 1 FROM 1 - kristallanish jarayoni va syujeti C 1 D 1 - kristallanish natijasida hosil bo'lgan qattiq jismni sovutish.
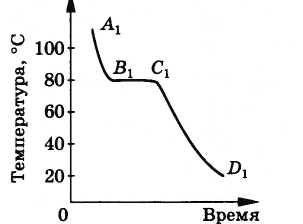
Kristallanish jarayonida suyuq holatdan qattiq holatga o'tadigan moddalar ham oraliq holatlarsiz keskin o'tadi.
Amorf jismning, masalan, smolaning qattiqlashishi uning barcha qismlarida asta-sekin va teng ravishda sodir bo'ladi; qatronlar bir hil bo'lib qoladi, ya'ni qattiqlashadi amorf jismlar- bu ularning asta-sekin qalinlashishi. Maxsus quritish harorati yo'q. 8.30-rasmda qatronlar haroratining vaqtga nisbatan grafigi ko'rsatilgan.
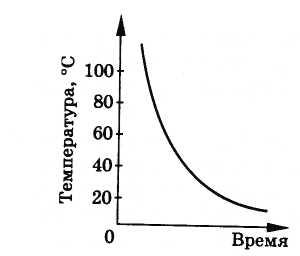
Shunday qilib, amorf moddalar ma'lum bir haroratga, erishga va qotib qolishga ega emas.
Naftalinning erishi va kristallanish grafigiga qaytaylik (198-rasm) va uning naftalinning sovishi bilan bog'liq qismini ko'rib chiqamiz.
Eritilgan naftalin sovutilganda uning harorati pasayadi. Lekin qanday naftalin qattiqlasha boshlagach, haroratning pasayishi to'xtaydi, garchi naftalin o'zining ichki energiyasini uni o'rab turgan jismlarga berishda davom etsa ham. Axir uning harorati bu jismlarning haroratidan yuqori. Va barcha naftalin qotib qolguncha, uning harorati o'zgarmaydi. Ammo barchasi qattiqlashishi bilan harorat yana pasayishni boshlaydi.
Bu hodisa har qanday kristall jismda kuzatiladi. Nima uchun kristall jismning qattiqlashishi paytida uning harorati pasaymaydi?
Biz allaqachon bilamizki, qattiqlashuv haroratida suyuqlik holatidagi jismning ichki energiyasi undan kattaroqdir ichki energiya qattiq holatda. Butun davolash jarayonida ortiqcha ichki energiya chiqariladi va sovutish tufayli yo'qolgan energiyani to'ldiradi. Shuning uchun molekulalarning o'rtacha energiyasi va, demak, tananing harorati o'zgarishsiz qoladi. quritish jarayoni tugaguncha. Shu paytdan boshlab qattiq jismning harorati pasayishni boshlaydi, chunki undagi ichki energiya yo'qolishi endi to'ldirilmaydi.
Ehtiyotkorlik bilan o'tkazilgan tajribalar shuni ko'rsatadiki, kristalli moddaning qotishi paytida uning erishi paytida so'rilgan issiqlik miqdori ajraladi. Shunday qilib, 0 ° S haroratda 1 kg og'irlikdagi suvni qattiqlashtirganda 3,4 10 6 J ajralib chiqadi.Ammo 0 °C haroratda og'irligi 1 kg bo'lgan muzning erishi uchun aynan shuncha issiqlik talab qilinadi.
Savollar.
- Moddaning qotib qolish jarayonida uning harorati 0 doimiy bo'lib qolishini qanday tushuntirish mumkin?
- 1 kg suv qotganda qancha energiya ajralib chiqadi?
Mashqlar.
- Eriydigan muz harorati 0 ° C bo'lgan xonaga keltirildi. Bu xonadagi muzlar erishda davom etadimi?
- Muz bo'laklari bir chelak suvda suzadi. Suv va muzning umumiy harorati 0°C. Muz eriydimi yoki suv muzlaydimi? Bu nimaga bog'liq?
- 4 kg muzni 0°C da eritish uchun qancha energiya ketadi?
- 20 kg qo'rg'oshinni erish nuqtasida eritish uchun qancha energiya kerak bo'ladi? Buning uchun qancha energiya kerak bo'lsa boshlang'ich harorati qo'rg'oshin 27 ° C?
Vazifalar.
- Ikkita bir xil bankalarni pechka ustiga qo'ying. Biriga 0,5 kg suv quying, ikkinchisiga 0,5 kg qor qo'ying. Suvga qancha vaqt ketishiga e'tibor bering ikkala bankda qaynatiladi. Tajribangiz haqida qisqacha ma'lumot yozing va natijalarni tushuntiring.
- Darslik oxiridagi shunday paragrafni o‘qib “Metal quyish” mavzusida ma’ruza tayyorlang.






