Atomdagi energiya almashinuvi
Qo'lyozma sifatida
Fizika
Ma'ruza matnlari
(7-qism. Atom fizikasi. lazerlar)
230400 yo'nalishi talabalari uchun
« Axborot tizimlari va texnologiyalar"
Elektron ta'lim resursi
Tuzuvchi: fizika-matematika fanlari nomzodi, dotsent V.V. Konovalenko
04.09.2013 yildagi 1-sonli bayonnoma
Atom fizikasi
Vodorod atomi.
Shuni eslang qo'zg'almas yadro va uning atrofida harakatlanuvchi elektrondan iborat sistema vodorodga o'xshash atom yoki vodorodga o'xshash ion deyiladi.
Elektron harakatlanadigan maydon markaziy simmetrikdir. Shuning uchun, bu holda Shredingenr tenglamasini echishda sferik koordinatalar tizimi qo'llaniladi: Zaryadli yadroning markaziy maydonidagi elektron uchun Shredingenr tenglamasi quyidagi ko'rinishga ega:
 (35.1)
(35.1)
Sferik koordinatalardagi Laplas operatorini ushbu tenglamaga qo‘yib, biz quyidagilarni olamiz:
Yechimlar (35.2) qoniqarli standart shartlar, har qanday ijobiy uchun olinadi E va diskret salbiy qiymatlar uchun:
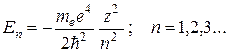 (35.3)
(35.3)
Ijobiy energiya qiymatlari yadro yaqinida uchadigan va cheksizlikka chekinadigan elektronga to'g'ri keladi. Bunday elektron yadro bilan bog'lanmaydi, atom (yoki ion) hosil qilmaydi va hech qanday qiziqish uyg'otmaydi.
Yadro bilan bog'langan elektron energiyaning salbiy qiymatlariga mos keladi (35.3). Shuni ta'kidlash kerakki, bu qiymatlar Bor nazariyasida olingan qiymatlarga mos keladi, ammo kvant mexanikasi ular Shredinger tenglamasining natijasidir va postulatlar ko'rinishidagi qo'shimcha taxminlar talab qilinmaydi.
Shredinger tenglamasining xos funktsiyalari uchta butun son parametrlarini o'z ichiga oladi: n,l,m:
![]()
n- deyiladi bosh kvant soni va (35.3)dagi energiya darajasi soniga to'g'ri keladi.
l va m – azimut va magnit kvant raqamlari , bu modul va burchak momentining ma'lum bir yo'nalishdagi proyeksiyasini aniqlaydi.
Standart shartlarga javob beradigan yechimlar faqat qiymatlar uchun olinadi l dan oshmaydi. Shuning uchun, berilgan uchun n, azimutal kvant soni l muhim bo'lishi mumkin
![]() (35.4)
(35.4)
Berilgan uchun l magnit kvant soni m turli qiymatlarni qabul qilishi mumkin:
(35.5)
Vodorod atomidagi elektronning elektron energiyasi faqat ga bog'liq n asosiy kvant soni(35.3-ga qarang), shuning uchun har bir energiya darajasi qiymatlari bilan farq qiluvchi bir nechta o'z funktsiyalariga mos keladi. l va m. Shunday qilib, vodorod atomi bir xil energiyaga ega bo'lishi mumkin, u turli to'lqin funktsiyalari bilan tavsiflangan holatda bo'lishi mumkin. Bu holatda energiya holatlari deyiladi degeneratsiya , va berilgan energiyaga mos keladigan turli holatlar soni mos keladigan energiya darajasining degeneratsiyasining ko'pligi.
Degeneratsiyaning ko'pligi energiya darajalari vodorodni hisoblash oson. Har biri n raqam qiymatlari l 2 ga mos keladi l+ 1 qiymat m. Shunday qilib, degeneratsiyaning ko'pligini quyidagi formula bilan hisoblash mumkin:
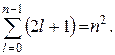
Eslatib o'tamiz, azimutal kvant soni burchak momentining qiymatini va azimutal kvant sonining turli qiymatlari bilan vodorod atomidagi elektronning holatini aniqlaydi. l burchak momentumining kattaligi bilan farqlanadi. bilan holatda bo'lgan elektron
l= 0 – chaqirdis -elektron ( s holat);
l= 1 - chaqirilganp -elektron (p holati)
l= 2 - chaqirildid -elektron (d holati)
l= 3 - chaqirilganf -elektron (f holati) va boshqalar.
Elektron joylashgan holatni belgilashda asosiy kvant sonining qiymati olinadi n kvant sonining belgisidan oldin ko'rsating l. Shunday qilib, elektron n= 3 da l = 1 3 belgilari bilan belgilanadi p.
Chunki l< n quyidagi holatlar mumkin:
2s 2p
3s 3p 3d
4s 4p 4d 4f va hokazo.
Bor nazariyasidagidek, kvant mexanikasi elektron bir darajadan ikkinchi darajaga o'tganda yorug'lik chiqariladi va so'riladi deb taxmin qiladi. Biroq, foton bor o'ziga xos burchak impulsi taxminan teng Shuning uchun, foton chiqarilganda yoki yutilganda, atomning burchak momenti quyidagicha o'zgarishi kerak. tanlash qoidasi azimutal kvant soni uchun:
Shubhasiz, bu qoida shunchaki burchak momentumining saqlanish qonunining natijasidir.
Vodorod atomining energiya darajalari diagrammasi.
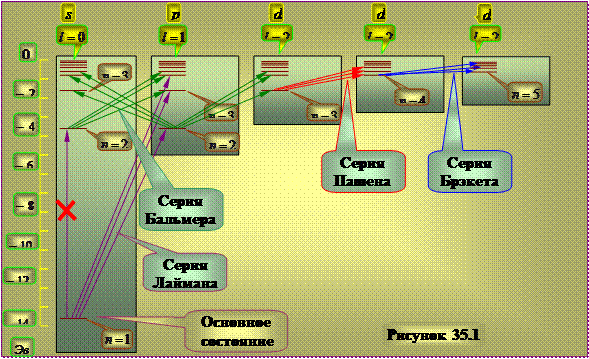 |
Tanlash qoidasi effekti(35.6) energiya darajalari orasidagi barcha o'tishlar haqiqatda amalga oshirilmasligiga olib keladi. Masalan, 2-holatdan o'tish s in 1s bo'lishi mumkin emas, chunki u tanlov qoidasiga ziddir. Shu munosabat bilan vodorod atomidagi elektronning energiya darajalari sxemasini 35.1-rasmda ko'rsatilgandek tasvirlash mumkin.
1s holati vodorod atomining asosiy holatidir bu erda vodorod atomi eng kam energiyaga ega. Atom tomonidan so'rilganida, foton butunlay yo'qolib, energiyasini atomga o'tkazadi, chunki u bo'linmaydi. Yutuvchi atom odatda asosiy holatda bo'ladi, shuning uchun vodorod atomining yutilish spektri 1 o'tishlarga mos keladigan chiziqlardan iborat bo'lishi kerak. s-np, bu tajriba natijalari bilan to'liq mos keladi.
Vodorod atomidagi elektron
Shredinger tenglamasining vodorod atomi uchun xos funktsiyalari ikkita omilga bo'linadi, ulardan biri faqat quyidagilarga bog'liq. r, ikkinchisi esa burchaklardan J va j.
Ko'paytiruvchi haqiqiy, - xayoliy. Funktsiya burchak momentum kvadrati operatorining xos funktsiyasidir. Uchun s-elektronning holatlari (ya'ni burchak impulsi nolga teng), bu funktsiya doimiydir va -shaklning funktsiyalari faqat bog'liq. r.
hajm elementi dV sferik koordinatalar tizimi sifatida ifodalanishi mumkin
![]()
qayerda d W = - qattiq burchakning elementi.
Ehtimollik dP elementdagi elektronni topish dV
Qattiq burchak ustidagi (35.7) integralini olish 4 p, radiusli yupqa sferik qatlamda elektronni topish ehtimolini topamiz r va qalinligi doktor:.
![]() (35.9)
(35.9)
Y normallashtirilgan deb qabul qilinganligi sababli (35.9) dagi integral bir ga teng va
![]() (35.10)
(35.10)
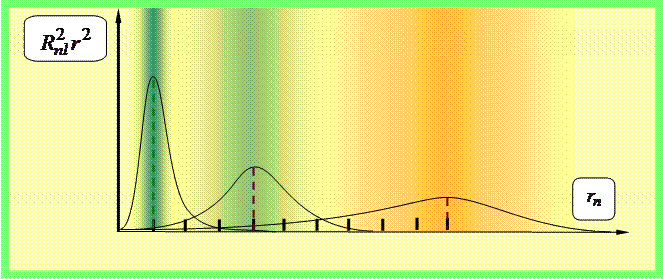
(35.9) dan shunday xulosa kelib chiqadi - yadrodan r masofada elektronni topish ehtimoli zichligi ,
Uzun vertikal chiziqlar mos keladigan Bor orbitalarining radiuslarini ko'rsatadi.
35.1-rasm
Spektrlar ishqoriy metallar
Bu spektrlar vodorod atomining emissiya spektriga o'xshaydi, lekin faqat sifat jihatidan. Bir nechta qator chiziqlar kuzatiladi va ularning eng qizg'inlari eksperimental kuzatilgan xususiyatlar asosida nomlanadi:
keskin(o'tkir) - Bu seriyaning chiziqlari juda aniq va tor ko'rinardi.
uy(asosiy) - bu seriyaning chiziqlari yutilish va emissiya spektrlarida ham kuzatildi, bu ularning atomlarning asosiy holatga o'tishiga mos kelishini ko'rsatdi;
loyqa(diffuz) - bu seriyaning chiziqlari loyqa, loyqa ko'rinardi;
asosiy(fundamental) - bu seriyaning chiziqlari vodorod atomining qator qatoriga o'xshardi.
Ko'rib chiqilganligi aniqlandi chiziqlar qatori tashqi (valentlik) yoki optik elektronning o'tishlari bilan bog'liq .
Ko'rsatilgan chiziqlar emissiyasiga mos keladigan energiya darajalari tizimi natriy atomi uchun taxminan 35.3-rasmda ko'rsatilgan shaklga ega.
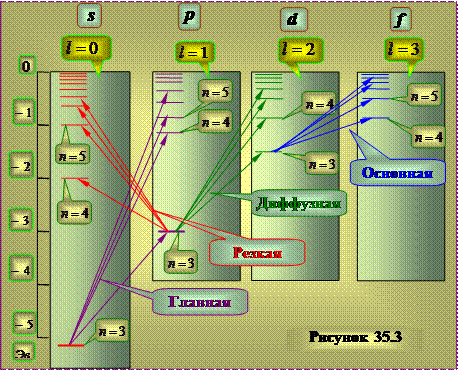 Vodorod atomidan farqli o'laroq, holatning energiyasi nafaqat n kvant sonining qiymatiga, balki hadlar qatori soniga ham bog'liq bo'lib chiqadi.
Terminlar qatori, vodorod atomidagi kabi, azimutal kvant sonining turli qiymatlariga mos keladi l.
Vodorod atomidan farqli o'laroq, holatning energiyasi nafaqat n kvant sonining qiymatiga, balki hadlar qatori soniga ham bog'liq bo'lib chiqadi.
Terminlar qatori, vodorod atomidagi kabi, azimutal kvant sonining turli qiymatlariga mos keladi l.
Bu xulosalar kvant-mexanik hisob-kitoblar natijalariga mos keladi - Shredinger tenglamasining ichida harakatlanuvchi elektron uchun markaziy simmetrik kulon bo'lmagan maydon. Ishqoriy metallar atomlarida yadro maydoni qisman atomlarning ichki elektron qobiqlari elektronlari tomonidan ekranlanadi. Bunday holda, maydon sferik simmetriyani saqlab qoladi, lekin Kulon qonunidan farqli qonun bo'yicha yadrogacha bo'lgan masofadan farq qiladi. Bunday maydonda elektronning energiyasi kvant soniga bog'liq bo'lib chiqadi: Buni aytish odatiy holdir. degeneratsiya ko'tariladi azimutal kvant soni . Biroq, Asosan, energiya bunga bog'liq bosh kvant soni n.
Buni aniqladi optik elektron olib tashlangandan keyin gidroksidi atomlarining atom qoldig'ining burchak momenti nolga teng . Shuning uchun azimutal kvant soni Olingan burchak momentining L atom bilan mos keladi azimutal kvant soni valentlik elektron. Atom qo'zg'alganda (ya'ni, u qandaydir harakat bilan minimal energiyali holatdan yuqori energiyali holatga o'tganda) va yorug'lik chiqaradi holat faqat o'zgaradi valent elektron , shuning uchun atomning sathlar sxemasi valentlik elektron tenglamasi sxemasi bilan bir xil.
Darajalar ustunlariga mos keladigan atamalar energiya darajasi diagrammasida belgilar bilan belgilanishi mumkin nS, nP, nD va nF. Keyin chastotalar spektral chiziqlar, yakuniy va boshlang'ich holatlar o'rtasidagi farqga teng, quyidagi shaklda ifodalanishi mumkin: hayajonlangan holatlarni qat'iy statsionar deb hisoblash mumkin emas. Vaqt va energiya kanonik konjugatsiyalangan miqdorlar bo'lganligi sababli, noaniqlik munosabati energiya darajalarining chekli kengligi G ni aniqlaydi:
Faqat asosiy holat o'z-o'zidan o'tishga ruxsat bermaydi va uning energiyasi qat'iy belgilangan qiymatga ega.
Cheklangan G ga muvofiq, chiqarilgan fotonlarning chastota diapazoni
Uchun ko'rinadigan yorug'lik mos keladigan bilan ![]() bu tabiiy chiziq kengligi deb ataladi
.
bu tabiiy chiziq kengligi deb ataladi
.
Atomlarning issiqlik harakati spektral chiziqlarning Doppler kengayishiga olib keladi. Bunday holda, haroratda to'lqin uzunligi bilan nurlanish uchun T\u003d 1000 K, qiymat olinadi ![]() , bu spektral chiziqlarning tabiiy kengligidan ko'p marta kattaroqdir.
, bu spektral chiziqlarning tabiiy kengligidan ko'p marta kattaroqdir.
Vodorod atomining energiyasi (6) dan ko'rinib turibdiki, faqat asosiy kvant soni bilan belgilanadi n. eng past energiya darajasi E 1 , mos keladi n \u003d 1, atomning mumkin bo'lgan minimal energiyasiga mos keladi va asosiy deb ataladi. Boshqa barcha energiya darajalari E n (E n > E 1 , n= 2,3,..) hayajonlangan deyiladi. Potensial energiya U(r) ning yadrogacha bo'lgan masofaga bog'liqligi grafigi bilan vodorod atomining energiya darajalarining diagrammasi shaklda ko'rsatilgan. 2. Energiyaning salbiy qiymatlari uchun (E<0) движение электрона является связанным. По мере роста главного квантового числа n уровни располагаются теснее и при n→ ∞ E ∞ =0.
Ijobiy energiya qiymatlari uchun elektronning harakati erkin, uzluksiz spektr mintaqasi E> 0 (2-rasmda soyali) ionlangan atomga mos keladi. Vodorod atomining ionlanish energiyasi

Vodorod atomining energiya darajalari sxemasi (2a-rasm) va o'tishlar
ular orasida (2b-rasm). [E] - eV.
Energiya o'rnatish nuqtasi bundan mustasno E 1, kvant sonlarining qiymatlari bilan farq qiluvchi atomning bir nechta turli holatlariga mos keladi l va m. Shartli qiymatlar bilan l= 0, 1, 2,… lotin harflari bilan belgilanadi s, p, d, f,… Asosiy kvant sonining qiymati orbital kvant sonining belgilanishidan oldingi raqam bilan ko'rsatiladi. Masalan, holatdagi elektronlar n= 1 va l= 0 holatida 1 lar bilan belgilanadi n= 2 va l\u003d 0, 1 - mos ravishda 2s va 2p; Bilan n=3 - 3s, 3p, 3d va boshqalar.
Kvant sonlarining turli qiymatlarini hisobga olgan holda n va l umumiy qabul qilingan shaklda ko'rsatilgan energiya darajalari tasvirining diagrammasi. 3.

Vodorod atomining energiya darajalari sxemasi va orbital kvant sonini hisobga olgan holda ular orasidagi o'tishlar l.
Atom tomonidan yorug'likning emissiyasi va yutilishi elektron bir energiya darajasidan boshqasiga o'tganda sodir bo'ladi va chiqarilgan (so'rilgan) kvantning energiyasi quyidagilarga teng:
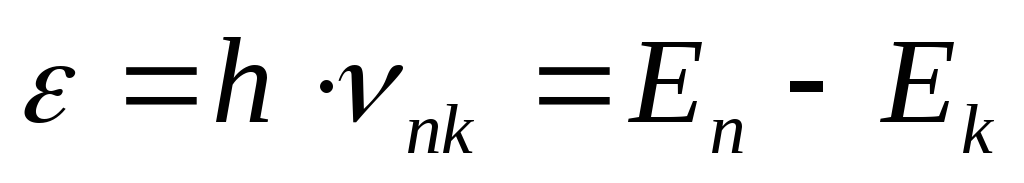 (18) qaerda n,
k
energiya darajalari (holatlari) raqamlari, mos ravishda n - o'tishning elektromagnit nurlanishining chastotasi n→
k.
Nurni chiqarish (yutish) jarayonida faqat shunday o'tishlar sodir bo'lishi mumkin, buning natijasida orbital va magnit kvant sonlarining o'zgarishi shartlar bilan belgilanadi:
(18) qaerda n,
k
energiya darajalari (holatlari) raqamlari, mos ravishda n - o'tishning elektromagnit nurlanishining chastotasi n→
k.
Nurni chiqarish (yutish) jarayonida faqat shunday o'tishlar sodir bo'lishi mumkin, buning natijasida orbital va magnit kvant sonlarining o'zgarishi shartlar bilan belgilanadi:
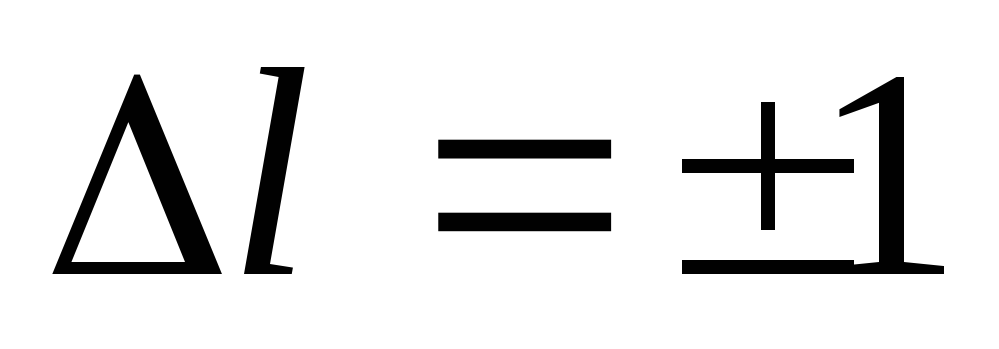 (19)
(19)
 (20)
(20)
Formulalar (19) va (20) tanlash qoidalari deb ataladi, ular atomdagi mumkin bo'lgan elektron o'tishlar sonini cheklaydi.
(6) ni hisobga olgan holda, vodorod atomining (Z = 1) statsionar holatdan o'tishidagi nurlanish chastotasi n barqaror holatga k kam energiya bilan:
 (21)
(21)
Qayerda k, n-butun sonlar; k < n.
Chunki  , keyin formula (21), mos keladigan o'tishlarning to'lqin uzunliklarini aniqlash orqali quyidagi shaklni oladi:
, keyin formula (21), mos keladigan o'tishlarning to'lqin uzunliklarini aniqlash orqali quyidagi shaklni oladi:
 (22)
(22)
Bu erda R Ridberg doimiysi ga teng
 (23)
(23)
(21) va (22) ifodalardan berilgan uchun degan xulosa kelib chiqadi k va qiymatlarni o'zgartirish n (n >k) spektral chiziqlar guruhlar yoki qatorlarni hosil qiladi. Vodorod atomining emissiya spektrida, (22) ga ko'ra, to'lqin uzunliklari formulalar bo'yicha topilgan quyidagi qatorlar ajralib turadi:
Lyman seriyasi (spektrning ultrabinafsha mintaqasi):
 , qayerda n=2,3,4,…
(24)
, qayerda n=2,3,4,…
(24)
 (24a)
(24a)
Balmer seriyasi (ko'rinadigan spektr):
 , qayerda n=
3,4,5,…
(25)
, qayerda n=
3,4,5,…
(25)
Paschen seriyasi (infraqizil spektr):
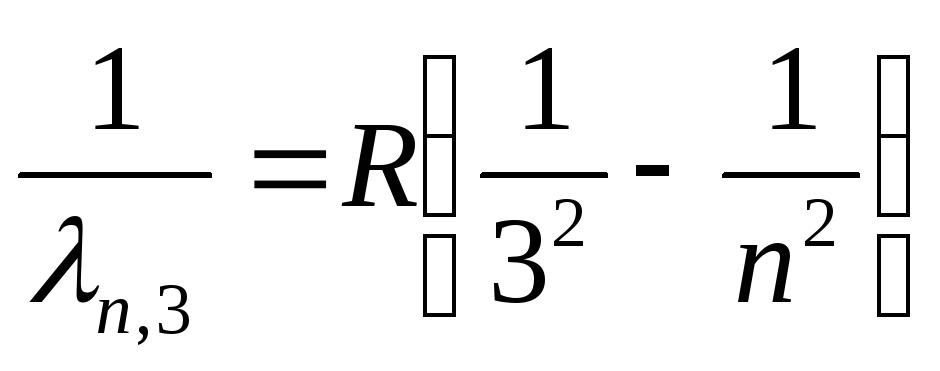 , qayerda n=
4,5,6,…
(26)
, qayerda n=
4,5,6,…
(26)
Qavslar seriyasi (uzoq infraqizil):
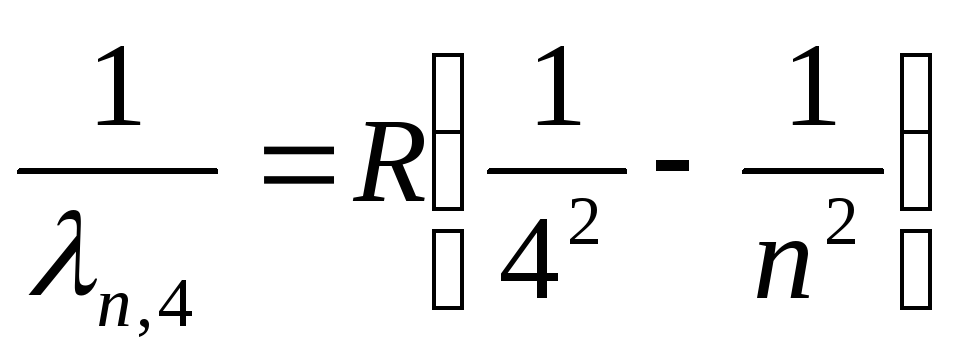 , qayerda n=5,6,7,…
(27)
, qayerda n=5,6,7,…
(27)
Formulalar (24a)-(27a), tanlash qoidalariga (19) muvofiq, elektronning holatlarini aniqlaydi, ular orasidagi o'tish paytida vodorod atomidagi qisqartirilgan qatorning spektral chiziqlari chiqariladi. Lyman va Balmer seriyalari uchun ular rasmda ko'rsatilgan. 3 to'liq.
Shuni ta'kidlash kerakki, vodorod atomining spektral chiziqlarining to'lqin uzunliklarini (chastotalarini) hisoblash uchun kvant mexanikasida nazariy jihatdan olingan (21)-(22) formulalar ilgari umumlashtirish orqali empirik tarzda olingan umumlashtirilgan Balmer formulasi (1) bilan mos keladi. eksperimental ma'lumotlar.
vodorod atomi
Vodorod atomi
vodorod atomi- musbat zaryadlangan yadro - proton va manfiy zaryadlangan elektrondan tashkil topgan bog`langan sistema.
Atomning kattaligi uning kattaligi bilan belgilanadi elektron qobiq≈ 10 -8 sm.
Elektronning bog'langan holatlarining energiyalari Shredinger tenglamasini potentsial V(r) = -e 2 /r bilan yechish orqali olinadi va bog'liqlik bilan aniqlanadi.
Bu erda n - vodorod atomidagi elektronning turli holatlari energiyasini aniqlaydigan asosiy kvant soni (n = 1, 2, 3 ...), R - Ridberg doimiysi
(R = 1,0974 10 5 sm -1).
Asosiy kvant soni n bo'lgan har bir daraja l = 0, 1, 2, ..., (n-1) kvant sonlari bilan farq qiluvchi n ta holatga mos keladi. Energiya darajasining bunday degeneratsiyasi faqat Kulon maydoniga xosdir. Bundan tashqari, bu l-degeneratsiya holatlarining har biri magnit sonida (2l + 1) marta degenerativ hisoblanadi.
m = ±l, ±(l-1),...±1, 0. Shunday qilib, statsionarning degeneratsiyasining umumiy ko'pligi. kvant holati bosh kvant soni n bilan berilgan.
Bu mulohaza elektronning spini nolga teng bo'lganda to'g'ri bo'ladi. Elektronning spini s = 1/2 bo'lganligi sababli, elektronning umumiy burchak momenti quyidagicha aniqlanadi. vektor yig'indisi uning orbital va aylanish momentlari
=
+
.
Elektronning spini s = 1/2 bo'lgani uchun uning umumiy burchak impulsi J faqat yarim butun bo'lishi mumkin.
Orbital momentum l ning ma'lum bir qiymati uchun vodorod atomida umumiy impuls qiymatlarida farq qiluvchi ikkita holat bo'lishi mumkin = + = l + 1/2 va
j = l - s = l - 1/2. Bu ikki qiymat orbital va spin vektorlarining o'zaro yo'nalishida farqlanadi. Protonning Kulon maydonida l + 1/2 va l - 1/2 holatlardagi elektronning energiyalari bir oz farq qiladi va holatlar energiyasidagi degeneratsiya ko'tariladi. Bu qo'shimcha o'zaro ta'sir spin-orbita o'zaro ta'siri deb ataladi. Degeneratsiyani olib tashlashni hisobga olgan holda, vodorod atomining past darajadagi holatlari spektri boyitiladi va energiya darajasining nozik bo'linishi sodir bo'ladi. Spin-orbitaning bo'linishini hisobga olmagan holda (asosiy 1s va birinchi qo'zg'atilgan 2s2p (1a-rasm)) ikkita past darajadagi vodorod o'rniga spin-orbitaning bo'linishiga ruxsat berilgan holda, ulardan to'rttasi mavjud (1b-rasm). . Bu darajalarning kvant xarakteristikalari jadvalda keltirilgan. J = l + 1/2 qiymati katta bo'lgan daraja j = l - 1/2 bo'lgan darajadan energiya jihatidan yuqoriroq joylashgan. l ning har xil qiymatlari, lekin bir xil nj qiymatiga ega bo'lgan davlatlar hali ham degenerativdir. Masalan, 2s 1/2 va 2p 1/2 .
Eng pastdagi elektronning kvant xarakteristikalari
vodorod atomining holatlari
| n | l | s | j = l ± s | darajani belgilash |
| 1 | 0 | 1/2 | 1/2 | 1s 1/2 |
| 2 | 0 1 |
1/2 1/2 |
1/2 1/2, 3/2 |
2s 1/2 2p 1/2, 2p 3/2 |
| 3 | 0 1 2 |
1/2 1/2 1/2 |
1/2 1/2, 3/2 3/2, 5/2 |
3s 1/2 3p 1/2 , 3p 3/2 3d 1/2 , 3d 3/2 |
Aniq yechimdan relativistik tenglama Spin s = 1/2 bo'lgan elektron uchun dirak vodorod atomi darajalari energiyasining n va j kvant raqamlariga bog'liqligini kuzatib boradi.
 ,
,
bu erda a = 1/137 - nozik tuzilish konstantasi. E nj dagi tuzatish l kvant soniga bog'liq emas. Demak, bir xil j va l ga ega bo'lgan holatlarning energiyalari teng bo'lishi kerak. Berilgan n uchun dE j+1,j darajalarining nozik bo‘linishi munosabat bilan aniqlanadi
n = 2 bilan darajaning bo'linishi ≈ 4,5·10 -5 eV.
Vodorod atomining yadrosi - proton ham o'z momentiga ega - spin s = 1/2. Bu, shuningdek, elektronning proton bilan o'zaro ta'sirini biroz o'zgartiradi, chunki protonning magnit momentining qo'shimcha o'zaro ta'siri uning spinining mavjudligi bilan yuzaga keladi. magnit maydon elektron. Ushbu o'zaro ta'sirning kattaligi protonning spin momenti va elektronning umumiy momentining o'zaro yo'nalishiga bog'liq. Shunday qilib, atom darajalarining bo'linishining yana bir turi paydo bo'ladi, bu giperfin deb ataladi, chunki uning qiymati nozik bo'linishdan ancha kichikdir. Giper nozik bo'linish allaqachon asosiy holat uchun kuzatiladi
(n = 1, l = 0). Vodorodning asosiy holatini yuqori darajada bo'linishning ikkita pastki darajasi o'rtasidagi o'tish to'lqin uzunligi l = 21 sm (radiatsiya chastotasi 1420 MGts) bo'lgan nurlanishga olib keladi. Ushbu nurlanish yordamida koinotdagi yulduzlararo vodorod odatda qayd etiladi.
n = 2 dan n = ∞ gacha bo'lgan holatlar hayajonlangan holatlar deyiladi. Qo'zg'alish energiyasi E ex (tizimga xabar qilinishi kerak bo'lgan energiya, u boshlang'ich holatdan n i dan yakuniy n f holatga o'tadi) munosabatdan aniqlanadi.

n = 1 dan n = ∞ gacha bo'lgan barcha holatlar manfiy energiyaga ega bo'lgani uchun bog'langan holatlardir. n cheksizlikka yaqinlashganda, holatlarning energiyalari bir-biriga yaqinlashadi va qo'shni davlatlar energiyalaridagi farq shunchalik kichik bo'ladiki, bo'linish darajalari birlashadi va darajalarning diskret spektri doimiy (uzluksiz)ga aylanadi. Elektronning energiyasi musbat bo'lganda (E > 0), sistema bog'lanmagan bo'ladi va elektron erkin bo'ladi. Erkin elektronning energiya spektri uzluksizdir.
n = 2, 3, … ∞ holatlardan n = 1 holatga o‘tishlar Liman qatorini tashkil qiladi. n = 3, 4, … ∞ holatdan n = 2 holatga o’tishlar Balmer qatoridir. Salbiy energiyaga ega davlatlar o'rtasidagi o'tishlar (E< 0) приводят
к образованию дискретного спектра переходов, в то время как переходы между
состояниями с E >0 va E bilan ifodalanadi< 0 дают непрерывный спектр переходов.
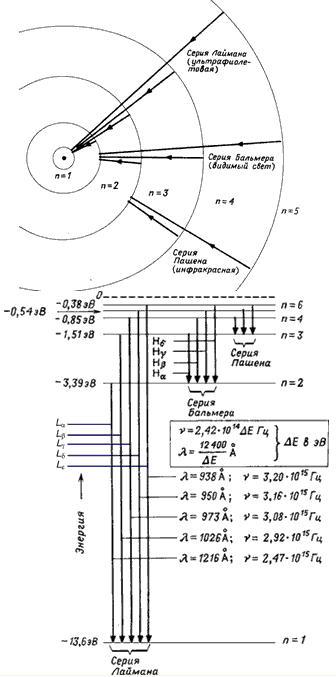
Guruch. 2. Vodorod atomining darajalari sxemasi.
Dirak tenglamasining aniq yechimiga ko'ra, n = 1, 2, 3,... kvant sonining bir xil qiymati va umumiy impulsning bir xil qiymati bo'lgan energiya darajalari.
j = 1/2, 3/2,... l kvant sonining qiymatidan qat'iy nazar energiyada mos kelishi kerak. 1947 yilda V. Lamb va R. Riserford vodorod atomida 2s 1/2 va 2p 1/2 darajalarining siljishini aniqladilar. Bu darajadagi siljish deyiladi Qo'zilarni almashtirish
. Qo'zi siljishining asosiy sababi radiatsiyaviy tuzatishlar bilan bog'liq:
- Bog'langan elektron tomonidan virtual fotonlarning emissiyasi.
- Vakuum polarizatsiyasi - vakuumda elektron-pozitron juftlarining tug'ilishi.
Ushbu ikkita tuzatish 2s 1/2 va 2p 1/2 darajalarining kuzatilgan Qo'zi siljishini to'liq tushuntiradi (DE = 4,5 · 10 -6 eV).
Fazoning ma'lum bir nuqtasida dV hajmdagi elektronni topish ehtimoli dw bilan berilgan
dw = |ps(x, y, z)|2 dV = |R nl (r)Y lm (th,ph)| 2 r 2 sinthddphdr =
= |R nl (r)| 2 r 2 |Y lm (th,ph)| 2 sinthdphdr,
radial ehtimoli ||R nl (r)| ga parchalanadi 2 r 2 | 2 r 2 dr va burchakli - |Y lm (th,ph)| 2 dŌ. Ushbu ehtimolliklarning taqsimoti shaklda keltirilgan. 3–5.
Aytaylik, ma'lum bir element atomlarining quyi energiya darajalari sxemasi rasmda ko'rsatilgan shaklga ega bo'lib, atomlar energiyali holatda bo'lsin.Elektron shunday tinch atomlardan biri bilan to'qnashib, qandaydir qo'shimcha energiya oldi. to'qnashuv natijasida. Atom bilan to'qnashuvdan keyingi elektronning impulsi teng bo'lib chiqdi. To'qnashuvdan oldingi elektronning kinetik energiyasini aniqlang. Elektron bilan to'qnashuvda atom tomonidan yorug'lik chiqarish imkoniyati e'tiborga olinmaydi. Qaytish effektiga e'tibor bermang.
Yechim.
p elektron uning kinetik energiyasi bilan bog'liqlik yoki qaerda m elektronning massasi.
Binobarin,
Mehmon 18.05.2012 17:00
Iltimos, nima uchun elektron E(0) holatga o'tganini va nima uchun bu energiyani (3,5 eV) elektron energiyasiga qo'shayotganimizni tushuntirib bering?
Mehmon
Hayrli kun!
Bor postulatlariga ko'ra, atom faqat qat'iy belgilangan holatlarda mavjud bo'lishi mumkin. Atom va elektron to'qnashganda energiyaning saqlanish qonuni bajariladi. Shartga ko'ra, elektronning energiyasi ortdi, ya'ni atom energiyasi kamayishi kerak edi. Atom birinchi energiya darajasida bo'lganligi sababli, uning energiyasini kamaytirishning yagona yo'li nol darajaga o'tishdir. Bunday holda, uning energiyasi kamayadi. Shartga ko'ra, nurlanish ehtimolini e'tiborsiz qoldirish va yadroning orqaga qaytish kinetik energiyasining qiymati uning kichikligi tufayli e'tiborsiz qolishi mumkinligi sababli, biz bu energiyaning barchasi elektronga o'tkaziladi.
Vitaliy 22.03.2016 07:54
Salom!
Fizikadan 3045-masalada bir nechta savollar mavjud:
1) Tizim bilvosita 2 ta elektronga ishora qilishini to'g'ri tushunamanmi? Ulardan biri yadroning markaziy kuchlari sohasida. Ikkinchisi - atomning yonidan uchib o'tadigan va shartli ravishda yadro bilan hech qachon o'zaro ta'sir qilmaydigan erkin elektron, lekin "atom" elektron bilan - faqat impuls o'tish momentida?
2) Agar birinchi savolga javob "ha" bo'lsa, unda "atomning energiya darajalari" sxemasi - bu bog'langan, "atom" elektronning ruxsat etilgan energiya darajalarimi?
3) Kiruvchi elektronning E (cheksizlik) yoki undan yuqori darajasida ekanligi to'g'rimi?
4) elektron pochta bilan o'zaro aloqada bo'lgan o'tuvchi elektron. atomda qo'lga olinmaganmi? U ko'proq kuch bilan uchib ketadimi?
5) O'tayotgan elektronning atomga yaqinlashish momentidagi energiyasini (kinetik va boshqalar) qanday energiya turiga kiritish mumkin?
Ushbu savollarga javob berganimdan so'ng, men topshiriqda xatolik bor yoki yo'qligini aniqlay olaman. Bu yerda yozganim uchun uzr, Xitoyda VK-ga kirishda muammolar mavjud.
Anton
1) Yo'q, muammo atom va erkin elektron haqida.
2) Bu masalada atom va uning yadrosi elektronlarining atomning energiya darajalariga qo'shgan hissasini hisobga olish shart emas. Atom ma'lum energiya spektriga ega bo'lgan yagona ob'ekt sifatida qaraladi.
3) Erkin elektron atomning bir qismi emas, uning energiyasini atomning energiya darajalari diagrammasida joylashtirish to'g'ri emas (uning energiyasini yonma-yon tasvirlash mumkin). Agar erkin elektronning kinetik energiyalarining mumkin bo'lgan spektri haqida gapiradigan bo'lsak, u uzluksiz (diskret emas): Bu masalada kinetik energiya to'qnashuvdan oldin erkin elektron 1,45 eV, keyin esa 4,95 eV bo'lgan.
4) Elektron butun atom bilan o'zaro ta'sir qildi va undan energiyaning bir qismini oldi.
5) Kinetik.
Aytaylik, ma'lum bir element atomlarining quyi energiya darajalarining sxemasi rasmda ko'rsatilgan shaklga ega bo'lib, atomlar energiyaga ega bo'lgan holatda bo'lsin.Bu atomlardan biri bilan to'qnashgan elektron, natijada qandaydir qo'shimcha energiya oldi. to'qnashuvdan. To'qnashuvdan oldingi elektronning kinetik energiyasi teng edi Atom bilan to'qnashuvdan keyingi elektronning momentumini aniqlang. Elektron bilan to'qnashuvda atom tomonidan yorug'lik chiqarish imkoniyati e'tiborga olinmaydi, to'qnashuvdan oldin atom harakatsiz hisoblanadi.
Yechim.
Agar atom bilan to'qnashganda elektron energiya olgan bo'lsa, u holda atom holatga o'tadi.Demak, to'qnashuvdan keyin elektronning kinetik energiyasi to'qnashuvgacha bo'lgan elektronning energiyasiga teng bo'ladi; bu yerdan: Impuls p elektron uning kinetik energiyasi bilan qaerda munosabati bilan bog'liq m elektronning massasi.
Binobarin,
Javob:
Rasmda atomning energiya darajalari ko'rsatilgan va bir darajadan ikkinchisiga o'tish paytida chiqarilgan va so'rilgan fotonlarning to'lqin uzunliklari ko'rsatilgan. Agar sathdan sathga o'tishda chiqarilgan fotonlarning to'lqin uzunligi qancha bo'ladi?
Yechim.
Bir energiya darajasidan ikkinchisiga o'tish paytida atom tomonidan chiqarilgan yoki yutilgan fotonning chastotasi bu darajalar orasidagi energiya farqiga proportsionaldir. Shuning uchun bizda:
Bu yerdan (chunki):
Rasmda atomning elektron qobig'ining energiya darajalari ko'rsatilgan va bir darajadan ikkinchisiga o'tish paytida chiqarilgan va so'rilgan fotonlarning chastotalarini ko'rsatadi. Agar sathdan darajaga o'tishda fotonlarning to'lqin uzunligi qancha yutilgan
Yechim.
Bir energiya darajasidan ikkinchisiga o'tish paytida atom tomonidan chiqarilgan yoki so'rilgan fotonning chastotasi ushbu darajalar orasidagi energiya farqiga proportsionaldir:
Shuning uchun biz yozamiz: Bu yerdan:
Javob:
Rasmda atomning bir nechta energiya darajalari ko'rsatilgan va bir darajadan ikkinchisiga o'tish paytida chiqarilgan va so'rilgan fotonlarning to'lqin uzunliklarini ko'rsatadi.
Eksperimental ravishda aniqlanganki, bu darajalar orasidagi o'tish paytida chiqariladigan fotonlar uchun minimal to'lqin uzunligi if ning qiymati qanday?
Yechim.
Minimal to'lqin uzunligi fotonning maksimal chastotasi va energiyasiga to'g'ri keladi. Ya'ni, va
Bir energiya darajasidan ikkinchisiga o'tish paytida atom tomonidan chiqarilgan yoki yutilgan fotonning chastotasi bu ikki daraja o'rtasidagi energiya farqiga proportsionaldir. Shunung uchun
Vodorod atomidagi elektronning energiya darajalari formula bilan berilgan, bu erda. Atom bir holatdan holatga o'tganda, atom foton chiqaradi. Fotokatod yuzasida bir marta foton fotoelektronni urib yuboradi. Fotokatodning sirt materiali uchun fotoelektr effektining qizil chegarasiga mos keladigan yorug'lik to'lqin uzunligi, Fotoelektronning maksimal mumkin bo'lgan kinetik energiyasi qancha?
Yechim.
Bor postulatlariga ko'ra, yorug'lik atom quyi energiya darajalariga o'tganda chiqariladi, fotonlar esa boshlang'ich va oxirgi holatlarning energiyalari orasidagi farqga teng energiyani olib yuradi. Shunday qilib, chiqarilgan foton energiyaga ega edi
Manba: Fizikadan yagona davlat imtihoni 06/06/2013. asosiy to'lqin. Sibir. Variant 1.
EV qaerda. Atom bir holatdan holatga o'tganda, atom foton chiqaradi. Fotokatod yuzasida bir marta bu foton fotoelektronni uradi. Fotokatod sirtining materiali uchun fotoelektr effektining qizil chegarasiga mos keladigan yorug'lik chastotasi, Hz. Fotoelektronning maksimal impulsi qanday?
Yechim.
Fotoelektr effekt tenglamasiga ko'ra, chiqarilgan fotoelektronlarning maksimal kinetik energiyasi foton energiyasiga va ish funktsiyasiga bog'liq.
Manba: Fizikadan yagona davlat imtihoni 06/06/2013. asosiy to'lqin. Sibir. Variant 2.
Vodorod atomidagi elektronning energiya darajalari eV formulasi bilan berilgan, bu erda. Atom bir holatdan holatga o'tganda, atom foton chiqaradi. Fotokatod yuzasida bir marta bu foton fotoelektronni uradi. Fotokatodning sirt materiali uchun fotoelektr effektining qizil chegarasiga to'g'ri keladigan yorug'lik to'lqin uzunligi, Fotoelektron impulsining maksimal mumkin bo'lgan moduli qancha?
Yechim.
Bor postulatlariga ko'ra, yorug'lik atom quyi energiya darajalariga o'tganda chiqariladi, fotonlar esa boshlang'ich va oxirgi holatlarning energiyalari orasidagi farqga teng energiyani olib yuradi. Shunday qilib, chiqarilgan foton energiyaga ega edi
Fotoelektr effekt tenglamasiga ko'ra, chiqarilgan fotoelektronlarning maksimal kinetik energiyasi foton energiyasiga va ish funktsiyasiga bog'liq.
Ish funktsiyasi qizil chegaraning to'lqin uzunligi bilan bog'liq:
Shunday qilib, fotoelektronning maksimal mumkin bo'lgan impulsi
Manba: Fizikadan yagona davlat imtihoni 06/06/2013. asosiy to'lqin. Sibir. Variant 3.
Energy levels of terms of of terms are given by the formula
qayerda. Atom bir holatdan holatga o'tganda, atom foton chiqaradi. Fotokatod yuzasida bir marta bu foton fotoelektronni uradi. Fotokatod sirtining materiali uchun fotoelektr effektining qizil chegarasiga mos keladigan yorug'lik chastotasi, Hz. Fotoelektronning maksimal mumkin bo‘lgan kinetik energiyasi qancha?
Yechim.
Bor postulatlariga ko'ra, yorug'lik atom quyi energiya darajalariga o'tganda chiqariladi, fotonlar esa boshlang'ich va oxirgi holatlarning energiyalari orasidagi farqga teng energiyani olib yuradi. Shunday qilib, chiqarilgan foton energiyaga ega edi
Fotoelektr effekt tenglamasiga ko'ra, chiqarilgan fotoelektronlarning maksimal kinetik energiyasi foton energiyasiga va ish funktsiyasiga bog'liq.
Ish funktsiyasi qizil chegara chastotasi bilan bog'liq:
Shunday qilib, fotoelektronning maksimal mumkin bo'lgan kinetik energiyasi






