Atomlarning energiya darajalari. Bor postulatlari va orbitani kvantlash
Yadroga tortish kuchlari ta'sirida elektron uchun Shredinger tenglamasi hech kim uchun emas, balki faqat ma'lum energiya qiymatlari uchun echimlarga ega. Shunday qilib, atomdagi elektronning energiya holatlarini kvantlash (ya'ni, Borning birinchi postulati) elektronga xos bo'lgan to'lqin xususiyatlarining oqibati bo'lib chiqadi va maxsus postulatlarni kiritishni talab qilmaydi.
Va biror narsa siz uchun yaxshi bo'lmasa, mushak aslida zaiflikni ko'rsatadi, lekin faqat u orqali o'tadigan energiya zaiflashgani uchun. O'zingiz yoki boshqalar haqida salbiy fikrlarga ega bo'lganingizda, shuningdek, biror modda, oziq-ovqat yoki dori, niyat yoki qaror sizga to'g'ri kelmasa yoki shunchaki sizning manfaatingizga mos kelmasa, energiyangiz zaiflashadi.
Energiya sinovi nima?
Bu sizning energiyangizning halol reaktsiyasi, tanangizdagi mushaklarning reaktsiyasiga "qulay". Rasmda ko'rsatilganidek, qo'lingizni yuqoriga va pastga ko'taring, qo'lingizni uzating, lekin juda ko'p siqmang va ismingizni ayting. Ehtimol, u qo'lini qimirlata olmaydi, chunki mushak kuchli bo'lib qoladi, chunki sizning energiyangiz bayonotga mos keladi va bu siz uchun to'g'ri ekanligini biladi.
Oxirgi iborani yaxshiroq tushunish uchun atomning soddalashtirilgan modelini, ya'ni "bir o'lchovli atom" ni ko'rib chiqing, unda elektron faqat hosil qilishi mumkin. tebranish harakatlari ekstremal nuqtalar orasida.
Shuningdek, atomning chegaralari elektron uchun o'tib bo'lmaydi, shuning uchun u faqat atom ichida bo'lishi mumkin deb hisoblaymiz. Biz allaqachon bilamizki, atomdagi elektronning holati ma'lum bir to'lqin ("de Broyl to'lqini") bilan tavsiflanadi. Ammo bu to'lqinning tarqalishini suv yuzasida tashlangan toshdan hosil bo'lgan to'lqinning harakatiga o'xshash narsa sifatida tasavvur qilish noto'g'ri bo'ladi: suv to'lqini o'z hosil bo'lgan joydan cheksiz harakat qiladi va asta-sekin tarqaladi, u qiladi. vaqt o'tishi bilan barqarorlikka ega emas, atomdagi elektron esa barqaror. Shuning uchun atomdagi elektronning holati va to'g'ridan-to'g'ri to'lqinlar hosil bo'lgan tovush chizig'ining holati o'rtasidagi o'xshashlik to'g'riroq bo'ladi.
Do'stingizga qo'lingizning kuchini sinab ko'ring va u uni qanchalik oson olib tashlashini ko'ring. Sizning energiya tizimingiz bu haqiqat emasligini biladi. Endi yoqimli va quvonchli narsani tasavvur qiling va sinov mushaklarning kuchini ko'rsatadi va sizning qo'lingiz cho'zilgan bo'lib qoladi. Salbiy fikrni yoki boshqa odam uchun yomon narsani ko'rib chiqing yoki yig'layotganingizni va xafa bo'lishingizni tasavvur qiling va qo'lingiz osongina olib tashlanadi. Salbiy bo'lganingizda, stressda bo'lganingizda yoki biror narsa noto'g'ri yoki siz uchun yaxshi bo'lmasa, u sizning energiyangizni qanday zaiflashtirishini ko'rasiz.
Albatta, bu oddiy va umumiy tavsif energiya sinovi. U sizga ko'p narsalarni aytib berishi mumkin edi va agar siz juda havaskor bo'lsangiz, u bilan shug'ullanasiz. Biroq, energiya psixologiyasida vosita sifatida foydalanilganda, u energiya meridianining blokirovkalarini aniqlashning o'ta ishonchli va xavfsiz vositasiga aylanadi, shuningdek, energiya oqimini muvozanatlash va tiklashning eng to'g'ri yo'lini va shuning uchun sog'lig'ingizni tiklash vositasiga aylanadi.
Shaklda. 6 sxematik tarzda tebranuvchi ipda paydo bo'ladigan, ekstremal nuqtalari mahkamlangan tik turgan to'lqinlarni tasvirlaydi. N harfi bilan belgilangan nuqtalarda antinodlar paydo bo'ladi - bu erda tebranish amplitudasi maksimal, y nuqtalarda ip tebranmaydi - bu tebranish amplitudasi nolga teng bo'lgan tugunlar; tugunlar va antinodlar o'rtasida joylashgan nuqtalarda tebranish amplitudasi oraliq qiymatlarga ega. Ipning so'nggi nuqtalari aniqlanganligi sababli, bu erda tugunlar bo'lishi kerak. Oddiy "sayohat qiluvchi" to'lqindan farqli o'laroq, tik turgan to'lqin kosmosda harakat qilmaydi va energiyani o'tkazmaydi, bu faqat ipning bir nuqtasidan ikkinchisiga o'tkaziladi. Ko'rish oson (6-rasm) uchlari mahkamlangan ipda turgan to'lqin uzunligi hech qanday bo'lmasligi mumkin, faqat butun ip mos keladigan tarzda bo'lishi mumkin. butun son yarim to'lqinlar: bitta (6-rasm, a), ikkita (6-rasm, b), uchta (6-rasm, c) va boshqalar.
Yuqorida tavsiflangan energiyani tekshirish usullari sizning terapevtingiz yoki do'stingiz bo'lishi mumkin bo'lgan sherik bilan amalga oshiriladi. O'zingizni sinab ko'rish va kerakli javoblarni olishning boshqa usullari mavjud. Ular murakkab emas, arzon va hazm qilish oson. Bu o'z sog'lig'ingiz uchun javobgarlikni o'z zimmangizga olish va o'z kuchingiz bilan "gapirish" ni o'rganishning yana bir usuli.
Shunday qilib, siz o'zingizda shubha tug'diradigan qarorlarni, duch keladigan sof hayotiy qarorlarni va sog'ligingiz va hayotingiz uchun muhim bo'lgan boshqa ko'plab narsalarni ishonchli tarzda sinab ko'rishingiz mumkin. Energiya testining imkoniyatlari deyarli cheksizdir, chunki bu sizning ongsiz ongingizga yorliq bo'lib, u erda barcha javoblar mavjud.
Ko'rib chiqilayotgan atomning bir o'lchovli modelida de Broyl to'lqini ham turishi kerak: bu elektronning atom chegarasidan tashqariga chiqa olmasligidan va natijada to'lqin funktsiyasidan kelib chiqadi (ya'ni, amplituda. to'lqin) atom chegaralarida yo'q bo'lib ketishi kerak. Shuning uchun shakl. 6 ni bu atomda hosil bo'lishi mumkin bo'lgan de Broyl to'lqinlari bilan bir o'lchovli atom modeli sifatida ko'rib chiqish mumkin.
Agar bir o'lchovli atomning uzunligi l bo'lsa, u holda a, b va c holatlar uchun shakl. 6 de Broyl to'lqin uzunligi quyidagicha ifodalanadi:
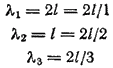
Shuning uchun, doimiy to'lqin faqat agar paydo bo'lishi mumkin
bu erda, ya'ni butun son.
Guruch. 6. Ip ustida turgan to‘lqinlar.
Boshqa tomondan, de Broyl tenglamasiga ko'ra
Oxirgi ikkita tenglamaning to'g'ri qismlarini tenglashtirib, biz elektron tezligining ifodasini olamiz:
Endi elektronning tezligini bilib, uni topishimiz mumkin kinetik energiya E:
n butun son bo‘lgani uchun oxirgi ifoda bir o‘lchovli atomdagi elektronning energiyasi ixtiyoriy qiymatlarga ega bo‘lmasligini ko‘rsatadi: n=1 uchun u kasr qiymatiga teng, n=2 uchun esa 4 marta katta. , n=3 uchun - 9 marta ko'p va hokazo. Shunday qilib, bir o'lchovli atomda to'lqin xususiyatlari de-Broyl tenglamasi bilan ifodalangan elektron haqiqatan ham elektronning energiya holatlarini kvantlashtirishga ega. Bunda elektronning ruxsat etilgan energiya darajalari kvant soni deb ataladigan n butun sonning qiymati bilan aniqlanadi.
Albatta, elektron energiyasining topilgan ifodasi atomning soddalashtirilgan modeliga ishora qiladi. Lekin haqiqiy atom uchun Shredinger tenglamasining yechimi ham atomdagi elektronning energiya holatlari kvantlangan degan xulosaga keladi.
Bir o'lchovli atom modeli nima uchun statsionar holatdagi atomdagi elektron elektromagnit energiyani chiqarmasligini tushunish imkonini beradi (Bor nazariyasining ikkinchi postulati). Bor-Rezerford modeliga ko'ra, atomdagi elektron tezlanish bilan uzluksiz harakat qilgan, ya'ni u doimo o'z holatini o'zgartirgan; elektrodinamika talablariga muvofiq, u bir vaqtning o'zida energiyani chiqarishi kerak. Atomning bir o'lchovli modelida statsionar holat turgan de Broyl to'lqinining hosil bo'lishi bilan tavsiflanadi; bu to'lqinning to'lqin uzunligi doimiy bo'lib qolar ekan, elektronning holati o'zgarishsiz qoladi, shuning uchun nurlanish sodir bo'lmasligi kerak.
Bir statsionar holatdan ikkinchisiga (Bor terminologiyasida, bir statsionar orbitadan ikkinchisiga) o'tishdagi elektronning holati to'g'risidagi masala ham aniq bo'ladi. Agar, masalan, shaklga mos keladigan holatdan elektron bo'lsa. 6, a, shaklga mos keladigan holatga o'tadi. 6b, keyin bu o'tish paytida de Broyl to'lqin uzunligi doimiy to'lqin hosil bo'lish shartiga javob bermaydigan o'zgaruvchan qiymatga ega bo'ladi. Shuning uchun bu vaqt oralig'idagi elektronning holati beqaror bo'ladi; u de-Broyl toʻlqin uzunligi yana turgan toʻlqin hosil boʻlish shartiga toʻgʻri kelguncha, yaʼni elektron yangi statsionar holatga kelguncha oʻzgaradi.
Atomning soddalashtirilgan bir o'lchovli modelida elektronning yadroga nisbatan joylashuvi bitta koordinata bilan, uning holati esa bitta kvant sonining qiymati bilan aniqlanadi. Atomning ikki o'lchovli (tekis) modelida elektronning holati ikkita koordinata bilan aniqlanadi; shunga ko'ra, uning holati ikkita kvant sonining qiymatlari bilan tavsiflanadi. Xuddi shunday, atomning uch o'lchovli (hajmli) modelida elektronning holati uchta kvant sonining qiymatlari bilan aniqlanadi. Va nihoyat, haqiqiy atomlarni tashkil etuvchi elektronlarning xususiyatlarini o'rganish elektronning elektronning fazoviy holatiga bog'liq bo'lmagan yana bir kvantlangan fizik xususiyatga ega ekanligini ko'rsatdi (spin deb ataladigan narsa, § 30-ga qarang). Shunday qilib, haqiqiy atomdagi elektronning holatini to'liq tavsiflash uchun to'rtta kvant sonining qiymatlarini ko'rsatish kerak.
28. Asosiy kvant soni. Demak, atomning bir o'lchovli modelida elektronning energiyasi faqat ma'lum qiymatlarni qabul qilishi mumkin, boshqacha aytganda, u kvantlangan. Haqiqiy atomdagi elektronning energiyasi ham kvantlangan kattalikdir. Atomdagi elektronning mumkin bo'lgan energiya holatlari musbat butun qiymatlarni qabul qilishi mumkin bo'lgan asosiy kvant soni n qiymati bilan aniqlanadi: 1, 2, ... va hokazo. Elektron n = 1 da eng past energiyaga ega. n ortishi bilan elektronning energiyasi ortadi. Shuning uchun elektronning asosiy kvant sonining ma'lum bir qiymati bilan tavsiflangan holati odatda atomdagi elektronning energiya darajasi deb ataladi: n=1 da elektron birinchi energiya darajasida, n=2 da. - ikkinchisida va boshqalar.
Asosiy kvant soni elektron bulutning hajmini ham aniqlaydi. Elektron bulutining hajmini oshirish uchun uning bir qismini yadrodan kattaroq masofaga o'tkazish kerak. Bunga elektronning yadroga elektrostatik tortishish kuchlari to'sqinlik qiladi, ularni engish energiya sarflashni talab qiladi. Shunung uchun katta o'lchamlar Elektron buluti atomdagi elektronning yuqori energiyasiga va shuning uchun n bosh kvant sonining kattaroq qiymatiga mos keladi. Asosiy kvant sonining bir xil qiymati bilan tavsiflangan elektronlar atomda taxminan bir xil o'lchamdagi elektron bulutlarni hosil qiladi; Shuning uchun biz atomda elektron qatlamlarning mavjudligi haqida gapirishimiz mumkin yoki elektron qobiqlar bosh kvant sonining ma'lum qiymatlariga mos keladi.
Atomdagi elektronning energiya darajalari uchun (ya'ni, elektron qatlamlar yoki qobiqlar uchun) n ning turli qiymatlariga mos keladigan quyidagi harf belgilari qabul qilinadi.
Atomdagi elektronning holati to'rtta kvant soni bilan tavsiflanadi. Asosiy kvant soni n atomdagi elektronning energiyasini va AO ning o'lchamini aniqlaydi, ya'ni. elektronning yadrodan uzoqligi. Asosiy kvant soni n 1, 2, 3, 4 butun sonlarning qiymatlarini oladi ... n ning qiymati bir xil bo'lgan elektronlar to'plami energiya darajasi deb ataladi. Yadrodan birinchi energiya darajasidagi elektronlar (n=1) eng kam energiyaga ega; n ortishi bilan elektronning energiyasi va uning yadrodan masofasi ortadi. Atomning holati, uning elektronlari shunday energiya darajasida bo'lib, ularning umumiy energiyasi minimal bo'lsa, asosiy yoki qo'zg'atilmagan holat deb ataladi. Yuqori energiya qiymatiga ega bo'lgan holatlar hayajonlangan holatlar deb ataladi. Energiya darajalari harflar bilan belgilanadi:
Raqamli qiymat n 1 2 3 4 5 6 7
Harf belgisi K L M N O P Q
Asosiy holatdagi atomdagi energiya darajalari soni element joylashgan davr soniga teng.
Xuddi shu energiya darajasida energiya jihatidan bir-biridan farq qiladigan turli shakldagi atom orbitallari bo'lishi mumkin. Shuning uchun energiya darajalari pastki darajalarga bo'linadi. Atom orbitalining pastki sathidagi elektron energiyasi va shakli orbital kvant soni bilan tavsiflanadi. l. Ma'nosi l asosiy kvant soniga bog'liq: l 0 dan (n-1) gacha bo'lgan qiymatlarni oladi, ya'ni 0, 1, 2, 3... (n-1). Berilgan energiya darajasida bir xil qiymat bilan tavsiflangan elektronlar to'plami l, energiya pastki darajasi deb ataladi. Pastki darajalar harflar bilan belgilanadi:
Orbital kvant soni l 0 1 2 3
Energiyaning pastki darajali belgisi s p d f
Shunday qilib, da l = 0, 1, 2, 3 elektronlar mos ravishda s-, p-, d-, f-kichik darajalarda. Har xil kichik darajadagi elektronlar s-, p-, d-, f-elektronlar deb ataladi. Bunda s-, p-, d-, f-elektronlarning yoki s-, p-, d-, f-atom orbitallarining holatlari haqida ham gap boradi.
18. Bosh kvant soni.
Bosh kvant soni butun son bo'lib, energiya darajasida elektronning holatini belgilaydi. Energiya darajasi yaqin energiya qiymatlariga ega bo'lgan atomdagi elektronning statsionar holatlari to'plamidir. Bosh kvant soni elektronning yadrodan uzoqligini aniqlaydi va xarakterlaydi elektron energiyasi bu darajani egallagan.
19. Orbital kvant soni. Elektron bulutlarning shakllari
Orbital kvant soni- kvant fizikasida elektronning atomdagi to'lqin funksiyasi amplitudasining taqsimlanish shaklini, ya'ni elektron bulutining shaklini belgilovchi kvant soni ℓ. Asosiy (radial) kvant soni bilan ko'rsatilgan energiya darajasining pastki darajasini aniqlaydi n va qiymatlarni qabul qilishi mumkin
Xususiy qiymatdir operator orbital impuls elektronning burchak momentidan farq qiladigan elektron j faqat aylanish operatorida s:
Orbital kvant soni va umumiy impulsning kvant soni o'rtasidagi farq mutlaq qiymatda (elektron spinidan) oshmaydi. Azimutal kvant soni elektron bulutining kosmosdagi yo'nalishini aniqlaydi.
Mexanik modelga ko'ra elektron bulut shakli atom atom yadrosi shaklining natijasidir. Atomlarni bir-biriga bog'laydigan kuchlarning manbalari elektron bulutlarning bir-biriga yopishgan zonalari hisoblanadi. Qoplash zonalari bir vaqtning o'zida ikkala aloqa qiluvchi atomlarning elektron bulutlarining bir qismidir. Qanchalik bir-biriga yopishgan zonalar ko'p bo'lsa, atomlar orasidagi bog'lanish shunchalik kuchli bo'ladi. Elektron bulutning har bir elektroni o'z traektoriyasining ko'p qismida asosan yadro protonlaridan biri bilan o'zaro ta'sir qiladi va elektron bulutning bir qismini - elektron lobni tashkil qiladi. Ammo bir-biriga yopishgan zonalarda elektronlar bir elektron lobdan ikkinchisiga o'tishi mumkin. Tugallangan yadro qobig'ining protonlari bilan bog'langan elektron barglari atomlararo bog'lanishlarda qatnashmaydi. Ular uzluksiz elektron bulutiga birlashadilar, ularning chegaralari ajratilgan elektron gulbarglarning uchlariga qaraganda yadro markaziga ancha yaqinroqdir. Shu sababli, uzluksiz elektron bulut qo'shni atomlarning elektron bulutlariga etib bormaydi va ular bilan bir-biriga yopishgan zonalarni yaratishga qodir emas. Atomlararo aloqalar faqat izolyatsiyalangan elektron gulbarglarni yaratishga qodir. Ular qattiq elektron bulutlaridan uzoqqa cho'ziladi va boshqa atomlarning o'xshash elektron bo'laklariga jalb qilinadi va bir-birining ustiga chiqadigan zonalarni yaratadi. Atomlarning tortishishi tortishishning tortishish kuchlari va elektron qobig'ining elastiklik kuchlari o'rtasida muvozanatga erishilgunga qadar sodir bo'ladi. Bundan kelib chiqadiki, atomning elektron bulutining chegaralari qat'iy belgilanmagan va atomlar zichligi o'zgarishi bilan o'zgarishi mumkin. Shunga ko'ra, atomning hajmi ham o'zgarishi mumkin. Maksimal qadoqlashda bir xil atom izomerlarining elektron bulutlari orasidagi o'zaro bog'lanish zonalarining nazariy jihatdan mumkin bo'lgan konfiguratsiyasini qurishga harakat qilaylik. Bunday bir-biriga yopishgan bir xil turdagi atomlar bitta kristall - davriy tuzilishga ega bo'lgan yirik yirik molekula hosil qilish qobiliyatiga ega.






