Какие вещества имеют постоянную температуру плавления. Плавление
РЕФЕРАТ
«Плавление тел»
Выполнила:
Присяжнюк Ольга 9-А
Проверила:
Невзорова Татьяна Игоревна
Введение
1) Расчет количества теплоты
2) Плавление
3) Удельная теплота плавления
4) Плавление металлов
5) Температура плавления и кипения воды
6) Расплавы
7) Интересное о плавлении
Использование знаний в других контекстах, связанных с ними условиях
Свойства материи и особенно воды играют определенную роль во многих явлениях. Здесь, например, следует упомянуть метеорологический цикл воды и эвапотранспирация живых организмов. Айсберги состоят из чистой воды, поэтому они считаются источниками питьевой воды. Но также производство пресной воды из соленой воды в морях теоретически и технически не является трудностью и является часто применяемой процедурой в странах с небольшой питьевой водой, но богатыми источниками энергии. Единственная проблема - экономическая жизнеспособность.
Заключение (выводы)
Введение
Агрега́тное состоя́ние - состояние вещества, характеризующееся определёнными качественными свойствами: способностью или неспособностью сохранять объём и форму, наличием или отсутствием дальнего и ближнего порядка и другими. Изменение агрегатного состояния может сопровождаться скачкообразным изменением свободной энергии, энтропии, плотности и других основных физических свойств.
В Интернете вы найдете много страниц, на которых написано плавление и испарение. Конечно, есть и многое. Но некоторые вопросы остаются такими же хорошими, как всегда без ответа. Почему некоторые вещества имеют очень низкую температуру плавления, другие имеют высокую температуру плавления?
- Какие процессы происходят во время плавления и испарения?
- Итак, почему ткани имеют такие разные точки кипения?
Какие процессы происходят во время плавления?
Почему некоторые вещества не тают или кипятят, а разлагаются раньше? . Термины кипения и испарения используются на этой странице одинаково. Более подробную информацию можно найти на этой странице.
Первый шаг: как создается твердое вещество
Каждое твердое вещество состоит из мельчайших частиц. Между частицами, которые удерживают их, есть силы. Они всегда являются электростатическими. Характер частиц и сила сил очень многочисленны. Вы можете найти точное собрание на моей странице о привязках. Вот краткое резюме.Выделяют три основных агрегатных состояния: твёрдое тело, жидкость и газ. Иногда не совсем корректно к агрегатным состоянием причисляют плазму. Существуют и другие агрегатные состояния, например, жидкие кристаллы или конденсат Бозе - Эйнштейна.
Изменения агрегатного состояния суть термодинамические процессы, называемые фазовыми переходами. Выделяют следующие их разновидности: из твёрдого в жидкое - плавление; из жидкого в газообразное - испарение и кипение; из твёрдого в газообразное - сублимация; из газообразного в жидкое или твёрдое - конденсация. Отличительной особенностью является отсутствие резкой границы перехода к плазменному состоянию.
Второй шаг: что происходит, когда твердое тело нагревается ниже его температуры плавления?
Если вещество нагревается нагреванием, наименьшие частицы поглощают эту энергию. Они говорят, что их внутренняя энергия растет. Внутренняя энергия может быть в трех типах: энергия вибрации, энергия вращения и энергия электронов. Энергия электронов не имеет значения для плавления и кипения. Электроны, которые достигают более высокого уровня энергии, остаются там только некоторое время, а затем возвращаются к исходному уровню. Энергия высвобождается и оставляет твердое тело. Здесь происходят такие явления, как фосфоресценция и флуоресценция.
Для описания различных состояний в физике используется более широкое понятие термодинамической фазы. Явления, описывающие переходы от одной фазы к другой, называют критическими явлениями.
Твёрдое тело: Состояние, характеризующееся способностью сохранять объём и форму. Атомы твёрдого тела совершают лишь небольшие колебания вокруг состояния равновесия. Присутствует как дальний, так и ближний порядок.
Давайте посмотрим на вибрацию? и вращательная сила немного ближе. Мелкие частицы движутся определенным образом. Некоторые возможности для этих движений теперь перечислены. Растяжка. 2 атома, соединенные связью, вибрируют вдоль оси связывания, так что связывание периодически становится короче и длиннее. Только молекулы могут выполнять валентные колебания, так как они обладают только связью внутри частицы. Изгиб вибрации. 3 атома, связанные облигациями, вибрируют так, что угол между двумя связями периодически меньше и больше. Молекулы не менее 3 атомов могут вызывать деформационные колебания. Большие и более сложные молекулы могут выполнять сложные комплексные колебания. Простым примером является инверсия молекулы аммиака. Вся частица может вращаться вокруг своего центра тяжести. Часть молекулы может вращаться вокруг одной связи.
- Вибрации частицы вокруг ее центрального положения.
- То есть ион или молекула колеблются взад-вперед, как маятник.
- Каждая из мельчайших частиц с первого шага может выполнять такие вибрации.
Жидкость: Состояние вещества, при котором оно обладает малой сжимаемостью, то есть хорошо сохраняет объём, однако неспособно сохранять форму. Жидкость легко принимает форму сосуда, в который она помещена. Атомы или молекулы жидкости совершают колебания вблизи состояния равновесия, запертые другими атомами, и часто перескакивают на другие свободные места. Присутствует только ближний порядок.
При низких температурах частицы несут только медленные колебания с низкой амплитудой и медленно вращаются. Если твердое тело нагревается, вибрации и вращения становятся быстрее, а вибрации увеличивают их амплитуду. Поэтому мельчайшие частицы поглощают теплоту тепла и преобразуют ее в энергию движения.
Третий шаг: Какие процессы происходят во время плавления?
Могут ли мельчайшие частицы поглощать неограниченное количество тепла? В предыдущих двух параграфах мы видели два свойства мельчайших частиц в твердом теле. Между ними работают электростатические аттракторы. Они приводят к определенной энергии связи. Он не зависит от температуры. С другой стороны, кинетическая энергия содержится в частицах. Это тем больше, чем выше температура.
Газ: Состояние, характеризующееся хорошей сжимаемостью, отсутствием способности сохранять как объём, так и форму. Газ стремится занять весь объём, ему предоставленный. Атомы или молекулы газа ведут себя относительно свободно, расстояния между ними гораздо больше их размеров.
Другие состояния: При глубоком охлаждении некоторые (далеко не все) вещества переходят в сверхпроводящее или сверхтекучее состояние. Эти состояния, безусловно, являются отдельными термодинамическими фазами, однако их вряд ли стоит называть новыми агрегатными состояниями вещества в силу их неуниверсальности. Неоднородные вещества типа паст, гелей, суспензий, аэрозолей и т. д., которые при определённых условиях демонстрируют свойства как твёрдых тел, так и жидкостей и даже газов, обычно относят к классу дисперсных материалов, а не к каким-либо конкретным агрегатным состояниям вещества.
Если твердое тело нагревается, кинетическая энергия его мельчайших частиц возрастает. В какой-то момент он больше, чем энергия связи. Можно представить себе, что силы притяжения между частицами уже недостаточно сильны, чтобы выдерживать силы, вызванные тепловыми колебаниями. Частицы теперь движутся независимо друг от друга, и это как раз характеристика жидкости. Твердое вещество плавится.
Почему жидкости жидкие?
В жидкости частицы, таким образом, больше не удерживаются силами электростатического притяжения. Красная стрелка показывает, что происходит, когда вы. твердое вещество нагревают при низком давлении. Этот процесс называется сублимацией. Это легко понять, потому что линия аргументации проста. Энергия связи слишком мала, силы притяжения слишком слабы, чтобы удерживать частицы вместе, поэтому они расходятся. Однако, если вы не просто знаете информацию о школьных книгах, вы найдете здесь противоречие и зададите себе вопрос.
Плавление
Рис. 1. Состояние чистого вещества (диаграмма)
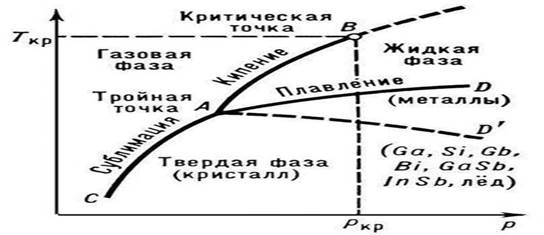
Рис. 2. Температура плавления кристаллического тела
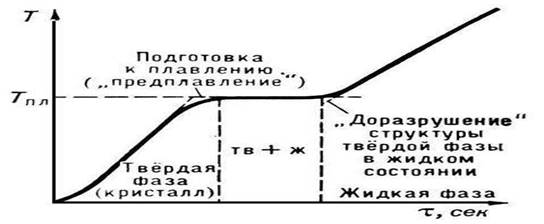
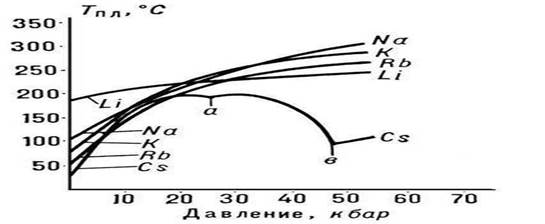
Рис. 3. Температура плавления щелочных металлов
Плавление - переход вещества из кристаллического (твёрдого) состояния в жидкое; происходит с поглощением теплоты (фазовый переход I рода). Главными характеристиками П. чистых веществ являются температура плавления (Тпл) и теплота, которая необходима для осуществления процесса П. (теплота плавления Qпл).
В жидкости частицы почти всегда не отделены друг от друга, они все еще почти так же близки, как и в твердом теле. Почему они не снимают себя, как в газе? Другими словами, почему твердое вещество не сразу попадает в газообразное состояние во время плавления?
Давление играет ключевую роль
Они делают это при низком давлении. Только при высоком давлении они становятся жидкими. Это давление, которое удерживает твердые частицы от прямого попадания в газообразное состояние? Является ли давление причиной того, что жидкости существуют вообще?
Температура П. зависит от внешнего давления р; на диаграмме состояния чистого вещества эта зависимость изображается кривой плавления (кривой сосуществования твёрдой и жидкой фаз, AD или AD" на рис. 1). П. сплавов и твёрдых растворов происходит, как правило, в интервале температур (исключение составляют эвтектики с постоянной Тпл). Зависимость температуры начала и окончания П. сплава от его состава при данном давлении изображается на диаграммах состояния специальными линиями (кривые ликвидуса и солидуса, см. Двойные системы). У ряда высокомолекулярных соединений (например, у веществ, способных образовывать жидкие кристаллы) переход из твёрдого кристаллического состояния в изотропное жидкое происходит постадийно (в некотором температурном интервале), каждая стадия характеризует определённый этап разрушения кристаллической структуры.
Давайте подробнее рассмотрим роль давления. Частицы внутри окружены соседями. окруженные и привлеченные ими. Частицы на поверхности имеют несколько соседей. Посмотрите на картинку справа. Он показывает часть жидкости, но отношения в твердых телах в принципе одинаковы.
Частицы в изображении являются сферическими, но отношения одинаковы для молекул или ионов различной формы. Во-первых, посмотрите на частицу внутри. Он окружен другими частицами во всех направлениях. Между частицей и всеми ее соседями есть аттракторы. Это кулоновские силы, которые были подробно описаны на первом этапе. Естественно, они присутствуют как в жидкости, так и в твердом теле, и они все еще сильны, как и до плавления. На рисунке они представлены черными линиями. Одна частица подсвечена, она имеет 7 соседей, к которым действуют кулоновские силы.
Наличие определённой температуры П.- важный признак правильного кристаллического строения твёрдых тел. По этому признаку их легко отличить от аморфных твёрдых тел, которые не имеют фиксированной Тпл. Аморфные твёрдые тела переходят в жидкое состояние постепенно, размягчаясь при повышении температуры (см. Аморфное состояние). Самую высокую температуру П. среди чистых металлов имеет вольфрам (3410 °С), самую низкую - ртуть (-38,9 °С). К особо тугоплавким соединениям относятся: TiN (3200 °С), HfN (3580 °С), ZrC (3805 °С), TaC (4070 °С), HfC (4160 °С) и др. Как правило, для веществ с высокой Тпл характерны более высокие значения Qпл. Примеси, присутствующие в кристаллических веществах, снижают их Тпл. Этим пользуются на практике для получения сплавов с низкой Тпл (см., например, Вуда сплав с Тпл = 68 °С) и охлаждающих смесей.
Один из них уже отошел далеко от него. Если он движется дальше, он полностью покинет среду первой частицы. Но он все еще находится в жидкости, потому что он приблизится к другой частице, и связь между ними сформируется на короткое время. Частицы внутри жидкости не могут их покинуть, поскольку они едва перемещаются от одной соседней частицы, их привлекает другая.
В случае частиц на поверхности жидкости ситуация другая. На изображении изображены две такие частицы. У них есть соседи только внутри жидкости, и только для них кулоновские силы. Внешне едва ли есть соседи. Есть воздух или какой-то другой газ. Он имеет очень низкую плотность по сравнению с жидкостью, поэтому он содержит гораздо меньше частиц на единицу объема. Вы поймете, что вам следует более внимательно смотреть на частицы на поверхности. Есть ключ к ответу.
П. начинается при достижении кристаллическим веществом Тпл. С начала П. до его завершения температура вещества остаётся постоянной и равной Тпл, несмотря на сообщение веществу теплоты (рис. 2). Нагреть кристалл до Т > Тпл в обычных условиях не удаётся (см. Перегрев), тогда как при кристаллизации сравнительно легко достигается значительное переохлаждение расплава.
Частицы с большей или меньшей энергией
Распределение энергии частиц в жидкости. Мы всегда говорили, что частицы имеют определенную энергию из-за тепловых колебаний, и можно было подумать, что все частицы в капле жидкости имеют одинаковую энергию. Некоторые из них имеют более высокую энергию, другие - более низкую. Это легко понять, учитывая, что частицы сталкиваются. В зависимости от скорости и направления, в которых они сталкиваются, энергия передается от одной частицы к другой. Поскольку столкновения происходят довольно случайным образом, есть победители, чья энергия поднимается от ударов к удару, а также проигравших.
Характер зависимости Тпл от давления р определяется направлением объёмных изменений (DVпл) при П. (см. Клапейрона - Клаузиуса уравнение). В большинстве случаев П. вещества сопровождается увеличением их объёма (обычно на несколько %). Если это имеет место, то возрастание давления приводит к повышению Тпл (рис. 3). Однако у некоторых веществ (воды, ряда металлов и металлидов, см. рис. 1) при П. происходит уменьшение объёма. Температура П. этих веществ при увеличении давления снижается.
Распределение энергии частиц в одном. Оба распределения отличаются незначительно. Частицы испаряются. Область справа от красной линии внизу. Поэтому при 20 ° С меньше частиц имеют энергию, необходимую для испарения. может быть как при 50 ° С, так и при этой температуре испарение более устойчиво. Что происходит с победителями? Их энергия настолько велика, что они могут преодолеть кулоновские силы своих соседей. Просто потому, что так мало соседей, у них есть шанс одолеть привлекательность всех соседей.
И только потому, что их энергия настолько велика, они могут не только преодолеть эти достопримечательности на короткое время, но и снова поймать, но навсегда. Эти несколько частиц с высокой энергией оставляют капли жидкости. Они двигаются настолько, насколько это возможно, и никогда не возвращаются к своим каплям. Все знают описанное выше явление.
П. сопровождается изменением физических свойств вещества: увеличением энтропии, что отражает разупорядочение кристаллической структуры вещества; ростом теплоёмкости, электрического сопротивления [исключение составляют некоторые полуметаллы (Bi, Sb) и полупроводники (Ge), в жидком состоянии обладающие более высокой электропроводностью]. Практически до нуля падает при П. сопротивление сдвигу (в расплаве не могут распространяться поперечные упругие волны, см. Жидкость), уменьшается скорость распространения звука(продольных волн) и т.д.
Вы только что узнали, почему выпадает капля воды. Тепловая энергия некоторых частиц на поверхности достаточно велика, чтобы оставить капли. Поскольку мы просто говорим об испарении, вы также можете быстро очистить, так как это зависит от температуры. Уже непосредственно над точкой плавления будет несколько частиц, у которых достаточно энергии, чтобы оставить каплю. Чем выше температура, тем выше средняя энергия частиц, и все больше и больше частиц будут иметь энергию, необходимую для выхода из поверхности.
Закрытые системы они приносят больше ясности
В результате капля испаряется быстрее. Иллюстрация ниже иллюстрирует это. Еще раз, мы смогли объяснить повседневный опыт. Открытая система - это система обмена веществами и энергией с окружающей средой. Например, капля воды является открытой системой. Напротив, закрытые системы и замкнутые системы. Баллон с минеральной водой рисунка является хорошим примером замкнутой системы. Это около одной трети, заполненной жидкостью. Чтобы не делать излишне сложный аргумент, он должен быть заполнен чистой жидкостью, например водой, а не смесью, такой как минеральная вода или бензин.
Согласно молекулярно-кинетическим представлениям, П. осуществляется следующим образом. При подведении к кристаллическому телу теплоты увеличивается энергия колебаний (амплитуда колебаний) его атомов, что приводит к повышению температуры тела и способствует образованию в кристалле различного рода дефектов (незаполненных узлов кристаллической решётки - вакансий; нарушений периодичности решётки атомами, внедрившимися между её узлами, и др., см. Дефекты в кристаллах). В молекулярных кристаллах может происходить частичное разупорядочение взаимной ориентации осей молекул, если молекулы не обладают сферической формой. Постепенный рост числа дефектов и их объединение характеризуют стадию предплавления. С достижением Тпл в кристалле создаётся критическая концентрация дефектов, начинается П.- кристаллическая решётка распадается на легкоподвижные субмикроскопические области. Подводимая при П. теплота идёт не на нагрев тела, а на разрыв межатомных связей и разрушение дальнего порядка в кристаллах (см. Дальний порядок и ближний порядок). В самих же субмикроскопических областях ближний порядок в расположении атомов при П. существенно не меняется (координационное число расплава при Тпл в большинстве случаев остаётся тем же, что и у кристалла). Этим объясняются меньшие значения теплот плавления Qпл по сравнению с теплотами парообразования и сравнительно небольшое изменение ряда физических свойств веществ при их П.
Процесс П. играет важную роль в природе (П. снега и льда на поверхности Земли, П. минералов в её недрах и т.д.) и в технике (производство металлов и сплавов, литьё в формы и др.).
Удельная теплота плавления
Уде́льная теплота́ плавле́ния (также: энтальпия плавления; также существует равнозначное понятие уде́льная теплота́ кристаллиза́ции) - количество теплоты, которое необходимо сообщить одной единице массы кристаллического вещества в равновесном изобарно-изотермическом процессе, чтобы перевести его из твёрдого (кристаллического) состояния в жидкое (то же количество теплоты выделяется при кристаллизации вещества). Теплота плавления - частный случай теплоты фазового перехода I рода. Различают удельную теплоту плавления (Дж/кг) и молярную (Дж/моль).
Удельная теплота плавления обозначается буквой
(греческая буква лямбда) Формула расчёта удельной теплоты плавления: , - удельная теплота плавления, - количество теплоты, полученное веществом при плавлении (или выделившееся при кристаллизации), - масса плавящегося (кристаллизующегося) вещества.
Плавление металлов
При плавлении металлов необходимо соблюдать известные правила. Положим, что собираются плавить свинец и цинк. Свинец быстро расплавится, имея температуру плавления 327°; цинк же еще долго будет оставаться твердым, так как его температура плавления выше 419°. Что произойдет со свинцом при таком перегреве? Он начнет покрываться пленкой радужного цвета, а потом его поверхность окажется скрытой под слоем неплавящегося порошка. Свинец угорел от перегрева, окислился, соединившись с кислородом воздуха. Этот процесс, как известно, происходит и при обычной температуре, но при нагревании он идет гораздо быстрее. Таким образом, к тому времени, когда начнет плавиться цинк, останется очень мало металлического свинца. Сплав получится совсем не того состава, как предполагался, и потеряется большое количество свинца в виде угара. Ясно, что надо сначала плавить более тугоплавкий цинк и затем класть в него свинец. То же самое произойдет, если сплавлять цинк с медью или латунью, разогревая сначала цинк. Цинк угорит к моменту расплавления меди. Значит, надо всегда сначала плавить металл с более высокой температурой плавления.
Но одним этим угара не избежать. Если правильно разогретый сплав долго держать на огне, опять образуется на поверхности жидкого металла пленка как следствие угара. Ясно, что опять обратится в окись более легкоплавкий металл и состав сплага изменится; значит, нельзя металл долго перегревать без надобности. Поэтому стараются всячески уменьшить угар металла, укладывая его компактной массой; мелкие куски, опилки, стружки сначала „пакетируют”, плавят куски более или менее одинаковой величины, ведут нагрев при достаточной температуре, оберегают поверхность металла от соприкосновения с воздухом. Для этой цели мастер может брать буру или просто прикрывать поверхность металла слоем золы, которая всегда будет плавать наверху (благодаря своему меньшему удельному весу) и при выливании металла не помешает. При застывании металла происходит еще одно явление, вероятно также знакомое юным мастерам. Металл, застывая, уменьшается в объеме, причем это уменьшение происходит за счет внутренних, еще не застывших частиц металла. На поверхности отливки или внутри нее образуется более или менее значительное воронкообразное углубление, так называемая усадочная раковина. Обычно форму делают так, чтобы усадочные раковины получились в тех местах отливки, которые впоследствии удаляются, стараясь по возможности предохранить самое изделие. Понятно, что усадочные раковины портят отливку и иногда могут сделать ее негодной. После расплавления металл несколько перегревают, чтобы он был жиже и горячее и поэтому лучше заполнил бы детали формы и не застыл бы преждевременно от соприкосновения с более холодной формой.
Так как температура плавления сплавов обычно ниже температуры плавления наиболее тугоплавкого из составляющих сплав металлов, то иногда выгодно поступать наоборот: сперва расплавить более легкоплавкий металл, а затем - более тугоплавкий. Однако это допустимо лишь для металлов, не сильно окисляющихся, или при условии предохранения этих металлов от излишнего окисления. Металла надо брать больше, чем требуется для самой вещи, чтобы он заполнил не только форму, но и литниковый канал. Ясно, что надо сначала рассчитать необходимое количество металла.
Температура плавления и кипения воды
Самое удивительное и благостное для живой природы свойство воды - это ее способность при "нормальных" условиях быть жидкостью. Молекулы очень похожих на воду соединений (например, молекулы H2S или H2Se) намного тяжелее, а образуют при тех же условиях газ. Тем самым вода как будто противоречит закономерностям таблицы Менделеева, которая, как известно, предсказывает, когда, где и какие свойства веществ будут близки. В нашем случае из таблицы следует, что свойства водородных соединений элементов (называемых гидридами), расположенных в одних и тех же вертикальных столбцах, с ростом массы атомов должны изменяться монотонно. Кислород - элемент шестой группы этой таблицы. В этой же группе находятся сера S (с атомным весом 32), селен Se (с атомным весом 79), теллур Te (с атомным весом 128) и поллоний Po (с атомным весом 209). Следовательно, свойства гидридов этих элементов должны меняться монотонно при переходе от тяжелых элементов к более легким, т.е. в последовательности H2Po → H2Te → H2Se → H2S → H2O. Что и происходит, но только с первыми четырьмя гидридами. Например, температуры кипения и плавления растут при увеличении атомного веса элементов. На рисунке крестиками отмечены температуры кипения этих гидридов, а кружочками - температуры плавления.

Как видно, при уменьшении атомного веса температуры снижаются совершенно линейно. Область существования жидкой фазы гидридов становится все более "холодной", и если бы гидрид кислорода Н2О был нормальным соединением, похожим на своих соседей по шестой группе, то жидкая вода существовала бы в диапазоне от -80° С до -95° С. При более высоких температурах Н2О всегда была бы газом. К счастью для нас и всего живого на Земле, вода аномальна, она не признает периодической закономерности а следует своим законам.
Объясняется это довольно просто - большая часть молекул воды соединена водородными связями. Именно этими связями отличается вода от жидких гидридов H2S, H2Se и H2Te. Если бы их не было, то вода кипела бы уже при минус 95 °C. Энергия водородных связей достаточно велика, и разорвать их можно лишь при значительно более высокой температуре. Даже в газообразном состоянии большое число молекул H2O сохраняет свои водородные связи, объединяясь в димеры (H2O)2. Полностью водородные связи исчезают только при температуре водяного пара 600 °C.
Напомним, что кипение заключается в том, что пузыри пара образуются внутри кипящей жидкости. При нормальном давлении чистая вода кипит при 100 "С. В случае подведения тепла через свободную поверхность будет ускоряться процесс поверхностного испарения, но объёмного парообразования, характерного для кипения, не возникает. Кипение может быть осуществлено и понижением внешнего давления, так как в этом случае давление пара, равное внешнему давлению, достигается при более низкой температуре. На вершине очень высокой горы давление и соответственно точка кипения настолько понижаются, что вода становится непригодной для варки пищи - не достигается требуемая температуры воды. При достаточно высоком давлении воду можно нагреть настолько, что в ней может расплавиться свинец (327 °С), и все же она не будет кипеть.
Помимо сверхбольших температур кипения плавления (причем последний процесс требует слишком большой для такой простой жидкости теплоты плавления), аномален сам диапазон существования воды - сто градусов, на которые разнятся эти температуры, - довольно большой диапазон для такой низкомолекулярной жидкости, как вода. Необычайно велики пределы допустимых значении переохлаждения и перегрева воды - при аккуратном нагревании или охлаждении вода остается жидкой от -40 °C до +200 °C. Тем самым температурный диапазон, в котором вода может оставаться жидкой, расширяется до 240 °C.
При нагревании льда сначала температура его повышается, но с момента образования смеси воды со льдом температура будет оставаться неизменной до того момента, пока не расплавится весь лёд. Это объясняется тем, что тепло, подводимое к тающему льду, прежде всего расходуется только на разрушение кристаллов. Температура тающего льда остаётся неизменной до тех пор, пока не произойдёт разрушение всех кристаллов (см. скрытую теплоту плавления).
Расплавы
Расплавы - жидкое расплавленное состояние веществ при температурах, в определённых границах удалённых от критической точки плавления и расположенных ближе к температуре плавления. Природа расплавов по своей сути определяется видом химических связей элементов в расплавленном веществе.
Расплавы находят широкое применение в металлургии, стекловарении и других областях техники. Обычно расплавы имеют сложный состав и содержат различные взаимодействующие компоненты (см. фазовая диаграмма).
Расплавы бывают
1.Металлические (Мета́ллы (название происходит от лат. metallum - шахта, рудник) - группа элементов, обладающая характерными металлическими свойствами, такими как высокая тепло- и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность и металлический блеск);
2.Ионные (Ио́н (др.-греч. ἰόν - идущее) - одноатомная или многоатомная электрически заряженная частица, образующаяся в результате потери или присоединения одного или нескольких электронов атомом или молекулой. Ионизация (процесс образования ионов) может происходить при высоких температурах, под воздействием электрического поля);
3.Полупроводниковые с ковалентными связями между атомами (Полупроводники́ - материалы, которые по своей удельной проводимости занимают промежуточное место между проводниками и диэлектриками и отличаются от проводников сильной зависимостью удельной проводимости от концентрации примесей, температуры и различных видов излучения. Основным свойством этих материалов является увеличение электрической проводимости с ростом температуры);
4.Органические расплавы с ван-дер-ваальсовыми связями;
5.Высокополимерные (Полимеры (греч. πολύ- - много; μέρος - часть) - неорганические и органические, аморфные и кристаллические вещества, получаемые путём многократного повторения различных групп атомов, называемых «мономерными звеньями», соединённых в длинные макромолекулы химическими или координационными связями)
Расплавы по типу химических соединений бывают:
1.Солевые;
2.Оксидные;
3.Оксидно-силикатные (шлаковые) и др.
Расплавы с особыми свойствами:
1.Эвтектические
Интересное о плавлении
Ледяные зёрна и звезды.
Внесите кусок чистого льда в тёплую комнату и понаблюдайте за тем, как он тает. Довольно быстро выяснится, что лёд, казавшийся монолитным и однородным, распадается на множество мелких зёрен - отдельных кристаллов. В объёме льда они расположены хаотично. Не менее интересную картину можно увидеть, когда лёд плавится с поверхности.
Поднесите к лампе гладкий кусок льда и подождите, пока он начнёт плавиться. Когда плавление затронет внутренние зёрна, там начнут появляться очень мелкие узоры. В сильную лупу видно, что они имеют форму шестиугольных снежинок. На самом же деле это протаявшие впадинки, заполненные водой. Форма и направление их лучей соответствуют ориентации монокристаллов льда. Эти узоры называются „звёздочками Тиндаля“ в честь английского физика, открывшего и описавшего их в 1855 году. "Звездочки Тиндаля", похожие на снежинки, на самом деле - впадинки на поверхности подтаявшего льда размером около 1,5 мм, заполненные водой. В их центре видны воздушные пузырьки, возникшие из-за разности объемов растаявшего льда и талой воды.
ЗНАЕТЕ ЛИ ВЫ?
Существут металл, так называемый, сплав Вуда, который можно запросто расплавить даже в теплой воде (+68 градусов Цельсия). Так при размешивании сахара в стакане металлическая ложка из этого сплава растает быстрее сахара!
Самое тугоплавкое вещество - карбид тантала ТаС0-88 плавится при температуре 3990°С.
В 1987 году немецкие исследователи смогли переохладить воду до температуры –700С, сохраняя ее в жидком состоянии.
Иногда, чтобы снег на тротуарах быстрее таял, их посыпают солью. Плавление льда происходит потому, что образуется раствор соли в воде, температура замерзания которого ниже температуры воздуха. Раствор просто стекает с тротуара.
Интересно, что ноги стынут больше на мокром тротуаре, так как температура раствора соли и воды ниже температуры чистого снега.
Если из чайника налить чай в две кружки: с сахаром и без сахара, то чай в кружке с сахаром будет холоднее, т.к. на растворение сахара (на разрушение его кристаллической решетки) тоже расходуется энергия.
При сильных морозах для восстановления гладкости льда поливку катка производят горячей водой.. Горячая вода расплавляет тонкий верхний слой льда, не так быстро замерзает, успевает растечься, и поверхность льда получается очень гладкой.
Заключение (выводы)
Плавление - переход вещества из твердого состояния в жидкое.
При нагревании увеличивается температура вещества, и возрастает скорость теплового движения частиц, при этом увеличивается внутренняя энергия тела.
Когда температура твердого тело достигает температуры плавления, кристаллическая решетка твердого вещества начинает разрушаться. Таким образом, основная часть энергия нагревателя, проводимая к твердому телу, идет на уменьшение связей между частицами вещества, т. е. на разрушение кристаллической решетки. При этом возрастает энергия взаимодействия между частицами.
Расплавленное вещество обладает большим запасом внутренней энергии, чем в твердом состоянии. Оставшаяся часть теплоты плавления расходуется на совершение работы по изменению объема тела при его плавлении.
При плавлении объем большинства кристаллических тел увеличивается (на 3-6%), а при отвердевании уменьшается. Но, существуют вещества, у которых при плавлении объем уменьшается, а при отвердевании - увеличивается. К ним относятся, например, вода и чугун, кремний и некоторые другие. . Именно поэтому лёд плавает на поверхности воды, а твердый чугун - в собственном расплаве.
Твердые тела, называемые аморфными (янтарь, смола, стекло) не имеют определенной температуры плавления.
Количество теплоты, необходимой для плавления вещества, равно произведению удельной теплоты плавления на массу данного вещества.
Удельная теплота плавления показывает, какое кол теплоты необходимо для полного превращения 1 кг вещества из твердого состояния в жидкое, взятого при темп плавления.
Единицей удельной теплоты плавления в СИ служит 1Дж/кг.
В процессе плавления температура кристалла остается постоянной. Эта температура называется температурой плавления. У каждого вещества своя температура плавления.
Температура плавления для данного вещества зависит от атмосферного давления.
Список использованной литературы
1) Данные электронной свободной энциклопедии «Викпедия»
http://ru.wikipedia.org/wiki/Заглавная_страница
2) Сайт «Класс!ная физика для любознательных» http://class-fizika.narod.ru/8_11.htm
3) Сайт «Физические свойства воды»
http://all-about-water.ru/boiling-temperature.php
4) Сайт «Металлы и конструкции»
http://metaloconstruction.ru/osnovy-plavleniya-metallov/
Нет такого твердого тела, которое сколько угодно противостояло бы повышению температуры. Рано или поздно твердый кусочек превращается в жидкость; правый, в некоторых случаях нам не удастся добраться до температуры плавления - может произойти химическое разложение.
По мере возрастания температуры молекулы движутся все интенсивнее. Наконец, наступает такой момент, когда поддержание порядка "среди сильно "раскачавшихся" молекул становится невозможным. Твердое тело плавится. Самой высокой температурой плавления обладает вольфрам: 3380°С. Золото плавится при 1063°С, железо - при 1539°С. Впрочем, есть и легкоплавкие металлы. Ртуть, как хорошо известно, плавится уже при температуре -39°С. Органические вещества не имеют высоких температур плавления. Нафталин плавится при 80°С, толуол - при -94,5°С.
Измерить температуру плавления тела, в особенности если оно плавится в интервале температур, которые измеряют обычным термометром, совсем нетрудно. Совсем не обязательно следить глазами за плавящимся телом. Достаточно смотреть на ртутный столбик термометра. Пока плавление не началось, температура тела растет (рис. 4.5). Как только плавление начинается, повышение температуры прекращается, и температура останется неизменной, пока процесс плавления не закончится полностью.
Как и превращение жидкости в пар, превращение твердого тела в жидкость требует тепла. Необходимая для этого теплота называется скрытой теплотой плавления. Например, плавление одного килограмма льда требует 80 ккал.
Лед относится к числу тел, обладающих большой теплотой плавления. Плавление льда требует, например, в 10 раз больше энергии, чем плавление такой же массы свинца. Разумеется, речь идет о самом плавлении, мы здесь не говорим, что до начала плавления свинца его надо нагреть до +327°С. Из-за большой теплоты плавления льда замедляется таяние снега. Представьте себе, что теплота, плавления была бы в 10 раз меньше. Тогда весенние паводки приводили бы ежегодно к невообразимым бедствиям.
Итак, теплота плавления льда велика, но она же и мала, если ее сравнить с удельной теплотой парообразования в 540 ккал / кг (в семь раз меньше). Впрочем, это различие совершенно естественно. Переводя жидкость в пар, мы должны оторвать молекулы одну от другой, а при плавлении нам приходится лишь разрушить порядок в расположении молекул, оставив их почти на тех же расстояниях. Ясно, что во втором случае требуется меньше работы.
Наличие определенной точки плавления есть важный признак кристаллических веществ. Именно по этому признаку их легко отличить от других твердых тел, называемых аморфными или стеклами. Стекла встречаются как среди неорганических, так и среди органических веществ. Оконные стекла делаются обычно из силикатов натрия и кальция; на письменный стол кладут часто органическое стекло (его называют еще плексиглас).
Аморфные вещества в противоположность кристаллам не имеют определенной температуры плавления. Стекло не плавится, а размягчается. При нагревании кусок стекла сначала становится из твердого мягким, его легко можно гнуть или растягивать; при более высокой температуре кусок начинает изменять свою форму под действием собственной тяжести. По мере нагревания густая вязкая масса стекла принимает форму того сосуда, в котором оно лежит. Эта масса сначала густа, как мед, потом - как сметана и, наконец, становится почти такой же маловязкой жидкостью, как вода. При всем желании мы не можем здесь указать определенной температуры перехода твердого тела в жидкое. Причины этого лежат в коренном отличии строения стекла от строения кристаллических тел. Как говорилось выше, атомы в аморфных телах расположены беспорядочно. Стекла по строению напоминают жидкости, Уже в твердом стекле молекулы расположены беспорядочно. Значит, повышение температуры стекла лишь увеличивает размах колебаний его молекул, дает им постепенно все большую и большую свободу перемещения. Поэтому стекло размягчается постепенно и не обнаруживает резкого перехода "твердое" - "жидкое", характерного для перехода от расположения молекул в строгом порядке к беспорядочному расположению.
Когда речь шла о кривой кипения, мы рассказали, что жидкость и пар могут, хотя и в неустойчивом состоянии, жить в чужих областях - пар можно переохладить и перевести влево от кривой кипения, жидкость - перегреть и оттянуть вправо от этой кривой.
Возможны ли аналогичные явления в случае кристалла с жидкостью? Оказывается, аналогия тут неполная.
Если нагреть кристалл, то он начнет плавиться при своей температуре плавления. Перегреть кристалл не удастся. Напротив, охлаждая жидкость, можно, если принять некоторые меры, сравнительно легко "проскочить" температуру плавления. В некоторых жидкостях удается достигнуть больших переохлаждений. Есть даже такие жидкости, которые легко переохладить, а трудно заставить кристаллизоваться. По мере охлаждения такой жидкости она становится все более вязкой и наконец затвердевает,не кристаллизуясь. Таково стекло.
Можно переохладить и воду. Капельки тумана могут не замерзать даже при сильных морозах. Если в переохлажденную жидкость бросить кристаллик вещества - затравку, то немедленно начнется кристаллизация.
Наконец, во многих случаях задержавшаяся кристаллизация может начаться от встряски или от других случайных событий. Известно, например, что кристаллический глицерин был впервые получен при транспортировке по железной дороге. Стекла после долгого стояния могут начать кристаллизоваться (расстекловываться, или "зарухать", как говорят в технике).






