Формула кристаллизации. Отвердевание кристаллических тел
Переход вещества из твердого состояния в жидкое называется плавлением, а переход из жидкого состояния в твердое - отвердеванием или кристаллизацией.
При плавлении твердого вещества увеличиваются расстояния между частицами, образующими кристаллическую решетку, и происходит разрушение самой решетки. Это означает, что в процессе плавления увеличивается молекулярно-потенциальная энергия вещества. Таким образом, плавление вещества самопроизвольно происходить не может, так как на этот процесс необходимо затрачивать энергию.
При кристаллизации происходит сближение частиц, которые образуют решетку, а их потенциальная энергия уменьшается. Следовательно, кристаллизация может происходить только тогда, когда жидкость отдает свою энергию каким-либо внешним телам.
Итак, единица массы жидкого вещества обладает большей внутренней энергией, чем единица массы того же вещества в твердом состоянии, даже если их температура одинакова.
Область, в которой вещество однородно по всем физическим и химическим свойствам, называется фазой состояния этого вещества. Отметим, что твердая и жидкая фазы вещества при одинаковой температуре могут оставаться в равновесии сколь угодно долго, если твердая фаза не сможет получить энергию, а жидкая - ее отдать. Например, лед может долго плавать в воде, если температура всех окружающих тел будет одинакова и равна 0°С.
Пусть имеется только твердая фаза вещества, которая получает энергию от других тел. Тогда сначала будет возрастать и молекулярно-потенциальная и молекулярно-кинетическая энергии этого вещества, так как и расстояния между частицами в кристаллической решетке и скорости их движения будут увеличиваться. Затем, при определенной температуре, начнется разрушение кристаллической решетки. Пока все вещество не расплавится, его температура остается неизменной, а вся получаемая веществом энергия идет только на работу по преодолению сил молекулярного сцепления. Когда останется только жидкая фаза, то, продолжая получать энергию, она будет уже нагреваться, т. е. начнет возрастать ее мо-лекулярно-кинетическая энергия.
Если жидкая фаза будет отдавать свою энергию окружающим телам, то все описанные процессы повторятся в обратном порядке.
На рис. 12.1 показаны графики изменения температуры вещества при плавлении и отвердевании. Отрезок (рис. 12.1, а) выражает количество теплоты, полученное веществом при нагревании в твердом состоянии (от Т до отрезок при плавлении и отрезок - при нагревании в жидком состоянии. Отрезок Q (рис. 12.1, б) выражает количество теплоты, отданной веществом при охлаждении в жидком состоянии (от до ), отрезок - при отвердевании и отрезок - при охлаждении в твердом состоянии. Опыт показывает, что плавление и отвердевание определенного вещества происходит при одинаковой температуре, не изменяющейся, пока совместно существуют твердая и жидкая фазы вещества. Эта температура называется температурой плавления.
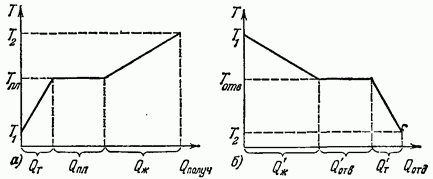
Отметим, что при плавлении и отвердевании вещества всегда существует резкая граница между твердой и жидкой фазами.
Как показывает опыт, у аморфных веществ процессов плавления и отвердевания не наблюдается. При нагревании они постепенно размягчаются, а при охлаждении постепенно густеют. Температура аморфных веществ в указанных случаях непрерывно изменяется, а границы между твердой и жидкой фазами не существует, так как вся их масса имеет однородный вид.
Итак, плавление и кристаллизацию можно наблюдать только у кристаллических тел.
В кристаллическое, а также из одного кристаллического состояния в другое (рекристаллизация, или вторичная кристаллизация); первого рода. Кристаллизация из жидкой или газовой фазы - экзотермический процесс, при котором выделяется теплота фазового перехода, или теплота кристаллизация; при этом изменение в большинстве случаев составляет [в Дж/(моль. К)]: для простых веществ 5-12, для неорганических соединений 20 - 30, для органических соединений 40-60. Рекристаллизация может протекать с выделением либо поглощением теплоты. В промышленности и лаб. практике кристаллизация используют для получения продуктов с заданными составом, содержанием примесей, размерами, формой и дефектностью (см. . . Кристаллы), а также для фракционного разделения смесей, выращивания монокристаллов и др.
Физико-химические основы процесса. Условия, при которых возможна кристаллизация, определяются видом . Чтобы кристаллизация протекала с конечной скоростью, исходную фазу необходимо переохладить (перегреть), пересытить кристаллизующимся веществом или внести во внеш. поле, снижающее растворимость кристаллизующейся фазы. В переохлажденной (перегретой) либо пересыщенной фазе происходит - образуются центры кристаллизация, которые превращаются в кристаллы и растут, как правило, изменяя форму, содержание примесей и дефектность. Центры кристаллизация возникают гомогенно в объеме начальной фазы и гетерогенно на поверхностях посторонних твердых частиц (первичное зародышеобразование), а также вблизи поверхности ранее сформировавшихся новой фазы (вторичное зародышеобразование). Общее число центров кристаллизация, возникших в единице объема раствора или в 1 с, или суммарную интенсивность их первичного и вторичного образования, находят по формуле:
где a - кинетический коэффициент первичного зародышеобразования, который рассматривают в рамках кинетической теории образования новой фазы; R -
. T - температура кристаллизация; у - удельная поверхностная свободная энергия кристаллов; V т -
молярный объем новой фазы; Dm=DHS и S = (Т 0 -7)/Т 0 для расплавов, am=RT1n(S + 1) и S = (c-c 0)/c 0 для растворов; DH-энтальпия кристаллизация; с - кристаллизующегося вещества; Т 0 и c 0 - соотв. температура вещества и насыщенного раствора; E акт - перехода из среды в центры кристаллизация; I ат - интенсивность вторичного зародышеобразования в объеме начальной фазы. Для измерения a, E aкт и I вт находят зависимость интенсивности образования центров кристаллизация от температуры, пересыщения и концентрации посторонних твердых частиц.
Величина I и проходит через один или нескристаллизация максимумов (рис. 1) с возрастанием переохлаждения (пересыщения) и увеличивается при мех. воздействиях (перемешивание,
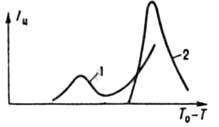
Рис. I Зависимость скорости зародышеобразования от переохлаждения InSb: I расплав массой 16 г перегревался в кварцевом тигле на 15 К выше температуры в течение 9 мин и затем охлаждался со скоростью 1 град/мин; 2 то же, на 55 К в течение 20 с под влиянием . При росте сначала кристаллизующееся вещество адсорбируется на поверхности сформировавшегося кристаллика, а затем встраивается в его кристаллическую решетку: при сильном переохлаждении равновероятно на любом участке поверхности (нормальный рост), при слабом - слоями тангенциально на ступенях, образованных винтовыми или двухмерными зародышами (послойный рост). Если переохлаждение ниже некоторого значения, называют пределом морфологической устойчивости, нормально растущий кристалл повторяет форму (обычно округлую) теплового либо концентрационного поля вокруг него, а послойно растущий кристалл имеет форму многогранника. При превышении указанного предела растут древовидные кристаллы (дендриты). Количественно рост характеризуют линейной скоростью, равной скорости перемещения их поверхности в нормальном к ней направлении. В промышленности используют эффективную линейную скорость роста (увеличение в 1 с радиуса шара, объем которого равен объему кристалла): I эфф =bS n ехр(E р /RT), где b - кинетический коэффициент роста (10 -5 -10 -14 м/с), n-параметр роста (обычно 1-3), Е р - роста (10-150 кДж/моль). Параметры b, n и E р находят, измеряя I эфф при разных температурах и пересыщениях раствора или переохлаждениях расплава. С увеличением переохлаждения I эфф проходит через максимум аналогично I m .
Скорость роста может лимитироваться массо- и со средой (соотв. внешнедиффузионный и теплообменный режимы роста), скоростью химического взаимодействия кристаллизующегося компонента с другими компонентами среды (внешнекинетический режим) или процессами на поверхности (адсорбционно-кинетический режим). Во внешнекинетическом режиме I эфф возрастает с повышением концентраций реагентов и . во внешнедиффузионном и теплообменном режимах - с увеличением интенсивности перемешивания, в адсорбционно-кинетическом режиме - с возрастанием поверхностной дефектности и уменьшением концентрации ПАВ.
При высоких скоростях роста кристаллы приобретают значительное число неравновесных дефектов (вакансий, дислокаций и др.). При превышении предела морфологической устойчивости в объем попадают трехмерные включения среды, замурованные между ветвями дендритов (окклюзия). Состав из-за окклюзии приближается к составу среды тем больше, чем выше I эфф. При своем росте кристаллы захватывают любую присутствующую в среде примесь, причем захваченной примеси зависит от скорости роста. Если кристаллизация происходит в растворе и кристаллы после завершения роста продолжают контактировать со средой, то неравновесно захваченная примесь выбрасывается из в среду, а их структура совершенствуется (структурная перекристаллизация). Одновременно в перемешиваемой среде при столкновениях друг с другом и со стенками кристаллизатора возникают дополнительные структурные дефекты. Поэтому в системе постепенно устанавливается стационарная дефектность кристаллов, которая зависит от интенсивности перемешивания. В наиб. распространенном случае образования при кристаллизация множества (массовая кристаллизация) выделяющаяся фаза полидисперсна, что обусловлено неодновременностью зарождения и флуктуациями их роста. Мелкие кристаллы более растворимы, чем крупные, поэтому при убывающем пересыщении наступает момент, когда среда, оставаясь пересыщенной относительно последних, становитcя

Рис. 2. Функция распределения по размерам (обычным r и наиб. вероятным r A)при изотермической (298 К) периодической кристаллизации из водного раствора в кристаллизаторе с мешалкой (число Re=10 4): 1 BaSO 4 , исходное пересышение S 0 =500. r A =7.6 мкм; 2 - K 2 SO 4 , высаливание метанолом (1 . 1)r A =1 мкм; t время процесса.
С этого момента начинаются их растворение и рост крупных (освальдoво созревание), в результате чего средний размер возрастает, а их число уменьшается. Одновременно в перемешиваемой среде кристаллы раскалываются при соударениях и через некоторое время приобретают стационарную дисперсность, определяемую интенсивностью механического воздействия. Осн. количеств, характеристика массовой кристаллизация - функция распределения по размеру f(r,t)=dN/dr, где N - число кристаллов, размер которых меньше текущего размера r, в единице объема в момент t. Эта функция часто имеет колоколообразный вид (рис. 2); восходящая ее ветвь чувствительна в основном к зародышеобразованию, росту, раскалыванию и растворению (при созревании) кристаллов, нисходящая к росту и образованию их агрегатов. Если среднее квадратичное отклонение размера от среднего не превышает половины, последнего, упомянутая функция наз. узкой, если превышает - широкой. Изменение функции f (r,t) при кристаллизация описывается уравнением:

где a - коэффициент флуктуации скорости роста кристаллов; D к и v
к - соотв. коэффициент диффузии и скорость перемещения в среде; I ar и I р - соотв. интенсивность образования данного размера за счет слипания более мелких частиц и раскалывания кристаллов.
Система уравнений материального и теплового балансов, уравнения (2), а также уравнения, связывающие размеры и скорость роста с их формой, дефектностью и содержанием примесей, - основа моделирования и расчета массовой кристаллизация и выбора оптимальных условий ее реализации. Массовую кристаллизация осуществляют периодически или непрерывно. При периодической кристаллизации охлаждают расплав или насыщенный раствор (пар), испаряют растворитель, добавляют высаливающие агенты (см. ниже) или смешивают порции реагентов, образующих продукционные кристаллы. При непрерывной кристаллизация в кристаллизатор вводят потоки расплава, пересыщенного раствора либо реагентов и непрерывно отводят кристаллический продукт.
При пeриодич. процессе скорость кристаллизация, определяемая по формуле:
![]() ,
,
где r и V - соотв. плотность твердой фазы и объем системы, сначала медленно растет (период индукции), затем резко увеличивается в результате одновременного возрастания r и f и, пройдя через максимум, уменьшается (рис. 3) вследствие снижения I эфф. В периоды индукции и увеличения скорости кристаллизация в системе преобладают зарождение и рост кристаллов, в период уменьшения скорости - их рост, агрегация и раскалывание и далее - освальдово созревание и структурная перекристаллизация. Период индукции сокращается под влиянием факторов, которые ускоряют зародышеобразование и рост кристаллов. Так, при охлаждении расплавов этот период с повышением интенсивности охлаждения сначала уменьшается, а затем
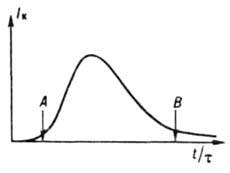
Рис. 3. Типичное изменение скорости периодической кристаллизации: t - время процесса; t - длительность периода индукции; A - моментпоявления новой фазы; В - начало стадии структурной перeкристаллизации и освальдова созревания возрастает из-за экстремальной зависимости скоростей зарождения и роста от переохлаждения; если темп охлаждения достаточно велик, расплав твердеет, оставаясь аморфным (см. Стеклообразное состояние
). Для сокращения периода индукции в систему добавляют кристаллы продукта (затравку), которые растут, что приводит к увеличению скорости кристаллизация В результате выделения при росте теплоты кристаллизация снижается переохлаждение и замедляется зародышеобразование. При малых переохлаждениях (пересыщениях) зародыши вообще не возникают, и затравка, введенная в систему в виде единичных кристаллов, может вырасти в монокристалл, а в виде порошка - в так называемый монодисперсный продукт с узкой функцией f
(r, t).
При непрерывной кристаллизации функция f
(r,t) в сопоставимых условиях шире, чем при периодическая кристаллизация, что объясняется разбросом времен пребывания в кристаллизаторах непрерывного действия. Чтобы сузить эту функцию, режим кристаллизации приближают к режиму идеального вытеснения, чтобы расширить - к режиму идеального (см. Структура потоков
). При малом пересыщении системы непрерывная кристаллизация устойчива к флуктуациям внеш. условий; при высоком пересыщении его значение и размер колеблются в ходе кристаллизации.
В хим. и смежных отраслях промышленности, а также в лабораториях преимущественно применяют кристаллизация из расплавов и растворов, реже - кристаллизация из паровой и твердой фаз. Кристаллизацию из расплавов используют главным образом для отверждения расплавленных веществ и, кроме того, для их фракционного разделения и . Отверждение веществ в виде отливок (блоков) осуществляют в специальных формах. В малотоннажных производствах (напр., реактивов) обычно применяют отдельные формы определенных размеров или конфигурации, в которых расплав охлаждается путем естественного теплообмена с окружающей средой; в крупнотоннажных производствах (нафталина и др.) кристаллизация проводят в секционированных, трубчатых, конвейерных и иных кристаллизаторах со встроенными формами, принудительно охлаждаемыми водой, жидким NH 3 , хладонами и т.п.
Для получения продуктов в виде тонких пластинок или чешуек используют непрерывно действующие ленточные, вальцевые и дисковые кристаллизаторы, где отверждение происходит значительно интенсивнее, чем в формах. В ленточном кристаллизаторе (рис. 4) исходный расплав
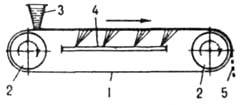
Рис. 4. Ленточный кристаллизатор: 1 лента; 2 приводные барабаны; 3 питающий бункер; 4 охлаждающее устройство; 5 отвержденный продукт тонким слоем подается на движущуюся металлическую ленту, на которой он охлаждается до полного затвердевания. В вальцевом аппарате (рис. 5) продукт кристаллизуется на наружной поверхности охлаждаемого изнутри вращающегося полого барабана (вальца), частично погруженного в ванну с расплавом; кристаллы снимаются с барабана неподвижным ножом. В дисковых аппаратах отверждение продуктов происходит на поверхности охлаждаемых изнутри вращающихся дисков.

Рис. 5. Вальцевый кристаллизатор: 1 барабан; 2 ванна; 3 нож; 4 труба для подачи хладагента; 5 форсунка; 6 расплав; 7 отвержденный продукт.
При приготовлении гранулировании продуктов расплав диспергируют непосредственно в поток хладагента газообразного, в основном воздуха (производство аммиачной селитры, карбамида и др.), или жидкого, например воды либо масла (производство пластмасс, серы и т. п.) в полых башнях или аппаратах с псевдоожнжeнным слоем, где кристаллизуются мелкие капли
Кристаллизацию из растворов используют преимущественно для выделения ценных компонентов из растворов, а также их концентрирования и очистки веществ от примесей. Вещества, растворимость которых сильно зависит от температуры (напр., KNO 3 в воде), кристаллизуют охлаждением горячих растворов, при этом исходное кол-во растворителя, который содержится в маточной жидкости, в системе не изменяется (изогидрическая кристаллизация). В малотоннажных производствах применяют емкостные кристаллизаторы периодического действия, снабженные охлаждаемыми рубашками. В таких аппаратах раствор охлаждают при непрерывном перемешивании по определенной программе. Для предотвращения интенсивной инкрустации поверхностей охлаждения разность температур между раствором и хладагентом должна быть не более 8-10°С. В крупнотоннажных производствах используют, как правило, скребковые, шнековые, дисковые, барабанные и роторные кристаллизаторы непрерывного действия. Скребковые аппараты обычно состоят из нескристаллизация последовательно соединенных трубчатых секций, в каждой из которых имеется вал со скребками и которые снабжены общей или индивидуальными охлаждающими рубашками. При вращении вала скребки очищают внутр. поверхность охлаждаемых труб от осевших на них и способствуют транспортированию образовавшейся сгущенной суспензии из секции в секцию. В шнековых кристаллизаторах раствор перемешивают и перемещают с помощью сплошных или ленточных шнеков.
Дисковые кристаллизаторы снабжены неподвижными либо вращающимися дисками. В первом случае (рис. 6) по оси аппарата расположен приводной вал со скребками для очистки поверхностей дисков от осаждающихся кристаллов; исходный раствор подается в кристаллизатор сверху, а образующаяся суспензия последовательно проходит в пространстве между охлаждаемыми дисками и выгружается через нижний штуцер. Во втором случае вал с дисками размещен внутри корыта или горизонтального цилиндрического сосуда; кристаллы снимаются с поверхности дисков неподвижными скребками.

Основной элемент барабанного кристаллизатора - полый барабан с опорными бандажами, установленный под углом 15° к горизонтальной оси и вращающийся с частотой 5-20 мин -1 . Раствор, охлаждаемый водяной рубашкой или воздухом (который нагнетают вентилятором через внутреннюю полость барабана), поступает с одного его конца, а суспензия отводится с другого.
Вязкие растворы (например, жирных кислот) часто охлаждают в роторных кристаллизаторах - цилиндрических аппаратах, внутри которых с большой скоростью вращается ротор с ножами. Последние под действием центробежной силы прижимаются к внутренней поверхности кристаллизатора, очищая ее от осевших кристаллов. Раствор обычно подастся в аппарат под избыточным давлением. Для увеличения времени пребывания в кристаллизаторе раствора и большего его переохлаждения последовательно соединяют несколько аппаратов.
При использовании скребковых, шнековых, роторных и иногда дисковых кристаллизаторов часто образуются мелкие кристаллы (0,1-0,15 мм), что приводит к увеличению слеживаемости и адсорбционного загрязнения продукта, а также ухудшает его фильтруемость. Поэтому для укрупнения продукта после упомянутых аппаратов устанавливают так называемые кристаллорастворители, в которых концентрированная суспензия выдерживается при медленном охлаждении, что приводит к росту до 2-3 мм.
Для получения крупнокристаллических однородных продуктов часто применяют кристаллизаторы с псевдоожиженным слоем (рис. 7). Исходный раствор вместе с циркулирующим осветленным маточником подается насосом в теплообменник, где в результате охлаждения раствор пересыщается и поступает по циркуляционной трубе в нижнюю часть кристаллорастворителя, в котором кристаллы поддерживаются во взвешенном состоянии восходящим потоком раствора. Кристаллизация происходит в основном на готовых центрах кристаллизации, при этом крупные кристаллы осаждаются на дно аппарата, откуда удаляются в виде сгущенной суспензии. Осветленный маточник разделяется на две части: одна отводится из верхней части аппарата, другая подается на рециркуляцию.

Рис. 7. Кристаллизатор с псевдоожиженмым слоем: I насос: 2 теплообмeнник: 3 циркуляционная труба; 4 кристаллорастворитель.
В ряде cлучаев кристаллизация растворов осуществляют непосредственным смешением их с жидкими, газообразными и испаряющимися хладагентами в смесительных, барботажных, распылительных и др. аппаратах. Если растворимость вещества мало изменяется с изменением температуры (напр., NaCl в воде), кристаллизация проводят частичным или практически полным испарением растворитeля путем выпаривания насыщенного раствора при почти постоянной температуре (изотермическая кристаллизация). По конструкции выпарные кристаллизаторы в значительной степени напоминают выпарные аппараты и могут иметь внутреннюю или выносную (рис. 8) греющие камеры. В таком кристаллизаторе исходный и циркулирующий растворы, проходя через камеру, нагреваются до температуры кипения. Образовавшаяся парожидкостная смесь поступает в сепаратор, где пар отделяется от раствора. Кристаллы, осаждающиеся в сепараторе, вместе с маточной жидкостью направляются в специальный аппарат, в котором отделяются от нее и выводятся в виде концентрированной суспензии;
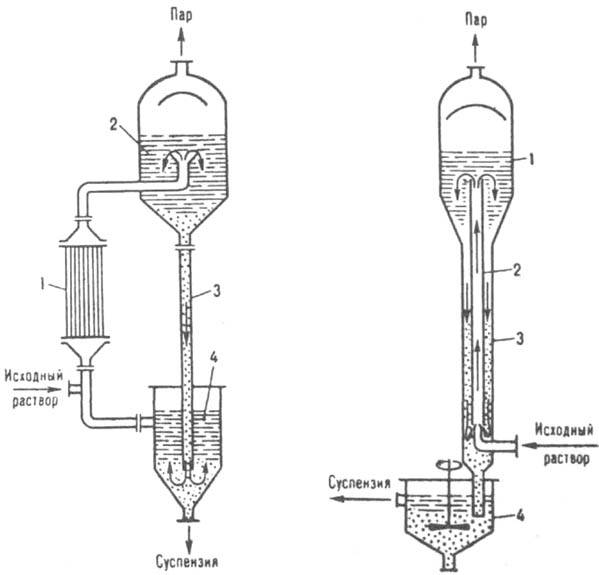
Рис. 8. Выпарной кристаллита гор: 1 выносная греющая камера: 2 сепаратор: 3 циркуляционная труба; 4 отделитель кристаллов.
Рис. 9. Вакуум-кристаллизатор: 1 - сепаратор: 2 - циркуляционная труба: 3 барометрическая труба; 4 гидрозатвор
осветленный маточник возвращается в камеру. Для предотвращения инкрустации (обрастания) поверхностей нагрева раствор должен циркулировать в кристаллизаторе с достаточно большой скоростью (до 3 м/с), что часто достигается применением осевых насосов.
При одновременном охлаждении и выпаривании растворителя кристаллизация осуществляют в вакуум-кристаллизаторах периодического или непрерывного действия, с принудительной либо естественной циркуляцией раствора. Раствор охлаждается вследствие адиабатического испарения части растворителя при создании в таком аппарате определенного разрежения. Кол-во испаренного растворителя обычно составляет 8-10% от общей массы раствора. В кристаллизаторе с естественной циркуляцией (рис. 9) исходный раствор подается в нижней часть циркуляционной трубы и вместе с циркулирующей суспензией поднимается вверх, где в результате понижения давления вскипает. Образовавшиеся пары проходят через сепаратор и поступают в барометрический конденсатор. Пересыщенный раствор и выделившиеся кристаллы движутся вниз по барометрической трубе, откуда кристаллы вместе с частью маточной жидкости выводятся в гидрозатвор. Для поддержания разрежения используют вакуум-насосы или пароструйные инжекторы. В крупнотоннажных производствах широко распространены многокорпусные вакуум-кристаллизационные установки с числом корпусов 4-24, в которых глубина разрежения постепенно возрастает от первого корпуса к последнему. Вакуум-кристаллизаторы более производительны и экономичны, чем выпарные кристаллизаторы.
Кристаллизацию некоторых веществ можно осуществить высаливанием. При выделении неорганических соединений используют органические вещества (напр., Na 2 SO 4 кристаллизуют, добавляя к его водному раствору метанол, этанол либо NH 3) или содержащие одинаковый ион с выделяемым соединением (напр., FeSO 4 кристаллизуют из травильных растворов добавкой концентрированной H 2 SO 4); при выделении орг. соединений - воду, водные растворы неорганических солей и т. п. Введение в раствор в качестве высаливателей органических веществ обычно удорожает процесс из-за сложности их регенерации.
Кристаллизация из паровой фазы позволяет кристаллизовать вещества, обладающие высоким парциальным давлением паров над твердой фазой и способные непосредственно переходить из газообразного состояния в кристаллическое (например, иод, фталевый ангидрид). Такую кристаллизацию используют для выделения ценных компонентов из парогазовых смесей, получения аэрозолей, нанесения тонких кристаллических слоев на поверхность различных тел (напр., в производстве полупроводниковых материалов) и т.д.
Кристаллизацию аморфной твердой фазы и рекристаллизацию осуществляют, как правило, при температурах, близких к температурам кристаллизуемых веществ. При этом в результате термодиффузионных процессов изменяется первичная кристаллическая структура вещества либо происходят зарождение и рост из аморфной фазы. Такую кристаллизация применяют для получения веществ и материалов с заданными кристаллической структурой либо степенью кристалличности (термопластичные полимеры, стекло и др.).
Лит.:
Маллин Дж.У.. Кристаллизация, пер. с англ., М., 1965; Магусевич Л.Н.. Кристаллизация из растворов в химической промышленности, М., 1968; Бэмфорт А В, Промышленная кристаллизация, пер. с англ., М., 1969; Пономаренко В. Г. Ткаченко кристаллизация П., Курлянд Ю. А., Кристаллизация в псевдоожиженном слое. кристаллизация, 1972; Мелихов И. В., Меркулова М.С.. Сокристаллизация, М.. 1975; Гельперин Н. И.. Носов Г. А., Основы техники кристаллизации расплавов, М., 1975; Кидяров Б. И., Кинетика образования
ОТВЕРДЕВАНИЕ КРИСТАЛЛИЧЕСКИХ ТЕЛ
При понижении температуры вещество может переходить из жидкого состояния в твердое.
Этот процесс называется отвердевание
или кристаллизация.
При отвердевании вещества выделяется
такое эже кол теплоты, которое поглощается при его плавлении.

Расчетные формулы для количества теплоты при плавлении и кристаллизации одинаковы.

Температура
плавления и отвердевания одного и того же вещества, если давление не меняется, одинакова.
На протяжении всего процесса кристаллизации температура вещества не меняется,
и оно может одновременно
существовать как в жидком, так и в твердом состояниях.
ЗАГЛЯНИ НА КНИЖНУЮ ПОЛКУ!
ВАУ, ИНТЕРЕСНЫЕ ЯВЛЕНИЯ!
Цветной лёд?
Если в пластмассовый стакан с водой добавить немного краски или заварки, размешать и, получив цветной раствор, укутать стакан сверху и выставить на мороз, то ото дна к поверхности начнет образовываться слой льда. Однако, не надейтесь получить разноцветный лёд!

Там, где начиналось замерзание воды, будет абсолютно прозрачный
слой льда. Верхняя его часть
будет окрашена,
причем даже сильнее,
чем первоначальный раствор. Если концентрация краски
была очень велика, то на поверхности льда может остаться лужица её раствора.
Дело в том, что в растворах краски и солей образуется прозрачный
пресный лёд, т.к. растущие кристаллы вытесняют
любые посторонние атомы и молекулы примесей,
стараясь построить идеальную решетку, пока это возможно. Только когда примесям деваться уже некуда, лёд начинает встраивать
их в свою структуру или оставляет
в виде капсул с концентрированной жидкостью.
Поэтому морской лёд пресный
, а даже самые грязные лужи покрываются прозрачным и чистым льдом.
При какой температуре замерзает вода?
Всегда при нуле градусов?
Но если в абсолютно
чистый и сухой стакан налить прокипяченую воду и поставить за окно на мороз при температуре минус 2-5 градусов С, прикрыв чистым стеклом и защитив от прямых солнечных лучей, то через несколько часов содержимое стакана охладится ниже нуля, но останется жидким.
Если затем открыть стакан и бросить в воду кусочек льда или, снега или даже просто пыли, то буквально на ваших глазах вода мгновенно
замёрзнет, прорастая по всему объёму длинными кристаллами.
Почему?
Превращение жидкости в кристалл происходит в первую очередь на примесях и неоднородностях - частичках пыли, пузырьках воздуха, неровностях на стенках сосуда. В чистой
воде нет центров
кристаллизации, и она может переохлаждаться,
оставаясь жидкой. Таким способом удавалось довести температуру воды до минус 70°С.
Как это происходит в природе?
Глубокой осенью очень чистые
речки и ручьи начинают замерзать со дна.
Сквозь слой чистой воды хорошо видно, что водоросли и коряги на дне обрастают рыхлой ледяной шубой. В какой-то момент этот донный лёд всплывает, и поверхность воды мгновенно
оказывается скованной ледяной коркой.
Температура верхних слоёв воды ниже, чем глубинных, и замерзание вроде бы должно начинаться с поверхности. Однако чистая вода замерзает неохотно,
и лёд в первую очередь образуется там, где имеются взвесь ила и твёрдая поверхность, - возле дна.
Ниже по течению от водопадов и водосбросов плотин часто появляется губчатая масса внутриводного льда, вырастающего во вспененной воде. Поднимаясь на поверхность, она порой забивает всё русло, образуя так называемые зажоры, которые могут даже запрудить речку.
Почему лёд легче воды?
Внутри льда много пор и промежутков, заполненных воздухом, но эта не причина,
которой можно объяснить то обстоятельство, что лед легче воды. Лёд и без микроскопических пор
все равно имеет плотность меньше, чем у воды. Все дело в особенностях
внутреннего строения льда. В кристалле льда молекулы воды расположены в узлах кристаллической решетки так, что каждая имеет четырех "соседок".
У воды же нет
кристаллической структуры, и молекулы в жидкости располагаются теснее,
чем в кристалле, т.е. вода плотнее льда.
Сначала при таянии льда освободившиеся молекулы ещё сохраняют
структуру кристаллической решётки, и плотность воды остаётся низкой
, но постепенно кристаллическая решетка разрушается, и плотность воды растёт.
При температуре + 4°С плотность воды достигает максимума,
а затем с увеличением температуры начинает уменьшаться из-за нарастания скорости теплового движения молекул.
Как замерзает лужа?
При охлаждении верхние слои воды становятся плотнее
и опускаются вниз. Их место занимает более плотная вода. Такое перемешивание
происходит до тех пор, пока температура воды не понизится
до +4 градусов
Цельсия. При такой температуре плотность воды максимальна.
При дальнейшем понижении температуры верхние слои воды уже нем могут более сжиматься,
и постепенно охлаждаясь до 0 градусов вода начинает замерзать.

Осенью температура воздуха ночью и днем сильно отличается, поэтому лёд намерзает слоями.
Нижняя поверхность льда на замерзающей луже очень похожа на поперечный срез ствола дерева:
видны концентрические
кольца. По ширине колец льда можно судить о погоде. Обычно лужа
начинает замерзать от краев, т.к. там глубина меньше. Площадь же образующихся колец с приближением к центру уменьшается.
ИНТЕРЕСНО!
Что в трубах подземной части зданий вода часто замерзает не в мороз, а в оттепель!
Это объясняется плохой теплопроводностью почвы. Тепло проходит сквозь землю так медленно,
что минимум температуры в почве наступает позднее, чем на поверхности земли. Чем глубже,
тем опоздание
больше. Часто за время морозов почва не успевает охладиться,
и лишь когда на земле наступает оттепель, под землю доходят
морозы.
Что, замерзая в закупоренной бутылке, вода разрывает её . Что же произойдет со стаканом, если в нем заморозить воду? Вода, замерзая, будет расширяться не только вверх, но и в стороны, а стекло будет сжимается. Это всё равно приведет к разрушению стакана!
ЗНАЕТЕ ЛИ ВЫ?
Известен случай, когда содержимое хорошо охлаждённой в морозильнике бутылки нарзана, открытой жарким летним днём, мгновенно превратилось в кусок льда.
Интересно ведет себя металл "чугун", который при кристаллизации расширяется. Это позволяет использовать его как материал для художественного литья тонких кружевных решёток и настольных скульптур малых форм. Ведь при застывании, расширяясь , чугун заполняет все, даже самые тонкие детали формы.
На Кубани зимой готовят крепкие напитки - „выморозки“ . Для этого вино выставляют на мороз. В первую очередь замерзает вода, а остаётся концентрированный раствор спирта. Его сливают и повторяют операцию, пока не добьются нужной крепости. Чем выше концентрация спирта, тем ниже температура замерзания.
Самая крупная градина
, зафиксированная людьми, упала в Канзасе,
США.
Вес ее составил почти 700 грамм.
Кислород
в газообразном состоянии при температуре минус 183 градусов С превращается в жидкость,
а при температуре минус 218,6градусов С из жидкого получается твердый кислород.

В старину для хранения продуктов люди пользовались льдом. Карл фон Линде создал первый домашний холодильник, работавший от парового двигателя, который перекачивал газ фреон по трубам. Позади холодильника газ в трубах, конденсируясь, превращался в жидкость. Внутри холодильника жидкий фреон испарялся и его температура резко снижалась, охлаждая холодильную камеру. Только в 1923 году шведские изобретатели – Бальцен фон Платен и Карл Мунтенс создали первый электрический холодильник, в котором фреон превращается из жидкости в газ и забирает тепло из воздуха в холодильнике.
ВОТ ЭТО ДА-А!
Несколько кусков сухого льда, брошенные в горящий бензин , гасят огонь.
Существует лёд, который обжег бы пальцы, если бы до него можно было дотронуться. Получают его под очень большим давлением, при котором вода переходит в твердое состояние при температуре значительно выше 0 градусов Цельсия.
При понижении температуры вещество может переходить из жидкого состояния в твердое.
Этот процесс называется отвердевание или кристаллизация.
При отвердевании вещества выделяется такое эже кол теплоты, которое поглощается при его плавлении.

Расчетные формулы для количества теплоты при плавлении и кристаллизации одинаковы.

Температура плавления и отвердевания одного и того же вещества, если давление не меняется, одинакова.
На протяжении всего процесса кристаллизации температура вещества не меняется, и оно может одновременно существовать как в жидком, так и в твердом состояниях.
ЗАГЛЯНИ НА КНИЖНУЮ ПОЛКУ
ИНТЕРЕСНОЕ О КРИСТАЛЛИЗАЦИИ
Цветной лёд?
Если в пластмассовый стакан с водой добавить немного краски или заварки, размешать и, получив цветной раствор, укутать стакан сверху и выставить на мороз, то ото дна к поверхности начнет образовываться слой льда. Однако, не надейтесь получить разноцветный лёд!

Там, где начиналось замерзание воды, будет абсолютно прозрачный слой льда. Верхняя его часть будет окрашена, причем даже сильнее, чем первоначальный раствор. Если концентрация краски была очень велика, то на поверхности льда может остаться лужица её раствора.
Дело в том, что в растворах краски и солей образуется прозрачный пресный лёд, т.к. растущие кристаллы вытесняют любые посторонние атомы и молекулы примесей, стараясь построить идеальную решетку, пока это возможно. Только когда примесям деваться уже некуда, лёд начинает встраивать их в свою структуру или оставляет в виде капсул с концентрированной жидкостью. Поэтому морской лёд пресный, а даже самые грязные лужи покрываются прозрачным и чистым льдом.
При какой температуре замерзает вода?
Всегда ли при нуле градусов?
Но если в абсолютно чистый и сухой стакан налить прокипяченую воду и поставить за окно на мороз при температуре минус 2-5 градусов С, прикрыв чистым стеклом и защитив от прямых солнечных лучей, то через несколько часов содержимое стакана охладится ниже нуля, но останется жидким.
Если затем открыть стакан и бросить в воду кусочек льда или, снега или даже просто пыли, то буквально на ваших глазах вода мгновенно замёрзнет, прорастая по всему объёму длинными кристаллами.
Почему?
Превращение жидкости в кристалл происходит в первую очередь на примесях и неоднородностях - частичках пыли, пузырьках воздуха, неровностях на стенках сосуда. В чистой воде нет центров кристаллизации, и она может переохлаждаться, оставаясь жидкой. Таким способом удавалось довести температуру воды до минус 70°С.
Как это происходит в природе?
Глубокой осенью очень чистые речки и ручьи начинают замерзать со дна. Сквозь слой чистой воды хорошо видно, что водоросли и коряги на дне обрастают рыхлой ледяной шубой. В какой-то момент этот донный лёд всплывает, и поверхность воды мгновенно оказывается скованной ледяной коркой.
Температура верхних слоёв воды ниже, чем глубинных, и замерзание вроде бы должно начинаться с поверхности. Однако чистая вода замерзает неохотно, и лёд в первую очередь образуется там, где имеются взвесь ила и твёрдая поверхность, - возле дна.
Ниже по течению от водопадов и водосбросов плотин часто появляется губчатая масса внутриводного льда, вырастающего во вспененной воде. Поднимаясь на поверхность, она порой забивает всё русло, образуя так называемые зажоры, которые могут даже запрудить речку.
Почему лёд легче воды?
Внутри льда много пор и промежутков, заполненных воздухом, но эта не причина, которой можно объяснить то обстоятельство, что лед легче воды. Лёд и без микроскопических пор
все равно имеет плотность меньше, чем у воды. Все дело в особенностях внутреннего строения льда. В кристалле льда молекулы воды расположены в узлах кристаллической решетки так, что каждая имеет четырех "соседок".
У воды же нет кристаллической структуры, и молекулы в жидкости располагаются теснее, чем в кристалле, т.е. вода плотнее льда.
Сначала при таянии льда освободившиеся молекулы ещё сохраняют структуру кристаллической решётки, и плотность воды остаётся низкой, но постепенно кристаллическая решетка разрушается, и плотность воды растёт.
При температуре + 4°С плотность воды достигает максимума, а затем с увеличением температуры начинает уменьшаться из-за нарастания скорости теплового движения молекул.
Как замерзает лужа?
При охлаждении верхние слои воды становятся плотнее и опускаются вниз. Их место занимает более плотная вода. Такое перемешивание происходит до тех пор, пока температура воды не понизится до +4 градусов Цельсия. При такой температуре плотность воды максимальна.
При дальнейшем понижении температуры верхние слои воды уже нем могут более сжиматься, и постепенно охлаждаясь до 0 градусов вода начинает замерзать.

Осенью температура воздуха ночью и днем сильно отличается, поэтому лёд намерзает слоями.
Нижняя поверхность льда на замерзающей луже очень похожа на поперечный срез ствола дерева:
видны концентрические кольца. По ширине колец льда можно судить о погоде. Обычно лужа начинает замерзать от краев, т.к. там глубина меньше. Площадь же образующихся колец с приближением к центру уменьшается.
ИНТЕРЕСНО
Что в трубах подземной части зданий вода часто замерзает не в мороз, а в оттепель!
Это объясняется плохой теплопроводностью почвы. Тепло проходит сквозь землю так медленно, что минимум температуры в почве наступает позднее, чем на поверхности земли. Чем глубже, тем опоздание больше. Часто за время морозов почва не успевает охладиться, и лишь когда на земле наступает оттепель, под землю доходят морозы.
Что, замерзая в закупоренной бутылке, вода разрывает её. Что же произойдет со стаканом, если в нем заморозить воду? Вода, замерзая, будет расширяться не только вверх, но и в стороны, а стекло будет сжимается. Это всё равно приведет к разрушению стакана!
ЗНАЕТЕ ЛИ ВЫ
Известен случай, когда содержимое хорошо охлаждённой в морозильнике бутылки нарзана, открытой жарким летним днём, мгновенно превратилось в кусок льда.
Интересно ведет себя металл "чугун", который при кристаллизации расширяется. Это позволяет использовать его как материал для художественного литья тонких кружевных решёток и настольных скульптур малых форм. Ведь при застывании, расширяясь, чугун заполняет все, даже самые тонкие детали формы.
На Кубани зимой готовят крепкие напитки - „выморозки“. Для этого вино выставляют на мороз. В первую очередь замерзает вода, а остаётся концентрированный раствор спирта. Его сливают и повторяют операцию, пока не добьются нужной крепости. Чем выше концентрация спирта, тем ниже температура замерзания.
Самая крупная градина, зафиксированная людьми, упала в Канзасе, США. Вес ее составил почти 700 грамм.
Кислород в газообразном состоянии при температуре минус 183 градусов С превращается в жидкость, а при температуре минус 218,6градусов С из жидкого получается твердый кислород






