Жидкое состояние вещества свойства жидкостей. Термины, определения и параметры. Если капилляры имеют круглое сечение, то
В жидком состоянии расстояние между частицами значительно меньше, чем в газообразном. Частицы занимают основную часть объема, постоянно соприкасаясь друг с другом и притягиваются друг к другу. Наблюдается некоторая упорядоченность частиц (ближний порядок). Частицы подвижны относительно друг друга.
В жидкостях между частицами возникают вандерваальсовы взаимодействия: дисперсионные, ориентационные и индукционные. Небольшие группы частиц, объединенных теми или иными силами, называются кластерами . В случае одинаковых частиц кластеры в жидкости называются ассоциатами
При погружении в горную порода вытесняется объем воды, равный объему горной породы. Для сравнения, блок дерева действует более тонким образом, погружаясь в воду под действием силы тяжести до тех пор, пока она не вытеснит объем воды, равный его собственному весу.
Испарение и конденсация жидкостей
Когда все силы стабилизируются, дерево перестает опускаться. Это тогда называется Принципом Архимеда, поскольку он был задуман древнегреческим математиком, физиком, астрономом и философом Архимедом. Архимед. Принцип далее утверждает, что силы, поддерживающие деревянный блок, будут фокусироваться вверх и внутрь на нем, достигая высшей точки в точке, называемой центром плавучести. Всегда над центром масс плавающего объекта местоположение центра плавучести является способный указывать устойчивость объекта.
В жидкостях при образовании водородных связей увеличивается упорядочение частиц. Однако водородные связи и вандерваальсовы силы непрочны – молекулы в жидком состоянии находятся в непрерывном хаотическом движении, которое получило название броуновского движения .
Для жидкого состояния справедливо распределение молекул по скоростям и энергиям Максвелла-Больцмана.
Чем больше расстояние между центром плавучести и центром масс, тем более устойчивым является объект, то есть, тем меньше вероятность опрокидывания. Другой характерной особенностью жидкостей является то, что если более плотная жидкость выливается в менее плотную жидкость, а две не смешиваются, они будут отделяться, оставляя менее плотную жидкость сверху и более плотную жидкость на дне. Классическим примером этого является разделение, которое происходит с нефтью и водой.
Подводные лодки - отличный пример плавучести на работе. Во время путешествия по поверхности океана подводная лодка обладает средней плотностью, несколько меньшей, чем у воды. Однако, когда он идет на погружение, подводной лодке нужно взять воду. Затем это увеличивает свою плотность за пределы воды, что приводит к ее способности к потоку.
Теория жидкостей разработана гораздо хуже, чем газов, поскольку свойства жидкостей зависят от геометрии и полярности взаимно близко расположенных молекул. Кроме того, отсутствие определенной структуры жидкостей затрудняет их формализованное описание – в большинстве учебников жидкостям уделено гораздо меньше места, чем газам и твердым кристаллическим веществам.
Чтобы снова подняться на поверхность, подводная лодка должна продуть резервуары с водой. Он выполняет эту задачу, вдувая в них воздух, который, в свою очередь, вытесняет воду и снижает плотность подводной лодки. Давление жидкости и поверхностное натяжение.
Хотя это и не обязательно является очевидным фактом, независимо от глубины, с которой он падает, фактическая плавучесть подводной лодки никоим образом не изменяется. Это связано с тем, что вода по существу несжимаема, а ее плотность практически одинакова на любой глубине. Но даже при том, что плотность не может измениться, существует конечная точка, налагаемая давлением воды, масса воды над объектом, которая линейно увеличивается с добавленной глубиной.
Между жидкостями и газами нет резкой границы – она полностью исчезает в критических точках . Для каждого газа известна температура, выше которой он не может быть жидким ни при каком давлении; при этой критической температуре исчезает граница (мениск) между жидкостью и ее насыщенным паром. Существование критической температуры ("температуры абсолютного кипения") установил Д.И.Менделеев в 1860 г
Поэтому, если вы удвоите глубину подводной лодки, вы также удвоете давление. Хотя это не такая сложная концепция, чтобы понять, что не совсем очевидно, так это то, что давление воды одинаково независимо от направления. Например, если бы вы надавили на верхнюю часть резервуара с водой, погрузив его, но проигнорировали идею о том, что, когда танк опускался все глубже и глубже, давление, действующее на все стороны и на дно резервуара, было равно что, нажимая на верхнюю часть бака, вы были бы удивлены, узнав, насколько тяжелым становится танк.
Однако, если вы должны были открыть клапан на дне резервуара, в потоке будет вытекать вода, уменьшая общее давление как внутри, так и снаружи резервуара. Плюс, поскольку вода сейчас движется, она имеет кинетическую энергию. И, как в соответствии с принципом Торричелли, чем больше давление на клапане, тем больше кинетическая энергия потока и тем больше его скорость.
Таблица 7.2 - Критические параметры (t к, p к, V к) некоторых веществ
| Вещество | t к, о С | p к, атм | V к, см 3 /моль | t плавл о С | t кип о С |
| He | -267,9 | 2,26 | 57,8 | -271,4 | -268,94 |
| H 2 | -239,9 | 12,8 | 65,0 | -259,2 | -252,77 |
| N 2 2 | -147,0 | 33,54 | 90,1 | -210,01 | -195,82 |
| O 2 2 | -118,4 | 50,1 | -218,76 | -182,97 | |
| CH 4 | -82,1 | 45,8 | 99,0 | -182,49 | -161,58 |
| CO 2 | +31,0 | 72,9 | 94,0 | -56,16 | -78,48(субл) |
| NH 3 | 132,3 | 111,3 | 72,5 | -77,76 | -33,43 |
| Cl 2 | 144,0 | 76,1 | -101,0 | -34,06 | |
| SO 2 | 157,5 | 77,8 | -75,48 | -10,02 | |
| H 2 O | 374,2 | 218,1 | 0,0 | 100,0 |
Давление насыщенных паров – парциальное давление, при котором скорости испарения и конденсации пара равны:
Напомним, что основные характеристики жидкости заключаются в следующем. Они являются жидкоподобными веществами, которые обладают способностью течь и не имеют возможности переконфигурировать их прежнюю форму после деформации. Они могут принимать форму любого контейнера, в который они наливают.
Они обладают сходными свойствами с твердыми веществами с точки зрения согласованности цвета и плотности. У них есть тенденция искать общий уровень. То, что мы видим вокруг нас, живое или неживое, состоит из материи. «Материя» может быть определена как «любое вещество, которое имеет и занимает пространство». Материя имеет разные формы. Существуют три разных формы материи; твердых веществ, жидкостей и газов. Они различаются друг от друга в зависимости от конкретной особенности, характерной для каждой формы, которая зависит от молекул в разных формах материи.
где А и В – константы.
Температура кипения – температура, при которой давление насыщенных паров жидкости равно атмосферному давлению.
Жидкости обладают текучестью – способность к перемещению под действием небольших сдвигающих усилия; жидкость занимает объем, в который ее помещают.
Сопротивление жидкости текучести получило название вязкости, [Па. с].
Характеристики каждого вещества; твердой, жидкой или зависит от различного притяжения между этими молекулами. В этой статье мы обсудим различия между двумя формами вещества, жидкостей и газов. Есть четыре основных момента различия, по которым мы можем различать жидкости и газы на самом базовом уровне; формы, объема, твердости и способности к течению.
Жидкости Молекулы жидкостей обладают умеренной силой притяжения; сила между молекулами меньше твердых веществ и больше газов. Это приводит к более легкому и свободному перемещению молекул внутри жидкостей. Молекулярное движение приводит к жидкостям, имеющим определенный и фиксированный объем. Жидкости принимают форму контейнера, в котором они хранятся, когда молекулы перемещаются, чтобы заполнить пространство. Они не имеют определенной формы и имеют способность течь. Жидкости могут течь; таким образом, их также называют «жидкостью».
Поверхностное натяжение [Дж/м 2 ] – работа, необходимая для создания единицы поверхности.
Жидкокристаллическое состояние – вещества в жидком состоянии, обладающие высокой степенью упорядочности, занимают промежуточное положение между кристаллами и жидкостью. Они обладают текучестью, но в то же время имеют дальний порядок. Например – производные коричневой кислоты, азолитинов, стероидов.
Жидкости не являются жесткими. Например, когда замораживается ниже 0 градусов Цельсия, он затвердевает на льду. Некоторые примеры жидкостей: вода, масла, молоко, соки и т.д. Газы Молекулы в газах имеют очень слабую силу притяжения между ними и очень слабо упакованы. Таким образом, они не имеют определенной формы, и они принимают форму контейнера. Из-за их молекулярной структуры газы также не имеют определенного объема и становятся объемом контейнера, в котором они хранятся. Газы могут течь легко; они могут быть показаны просто путем освещения ладана.
Температура просветления – температура, при которой жидкие кристаллы (жк) переходят в обычное жидкое состояние.
7.5 Твёрдые вещества
В твёрдом состоянии частицы настолько сближаются друг с другом, что между ними возникают прочные связи, отсутствует поступательное движение и сохраняются колебания около своего положения. Твёрдые вещества могут находиться в аморфном и кристаллическом состоянии.
Свойства жидкостных пленок
Запах ладана перемещается из одной части комнаты в другую. Они могут быть легко сжаты, поскольку у них много места между молекулами. Жидкости обладают меньшей силой притяжения между молекулами, чем твердые вещества, и больше газов; газы имеют очень слабую силу притяжения между молекулами, которая является наименее из трех состояний материи. Жидкости имеют определенный объем; газы не имеют определенного объема. Жидкости не могут быть легко сжаты; газы могут быть легко сжаты.
Все на Земле состоит из материи, но эта материя не всегда одинакова. Материя может существовать в четырех разных фазах, и кинетическая теория материи помогает нам понять различия между этими фазами. Твердые вещества, жидкости, газы и плазма: эти слова должны быть вам знакомы, потому что они являются четырьмя фазами материи, которые могут быть разными, которые могут иметь дело с различными формами. То, что существует, состоит в том, что многие вещества могут существовать как более чем одна фаза. Возьмите воду, например: вода может существовать как твердое тело, жидкость и газ.
7.5.1 Вещества в аморфном состоянии
В аморфном состоянии вещества не имеют упорядоченной структуры.
Стеклообразное состояние – твердое аморфное состояние вещества, которое получается в результате глубокого переохлаждения жидкости. Это состояние неравновесно, однако стекла могут существовать длительное время. Размягчение стекла происходит в некотором диапазоне температур – интервале стеклования, границы которого зависят от скорости охлаждения. С увеличением скорости охлаждения жидкости или пара возрастает вероятность получения данного вещества в стеклообразном состоянии.
Разница между этими состояниями - это количество энергии. Твердые частицы имеют наименьшее количество энергии, что является частью того, почему их частицы так тесно связаны. Жидкости имеют больше энергии, чем твердые частицы, поэтому они будут принимать форму своего контейнера, но только до поверхности.
Механические свойства жидкости
Газы имеют еще больше энергии, чем жидкости. Тем более, что их частицы распространяются, чтобы заполнить все пространство их контейнера. Частицы газа имеют так много энергии, что они просто не могут оставаться неподвижными. Они летают во всех направлениях, располагая как можно больше расстояния между собой и остальными частицами газа.
В конце 60-х годов XX века получены аморфные металлы (металлические стекла) – для этого потребовалось охлаждать расплавленный металл со скоростью 10 6 - 10 8 град/с. Большинство аморфных металлов и сплавов кристаллизуются при нагреве свыше 300 о С. Одно из важнейших применений – микроэлектроника (диффузионные барьеры на границе металл-полупроводник) и магнитные накопители (головки ЖМД). Последнее – благодаря уникальной магнитомягкости (магнитная анизотропия меньше на два порядка, чем в обычных сплавах).
Плазмы представляют собой ионизированные газы, и в их естественной форме на Земле необычны. Вы видели их как искусственные вещи, такие как неоновые знаки и флуоресцентные лампочки. Но в остальной части вселенной плазма на самом деле является самой распространенной фазой материи! Большинство звезд - это плазма, как и северное сияние, которое вы видите вокруг Полярные регионы. Плазма существует только при определенных условиях, поэтому мы закончим наше обсуждение этого здесь для этого урока.
Кинетическая теория материи утверждает, что вся материя состоит из мелких частиц, которые находятся в случайном движении и имеют пространство между ними. Это означает, что независимо от того, какой фазовый материал находится, он состоит из отдельных движущихся частиц.
Аморфные вещества изотропны , т.е. имеют одинаковые свойства во всех направлениях.
7.5.2 Вещества в кристаллическом состоянии
Твердые кристаллические вещества обладают упорядоченной структурой с повторяющимися элементами, что позволяет исследовать их методом дифракции рентгеновских лучей (метод рентгеноструктурного анализа, используется с 1912 г.
Эта теория звучит довольно просто, но на самом деле она многое объясняет о физических свойствах материи и ее действиях. Вы можете быть удивлены, узнав, что частицы твердого тела на самом деле движутся, этого вам просто не достаточно. Этот тип вибрационного движения - это то, почему твердое тело не изменило форму независимо от того, какой контейнер вы положили.
Помните, как жидкие частицы имеют больше энергии, чем твердые частицы? Дополнительная энергия в этом состоянии позволяет частицам перемещаться более свободно, и они распространяются больше, чем частицы твердого тела, что создает больше пространства между этими частицами. Вот почему жидкость примет форму своего контейнера до его поверхности.
Монокристаллы (одиночные соединения) характеризуются анизотропностью – зависимость свойств от направления в пространстве.
Регулярное расположение частиц в твёрдом теле изображается в виде кристаллической решётки. Кристаллические вещества плавятся при определённой температуре, называемой температурой плавления .
А поскольку газы имеют еще больше энергии, чем жидкости, их частицы движутся намного больше. Вот почему газ будет расширяться, чтобы заполнить весь контейнер, а не только его поверхность, как жидкость. Мало того, что частицы твердого тела не очень сильно движутся, но они также очень сильно соприкасаются друг с другом сильными силами притяжения. Эти силы удерживают частицы на месте и являются то, что придает твердому фиксированный размер и форму.
С другой стороны, частицы газа настолько далеки друг от друга, что силы притяжения между ними считаются пренебрежимо малыми. Частицы газа рассматриваются как независимые друг от друга, что означает, что газ является противоположным твердому веществу и не имеет фиксированного размера или формы.
Кристаллы характеризуются энергией, постоянной кристаллической решётки и координационном числом.
Постоянная решётка характеризует расстояние между центрами частиц, занимающих узлы в кристалле, в направлении характеристических осей.
Координационным числом обычно называется число частиц, непосредственно примыкающих к данной частице в кристалле (смотри рисунок 7.2 – координационное число восемь и по цезию и по хлору)
Поскольку движение жидких частиц находится между твердым телом и газом, силы притяжения между его частицами также находятся в среднем диапазоне двух других фаз. Жидкие частицы обладают большей свободой, чем твердые частицы, поэтому жидкость может свободно течь. Это означает, что, как и газ, жидкость не имеет фиксированной формы. Но поскольку частицы не настолько свободны, как частицы газа, жидкость имеет фиксированный объем.
Кинетическая теория материи также полезна для объяснения того, почему вещества могут изменять фазу при определенных условиях. Вы знаете, что вода может быть твердой, жидкой или газообразной, но как это происходит? Изменение фазы происходит, когда энергия добавляется или отбирается от вещества, обычно в виде тепла.
Энергией кристаллической решётки называют энергию, необходимую для разрушения одного моля кристалла и удаления частиц за пределы их взаимодействия.
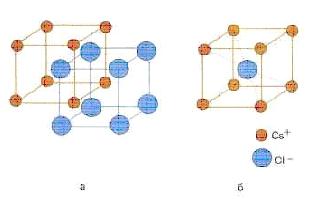
Рисунок 7.2 - Строение кристалла хлористого цезия CsCl (а) и объемноцентрированная кубическая элементарная ячейка этого кристалла (б)
7.5.3 Кристаллические структуры
Наименьшей структурной единицей кристалла, которая выражает все свойства его симметрии, является элементарная ячейка. При многократном повторении ячейки по трём измерениям получают кристаллическую решётку.
Имеется семь основных ячеек: кубическая, тетраэдрическая, гексагональная, ромбоэдрическая, орто ромбоэдрическая, моноклинная и триклинная. Имеется семь производных о основных элементарных ячеек, например объёмно центрированная, кубическая гранецентрированная.
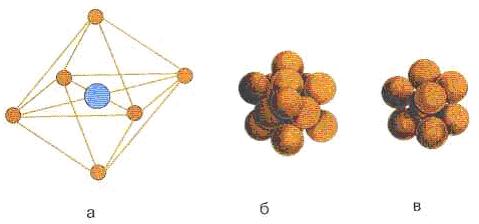
а - элементарная ячейка кристалла NaCl; б - плотная гранецентрированная кубическая упаковка NaCl; в- объемноцентрированная кубическая упаковка кристалла CsCl Рисунок Рисунок 7.3 - Элементарная ячейка
Изоморфные вещества – вещества близкой химической природы, образующие одинаковые кристаллические структуры: CaSiO 4 и MgSiO 4
Полиморфизм – соединения, существующие в двух и более кристаллических структурах, например SiO 2 (в виде гексагонального кварца, ромбического тридимита и кубического кристобаллита.)
Аллотропные модификации – полиморфные модификации простых веществ, например, углерод: алмаз, графит, карбин, фуллерен.
По природе частиц в узлах кристаллической решётки и химических связей между ними кристаллы подразделяются на:
1) молекулярные – в узлах находятся молекулы, между которыми действуют вандерваальсовы силы, имеющие невысокую энергию: кристаллы льда;
2) атомно – ковалентные кристаллы – в узлах кристаллов располагаются атомы, образующие друг с другом прочные ковалентные связи, обладают высокой энергией решётки, например, алмаз (углерод);
3) ионные кристаллы – структурными единицами кристаллов этого типа являются положительно и отрицательно заряженные ионы, между которыми происходит электрическое взаимодействие, характеризуемое достаточно высокой энергией, например NaCL, KCL;
4) металлические кристаллы – вещества, которые обладают высокой электропроводимостью, теплопроводимостью, ковкостью, пластичностью, металлическим бликом и высокой отражательной способностью по отношению к свету; связь в кристаллах металлическая, энергия металлической связи является промежуточной между энергиями ковалентных и молекулярных кристаллов;
5) кристаллы со смешанными связями – между частицами существуют сложные взаимодействия, которые можно описать наложениям двух или более видов связей друг на друга, например клатраты (соединения включены) – образованы включением молекул (гостей) в полости кристаллического каркаса, состоящего из частиц другого вида (хозяев): газовые клатраты CH 4 . 6H 2 O, клатраты мочевины.
Жидкость, занимая промежуточное положение между газами и кристаллами, сочетает в себе свойства обоих видов этих тел .
1. Как и твёрдое тело, жидкость малосжимаема из-за плотного расположения молекул. (Однако если бы вода могла полностью освободиться от сжатия, то уровень воды в мировом океане поднялся бы на 35 м и вода затопила бы 5 000 000 км 2 суши.)
2. Как и твёрдое тело, жидкость сохраняет объём , но подобно газу принимает форму сосуда .
3. Для кристаллов характерен дальний порядок в расположении атомов (кристаллическая решетка), для газов – полный хаос . Для жидкости существует промежуточное состояние – ближний порядок , т.е. расположение только ближайших молекул упорядоченно. При удалении от данной молекулы на расстояние 3–4 эффективных диаметра молекулы упорядоченность размывается. Поэтому жидкости близки к поликристаллическим телам, состоящим из очень мелких кристаллов (размерами около 10 9 м), произвольно ориентированных друг относительно друга. Благодаря этому свойства большинства жидкостей одинаковы по всем направлениям (и нет анизотропии, как в кристаллах).
4. Большинство жидкостей , как и твёрдые тела, при увеличении температуры увеличивают свой объём , уменьшая при этом свою плотность (при критической температуре плотность жидкости равна плотности её пара). Вода отличается известной аномалией , состоящей в том, что при +4 С вода обладает максимальной плотностью. Эта аномалия объясняется тем, что молекулы воды частично собираются в группы из нескольких молекул (кластеры), образуя своеобразные большие молекулы Н 2 О , (Н 2 О ) 2 , (Н 2 О ) 3 … с разной плотностью. При различных температурах соотношение концентраций этих групп молекул разное.
Существуют аморфные тела (стекло, янтарь, смолы, битумы...), которые принято рассматривать как переохлажденные жидкости с очень высоким коэффициентом вязкости. Они имеют одинаковые свойства по всем направлениям (изотропны), ближний порядок в расположении частиц, у них нет температуры плавления (при нагреве вещество постепенно размягчается и переходит в жидкое состояние).
В технике применяются магнитные жидкости – это обычные жидкости (вода, керосин, различные масла), в которые введены (до 50%) мельчайшие частицы (размером в несколько микрон) твердого ферромагнитного материала (например, Fe 2 O 3). Перемещением магнитной жидкости и её вязкостью можно управлять магнитным полем. В сильных магнитных полях магнитная жидкость мгновенно твердеет.
Некоторые органические вещества, молекулы которых имеют нитевидную форму или форму плоских пластин, могут находиться в особом состоянии, обладая одновременно свойствами анизотропии и текучести. Они называются жидкими кристаллами . Для изменения ориентации молекул жидкого кристалла (при этом изменяется его прозрачность) требуется напряжение около 1 В и мощность порядка микроватт, что можно обеспечить непосредственной подачей сигналов с интегральных схем без дополнительного усиления. Поэтому жидкие кристаллы широко применяются в индикаторах электронных часов, калькуляторах, дисплеях.
При замерзании вода увеличивается в объеме на 11%, и если вода замерзает в замкнутом пространстве, может достигаться давление 2500 атмосфер (разрушаются водопроводные трубы, горные породы...).
Уводыодна из самых больших : 1) диэлектрическая проницаемость (поэтому вода является хорошим растворителем, особенно солей с ионными связями – в Мировом океане содержится вся таблица Менделеева); 2) теплота плавления (медленное таяние снега весной); 3) теплота парообразования ; 4) поверхностное натяжение ; 5) теплоёмкость (мягкий климат прибрежных районов).
Существует легкая (1 г/см 3) и тяжелая (1,106 г/см 3) вода . Легкая вода («живая») – биологически активна – это окись протия Н 2 О . Тяжелая вода («мертвая») – подавляет жизнедеятельность организмов – это окись дейтерия D 2 O . Протий (1 а.е.м.), дейтерий (2 а.е.м.) и тритий (3 а.е.м.) – это изотопы водорода. Существуют также и 6 изотопов кислорода: от 14 О до 19 О , которые могут находиться в молекуле воды.
При обработке воды магнитным полем изменяются её свойства: изменяется смачиваемость твердых тел, ускоряется их растворение, изменяется концентрация растворенных газов, предотвращается образование накипи в паровых котлах, ускоряется в 4 раза затвердевание бетона и повышается его прочность на 45%, оказывается биологическое воздействие на человека (магнитные браслеты и серьги, магнитофоры и т.п.) и растения (повышается всхожесть и урожайность сельскохозяйственных культур).
Серебряная вода может долго храниться (около полугода), так как происходит обезвреживание воды от микробов и бактерий ионами серебра (применяется в космонавтике, для консервирования продуктов, обеззараживания воды в бассейнах, в лечебных целях для профилактики и борьбы с желудочно-кишечными заболеваниями и воспалительными процессами).
Обеззараживание питьевой воды в городских водопроводах осуществляется хлорированием и озонированием воды. Существуют и физические методы обеззараживания при помощи ультрафиолетового излучения и ультразвука.
Растворимость газов в воде зависит от температуры, давления, минерализации, присутствия в водном растворе других газов. В 1 л воды при 0 С может быть растворено: гелия – 10 мл, углекислого газа – 1713 мл, сероводорода – 4630 мл, аммиака – 1300000 мл (нашатырный спирт). Аквалангисты при погружении на большие глубины используют специальные дыхательные смеси, чтобы при всплытии не получилась «газированная кровь» из-за растворения в ней азота.
Все живые организмы на 60–80% состоят из воды. Кровь человека и животных по составу солей близка к океанической воде. Человек и животные могут в своих организмах синтезировать воду, образовывать её при сгорании пищевых продуктов и самих тканей. У верблюда, например, жир, содержащийся в горбу, может в результате окисления дать 40 л воды.
При электролизе воды можно получить два её вида: 1) кислую воду («мертвую»), которая действует как антисептическое средство (аналогично тому, как в кислом желудочном соке погибают многие болезнетворные микробы); 2) щелочную воду («живую»), которая активизирует биологические процессы (повышает урожайность, быстрее заживляет раны и т.п.).
О других особенностях воды (структурированной, энергоинформационной и др.) можно узнать из Интернета.
ТРИЗ-задание 27. Вода-работница
Чаще всего различные механизмы имеют «твёрдотельные» рабочие органы . Приведите примеры технических устройств, в которых рабочим органом является вода (жидкость). Каким законам развития технических систем соответствует такой рабочий орган?
ТРИЗ-задание 28. Вода в решете
В известной задаче «Как носить воду в решете ?» имеется явное физическое противоречие : в решете должны быть отверстия, чтобы через него можно было просеивать сыпучие вещества, и не должно быть отверстий, чтобы вода не выливалась. Одно из возможных решений этой задачи можно найти у Я.И. Перельмана в «Занимательной физике», где предложено опустить решето в расплавленный парафин, чтобы сетка решета не смачивалась водой. На основе приёмов устранения технических и физических противоречий предложите ещё 10–20 других способов решения этой задачи.






