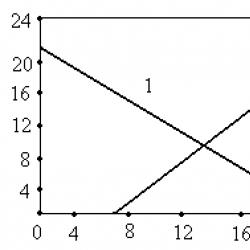
Prezentare pe tema „utilizarea izotopilor radioactivi”. Aplicații ale izotopilor Care sunt posibilele aplicații ale izotopilor radioactivi, dați exemple
Lucrări de curs
Pe tema: „Radioactivitate.
Aplicarea izotopilor radioactivi în tehnologie”
Introducere
1. Tipuri de radiații radioactive
2.Alte tipuri de radioactivitate
3. Dezintegrarea alfa
4. Dezintegrare beta
5. Dezintegrarea gamma
6.Legea dezintegrarii radioactive
7.Serii radioactive
8. Efectul radiațiilor radioactive asupra oamenilor
9.Utilizarea izotopilor radioactivi
Lista literaturii folosite
Introducere
Radioactivitate– transformarea nucleelor atomice în alte nuclee, însoțită de emisia de diverse particule și radiații electromagnetice. De aici și numele fenomenului: în latină radio - radiate, activus - efectiv. Acest cuvânt a fost inventat de Marie Curie. Când un nucleu instabil - un radionuclid - se descompune, una sau mai multe particule cu energie mare zboară din el cu viteză mare. Fluxul acestor particule se numește radiație radioactivă sau pur și simplu radiație.
raze X. Descoperirea radioactivității a fost direct legată de descoperirea lui Roentgen. Mai mult, de ceva timp au crezut că acestea sunt același tip de radiații. Sfârșitul secolului al XIX-lea În general, el a fost bogat în descoperirea diferitelor tipuri de „radiații” necunoscute anterior. În anii 1880, fizicianul englez Joseph John Thomson a început să studieze purtătorii elementari de sarcină negativă; în 1891, fizicianul irlandez George Johnston Stoney (1826–1911) a numit aceste particule electroni. În cele din urmă, în decembrie, Wilhelm Conrad Roentgen a anunțat descoperirea unui nou tip de raze, pe care l-a numit raze X. Până acum, în majoritatea țărilor ele sunt numite așa, dar în Germania și Rusia a fost acceptată propunerea biologului german Rudolf Albert von Kölliker (1817–1905) de a numi razele raze X. Aceste raze sunt create atunci când electronii care zboară rapid în vid (razele catodice) se ciocnesc de un obstacol. Se știa că atunci când razele catodice lovesc sticla, aceasta emite lumină vizibilă - luminiscență verde. Raze X au descoperit că, în același timp, alte raze invizibile emanau din pata verde de pe sticlă. Acest lucru s-a întâmplat întâmplător: într-o cameră întunecată, strălucea un ecran din apropiere acoperit cu tetracianoplatinat de bariu Ba (numit anterior sulfură de platină de bariu). Această substanță produce luminiscență galben-verde strălucitoare sub influența razelor ultraviolete și catodice. Dar razele catodice nu au lovit ecranul și, în plus, atunci când dispozitivul a fost acoperit cu hârtie neagră, ecranul a continuat să strălucească. Roentgen a descoperit curând că radiațiile au trecut prin multe substanțe opace și au cauzat înnegrirea unei plăci fotografice învelite în hârtie neagră sau chiar plasată într-o carcasă metalică. Razele au trecut printr-o carte foarte groasă, printr-o scândură de molid de 3 cm grosime, printr-o placă de aluminiu de 1,5 cm grosime... Roentgen și-a dat seama de posibilitățile descoperirii sale: „Dacă ții mâna între tubul de descărcare și ecran,” el a scris: „puteți vedea oasele umbre întunecate pe fundalul contururilor mai deschise ale mâinii”. Acesta a fost primul examen fluoroscopic din istorie.
Descoperirea lui Roentgen s-a răspândit instantaneu în întreaga lume și i-a uimit nu numai pe specialiști. În ajunul anului 1896, o fotografie a unei mâini a fost expusă într-o librărie dintr-un oraș german. Pe ea erau vizibile oasele unei persoane vii, iar pe unul dintre degete era o verigheta. Era o fotografie cu raze X a mâinii soției lui Roentgen. Primul mesaj al lui Roentgen „ Despre un nou tip de raze" a fost publicată în „Rapoartele Societății Fizico-Medicale Würzburg” pe 28 decembrie, a fost tradusă și publicată imediat în diferite țări, cea mai faimoasă revistă științifică „Nature” publicată la Londra a publicat articolul lui Roentgen la 23 ianuarie 1896.
Noi raze au început să fie explorate în întreaga lume; doar într-un an au fost publicate peste o mie de lucrări pe această temă. În spitale au apărut și aparate cu raze X de design simplu: utilizarea medicală a noilor raze era evidentă.
Acum, razele X sunt utilizate pe scară largă (și nu numai în scopuri medicale) în întreaga lume.
razele lui Becquerel. Descoperirea lui Roentgen a dus curând la o descoperire la fel de remarcabilă. A fost realizată în 1896 de către fizicianul francez Antoine Henri Becquerel. La 20 ianuarie 1896, a participat la o întâlnire a Academiei, la care fizicianul și filozoful Henri Poincaré a vorbit despre descoperirea lui Roentgen și a demonstrat fotografii cu raze X ale unei mâini umane făcute în Franța. Poincare nu s-a limitat la a vorbi despre noi raze. El a sugerat că aceste raze sunt asociate cu luminiscența și, probabil, apar întotdeauna simultan cu acest tip de strălucire, astfel încât probabil că este posibil să se facă fără raze catodice. Luminescența substanțelor sub influența radiațiilor ultraviolete - fluorescență sau fosforescență (în secolul al XIX-lea nu exista o distincție strictă între aceste concepte) îi era familiară lui Becquerel: atât tatăl său Alexander Edmond Becquerel (1820-1891), cât și bunicul său Antoine Cesar Becquerel (1788-1878) au fost implicați în ea - ambii fizicieni; Fiul lui Antoine Henri Becquerel, Jacques, a devenit și el fizician, care a „moștenit” catedra de fizică la Muzeul de Istorie Naturală din Paris; Becquerel a condus această catedra timp de 110 ani, din 1838 până în 1948.
Becquerel a decis să testeze dacă razele X sunt asociate cu fluorescența. Unele săruri de uraniu, de exemplu, nitratul de uranil UO2 (NO3)2, prezintă fluorescență galben-verde strălucitoare. Astfel de substanțe se aflau în laboratorul lui Becquerel, unde lucra. Tatăl său a lucrat și cu preparate cu uraniu, care a arătat că, după încetarea luminii solare, strălucirea lor dispare foarte repede - în mai puțin de o sutime de secundă. Cu toate acestea, nimeni nu a verificat dacă această strălucire este însoțită de emisia altor raze care pot trece prin materiale opace, așa cum a fost cazul Roentgen. Acesta este exact ceea ce Becquerel a decis să verifice după raportul lui Poincaré. La 24 februarie 1896, la ședința săptămânală a Academiei, a spus că a luat o placă fotografică înfășurată în două straturi de hârtie neagră groasă, a așezat pe ea cristale de uranil sulfat dublu de potasiu K 2 UO 2 (SO 4) 2 2H2O. și a expus totul timp de câteva ore la lumina soarelui, apoi după dezvoltarea plăcii fotografice puteți vedea un contur oarecum neclar al cristalelor de pe ea. Dacă o monedă sau o figură tăiată din tablă este plasată între farfurie și cristale, atunci după dezvoltare apare o imagine clară a acestor obiecte pe farfurie.
Toate acestea ar putea indica o legătură între fluorescență și radiația cu raze X. Razele X descoperite recent pot fi obținute mult mai simplu - fără raze catodice și tubul vid și tensiunea înaltă necesare pentru aceasta, dar a fost necesar să se verifice dacă se dovedește că sarea de uraniu, atunci când este încălzită la soare, eliberează unele fel de gaz care pătrunde sub hârtia neagră și acționează asupra emulsiei fotografice.Pentru a exclude această posibilitate, Becquerel a așezat o foaie de sticlă între sarea de uraniu și placa fotografică - încă lumina. „De aici”, a încheiat Becquerel scurtul său mesaj, „putem concluziona că sarea luminoasă emite raze care pătrund prin hârtia neagră, opace la lumină, și refac sărurile de argint din placa fotografică”. Ca și cum Poincaré ar avea dreptate și razele X din raze X pot fi obținute într-un mod complet diferit.
Becquerel a început să efectueze numeroase experimente pentru a înțelege mai bine condițiile în care apar razele care luminează o placă fotografică și pentru a investiga proprietățile acestor raze. El a plasat diferite substanțe între cristale și placa fotografică - hârtie, sticlă, aluminiu, cupru și plăci de plumb de diferite grosimi. Rezultatele au fost aceleași cu cele obținute de Roentgen, care ar putea servi și ca argument în favoarea asemănării ambelor radiații. Pe lângă lumina directă a soarelui, Becquerel a iluminat sarea de uraniu cu lumină reflectată dintr-o oglindă sau refractată de o prismă. El a primit că rezultatele tuturor experimentelor anterioare nu erau în niciun fel legate de soare; tot ce conta era cât de mult era sarea de uraniu lângă placa fotografică. A doua zi, Becquerel a raportat despre acest lucru la o ședință a Academiei, dar, după cum s-a dovedit mai târziu, a tras concluzia greșită: a decis că sarea de uraniu, cel puțin o dată „încărcată” în lumină, este apoi capabilă să emită raze penetrante invizibile pentru o lungă perioadă de timp.
Până la sfârșitul anului, Becquerel a publicat nouă articole pe această temă, într-unul dintre ele scria: „Într-o cutie de plumb cu pereți groși au fost așezate diferite săruri de uraniu... Ferite de acțiunea oricărei radiații cunoscute, aceste substanțe au continuat. să emită raze care trec prin sticlă și hârtie neagră..., în opt luni.”
Aceste raze proveneau din orice compus de uraniu, chiar și din cei care nu strălucesc la soare. Radiația de la uraniul metalic s-a dovedit a fi și mai puternică (de aproximativ 3,5 ori). A devenit evident că radiația, deși similară în unele manifestări cu razele X, avea o putere de penetrare mai mare și era cumva legată de uraniu, așa că Becquerel a început să-l numească „razele de uraniu”.
Becquerel a mai descoperit că „razele de uraniu” ionizează aerul, făcându-l un conductor de electricitate. Aproape simultan, în noiembrie 1896, fizicienii englezi J. J. Thomson și Ernest Rutherford (au descoperit ionizarea aerului sub influența razelor X. Pentru a măsura intensitatea radiațiilor, Becquerel a folosit un electroscop în care cele mai ușoare frunze de aur, suspendate de capetele lor si incarcate electrostatic, se resping si capetele lor libere diverg.Daca aerul conduce curent, sarcina se scurge din frunze si acestea cad - cu cat mai repede cu atat conductivitatea electrica a aerului este mai mare si, prin urmare, cu atat intensitatea radiatiei este mai mare.
A rămas întrebarea cum o substanță emite radiații continue care nu slăbesc de-a lungul multor luni fără furnizarea de energie dintr-o sursă externă.Becquerel însuși a scris că nu a putut înțelege de unde a primit uraniul energia pe care o emite în mod continuu. Au fost înaintate o varietate de ipoteze pe această temă, uneori destul de fantastice. De exemplu, chimistul și fizicianul englez William Ramsay a scris: „... fizicienii erau nedumeriți de unde putea proveni oferta inepuizabilă de energie din sărurile de uraniu. Lordul Kelvin a fost înclinat să presupună că uraniul servește ca un fel de capcană, care prinde energia radiantă nedetectabilă care ajunge la noi prin spațiu și o transformă într-o asemenea formă încât să-l facă capabil să producă efecte chimice.”
Becquerel nu putea nici să accepte această ipoteză, nici să vină cu ceva mai plauzibil, nici să abandoneze principiul conservării energiei. S-a încheiat cu el renunțând complet la lucrul cu uraniu de ceva timp și preluând divizarea liniilor spectrale într-un câmp magnetic. Acest efect a fost descoperit aproape simultan cu descoperirea lui Becquerel de către tânărul fizician olandez Pieter Zeeman și explicat de un alt olandez, Hendrik Anton Lorentz.
Aceasta a finalizat prima etapă a cercetării radioactivității. Albert Einstein a comparat descoperirea radioactivității cu descoperirea focului, deoarece el credea că atât focul, cât și radioactivitatea sunt la fel de repere majore în istoria civilizației.
1. Tipuri de radiații radioactive
Când în mâinile cercetătorilor au apărut surse puternice de radiații, de milioane de ori mai puternice decât uraniul (acestea erau preparate din radiu, poloniu, actiniu), a fost posibil să ne familiarizăm mai mult cu proprietățile radiațiilor radioactive. Ernest Rutherford, soții Maria și Pierre Curie, A. Becquerel și mulți alții au participat activ la primele studii pe această temă. În primul rând, a fost studiată capacitatea de penetrare a razelor, precum și efectul asupra radiației câmpului magnetic. S-a dovedit că radiația nu este uniformă, ci este un amestec de „raze”. Pierre Curie a descoperit că atunci când un câmp magnetic acționează asupra radiației de radiu, unele raze sunt deviate, în timp ce altele nu. Se știa că un câmp magnetic deviază doar particulele zburătoare încărcate, pozitive și negative în direcții diferite. Pe baza direcției de deviere, am fost convinși că razele β deviate erau încărcate negativ. Experimente ulterioare au arătat că nu există nicio diferență fundamentală între catod și razele β, ceea ce însemna că acestea reprezintă un flux de electroni.
Razele deviate aveau o capacitate mai puternică de a pătrunde în diverse materiale, în timp ce razele nedeviate erau absorbite cu ușurință chiar și de folia subțire de aluminiu - așa s-a comportat, de exemplu, radiația noului element poloniu - radiația sa nu a pătruns nici măcar prin carton. pereții cutiei în care a fost depozitat medicamentul.
Când folosiți magneți mai puternici, s-a dovedit că razele α sunt, de asemenea, deviate, doar mult mai slabe decât razele β și în cealaltă direcție. De aici rezultă că erau încărcate pozitiv și aveau o masă semnificativ mai mare (după cum s-a descoperit mai târziu, masa particulelor α este de 7740 de ori mai mare decât masa electronului). Acest fenomen a fost descoperit pentru prima dată în 1899 de A. Becquerel și F. Giesel. Mai târziu s-a dovedit că particulele α sunt nucleele atomilor de heliu (nuclidul 4 He) cu o sarcină de +2 și o masă de 4 unități. Când în 1900, fizicianul francez Paul Villar (1860–1934) a studiat mai detaliat abaterea razelor α- și β, el a descoperit în radiația de radiu un al treilea tip de raze care nu deviază în cele mai puternice câmpuri magnetice; această descoperire a fost în curând confirmată de Becquerel. Acest tip de radiație, prin analogie cu razele alfa și beta, a fost numită raze gamma; desemnarea diferitelor radiații cu primele litere ale alfabetului grecesc a fost propusă de Rutherford. Razele gamma s-au dovedit a fi similare cu razele X, adică. sunt radiații electromagnetice, dar cu lungimi de undă mai scurte și prin urmare mai multă energie. Toate aceste tipuri de radiații au fost descrise de M. Curie în monografia sa „Radium and Radioactivity”. În loc de un câmp magnetic, un câmp electric poate fi folosit pentru a „diviza” radiația, numai particulele încărcate din acesta nu vor fi deviate perpendicular pe liniile de forță, ci de-a lungul acestora - spre plăcile de deviere.
Multă vreme nu a fost clar de unde provin toate aceste raze. Pe parcursul mai multor decenii, prin munca multor fizicieni, natura radiațiilor radioactive și proprietățile acesteia au fost clarificate și au fost descoperite noi tipuri de radioactivitate.γ
Razele alfa sunt emise în principal de nucleele celor mai grei și deci mai puțin stabili atomi (acestea sunt localizate după plumb în tabelul periodic). Acestea sunt particule de înaltă energie. De obicei, se observă mai multe grupuri de particule α, fiecare dintre ele având o energie strict definită. Astfel, aproape toate particulele α emise din nucleele de 226 Ra au o energie de 4,78 MeV (megaelectron volți) și o mică fracțiune de particule α au o energie de 4,60 MeV. Un alt izotop de radiu, 221 Ra, emite patru grupuri de particule α cu energii de 6,76, 6,67, 6,61 și 6,59 MeV. Aceasta indică prezența mai multor niveluri de energie în nuclee; diferența lor corespunde energiei α-quantilor emise de nucleu. Sunt cunoscuți și emițători alfa „puri” (de exemplu, 222 Rn).
Conform formulei E = mu 2 /2 este posibil să se calculeze viteza particulelor α cu o anumită energie. De exemplu, particule α de 1 mol cu E= 4,78 MeV are energie (în unități SI) E= 4,78 10 6 eV 96500 J/(eV mol) = 4,61 10 11 J/mol și masă m= 0,004 kg/mol, de unde uα 15200 km/s, care este de zeci de mii de ori mai rapidă decât viteza unui glonț de pistol. Particulele alfa au cel mai puternic efect de ionizare: atunci când se ciocnesc cu orice alți atomi dintr-un gaz, lichid sau solid, ei „decapară” electronii din ei, creând particule încărcate. În acest caz, particulele α pierd energie foarte repede: sunt reținute chiar și de o coală de hârtie. În aer, radiația α din radiu parcurge doar 3,3 cm, radiația α din toriu – 2,6 cm etc. În cele din urmă, particula α, care și-a pierdut energia cinetică, captează doi electroni și se transformă într-un atom de heliu. Primul potențial de ionizare al unui atom de heliu (He – e → He +) este de 24,6 eV, al doilea (He + – e → He +2) este de 54,4 eV, ceea ce este mult mai mare decât cel al oricăror alți atomi. Când electronii sunt capturați de particulele α, se eliberează o energie enormă (mai mult de 7600 kJ/mol), astfel încât niciun atom, cu excepția atomilor de heliu însuși, nu este capabil să-și rețină electronii dacă se întâmplă că o particulă α se află în apropiere. .
Energia cinetică foarte mare a particulelor α face posibilă „vederea” acestora cu ochiul liber (sau cu ajutorul unei lupe obișnuite), acest lucru a fost demonstrat pentru prima dată în 1903 de fizicianul și chimistul englez William Crookes (1832 - 1919. A lipit de vârful acului un grăunte de sare de radiu, abia vizibil pentru ochi, și a întărit acul într-un tub larg de sticlă.La un capăt al acestui tub, nu departe de vârful acului, a fost pus. o placă acoperită cu un strat de fosfor (era sulfură de zinc), iar la celălalt capăt era o lupă.Dacă examinezi fosforul în întuneric, poți vedea: întregul câmp de viziune este punctat cu scântei intermitente și acum stingându-se. Fiecare scânteie este rezultatul impactului unei particule α. Crookes a numit acest dispozitiv spinthariscop (din grecescul spintharis - scânteie și skopeo - uitați, observați). Folosind această metodă simplă de numărare a particulelor α, un număr au fost efectuate studii, de exemplu, folosind această metodă, a fost posibil să se determine destul de precis constanta lui Avogadro.
În nucleu, protonii și neutronii sunt ținuți împreună de forțele nucleare.De aceea, nu era clar cum o particulă alfa, formată din doi protoni și doi neutroni, ar putea părăsi nucleul. Răspunsul a fost dat în 1928 de fizicianul american (care a emigrat din URSS în 1933) George (Georgi Antonovich) Gamow). Conform legilor mecanicii cuantice, particulele α, ca orice particule de masă mică, au o natură ondulatorie și, prin urmare, au o mică probabilitate de a ajunge în afara nucleului, pe un mic (aproximativ 6). · 10–12 cm) distanță de acesta. De îndată ce se întâmplă acest lucru, particula începe să experimenteze repulsia Coulomb de la un nucleu încărcat pozitiv foarte apropiat.
Este vorba în principal de nuclee grele care sunt supuse dezintegrarii alfa - mai mult de 200 dintre ele sunt cunoscute; particulele alfa sunt emise de majoritatea izotopilor elementelor care urmează bismutului. Sunt cunoscuți emițători alfa mai lumini, în principal atomi de elemente de pământuri rare. Dar de ce particulele alfa zboară din nucleu și nu protonii individuali? Calitativ, acest lucru se explică prin câștigul de energie în timpul dezintegrarii α (particulele α - nucleii de heliu sunt stabili). Teoria cantitativă a dezintegrarii α a fost creată abia în anii 1980; la dezvoltarea sa au participat și fizicieni autohtoni, inclusiv Lev Davidovich Landau, Arkady Beinusovich Migdal (1911–1991), șeful departamentului de fizică nucleară de la Universitatea Voronezh Stanislav Georgievich Kadmensky si colegii.
Ieșirea unei particule alfa din nucleu duce la nucleul altui element chimic, care este deplasat cu două celule la stânga în tabelul periodic. Un exemplu este transformarea a șapte izotopi ai poloniului (sarcină nucleară 84) în diferiți izotopi de plumb (sarcină nucleară 82): 218 Po → 214 Pb, 214 Po → 210 Pb, 210 Po → 206 Pb, 211 Po → 207 Pb, 215 Po → 211 Pb, 212 Po → 208 Pb, 216 Po → 212 Pb. Izotopii de plumb 206 Pb, 207 Pb și 208 Pb sunt stabili, restul sunt radioactivi.
Dezintegrarea beta apare atât în nucleele grele, cât și în cele ușoare, cum ar fi tritiul. Aceste particule de lumină (electroni rapizi) au o putere de penetrare mai mare. Astfel, în aer, particulele β pot zbura câteva zeci de centimetri, în substanțe lichide și solide - de la fracțiuni de milimetru până la aproximativ 1 cm. Spre deosebire de particulele α, spectrul energetic al razelor β nu este discret. Energia electronilor care scapă din nucleu poate varia de la aproape zero până la o anumită valoare maximă caracteristică unui radionuclid dat. De obicei, energia medie a particulelor β este mult mai mică decât cea a particulelor α; de exemplu, energia radiației β de la 228 Ra este de 0,04 MeV. Dar există și excepții; deci radiația β a nuclidului de scurtă durată 11 Be poartă o energie de 11,5 MeV. Multă vreme nu a fost clar cum particulele zboară din atomi identici ai aceluiași element la viteze diferite. Când structura atomului și nucleul atomic au devenit clare, a apărut un nou mister: de unde provin particulele β care scapă din nucleu - la urma urmei, nu există electroni în nucleu. După ce fizicianul englez James Chadwick a descoperit neutronul în 1932, fizicienii ruși Dmitry Dmitrievich Ivanenko (1904–1994) și Igor Evgenievich Tamm și, în mod independent, fizicianul german Werner Heisenberg au sugerat că nucleele atomice constau din protoni și neutroni. În acest caz, particulele β ar trebui să se formeze ca rezultat al procesului intranuclear de conversie a unui neutron într-un proton și un electron: n → p + e. Masa unui neutron este puțin mai mare decât masa combinată a unui proton și a unui electron, un exces de masă, în conformitate cu formula lui Einstein E = mc 2, oferă energia cinetică a unui electron care iese din nucleu, prin urmare dezintegrarea β este observată în principal în nucleele cu un număr în exces de neutroni. De exemplu, nuclidul 226 Ra este un emițător α, iar toți izotopii mai grei ai radiului (227 Ra, 228 Ra, 229 Ra și 230 Ra) sunt emițători β.
A rămas de aflat de ce particulele β, spre deosebire de particulele α, au un spectru energetic continuu, ceea ce însemna că unele dintre ele au energie foarte scăzută, în timp ce altele au energie foarte mare (și în același timp se mișcă cu o viteză apropiată de viteza luminii). Mai mult, energia totală a tuturor acestor electroni (a fost măsurată cu ajutorul unui calorimetru) s-a dovedit a fi mai mică decât diferența de energie a nucleului original și produsul dezintegrarii acestuia. Din nou, fizicienii s-au confruntat cu o „încălcare” a legii conservării energiei: o parte din energia nucleului original a dispărut într-o locație necunoscută. Legea fizică de nezdruncinat a fost „salvată” în 1931 de către fizicianul elvețian Wolfgang Pauli, care a sugerat că, în timpul dezintegrarii β, două particule zboară din nucleu: un electron și o particulă neutră ipotetică - un neutrin cu masă aproape zero, care transportă. exces de energie. Spectrul continuu al radiației β se explică prin distribuția energiei între electroni și această particulă. Neutrinii (după cum s-a dovedit mai târziu, așa-numitul antineutrin electronic se formează în timpul dezintegrarii beta) interacționează foarte slab cu materia (de exemplu, străpung cu ușurință diametrul globului și chiar o stea uriașă) și, prin urmare, nu au fost detectați pentru o perioadă de timp. mult timp - neutrinii liberi experimental au fost înregistrați abia în 1956 Astfel, schema de dezintegrare beta rafinată este următoarea: n → p +. Teoria cantitativă a dezintegrarii β, bazată pe ideile lui Pauli despre neutrini, a fost dezvoltată în 1933 de către fizicianul italian Enrico Fermi, care a propus și numele neutrin (în italiană „neutron”).
Transformarea unui neutron într-un proton în timpul dezintegrarii beta practic nu modifică masa nuclidului, ci crește sarcina nucleului cu unul. În consecință, se formează un nou element, deplasat cu o celulă la dreapta în tabelul periodic, de exemplu: →, →, → etc. (un electron și un antineutrin zboară din nucleu în același timp).
2. Alte tipuri de radioactivitate
Pe lângă descompunerea alfa și beta, sunt cunoscute și alte tipuri de transformări radioactive spontane. În 1938, fizicianul american Louis Walter Alvarez a descoperit un al treilea tip de transformare radioactivă - captarea electronilor (E-capture). În acest caz, nucleul captează un electron din învelișul energetic cel mai apropiat de acesta (K-shell). Când un electron interacționează cu un proton, se formează un neutron, iar un neutrin zboară din nucleu, ducând excesul de energie. Transformarea unui proton într-un neutron nu modifică masa nuclidului, ci reduce sarcina nucleului cu unul. În consecință, se formează un nou element, situat cu o celulă la stânga în tabelul periodic, de exemplu, se obține un nuclid stabil (în acest exemplu Alvarez a descoperit acest tip de radioactivitate).
În timpul captării K în învelișul de electroni a unui atom, un electron de la un nivel de energie superior „coboară” la locul electronului dispărut, excesul de energie fie este eliberat sub formă de raze X, fie este cheltuit la plecarea de la atomul unuia sau mai multor electroni legați mai slab - așa-numiții electroni Auger, numiti după fizicianul francez Pierre Auger (1899–1993), care a descoperit acest efect în 1923 (a folosit radiațiile ionizante pentru a elimina electronii interni).
În 1940, Georgy Nikolaevich Flerov (1913–1990) și Konstantin Antonovich Petrzhak (1907–1998), folosind exemplul uraniului, au descoperit fisiunea spontană, în care un nucleu instabil se descompune în două nuclee mai ușoare, ale căror mase nu diferă foarte mult. mult, de exemplu: → + + 2n. Acest tip de degradare se observă numai în uraniu și elemente mai grele - peste 50 de nuclizi în total. În cazul uraniului, fisiunea spontană are loc foarte lent: durata medie de viață a unui atom de 238 U este de 6,5 miliarde de ani. În 1938, fizicianul și chimistul german Otto Hahn, radiochimistul și fizicianul austriac Lise Meitner (elementul Mt - meitnerium poartă numele ei) și fizicianul german Fritz Strassmann (1902–1980) au descoperit că atunci când sunt bombardate de neutroni, nucleele de uraniu sunt împărțite în fragmente, iar cele emise de neutroni pot provoca fisiunea nucleelor de uraniu învecinate, ceea ce duce la o reacție în lanț). Acest proces este însoțit de eliberarea de energie enormă (în comparație cu reacțiile chimice), care a dus la crearea de arme nucleare și la construirea de centrale nucleare.
În 1934, fiica lui Marie Curie Irène Joliot-Curie și soțul ei Frédéric Joliot-Curie au descoperit degradarea pozitronilor. În acest proces, unul dintre protonii nucleului se transformă într-un neutron și un antielectron (pozitron) - o particulă cu aceeași masă, dar încărcată pozitiv; simultan, un neutrin zboară din nucleu: p → n + e + + 238. Masa nucleului nu se modifică, dar are loc o deplasare, spre deosebire de β – dezintegrare, spre stânga, dezintegrarea β+ este caracteristică nucleelor cu un exces de protoni (așa-numitele nuclee cu deficit de neutroni). Astfel, izotopii grei ai oxigenului 19 O, 20 O și 21 O β - sunt activi, iar izotopii săi ușori 14 O și 15 O β + sunt activi, de exemplu: 14 O → 14 N + e + + 238. Ca și antiparticulele , pozitronii sunt imediat distruși (anihilati) atunci când întâlnesc electroni cu formarea a două cuante γ. Dezintegrarea pozitronilor concurează adesea cu captarea K.
În 1982, a fost descoperită radioactivitatea protonilor: emisia unui proton de către un nucleu (acest lucru este posibil doar pentru unele nuclee produse artificial cu exces de energie). În 1960, fizicianul Vitali Iosifovich Goldansky (1923–2001) a prezis teoretic radioactivitatea cu doi protoni: ejecția a doi protoni cu spini perechi dintr-un nucleu. A fost observată pentru prima dată în 1970. Radioactivitatea cu doi neutroni este, de asemenea, observată foarte rar (descoperită în 1979).
În 1984, a fost descoperită radioactivitatea clusterului (din clusterul englezesc - ciorchine, roi). În acest caz, spre deosebire de fisiunea spontană, nucleul se descompune în fragmente cu mase foarte diferite, de exemplu, nucleele cu mase de la 14 la 34 zboară dintr-un nucleu greu. Dezintegrarea clusterului este, de asemenea, observată foarte rar, ceea ce a făcut-o. greu de detectat pentru o lungă perioadă de timp.
Unele nuclee sunt capabile să se descompună în direcții diferite. De exemplu, 221 Rn se descompune 80% cu emisia de particule α și 20% cu particule β; mulți izotopi ai elementelor pământurilor rare (137 Pr, 141 Nd, 141 Pm, 142 Sm etc.) se descompun fie prin captarea electronilor. sau cu emisie de pozitroni. Diverse tipuri de radiații radioactive sunt adesea (dar nu întotdeauna) însoțite de radiații γ. Acest lucru se întâmplă deoarece nucleul rezultat poate avea exces de energie, din care este eliberat prin emiterea de raze gamma. Energia radiației γ se află într-un interval larg, de exemplu, în timpul dezintegrarii de 226 Ra este egală cu 0,186 MeV, iar în timpul dezintegrarii de 11 Be ajunge la 8 MeV.
Aproape 90% din cele 2500 de nuclee atomice cunoscute sunt instabile. Un nucleu instabil se transformă spontan în alte nuclee, emițând particule. Această proprietate a nucleelor se numește radioactivitate. În nucleele mari, instabilitatea apare din cauza competiției dintre atracția nucleonilor de către forțele nucleare și respingerea coulombiană a protonilor. Nu există nuclee stabile cu un număr de sarcină Z > 83 și un număr de masă A > 209. Dar nucleele atomice cu valori semnificativ mai mici ale numerelor Z și A pot fi, de asemenea, radioactive. Dacă nucleul conține mult mai mulți protoni decât neutroni, atunci instabilitatea este cauzată de un exces de energie de interacțiune Coulomb . Nucleele care ar conține un exces mare de neutroni față de numărul de protoni se dovedesc a fi instabile datorită faptului că masa neutronului depășește masa protonului. O creștere a masei nucleului duce la o creștere a energiei acestuia.
Fenomenul de radioactivitate a fost descoperit în 1896 de către fizicianul francez A. Becquerel, care a descoperit că sărurile de uraniu emit radiații necunoscute care pot pătrunde în barierele opace la lumină și pot provoca înnegrirea emulsiei fotografice. Doi ani mai târziu, fizicienii francezi M. și P. Curie au descoperit radioactivitatea toriului și au descoperit două noi elemente radioactive - poloniul și radiul.
În anii următori, mulți fizicieni, inclusiv E. Rutherford și studenții săi, au studiat natura radiațiilor radioactive. S-a constatat că nucleele radioactive pot emite particule de trei tipuri: încărcate pozitiv și negativ și neutre. Aceste trei tipuri de radiații au fost numite radiații α-, β- și γ. Aceste trei tipuri de radiații radioactive diferă foarte mult unele de altele prin capacitatea lor de a ioniza atomii de materie și, prin urmare, prin capacitatea lor de penetrare. Radiația α are cea mai mică capacitate de penetrare. În aer, în condiții normale, razele α parcurg o distanță de câțiva centimetri. Razele β sunt mult mai puțin absorbite de materie. Ele sunt capabile să treacă printr-un strat de aluminiu gros de câțiva milimetri. razele γ au cea mai mare capacitate de penetrare, capabile să treacă printr-un strat de plumb de 5–10 cm grosime.
În al doilea deceniu al secolului XX, după descoperirea lui E. Rutherford a structurii nucleare a atomilor, s-a stabilit ferm că radioactivitatea este o proprietate a nucleelor atomice. Cercetările au arătat că razele α reprezintă un flux de particule α - nuclee de heliu, razele β sunt un flux de electroni, razele γ sunt radiații electromagnetice de undă scurtă cu o lungime de undă extrem de scurtă λ< 10 –10 м и вследствие этого – ярко выраженными корпускулярными свойствами, т.е. является потоком частиц – γ-квантов.
3. Dezintegrarea alfa
Dezintegrarea alfa este transformarea spontană a unui nucleu atomic cu numărul de protoni Z și neutroni N într-un alt nucleu (fiică) care conține numărul de protoni Z – 2 și neutroni N – 2. În acest caz, este emisă o particulă α - nucleul unui atom de heliu. Un exemplu de astfel de proces este dezintegrarea α a radiului: ![]() Particulele alfa emise de nucleele atomilor de radiu au fost folosite de Rutherford în experimente privind împrăștierea de către nucleele elementelor grele. Viteza particulelor α emise în timpul dezintegrarii α a nucleelor de radiu, măsurată din curbura traiectoriei într-un câmp magnetic, este de aproximativ 1,5 10 7 m/s, iar energia cinetică corespunzătoare este de aproximativ 7,5 10 –13 J ( aproximativ 4. 8 MeV). Această valoare poate fi determinată cu ușurință din valorile cunoscute ale maselor nucleelor mamei și fiice și ale nucleului de heliu. Deși viteza particulei α care scapă este enormă, este totuși doar 5% din viteza luminii, așa că atunci când calculezi, poți folosi o expresie non-relatistică pentru energia cinetică. Cercetările au arătat că o substanță radioactivă poate emite particule alfa cu mai multe energii discrete. Acest lucru se explică prin faptul că nucleele pot fi, ca și atomii, în diferite stări excitate. Nucleul fiică poate ajunge într-una dintre aceste stări excitate în timpul dezintegrarii α.
Particulele alfa emise de nucleele atomilor de radiu au fost folosite de Rutherford în experimente privind împrăștierea de către nucleele elementelor grele. Viteza particulelor α emise în timpul dezintegrarii α a nucleelor de radiu, măsurată din curbura traiectoriei într-un câmp magnetic, este de aproximativ 1,5 10 7 m/s, iar energia cinetică corespunzătoare este de aproximativ 7,5 10 –13 J ( aproximativ 4. 8 MeV). Această valoare poate fi determinată cu ușurință din valorile cunoscute ale maselor nucleelor mamei și fiice și ale nucleului de heliu. Deși viteza particulei α care scapă este enormă, este totuși doar 5% din viteza luminii, așa că atunci când calculezi, poți folosi o expresie non-relatistică pentru energia cinetică. Cercetările au arătat că o substanță radioactivă poate emite particule alfa cu mai multe energii discrete. Acest lucru se explică prin faptul că nucleele pot fi, ca și atomii, în diferite stări excitate. Nucleul fiică poate ajunge într-una dintre aceste stări excitate în timpul dezintegrarii α.
În timpul tranziției ulterioare a acestui nucleu la starea fundamentală, este emis un γ-cuantic. O diagramă a dezintegrarii α a radiului cu emisia de particule α cu două valori ale energiilor cinetice este prezentată în Fig. 2. Astfel, dezintegrarea α a nucleelor este în multe cazuri însoțită de radiații y.
În teoria dezintegrarii α, se presupune că în interiorul nucleelor se pot forma grupuri formate din doi protoni și doi neutroni, adică. particulă α. Nucleul mamă este un put de potențial pentru particulele α, care este limitat de o barieră potențială. Energia particulei α din nucleu nu este suficientă pentru a depăși această barieră (Fig. 3). Scăparea unei particule alfa din nucleu este posibilă numai datorită unui fenomen mecanic cuantic numit efect de tunel. Conform mecanicii cuantice, există o probabilitate diferită de zero ca o particulă să treacă sub o barieră de potențial. Fenomenul tunelului este de natură probabilistică.
4. Dezintegrarea beta
În timpul dezintegrarii beta, un electron este ejectat din nucleu. Electronii nu pot exista în interiorul nucleelor; ei apar în timpul dezintegrarii beta ca urmare a transformării unui neutron într-un proton. Acest proces poate avea loc nu numai în interiorul nucleului, ci și cu neutroni liberi. Durata medie de viață a unui neutron liber este de aproximativ 15 minute. În timpul dezintegrarii, un neutron se transformă într-un proton și un electron
Măsurătorile au arătat că în acest proces există o încălcare aparentă a legii conservării energiei, deoarece energia totală a protonului și electronului rezultată din dezintegrarea unui neutron este mai mică decât energia neutronului. În 1931, W. Pauli a sugerat că în timpul dezintegrarii unui neutron este eliberată o altă particulă cu masă și sarcină zero, care ia o parte din energie. Noua particulă se numește neutrin (neutron mic). Din cauza lipsei de sarcină și a masei unui neutrin, această particulă interacționează foarte slab cu atomii materiei, deci este extrem de dificil de detectat în experiment. Capacitatea de ionizare a neutrinilor este atât de mică încât un eveniment de ionizare în aer are loc la aproximativ 500 km de parcurs. Această particulă a fost descoperită abia în 1953. Acum se știe că există mai multe tipuri de neutrini. În timpul dezintegrarii unui neutron, este creată o particulă, care se numește antineutron electronic. Este indicat prin simbol. Prin urmare, reacția de dezintegrare a neutronilor este scrisă sub formă
Un proces similar are loc în interiorul nucleelor în timpul dezintegrarii β. Un electron format ca urmare a dezintegrarii unuia dintre neutronii nucleari este imediat ejectat din „casa părintească” (nucleu) cu o viteză enormă, care poate diferi de viteza luminii doar cu o fracțiune de procent. Deoarece distribuția energiei eliberate în timpul dezintegrarii β între electron, neutrin și nucleul fiu este aleatorie, electronii β pot avea viteze diferite pe o gamă largă.
În timpul dezintegrarii β, numărul de sarcină Z crește cu unu, dar numărul de masă A rămâne neschimbat. Nucleul fiică se dovedește a fi nucleul unuia dintre izotopii elementului, al cărui număr de serie în tabelul periodic este cu unul mai mare decât numărul de serie al nucleului original. Un exemplu tipic de degradare β este transformarea izotonei de toriu rezultată din descompunerea α a uraniului în paladiu
5. Dezintegrarea gamma
Spre deosebire de α- și β-radioactivitate, γ-radioactivitatea nucleelor nu este asociată cu o modificare a structurii interne a nucleului și nu este însoțită de o modificare a sarcinii sau a numerelor de masă. Atât în timpul dezintegrarii α- cât și β, nucleul fiică se poate găsi într-o stare excitată și are un exces de energie. Tranziția unui nucleu de la o stare excitată la o stare fundamentală este însoțită de emisia uneia sau mai multor cuante γ, a căror energie poate atinge câțiva MeV.
6. Legea dezintegrarii radioactive
Orice probă de substanță radioactivă conține un număr mare de atomi radioactivi. Deoarece degradarea radioactivă este de natură aleatorie și nu depinde de condițiile externe, legea scăderii numărului N(t) de nuclee care nu s-au degradat într-un timp dat t poate servi ca o caracteristică statistică importantă a procesului de dezintegrare radioactivă.
Fie ca numărul de nuclee nedegradate N(t) să se modifice cu ΔN într-o perioadă scurtă de timp Δt< 0. Так как вероятность распада каждого ядра неизменна во времени, что число распадов будет пропорционально количеству ядер N(t) и промежутку времени Δt:
Coeficientul de proporționalitate λ este probabilitatea dezintegrarii nucleare în timp Δt = 1 s. Această formulă înseamnă că rata de schimbare a funcției N(t) este direct proporțională cu funcția în sine.
unde N 0 este numărul inițial de nuclee radioactive la t = 0. În timpul τ = 1 / λ, numărul de nuclee nedezintegrate va scădea de e ≈ de 2,7 ori. Valoarea τ se numește durata medie de viață a unui nucleu radioactiv.
Pentru utilizare practică, este convenabil să scrieți legea dezintegrarii radioactive într-o formă diferită, folosind numărul 2 mai degrabă decât e ca bază:
Valoarea T se numește timp de înjumătățire. În timpul T, jumătate din numărul inițial de nuclee radioactive se descompune. Mărimile T și τ sunt legate prin relație
Timpul de înjumătățire este principala mărime care caracterizează rata dezintegrarii radioactive. Cu cât timpul de înjumătățire este mai scurt, cu atât degradarea este mai intensă. Deci, pentru uraniu T ≈ 4,5 miliarde de ani, iar pentru radiu T ≈ 1600 de ani. Prin urmare, activitatea radiului este mult mai mare decât cea a uraniului. Există elemente radioactive cu timpi de înjumătățire de o fracțiune de secundă.
În timpul descompunerii radioactive α și β, nucleul fiică poate deveni, de asemenea, instabil. Prin urmare, sunt posibile o serie de dezintegrari radioactive succesive, care se termină cu formarea de nuclee stabile. Există mai multe astfel de serii în natură. Cea mai lungă este o serie formată din 14 dezintegrari consecutive (8 dezintegrari alfa și 6 dezintegrari beta). Această serie se încheie cu un izotop stabil de plumb (Fig. 5).
În natură, există mai multe serii radioactive similare cu seria. Se cunoaste si o serie care incepe cu neptuniu, care nu se gaseste in conditii naturale, si se termina cu bismut. Această serie de dezintegrari radioactive are loc în reactoarele nucleare.
Regula de compensare. Regula deplasării specifică exact ce transformări suferă un element chimic atunci când emite radiații radioactive.
7. Serii radioactive
Regula deplasării a făcut posibilă urmărirea transformărilor elementelor radioactive naturale și construirea din ele a trei arbori genealogic, ai căror strămoși sunt uraniu-238, uraniu-235 și toriu-232. Fiecare familie începe cu un element radioactiv extrem de longeviv. Familia uraniului, de exemplu, este condusă de uraniu cu un număr de masă de 238 și un timp de înjumătățire de 4,5·10 9 ani (în Tabelul 1, în conformitate cu numele original, desemnat uraniu I).
| Tabelul 1. Familia radioactivă a uraniului | |||||
| Element radioactiv | Z | Element chimic | A | Tipul de radiație |
Jumătate de viață |
| Uranus I | 92 | Uranus | 238 | | 4,510 9 ani |
| Uraniu X 1 | 90 | Toriu | 234 | | 24,1 zile |
| Uraniu X 2 Uraniu Z |
Protactiniu Protactiniu |
–
(99,88%) (0,12%) |
|||
| Uranus II | 92 | Uranus | 234 | | 2,510 5 ani |
| ioniu | 90 | Toriu | 230 | | 810 4 ani |
| Radiu | 88 | Radiu | 226 | | 1620 de ani |
| Radon | 86 | Radon | 222 | | 3,8 zile |
| Radioul A | 84 | Poloniu | 218 | | 3,05 min |
| Radiul B | 82 | Conduce | 214 | | 26,8 min |
| 83 83 |
Bismut Bismut |
214 214 |
(99,96%) (0,04%) |
||
| Radiu C | 84 | Poloniu | 214 | | 1,610 –4 s |
| Radiu C | 81 | Taliu | 210 | | 1,3 min |
| radiu D | 82 | Conduce | 210 | | 25 de ani |
| Radiu E | 83 | Bismut | 210 | | 4,85 zile |
| Radio F | 84 | Poloniu | 210 | | 138 de zile |
| Radio G | 82 | Conduce | 206 | Grajd | |
Familia uraniului. Majoritatea proprietăților transformărilor radioactive discutate mai sus pot fi urmărite la elementele familiei uraniului. De exemplu, al treilea membru al familiei prezintă izomerie nucleară. Uraniul X 2, care emite particule beta, se transformă în uraniu II (T = 1,14 min). Aceasta corespunde dezintegrarii beta a stării excitate a protactiniului-234. Cu toate acestea, în 0,12% din cazuri, protactiniul-234 excitat (uraniu X 2) emite un quantum gamma și trece la starea fundamentală (uraniu Z). Dezintegrarea beta a uraniului Z, care duce și la formarea uraniului II, are loc în 6,7 ore.
Radiul C este interesant deoarece se poate degrada în două moduri: emițând fie o particulă alfa, fie o particulă beta. Aceste procese concurează între ele, dar în 99,96% din cazuri dezintegrarea beta are loc odată cu formarea de radiu C. În 0,04% din cazuri, radiul C emite o particulă alfa și se transformă în radiu C (RaC). La rândul lor, RaC și RaC sunt convertite în radiu D prin emisia de particule alfa și, respectiv, beta.
Izotopi. Printre membrii familiei uraniului se numără cei ai căror atomi au același număr atomic (aceeași sarcină nucleară) și numere de masă diferite. Ele sunt identice ca proprietăți chimice, dar diferă prin natura radioactivității. De exemplu, radiul B, radiul D și radiul G, care au același număr atomic 82 ca și plumbul, sunt similare cu plumbul în comportament chimic. Este evident că proprietățile chimice nu depind de numărul de masă; ele sunt determinate de structura învelișurilor de electroni ale atomului (deci, Z). Pe de altă parte, numărul de masă este critic pentru stabilitatea nucleară a proprietăților radioactive ale unui atom. Atomii cu același număr atomic și numere de masă diferite se numesc izotopi. Izotopii elementelor radioactive au fost descoperiți de F. Soddy în 1913, dar în curând F. Aston, folosind spectroscopie de masă, a demonstrat că multe elemente stabile au și izotopi.
8. Efectul radiațiilor radioactive asupra oamenilor
Radiațiile radioactive de toate tipurile (alfa, beta, gamma, neutroni), precum și radiațiile electromagnetice (razele X) au un efect biologic foarte puternic asupra organismelor vii, care constă în procesele de excitare și ionizare a atomilor și moleculelor care fac sus celulele vii. Sub influența radiațiilor ionizante, moleculele complexe și structurile celulare sunt distruse, ceea ce duce la deteriorarea organismului prin radiații. Prin urmare, atunci când lucrați cu orice sursă de radiații, este necesar să luați toate măsurile pentru a proteja persoanele care pot fi expuse la radiații.
Cu toate acestea, o persoană poate fi expusă la radiații ionizante acasă. Gazul inert, incolor, radioactiv, radonul poate reprezenta un pericol grav pentru sănătatea umană.Așa cum se poate observa din diagrama prezentată în Fig. 5, radonul este un produs al dezintegrarii α a radiului și are un timp de înjumătățire T = 3,82 zile. Radiul se găsește în cantități mici în sol, pietre și diferite structuri de construcție. În ciuda duratei de viață relativ scurte, concentrația de radon este reîncărcată în mod continuu datorită noilor degradari ale nucleelor de radiu, astfel încât radonul se poate acumula în spații închise. Odată ajuns în plămâni, radonul emite particule α și se transformă în poloniu, care nu este o substanță inertă din punct de vedere chimic. Urmează un lanț de transformări radioactive ale seriei uraniului (Fig. 5). Potrivit Comisiei Americane pentru Siguranța și Controlul Radiațiilor, o persoană obișnuită primește 55% din radiațiile ionizante din radon și doar 11% din îngrijirea medicală. Contribuția razelor cosmice este de aproximativ 8%. Doza totală de radiații pe care o persoană o primește în timpul vieții este de multe ori mai mică decât doza maximă admisă (MAD), care este stabilită pentru persoanele din anumite profesii care sunt supuse expunerii suplimentare la radiații ionizante.
9. Aplicarea izotopilor radioactivi
Unul dintre cele mai remarcabile studii efectuate folosind „atomi marcați” a fost studiul metabolismului în organisme. S-a dovedit că într-un timp relativ scurt organismul suferă o reînnoire aproape completă. Atomii care o alcătuiesc sunt înlocuiți cu alții noi. Doar fierul, așa cum au arătat experimentele cu studiile izotopice ale sângelui, este o excepție de la această regulă. Fierul face parte din hemoglobina celulelor roșii din sânge. Când atomii de fier radioactiv au fost introduși în alimente, sa constatat că oxigenul liber eliberat în timpul fotosintezei a fost inițial parte din apă, nu dioxid de carbon. Izotopii radioactivi sunt utilizați în medicină atât pentru diagnostic, cât și în scop terapeutic. Sodiul radioactiv, injectat în cantități mici în sânge, este folosit pentru a studia circulația sângelui; iodul este depus intens în glanda tiroidă, în special în boala Graves. Prin observarea depunerilor de iod radioactiv cu ajutorul unui contor, se poate face un diagnostic rapid. Dozele mari de iod radioactiv provoacă distrugerea parțială a țesuturilor cu dezvoltare anormală și, prin urmare, iodul radioactiv este utilizat pentru a trata boala Graves. Radiația gamma intensă de cobalt este utilizată în tratamentul cancerului (pistol cu cobalt).
Nu mai puțin extinse sunt aplicațiile izotopilor radioactivi în industrie. Un exemplu în acest sens este următoarea metodă de monitorizare a uzurii segmentului pistonului la motoarele cu ardere internă. Prin iradierea segmentului pistonului cu neutroni, aceștia provoacă reacții nucleare în el și îl fac radioactiv. Când motorul funcționează, particulele de material inelului intră în uleiul de lubrifiere. Prin examinarea nivelului de radioactivitate din ulei după un anumit timp de funcționare a motorului, se determină uzura inelului. Izotopii radioactivi fac posibilă aprecierea difuziei metalelor, proceselor în furnalele înalte etc.
Radiația gamma puternică de la medicamentele radioactive este utilizată pentru a examina structura internă a pieselor turnate metalice pentru a detecta defectele acestora.
Izotopii radioactivi sunt din ce în ce mai folosiți în agricultură. Iradierea semințelor de plante (bumbac, varză, ridichi etc.) cu doze mici de raze gamma de la medicamentele radioactive duce la o creștere vizibilă a randamentului. Dozele mari de radiații provoacă mutații la plante și microorganisme, ceea ce duce în unele cazuri la apariția unor mutanți cu noi proprietăți valoroase (selecție radio).Așa s-au dezvoltat soiuri valoroase de grâu, fasole și alte culturi și s-au folosit microorganisme foarte productive. în producția de antibiotice s-au obținut. Radiația gamma de la izotopii radioactivi este folosită și pentru combaterea insectelor dăunătoare și pentru conservarea alimentelor. „Atomii marcați” sunt utilizați pe scară largă în tehnologia agricolă. De exemplu, pentru a afla ce îngrășământ cu fosfor este mai bine absorbit de către plante, diferite îngrășăminte sunt etichetate cu fosfor radioactiv 15 32P. Cercetare Apoi plantele sunt testate pentru radioactivitate și se poate determina cantitatea de fosfor pe care au absorbit-o din diferite tipuri de îngrășăminte.
O aplicație interesantă a radioactivității este metoda de datare a descoperirilor arheologice și geologice prin concentrația de izotopi radioactivi. Cea mai des folosită metodă de datare este datarea cu radiocarbon. Un izotop instabil al carbonului apare în atmosferă din cauza reacțiilor nucleare cauzate de razele cosmice. Un mic procent din acest izotop se găsește în aer împreună cu izotopul stabil obișnuit.Plantele și alte organisme preiau carbonul din aer, iar ambii izotopi se acumulează în ei în aceeași proporție ca și în aer. După ce plantele mor, ele nu mai consumă carbon și izotopul instabil se transformă treptat în azot ca urmare a descompunerii β cu un timp de înjumătățire de 5730 de ani. Măsurând cu precizie concentrația relativă de carbon radioactiv din rămășițele organismelor antice, se poate determina momentul morții lor.
Lista literaturii folosite
1. Doctrina radioactivității. Istorie și modernitate. M. Nauka, 1973 2. Radiația nucleară în știință și tehnologie. M. Nauka, 1984 Furman V.I. 3. Dezintegrarea alfa și reacțiile nucleare aferente. M. Nauka, 1985
4. Landsberg G.S. Manual elementar de fizică. Volumul III. – M.: Nauka, 19865. Seleznev Yu. A. Fundamentele fizicii elementare. –M.: Nauka, 1964.6. CD-ROM „Marea Enciclopedie a lui Chiril și Metodiu”, 1997.
7. Curie M., Radioactivitate, trad. din franceză, ed. a II-a, M. - L., 1960
8. Murin A.N., Introducere în radioactivitate, Leningrad, 1955
9. Davydov A.S., Teoria nucleului atomic, M., 1958
10. Gaisinsky M.N., Chimia nucleară și aplicațiile sale, trad. din franceză, M., 1961
11. Fizica nucleară experimentală, ed. E. Segre, trad. din engleză, vol. 3, M., 1961; Instrumente INTERNET
Slide 2
În biologie și medicină - în industrie - în agricultură - în arhiologie
Slide 3
Izotopi în medicină și biologie
Slide 4
Tabelul 1. Principalele caracteristici ale radionuclizilor - emițători γ pentru utilizare în scopuri de diagnostic
Slide 5
Slide 6
Co60 este utilizat pentru tratarea tumorilor maligne localizate atât la suprafața corpului, cât și în interiorul corpului. Pentru a trata tumorile localizate superficial (de exemplu, cancerul de piele), cobaltul este utilizat sub formă de tuburi care sunt aplicate pe tumoră sau sub formă de ace care sunt injectate în aceasta. Tuburile și acele care conțin radiocobalt sunt menținute în această poziție până când tumora este distrusă. În acest caz, țesutul sănătos din jurul tumorii nu ar trebui să sufere prea mult. Dacă tumora este localizată adânc în organism (cancer de stomac sau pulmonar), se folosesc dispozitive speciale γ care conțin cobalt radioactiv. Această instalație creează un fascicul îngust, foarte puternic de raze γ, care este îndreptat către locul unde se află tumora. Radiațiile nu provoacă nicio durere, pacienții nu o simt.
Slide 7
Cameră radiografică digitală pentru dispozitive fluorografice KRTS 01-"PONI"
Slide 8
Mamograful este un sistem modern de mamografie, cu o doză mică de radiații și rezoluție mare, care oferă imagini de înaltă calitate ale sânului necesare pentru un diagnostic precis.
Slide 9
Dispozitivul fluorografic digital FC-01 „Electron” este destinat efectuării de examinări cu raze X preventive în masă ale populației pentru a detecta în timp util tuberculoza, cancerul și alte boli pulmonare cu expunere scăzută la radiații.
Slide 10
tomograf computerizat Tomografia computerizată este o metodă de examinare cu raze X strat cu strat a organelor și țesuturilor. Se bazează pe procesarea computerizată a mai multor imagini cu raze X ale stratului transversal luate în unghiuri diferite.
Slide 11
Brahiterapia nu este o operație radicală, ci aproape ambulatorie, în timpul căreia injectăm în organul afectat boabe de titan care conțin un izotop. Acest nuclid radioactiv ucide tumora până la moarte. În Rusia, până acum doar patru clinici efectuează o astfel de operație, dintre care două sunt la Moscova, Obninsk și Ekaterinburg, deși țara are nevoie de 300-400 de centre unde se folosește brahiterapie.
Slide 12
Izotopi în industrie
Slide 13
Controlul uzurii segmentelor de piston la motoarele cu ardere internă. Prin iradierea segmentului pistonului cu neutroni, aceștia provoacă reacții nucleare în el și îl fac radioactiv. Când motorul funcționează, particulele de material inelului intră în uleiul de lubrifiere. Prin examinarea nivelului de radioactivitate din ulei după un anumit timp de funcționare a motorului, se determină uzura inelului.
Slide 14
Radiația Y puternică a medicamentelor este utilizată pentru a studia structura internă a turnărilor metalice pentru a detecta defectele acestora.
Slide 15
Materialele radioactive fac posibilă aprecierea difuzării materialelor, proceselor în furnalele înalte etc.
Slide 16
Izotopi în agricultură
Slide 17
Iradierea semințelor de plante (bumbac, varză, ridichi etc.) cu doze mici de raze y de la medicamentele radioactive duce la o creștere vizibilă a randamentului.
Slide 18
Dozele mari de radiații provoacă mutații la plante și microorganisme, ceea ce duce în unele cazuri la apariția unor mutanți cu noi proprietăți valoroase (selecție radio). Așa s-au dezvoltat soiuri valoroase de grâu, fasole și alte culturi. Așa s-au dezvoltat soiuri valoroase de grâu, fasole și alte culturi și s-au obținut microorganisme extrem de productive utilizate în producția de antibiotice.
Slide 19
Radiația gamma de la izotopii radioactivi este, de asemenea, utilizată pentru a controla insectele dăunătoare și pentru conservarea alimentelor.
Slide 20
Izotopi în arhiologie
Slide 21
Metoda carbonului radioactiv a primit o aplicație interesantă pentru determinarea vârstei obiectelor antice de origine organică (lemn, cărbune, țesături etc.). Plantele conțin întotdeauna izotopul de carbon radioactiv B 166C cu un timp de înjumătățire de T=5700 de ani. Se formează în atmosfera Pământului în cantități mici din azot sub influența neutronilor. Acestea din urmă apar din cauza reacțiilor nucleare cauzate de particulele rapide care intră în atmosferă din spațiu (razele cosmice). Combinându-se cu oxigenul, acest carbon formează dioxid de carbon, care este absorbit de plante și, prin intermediul acestora, de animale. Un gram de carbon din probele tinere de pădure emite aproximativ cincisprezece particule B pe secundă.
Slide 22
După moartea organismului, reaprovizionarea acestuia cu carbon radioactiv încetează. Cantitatea disponibilă din acest izotop scade din cauza radioactivității. Prin determinarea procentului de carbon radioactiv din resturile organice, este posibil să se determine vârsta acestora dacă acesta se află în intervalul de la 1000 la 50.000 și chiar până la 100.000 de ani. În acest fel, se cunoaște epoca mumiilor egiptene, a rămășițelor incendiilor preistorice etc.
Vizualizați toate diapozitivele
Trimiteți-vă munca bună în baza de cunoștințe este simplu. Utilizați formularul de mai jos
Studenții, studenții absolvenți, tinerii oameni de știință care folosesc baza de cunoștințe în studiile și munca lor vă vor fi foarte recunoscători.
postat pe http://www.allbest.ru/
Instituție de învățământ autonomă de stat
învăţământ secundar profesional -
Colegiul de Stat de Științe Umaniste și Tehnologie Novokuybyshevsk
Eseu
dupa disciplina:"Chimie"
subiect: „Utilizarea izotopilor radioactivi în tehnologie”
Grazhdankina Daria Igorevna
Elevii anul I grupa 16
specialitatea 230115
2013
1. Ce sunt izotopii și producția lor
Bibliografie
detectarea defectelor atomului izotop radioactiv
1. Ce sunt izotopii?
Izotopii sunt varietăți ale oricărui element chimic din tabelul periodic D.I. Mendeleev, având greutăți atomice diferite. Diferiți izotopi ai oricărui element chimic au același număr de protoni în nucleu și același număr de electroni pe învelișurile atomului, au același număr atomic și ocupă anumite locuri în tabelul D.I., caracteristic unui element chimic dat. Mendeleev. Diferența de greutate atomică dintre izotopi se explică prin faptul că nucleele atomilor lor conțin un număr diferit de neutroni.
Izotopii radioactivi sunt izotopi ai oricărui element din tabelul periodic al lui D.I. Mendeleev, atomii cărora au nuclee instabile și trec într-o stare stabilă prin dezintegrare radioactivă însoțită de radiație. Pentru elementele cu numere atomice mai mari de 82, toți izotopii sunt radioactivi și se descompun prin descompunere alfa sau beta. Aceștia sunt așa-numiții izotopi radioactivi naturali, găsiți de obicei în natură. Atomii formați în timpul dezintegrarii acestor elemente, dacă au un număr atomic peste 82, suferă la rândul lor dezintegrare radioactivă, ai căror produse pot fi și radioactivi. Se dovedește a fi un lanț secvenţial sau o așa-numită familie de izotopi radioactivi. Sunt cunoscute trei familii radioactive naturale, numite după primul element al seriei, familiile de uraniu, toriu și actinouraniu (sau actiniu). Familia uraniului include radiul și radonul. Ultimul element al fiecărei serii se transformă ca urmare a descompunerii într-unul dintre izotopii stabili ai plumbului cu numărul de serie 82. Pe lângă aceste familii, sunt cunoscuți și anumiți izotopi radioactivi naturali ai elementelor cu numere de serie mai mici de 82. Aceștia sunt potasiu- 40 și alții. Dintre acestea, potasiul-40 este important, deoarece se găsește în orice organism viu.
Izotopii radioactivi ai tuturor elementelor chimice pot fi obținuți artificial.
Există mai multe modalități de a le obține. Izotopii radioactivi ai elementelor precum stronțiul, iodul, bromul și altele, care ocupă locurile mijlocii în tabelul periodic, sunt produse de fisiune ai nucleului uraniului. Dintr-un amestec de astfel de produse obținute într-un reactor nuclear, aceștia sunt izolați folosind metode radiochimice și alte metode. Izotopii radioactivi ai aproape tuturor elementelor pot fi produși într-un accelerator de particule prin bombardarea anumitor atomi stabili cu protoni sau deuteroni. O metodă comună de producere a izotopilor radioactivi din izotopi stabili ai aceluiași element este iradierea acestora cu neutroni într-un reactor nuclear. Metoda se bazează pe așa-numita reacție de captare a radiațiilor. Dacă o substanță este iradiată cu neutroni, aceștia din urmă, neavând încărcătură, se pot apropia liber de nucleul unui atom și, parcă, se pot „lipi” de el, formând un nou nucleu al aceluiași element, dar cu un neutron în plus. În acest caz, o anumită cantitate de energie este eliberată sub formă de radiații gamma, motiv pentru care procesul se numește captarea radiațiilor. Nucleii cu un exces de neutroni sunt instabili, deci izotopul rezultat este radioactiv. Cu rare excepții, izotopii radioactivi ai oricărui element pot fi obținuți în acest mod.
Când un izotop se descompune, se poate forma un izotop care este și radioactiv. De exemplu, stronțiul-90 se transformă în ytriu-90, bariul-140 în lantan-140 etc.
Au fost obținute artificial elemente transuraniu necunoscute în natură cu un număr de serie mai mare de 92 (neptuniu, plutoniu, americiu, curiu etc.), toți izotopii fiind radioactivi. Una dintre ele dă naștere unei alte familii radioactive - familia neptunium.
În timpul funcționării reactoarelor și acceleratoarelor, în materialele și părțile acestor instalații și echipamentele din jur se formează izotopi radioactivi. Această „activitate indusă”, care persistă mai mult sau mai puțin îndelungată după ce instalațiile au încetat să funcționeze, reprezintă o sursă nedorită de radiații. Activitatea indusă apare și într-un organism viu expus la neutroni, de exemplu în timpul unui accident sau a unei explozii atomice.
Activitatea izotopilor radioactivi se măsoară în unități de curie sau derivați ai săi - milicurie și microcurie.
În ceea ce privește proprietățile chimice și fizico-chimice, izotopii radioactivi nu se deosebesc practic de elementele naturale; amestecul lor cu orice substanță nu își schimbă comportamentul într-un organism viu.
Este posibilă înlocuirea izotopilor stabili din diverși compuși chimici cu astfel de atomi marcați. Proprietățile acestora din urmă nu se vor schimba ca urmare, iar dacă sunt introduse în organism, se vor comporta ca substanțe obișnuite, neetichetate. Cu toate acestea, datorită radiațiilor, este ușor de detectat prezența lor în sânge, țesuturi, celule etc. Izotopii radioactivi din aceste substanțe servesc astfel ca indicatori, sau indicatori, ai distribuției și destinului substanțelor introduse în organism. De aceea se numesc „trasori radioactivi”. O varietate de compuși anorganici și organici marcați cu diferiți izotopi radioactivi au fost sintetizați pentru diagnosticarea radioizotopilor și pentru diferite studii experimentale.
2. Aplicarea izotopilor radioactivi în tehnologie
Unul dintre cele mai remarcabile studii efectuate folosind „atomi marcați” a fost studiul metabolismului în organisme. S-a dovedit că într-un timp relativ scurt organismul suferă o reînnoire aproape completă. Atomii care o alcătuiesc sunt înlocuiți cu alții noi. Doar fierul, așa cum au arătat experimentele cu studiile izotopice ale sângelui, este o excepție de la această regulă. Fierul face parte din hemoglobina celulelor roșii din sânge. Când atomii de fier radioactiv au fost introduși în alimente, sa constatat că oxigenul liber eliberat în timpul fotosintezei a fost inițial parte din apă, nu dioxid de carbon. Domeniul de aplicare al izotopilor radioactivi în industrie este extins. Un exemplu în acest sens este următoarea metodă de monitorizare a uzurii segmentului pistonului la motoarele cu ardere internă. Prin iradierea segmentului pistonului cu neutroni, aceștia provoacă reacții nucleare în el și îl fac radioactiv. Când motorul funcționează, particulele de material inelului intră în uleiul de lubrifiere. Prin examinarea nivelului de radioactivitate din ulei după un anumit timp de funcționare a motorului, se determină uzura inelului. Izotopii radioactivi fac posibilă aprecierea difuziei metalelor, proceselor în furnalele înalte etc.
Radiația gamma puternică de la medicamentele radioactive este utilizată pentru a examina structura internă a pieselor turnate metalice pentru a detecta defectele acestora.
Izotopii radioactivi care emit raze gamma pot fi utilizați în locul unităților voluminoase de raze X pentru produsele transiluminate, deoarece proprietățile razelor gamma sunt similare cu proprietățile razelor X. O sursă de raze gamma este plasată pe o parte a produsului testat, iar filmul fotografic este plasat pe cealaltă parte. Această metodă de testare se numește detectarea defectelor gamma. În acest fel se verifică în prezent piesele turnate feroase și neferoase, produsele finite (produse din oțel cu grosimea de până la 300 mm) și calitatea sudurilor. Cu ajutorul izotopilor radioactivi, este ușor să măsurați grosimea unei benzi metalice sau a foilor de metal laminate din mers și fără contact și să mențineți automat o grosime constantă. O sursă de particule beta este plasată sub cureaua în mișcare care iese de sub rolele mașinii. O modificare a grosimii benzii duce, prin urmare, la o modificare a curentului din contor. Acest curent este amplificat și trimis fie către un dispozitiv de măsurare, fie către o mașină automată, care va apropia instantaneu rolele sau, dimpotrivă, le va împinge separat. Dispozitivele de acest tip sunt folosite și în industria hârtiei, cauciucului și a pielii. Au fost create surse radioizotopice de energie electrică. Ei folosesc căldura generată într-o probă care absoarbe radiația. Cu ajutorul termoelementelor, această căldură este transformată în curent electric. O sursă care cântărește câteva kilograme oferă o putere de câteva zeci de wați pentru 10 ani de funcționare neîntreruptă. Astfel de surse sunt folosite pentru alimentarea balizelor automate și a stațiilor meteo automate care funcționează în zone greu accesibile. Surse mai puternice au fost instalate pe roverele lunare sovietice lansate pe Lună. Au funcționat fiabil la temperaturi de la -140 la +120.
Unul dintre cele mai remarcabile studii efectuate folosind „atomi marcați” a fost studiul metabolismului în organisme. S-a dovedit că într-un timp relativ scurt organismul suferă o reînnoire aproape completă. Atomii care o alcătuiesc sunt înlocuiți cu alții noi. Doar fierul, așa cum au arătat experimentele cu studiile izotopice ale sângelui, este o excepție de la această regulă. Fierul face parte din hemoglobina celulelor roșii din sânge. Când atomii de fier radioactiv au fost introduși în alimente, sa constatat că oxigenul liber eliberat în timpul fotosintezei a fost inițial parte din apă, nu dioxid de carbon. Izotopii radioactivi sunt utilizați în medicină atât pentru diagnostic, cât și în scop terapeutic. Sodiul radioactiv, injectat în cantități mici în sânge, este folosit pentru a studia circulația sângelui; iodul este depus intens în glanda tiroidă, în special în boala Graves. Prin observarea depunerilor de iod radioactiv cu ajutorul unui contor, se poate face un diagnostic rapid. Dozele mari de iod radioactiv provoacă distrugerea parțială a țesuturilor cu dezvoltare anormală și, prin urmare, iodul radioactiv este utilizat pentru a trata boala Graves. Radiația gamma intensă de cobalt este utilizată în tratamentul cancerului (pistol cu cobalt).
Lista literaturii folosite
1. Gaisinsky M.N., Chimia nucleară și aplicațiile sale, trad. din franceză, M., 1961
2. Fizica nucleară experimentală, ed. E. Segre, trad. din engleză, vol. 3, M., 1961; Instrumente INTERNET
Postat pe Allbest.ru
Documente similare
Esența fenomenului radioactivității, istoria descoperirii și studiului acestuia, cunoștințele moderne, semnificația și aplicarea sa în diverse domenii. Tipuri de radiații radioactive, caracteristicile și caracteristicile lor distinctive. Ordinea și etapele dezintegrarii alfa, beta și gamma.
lucrare de curs, adăugată 05.10.2009
Radioactivitatea naturală este cauzată de izotopii radioactivi prezenți în toate straturile pământului. Strămoșii izotopilor radioactivi care fac parte din familiile radioactive sunt radiul și toriu.
lucrare de curs, adăugată 25.11.2008
Legea dezintegrarii radioactive. Determinarea ionilor elementelor chimice. Metoda de titrare radiometrică, diluare izotopică, analiza activării, determinarea conținutului de elemente chimice prin radiația izotopilor lor radioactivi naturali.
prezentare, adaugat 05.07.2016
Determinarea conținutului relativ de izotopi de plutoniu prin analiza spectrelor, raportul cantitativ al conținutului de izotopi de-a lungul liniilor identificate. Evaluarea găsirii scăderilor și secțiunilor liniare ale spectrului. Calculul erorii de conținut.
lucrare curs, adaugat 23.08.2016
Serii radioactive naturale și artificiale. Tipuri de dezintegrare radioactivă. Principala serie radioactivă observată în natură. Caracteristicile seriei de toriu, neptunium, radiu, actiniu. Transformări radioactive ale nucleelor. Lanțuri consecutive de nuclizi.
prezentare, adaugat 30.05.2015
Caracteristicile proprietăților chimice și fizice ale hidrogenului. Diferențele de masă atomică între izotopii hidrogenului. Configurația unui singur strat de electroni al unui atom de hidrogen neutru, neexcitat. Istoria descoperirii, apariția în natură, metodele de producție.
prezentare, adaugat 14.01.2011
Caracteristicile proprietăților chimice ale actinidelor. Determinarea cantitativă a elementelor transplutoniului. Separarea prin precipitare cu reactivi anorganici si organici. Metode de izolare și separare a elementelor de transplutoniu. Obținerea uraniului metalic.
rezumat, adăugat 10.03.2010
Principii generale de clasificare a substanţelor anorganice complexe şi simple. Dimensiunile atomice și relația lor cu poziția în tabelul periodic al elementelor. Conceptul de disociere electrică și soluții electrolitice. Legături de hidrogen și senzori cu membrană.
test, adaugat 02.01.2011
Metode de ionizare și scintilație a radiațiilor radioactive. Determinarea ionilor elementelor chimice în soluție folosind reactivi radioactivi. Timp optim pentru înregistrarea radiațiilor. Metoda de titrare radiometrică și analiză de activare.
lucrare curs, adăugată 05.07.2016
Proprietățile fizico-chimice ale acidului acetic. Caracteristicile procesului de oxidare a aldehidelor. Metodă de producere a acetaldehidei și etanalului. Principii pentru calcularea cantității de produse secundare formate în timpul producerii acidului acetic. Esența metodei Kolbe.
Prepararea și aplicarea izotopilor radioactivi Elev grupa 1 BC Galtsova Vlada
IZOTOPII sunt varietăți ale aceluiași element chimic care sunt similare în proprietățile lor fizico-chimice, dar au mase atomice diferite. Un atom al oricărui element chimic constă dintr-un nucleu încărcat pozitiv și un nor de electroni încărcați negativ care îl înconjoară (vezi și NUCLEUL ATOM). Poziția unui element chimic în tabelul periodic al lui Mendeleev (numărul său de serie) este determinată de sarcina nucleului atomilor săi. Izotopii sunt, prin urmare, numiți varietăți ale aceluiași element chimic, atomii cărora au aceeași sarcină nucleară (și, prin urmare, practic aceleași învelișuri de electroni), dar diferă în valorile masei nucleare. Conform expresiei figurative a lui F. Soddy, atomii izotopilor sunt aceiași „în exterior”, dar diferiți „în interior”.
Istoria descoperirii izotopilor Prima dovadă că substanțele având același comportament chimic pot avea proprietăți fizice diferite a fost obținută din studiul transformărilor radioactive ale atomilor elementelor grele. În 1906-07, s-a dovedit că produsul dezintegrarii radioactive a uraniului - ioniu și produsul dezintegrarii radioactive a toriului - radiotoriul, au aceleași proprietăți chimice ca și toriul, dar diferă de acesta prin masa atomică și caracteristicile dezintegrarii radioactive. În 1932, a fost descoperit neutronul - o particulă care nu are sarcină, cu o masă apropiată de masa nucleului unui atom de hidrogen - un proton și a fost creat un model proton-neutron al nucleului. Drept urmare, știința a stabilit definiția modernă finală a conceptului de izotopi
Producția de izotopi radioactivi Izotopii radioactivi sunt produși în reactoare nucleare și acceleratoare de particule
Aplicarea izotopilor radioactivi medicina biologiei industriei arheologiei agricole
Izotopi radioactivi în biologie. Unul dintre cele mai remarcabile studii efectuate folosind „atomi marcați” a fost studiul metabolismului în organisme.
Izotopi radioactivi în medicină Pentru diagnostic și în scop terapeutic. Sodiul radioactiv este folosit pentru a studia circulația sângelui. Iodul este depus intens în glanda tiroidă, în special în boala Graves.
Izotopi radioactivi în fermă Iradierea semințelor de plante (bumbac, varză, ridichi). Radiațiile provoacă mutații în plante și microorganisme.
Izotopi radioactivi în arheologie O aplicație interesantă pentru determinarea vârstei obiectelor antice de origine organică (lemn, cărbune). Această metodă este folosită pentru a determina vârsta mumiilor egiptene și a rămășițelor incendiilor preistorice.
Izotopi radioactivi în industrie O metodă de monitorizare a uzurii segmentelor de piston în motoarele cu ardere internă. Permite aprecierea difuziei metalelor si proceselor in furnalele inalte
Spărgătorul de gheață nuclear „Lenin” Creat în 1959. Verificarea ratei dozei de radiație în incinta acestuia.
Lucrul cu substanțe radioactive folosind un manipulator
"Eter" - un convertor de radioizotopi pentru alimentarea dispozitivelor situate în spațiul cosmic și în mare
Studiul sudurilor folosind radiația γ. Iradierea produselor agricole pentru creșterea randamentului acestora
Distribuția fosforului radioactiv adăugat la îngrășăminte în frunzele de roșii.Topedo pentru lucrul cu substanțe radioactive.
Dispozitiv de Gammaterapie. Studiul glandei tiroide folosind iod radioactiv
Instituția de învățământ municipală „Școala secundară Pobedinskaya” districtul Shegarsky, regiunea Tomsk
CERTIFICAREA DE STAT (FINALA) A ABSOLUTENȚILOR CLASA A IX-A
REZUMAT DE FIZICĂ
FENOMENUL DE RADIOACTIVITATE. IMPORTANȚA SA ÎN ȘTIINȚĂ, TEHNOLOGIE, MEDICINĂ
Efectuat: Dadaev Aslan, elev în clasa a IX-a
supraveghetor: Gagarina Lyubov Alekseevna, profesor de fizică
Pobeda 2010
1. Introducere……………………………………………………………………...pagina 1
2. Fenomenul de radioactivitate………..……………………….................pag. 2
2.1.Descoperirea radioactivității…………………………………………………….pagina 2
2.2. Surse de radiații…………………………………………………….. pagina 6
3. Producerea și utilizarea izotopilor radioactivi……………..pagina 8
3.1.Utilizarea izotopilor în medicină……………………………….pag. 8
3.2. Izotopi radioactivi în agricultură……… pagina 10
3.3.Cronometria radiațiilor…………………………………p.11
3.4. Aplicarea izotopilor radioactivi în industrie...p. 12
3.5. Utilizarea izotopilor în știință……………………………...pagina 12
4. Concluzie…………………………………………………………………...pagina 13
5. Literatură………………………………………………………..pagina 14
INTRODUCERE
Ideea atomilor ca particule minuscule imuabile de materie a fost distrusă de descoperirea electronului, precum și de fenomenul de dezintegrare radioactivă naturală descoperit de fizicianul francez A. Becquerel. O contribuție semnificativă la studiul acestui fenomen a fost adusă de remarcabilii fizicieni francezi Maria Sklodowska-Curie și Pierre Curie.
Radioactivitatea naturală există de miliarde de ani și este literalmente peste tot. Radiațiile ionizante au existat pe Pământ cu mult înainte de originea vieții pe acesta și au fost prezente în spațiu înainte de apariția Pământului însuși. Materialele radioactive au făcut parte din Pământ încă de la naștere. Orice persoană este ușor radioactivă: în țesuturile corpului uman, una dintre principalele surse de radiații naturale este potasiul - 40 și rubidiul - 87 și nu există nicio modalitate de a scăpa de ele.
Efectuând reacții nucleare prin bombardarea nucleelor atomilor de aluminiu cu particule a, celebrii fizicieni francezi Frederic și Irene Curie-Joliot au reușit să creeze artificial nuclee radioactive în 1934. Radioactivitatea artificială nu este în principiu diferită de radioactivitatea naturală și se supune acelorași legi.
În prezent, izotopii radioactivi artificiali sunt produși în moduri diferite. Cea mai frecventă este iradierea unei ținte (viitorul medicament radioactiv) într-un reactor nuclear. Este posibil să iradiezi o țintă cu particule încărcate în instalații speciale în care particulele sunt accelerate la energii mari.
Ţintă: afla in ce domenii ale vietii este folosit fenomenul de radioactivitate.
Sarcini:
· Studiați istoria descoperirii radioactivității.
· Aflați ce se întâmplă cu o substanță în timpul radiațiilor radioactive.
· Aflați cum să obțineți izotopi radioactivi și unde vor fi folosiți.
· Dezvoltați abilitățile de a lucra cu literatură suplimentară.
· Realizați o prezentare computerizată a materialului.
PARTE PRINCIPALĂ
2.Fenomenul de radioactivitate
2.1.Descoperirea radioactivitatii
Poveste radioactivitate a început cu lucrarea fizicianului francez Henri Becquerel asupra luminiscenței și razelor X în 1896.
Descoperirea radioactivității, cea mai izbitoare dovadă a structurii complexe a atomului .
Comentând descoperirea lui Roentgen, oamenii de știință emit ipoteza că razele X sunt emise în timpul fosforescenței, indiferent de prezența razelor catodice. A. Becquerel a decis să testeze această ipoteză. Învelind placa fotografică în hârtie neagră, a așezat pe ea o placă de metal de formă bizară acoperită cu un strat de sare de uraniu. După ce a expus-o la lumina soarelui timp de patru ore, Becquerel a dezvoltat placa fotografică și a văzut pe ea silueta exactă a unei figuri de metal. A repetat experimentele cu mari variații, obținând amprente ale unei monede și ale unei chei. Toate experimentele au confirmat ipoteza testată, pe care Becquerel a raportat-o pe 24 februarie la o ședință a Academiei de Științe. Cu toate acestea, Becquerel nu oprește experimentele, pregătind din ce în ce mai multe opțiuni noi.

Henri Becquerel Welhelm Conrad Roentgen
Pe 26 februarie 1896, vremea peste Paris s-a deteriorat și plăcile fotografice pregătite cu bucăți de sare de uraniu au trebuit să fie așezate într-un sertar întunecat de birou până la apariția soarelui. A apărut peste Paris pe 1 martie, iar experimentele au putut fi continuate. Luând înregistrările, Becquerel a decis să le dezvolte. După ce a dezvoltat plăcile, omul de știință a văzut pe ele siluete de mostre de uraniu. Neînțelegând nimic, Becquerel a decis să repete experimentul la întâmplare.
El a pus două farfurii într-o cutie rezistentă la lumină, a turnat sare de uraniu peste ele, punând mai întâi sticlă pe una dintre ele și o farfurie de aluminiu pe cealaltă. Toate acestea au fost într-o cameră întunecată timp de cinci ore, după care Becquerel a dezvoltat plăcile fotografice. Și bine, siluetele mostrelor sunt din nou clar vizibile. Aceasta înseamnă că unele raze se formează în sărurile de uraniu. Arata ca raze X, dar de unde vin? Un lucru este clar: nu există nicio legătură între razele X și fosforescență.
El a raportat acest lucru la o ședință a Academiei de Științe din 2 martie 1896, derutând complet toți membrii acesteia.
Becquerel a mai stabilit că intensitatea radiației din aceeași probă nu se modifică în timp și că o nouă radiație este capabilă să descarce corpuri electrificate.
Majoritatea membrilor Academiei din Paris, după următorul raport al lui Becquerel la întâlnirea din 26 martie, credeau că are dreptate.
Fenomenul descoperit de Becquerel a fost numit radioactivitate, la propunerea Mariei Sklodowska-Curie.


Maria Skłodowska – Curie
Radioactivitate - capacitatea atomilor unor elemente chimice de a emite spontan.
În 1897, Maria, în timp ce își urmărea teza de doctorat, după ce a ales un subiect de cercetare - descoperirea lui Becquerel (Pierre Curie și-a sfătuit soția să aleagă acest subiect), a decis să găsească răspunsul la întrebarea: care este adevărata sursă de uraniu radiatii? În acest scop, ea decide să examineze un număr mare de mostre de minerale și săruri și să afle dacă numai uraniul are proprietatea de a radia. Lucrând cu mostre de toriu, ea descoperă că, la fel ca uraniul, produce aceleași raze și aproximativ aceeași intensitate. Aceasta înseamnă că acest fenomen se dovedește a fi o proprietate nu numai a uraniului și trebuie să i se dea un nume special. Uraniul și toriu au fost numite elemente radioactive. Lucrările au continuat cu noi minerale.
Pierre, ca fizician, simte importanța lucrării și, părăsind temporar studiul cristalelor, începe să lucreze împreună cu soția sa. În urma acestei lucrări comune au fost descoperite noi elemente radioactive: poloniu, radiu etc.
În noiembrie 1903, Royal Society i-a acordat lui Pierre și Marie Curie unul dintre cele mai înalte premii științifice ale Angliei, Medalia Davy.
Pe 13 noiembrie, familia Curie și Becquerel au primit o telegramă de la Stockholm prin care anunța că cei trei au primit Premiul Nobel pentru Fizică pentru descoperirile lor remarcabile în domeniul radioactivității.
Lucrarea începută de soții Curie a fost preluată de studenții lor, printre care fiica Irene și ginerele Frédéric Joliot, care au devenit laureați ai Premiului Nobel pentru descoperire în 1935. radioactivitate artificială .

Irene și Frederic Curie - Joliot
fizicienii englezi E. RutherfordȘi F. Soddy S-a dovedit că în toate procesele radioactive au loc transformări reciproce ale nucleelor atomice ale elementelor chimice. Un studiu al proprietăților radiațiilor care însoțesc aceste procese în câmpurile magnetice și electrice a arătat că aceasta este împărțită în particule a, particule b și raze g (radiație electromagnetică cu o lungime de undă foarte scurtă).


E. Rutherford F. Soddy
Un timp mai târziu, ca urmare a studierii diferitelor caracteristici și proprietăți fizice ale acestor particule (sarcină electrică, masă etc.), a fost posibil să se stabilească că particula b este un electron, iar particula a este un atom complet ionizat de elementul chimic heliu (adică un atom de heliu care și-a pierdut ambii electroni).
În plus, s-a dovedit că radioactivitate este capacitatea unor nuclee atomice de a se transforma spontan în alte nuclee cu emisia de particule.
De exemplu, au fost găsite mai multe varietăți de atomi de uraniu: cu mase nucleare aproximativ egale cu 234 amu, 235 amu, 238 amu. și 239 amu Mai mult, toți acești atomi aveau aceleași proprietăți chimice. Au intrat în reacții chimice în același mod, formând aceiași compuși.
Unele reacții nucleare produc radiații puternic penetrante. Aceste raze pătrund într-un strat de plumb gros de câțiva metri. Această radiație este un flux de particule încărcate neutru. Aceste particule sunt numite neutroni.
Unele reacții nucleare produc radiații puternic penetrante. Aceste raze vin în diferite tipuri și au puteri de penetrare diferite. De exemplu, flux de neutroni pătrunde printr-un strat de plumb gros de câțiva metri.
2.2. Surse de radiații
Radiațiile sunt foarte numeroase și variate, dar putem distinge aproximativ Șapte sursele sale principale.
Prima sursă este Pământul nostru. Această radiație se explică prin prezența elementelor radioactive pe Pământ, a căror concentrație variază mult în diferite locuri.
A doua sursă radiație - spațiu, de unde un flux de particule de înaltă energie cade constant pe Pământ. Sursele de radiație cosmică sunt exploziile stelare din galaxie și erupțiile solare.
A treia sursă Radiațiile sunt materiale naturale radioactive folosite de oameni pentru construcția spațiilor rezidențiale și industriale. În medie, rata dozei în interiorul clădirilor este cu 18% - 50% mai mare decât în exterior. O persoană își petrece trei sferturi din viață în interior. O persoană care stă constant într-o cameră construită din granit poate primi - 400 mrem/an, din cărămidă roșie – 189 mrem/an, din beton – 100 mrem/an, din lemn – 30 mrem/an.
Al patrulea Sursa de radioactivitate este puțin cunoscută de populație, dar nu mai puțin periculoasă. Acestea sunt materiale radioactive pe care oamenii le folosesc în activitățile de zi cu zi.
Cernelurile pentru imprimarea cecurilor bancare includ carbon radioactiv, care asigură identificarea ușoară a documentelor falsificate.
Uraniul este folosit pentru a produce vopsea sau email pe ceramică sau bijuterii.
Uraniul și toriul sunt folosite în producția de sticlă.
Dinții din porțelan artificial sunt întăriți cu uraniu și ceriu. În același timp, radiația către membranele mucoase adiacente dinților poate ajunge la 66 rem/an, în timp ce rata anuală pentru întregul corp nu trebuie să depășească 0,5 rem (adică de 33 de ori mai mult)
Un ecran TV emite 2-3 mrem/an de persoană.
a cincea sursă – întreprinderi de transport și prelucrare a materialelor radioactive.
Şaselea Sursa de radiații sunt centralele nucleare. La centralele nucleare,
Pe lângă deșeurile solide, există și deșeuri lichide (apa contaminată din circuitele de răcire a reactorului) și deșeuri gazoase conținute în dioxidul de carbon folosit pentru răcire.
Al șaptelea Sursa de radiații radioactive sunt instalațiile medicale. În ciuda caracterului comun al utilizării lor în practica de zi cu zi, pericolul radiațiilor de la ele este mult mai mare decât din toate sursele discutate mai sus și ajunge uneori la zeci de rem. Una dintre metodele comune de diagnosticare este un aparat cu raze X. Deci, cu radiografia dinților - 3 rem, cu fluoroscopia stomacului - la fel, cu fluorografie - 370 mrem.
Ce se întâmplă cu materia în timpul radiațiilor radioactive?
in primul rand, uimitoarea consistență cu care elementele radioactive emit radiații. Pe parcursul zilelor, lunilor, anilor, intensitatea radiației nu se schimbă în mod semnificativ. Nu este afectat de încălzire sau presiune crescută; reacțiile chimice în care a intrat elementul radioactiv nu au afectat nici intensitatea radiației.
În al doilea rând, radioactivitatea este însoțită de eliberarea de energie și este eliberată continuu de-a lungul unui număr de ani. De unde vine această energie? Când o substanță devine radioactivă, experimentează unele schimbări profunde. S-a presupus că atomii înșiși suferă transformări.
Prezența acelorași proprietăți chimice înseamnă că toți acești atomi au același număr de electroni în învelișul de electroni și, prin urmare, aceleași sarcini nucleare.
Dacă sarcinile nucleelor atomice sunt aceleași, atunci acești atomi aparțin aceluiași element chimic (în ciuda diferențelor dintre masele lor) și au același număr atomic în tabelul D.I. Mendeleev. Sunt numite varietăți ale aceluiași element chimic care diferă în masa nucleelor atomice izotopi .
3. Producerea și utilizarea izotopilor radioactivi
Izotopii radioactivi găsiți în natură se numesc natural. Dar multe elemente chimice apar în natură numai într-o stare stabilă (adică, radioactivă).
În 1934, oamenii de știință francezi Irène și Frédéric Joliot-Curie au descoperit că izotopii radioactivi pot fi creați artificial ca urmare a reacțiilor nucleare. Acești izotopi au fost numiți artificial .
Reactoarele nucleare și acceleratoarele de particule sunt de obicei folosite pentru a produce izotopi radioactivi artificiali. Există o industrie specializată în producerea unor astfel de elemente.
Ulterior, s-au obținut izotopi artificiali ai tuturor elementelor chimice. În total, în prezent sunt cunoscuți aproximativ 2000 de izotopi radioactivi, iar 300 dintre ei sunt naturali.
În prezent, izotopii radioactivi sunt utilizați pe scară largă în diverse domenii ale activității științifice și practice: tehnologie, medicină, agricultură, comunicații, armată și altele. În acest caz, așa-numitul metoda atomului etichetat.
3.1.Utilizarea izotopilor în medicină
Aplicarea izotopilor Unul dintre cele mai remarcabile studii efectuate folosind „atomi marcați” a fost studiul metabolismului în organisme.
Cu ajutorul izotopilor au fost dezvăluite mecanismele de dezvoltare (patogeneza) a unui număr de boli; De asemenea, sunt folosite pentru a studia metabolismul și a diagnostica multe boli.
Izotopii sunt introduși în corpul uman în cantități extrem de mici (sigure pentru sănătate) și nu sunt capabili să provoace modificări patologice. Ele sunt distribuite inegal pe tot corpul prin sânge. Radiația produsă în timpul dezintegrarii unui izotop este înregistrată de instrumente (contoare speciale de particule, fotografie) situate în apropierea corpului uman. Ca rezultat, puteți obține o imagine a oricărui organ intern. Din această imagine se poate aprecia dimensiunea și forma acestui organ, concentrația crescută sau scăzută a izotopului în
diferitele sale părți. De asemenea, puteți evalua starea funcțională (adică munca) a organelor interne prin rata de acumulare și eliminare a radioizotopului.
Astfel, starea circulației cardiace, viteza fluxului sanguin și imaginea cavităților inimii sunt determinate folosind compuși incluzând izotopi de sodiu, iod și tehnețiu; izotopii de tehnețiu și xenon sunt utilizați pentru a studia ventilația pulmonară și bolile măduvei spinării; macroagregatele de albumină serică umană cu izotop de iod sunt utilizate pentru a diagnostica diferite procese inflamatorii în plămâni, tumorile acestora și pentru diferite boli ale glandei tiroide.


Utilizarea izotopilor în medicină
Funcțiile de concentrare și excreție ale ficatului sunt studiate folosind vopsea de trandafir Bengal cu un izotop de iod și aur. Imaginile intestinelor și stomacului sunt obținute folosind un izotop de tehnețiu, splina este obținută folosind celule roșii din sânge cu un izotop de tehnețiu sau crom; Bolile pancreatice sunt diagnosticate folosind un izotop de seleniu. Toate aceste date ne permit să facem un diagnostic corect al bolii.
Folosind metoda „atomilor marcați”, sunt studiate și diverse anomalii în funcționarea sistemului circulator și sunt detectate tumori (deoarece în ele se acumulează unii radioizotopi). Datorită acestei metode, s-a descoperit că într-un timp relativ scurt corpul uman este aproape complet reînnoit. Singura excepție este fierul, care face parte din sânge: începe să fie absorbit de organism din alimente numai atunci când rezervele sale sunt epuizate.
Atunci când alegeți un izotop, aspectele importante includ sensibilitatea metodei de analiză a izotopilor, precum și tipul de dezintegrare radioactivă și energia radiației.
În medicină, izotopii radioactivi sunt utilizați nu numai pentru diagnostic, ci și pentru tratamentul anumitor boli, precum cancerul, boala Graves etc.
Datorită utilizării unor doze foarte mici de radioizotopi, expunerea la radiații a organismului în timpul diagnosticării și tratamentului cu radiații nu reprezintă un pericol pentru pacienți.
3.2. Izotopi radioactivi în agricultură
Izotopii radioactivi devin din ce în ce mai folosiți în agricultură. Iradierea semințelor de plante (bumbac, varză, ridichi etc.) cu doze mici de raze gamma de la medicamentele radioactive duce la o creștere vizibilă a randamentului. Dozele mari de radiații provoacă mutații în plante și microorganisme, ceea ce în unele cazuri duce la apariția unor mutanți cu noi proprietăți valoroase ( selecție radio). Așa s-au dezvoltat soiuri valoroase de grâu, fasole și alte culturi și s-au obținut microorganisme extrem de productive utilizate în producția de antibiotice.
Radiația gamma de la izotopii radioactivi este, de asemenea, utilizată pentru combaterea insectelor dăunătoare și pentru conservarea alimentelor. „Atomii marcați” sunt utilizați pe scară largă în tehnologia agricolă. De exemplu, pentru a afla ce îngrășământ cu fosfor este mai bine absorbit de o plantă, diferite îngrășăminte sunt etichetate cu fosfor radioactiv. Prin examinarea plantelor pentru radioactivitate, este posibil să se determine cantitatea de fosfor pe care au absorbit-o din diferite tipuri de îngrășăminte.
Metoda carbonului radioactiv a primit o aplicație interesantă pentru determinarea vârstei obiectelor antice de origine organică (lemn, cărbune, țesături etc.). Plantele conțin întotdeauna un izotop radioactiv beta de carbon cu un timp de înjumătățire de T = 5700 de ani. Se formează în atmosfera Pământului în cantități mici din azot sub influența neutronilor. Acestea din urmă apar din cauza reacțiilor nucleare cauzate de particulele rapide care intră în atmosferă din spațiu (razele cosmice). Combinându-se cu oxigenul, acest carbon formează dioxid de carbon, care este absorbit de plante și, prin intermediul acestora, de animale.
Izotopii sunt folosiți pe scară largă pentru a determina proprietățile fizice ale solului
și rezervele de elemente de hrană vegetală din acesta, pentru a studia interacțiunea solului și îngrășămintele, procesele de absorbție a nutrienților de către plante și intrarea alimentelor minerale în plante prin frunze. Izotopii sunt utilizați pentru a identifica efectul pesticidelor asupra organismului plantei, ceea ce face posibilă determinarea concentrației și momentul tratării culturilor. Prin metoda izotopilor sunt studiate cele mai importante proprietăți biologice ale culturilor agricole (la evaluarea și selectarea materialului de reproducere), randamentul, coacerea timpurie și rezistența la frig.
ÎN creșterea animalelor studiază procesele fiziologice care au loc în corpul animalelor, analizează hrana pentru conținutul de substanțe toxice (din care doze mici sunt greu de determinat prin metode chimice) și microelemente. Cu ajutorul izotopilor, sunt dezvoltate tehnici de automatizare a proceselor de producție, de exemplu, separarea culturilor de rădăcină de pietre și bulgări de sol atunci când se recoltează cu o combină pe soluri stâncoase și grele.
3.3.Cronometria radiatiilor
Unii izotopi radioactivi pot fi utilizați cu succes pentru a determina vârsta diferitelor fosile ( cronometria radiatiilor). Cea mai comună și eficientă metodă de cronometrie a radiațiilor se bazează pe măsurarea radioactivității substanțelor organice, care este cauzată de carbonul radioactiv (14C).
Cercetările au arătat că pentru fiecare gram de carbon din orice organism apar 16 dezintegrari beta radioactive pe minut (mai precis, 15,3 ± 0,1). După 5730 de ani, în fiecare gram de carbon se vor descompune doar 8 atomi pe minut, după 11.460 de ani - 4 atomi.
Un gram de carbon din probele tinere de pădure emite aproximativ cincisprezece particule beta pe secundă. După moartea organismului, reaprovizionarea acestuia cu carbon radioactiv încetează. Cantitatea disponibilă din acest izotop scade din cauza radioactivității. Prin determinarea procentului de carbon radioactiv din resturile organice, este posibil să se determine vârsta acestora dacă acesta se află în intervalul de la 1000 la 50.000 și chiar până la 100.000 de ani.
Numărul de dezintegrari radioactive, adică radioactivitatea probelor studiate, este măsurat de detectoare de radiații radioactive.
Astfel, prin măsurarea numărului de dezintegrari radioactive pe minut într-o anumită cantitate de greutate a materialului probei studiate și recalculând acest număr per gram de carbon, putem determina vârsta obiectului de la care a fost prelevată proba. Această metodă este folosită pentru a determina vârsta mumiilor egiptene, a resturilor de incendii preistorice etc.
3.4. Aplicarea radioactivelor izotopi în industrie
Un exemplu este următoarea metodă de monitorizare a uzurii segmentului pistonului la motoarele cu ardere internă. Prin iradierea segmentului pistonului cu neutroni, aceștia provoacă reacții nucleare în el și îl fac radioactiv. Când motorul funcționează, particulele de material inelului intră în uleiul de lubrifiere. Prin examinarea nivelului de radioactivitate din ulei după un anumit timp de funcționare a motorului, se determină uzura inelului. Izotopii radioactivi fac posibilă aprecierea difuziei metalelor, proceselor în furnalele înalte etc. Radiația gamma puternică de la medicamentele radioactive este utilizată pentru a studia structura internă a turnărilor metalice pentru a detecta defectele acestora.
Izotopii sunt utilizați și în echipamentele de fizică nucleară pentru fabricarea contoarelor de neutroni, ceea ce face posibilă creșterea eficienței de numărare de peste 5 ori, iar în energia nucleară ca moderatori și absorbanți de neutroni.
3.5. Utilizarea izotopilor în știință
Utilizarea izotopilor în biologie a condus la o revizuire a ideilor anterioare despre natura fotosintezei, precum și despre mecanismele care asigură asimilarea de către plante a substanțelor anorganice a carbonaților, nitraților, fosfaților etc. o populație dată, migrarea microbilor, precum și compuși individuali în organism. Prin introducerea unei etichete în organisme cu hrană sau prin injecție, s-a putut studia viteza și rutele de migrație ale multor insecte (țânțari, muște, lăcuste), păsări, rozătoare și alte animale mici și să se obțină date despre mărimea populațiilor acestora.
În zonă fiziologia și biochimia plantelor Cu ajutorul izotopilor au fost rezolvate o serie de probleme teoretice și aplicate: au fost clarificate căile de intrare a mineralelor, lichidelor și gazelor în plante, precum și rolul diferitelor elemente chimice, inclusiv microelemente, în viața plantelor. S-a demonstrat, în special, că carbonul pătrunde în plante nu numai prin frunze, ci și prin sistemul radicular; căile și vitezele de mișcare a unui număr de substanțe de la sistemul radicular la tulpină și frunze și de la aceste organe la rădăcinile au fost stabilite.
În zonă fiziologia și biochimia animalelor și oamenilor au fost studiate ratele de intrare a diferitelor substanțe în țesuturile lor (inclusiv rata de încorporare a fierului în hemoglobină, fosfor în țesutul nervos și muscular, calciu în oase). Utilizarea alimentelor „etichetate” a condus la o nouă înțelegere a ratelor de absorbție și distribuție a nutrienților, „soarta” acestora în organism și a ajutat la monitorizarea influenței factorilor interni și externi (foame, asfixie, surmenaj etc.) asupra metabolismului.
CONCLUZIE
Fizicienii francezi remarcabili Maria Sklodowska-Curie și Pierre Curie, fiica lor Irene și ginerele Frédéric Joliot și mulți alți oameni de știință nu numai că au avut o mare contribuție la dezvoltarea fizicii nucleare, dar au fost luptători pasionați pentru pace. Ei au efectuat lucrări semnificative privind utilizarea pașnică a energiei atomice.
În Uniunea Sovietică, lucrările asupra energiei atomice au început în 1943 sub conducerea remarcabilului om de știință sovietic I.V. Kurchatov. În condițiile dificile ale unui război fără precedent, oamenii de știință sovietici au rezolvat cele mai complexe probleme științifice și tehnice legate de stăpânirea energiei atomice. La 25 decembrie 1946, sub conducerea lui I.V. Kurchatov, a avut loc pentru prima dată o reacție în lanț pe continentul Europa și Asia. A început în Uniunea Sovietică era atomului pașnic.
În timpul muncii mele, am aflat că izotopii radioactivi obținuți artificial și-au găsit aplicații pe scară largă în știință, tehnologie, agricultură, industrie, medicină, arheologie și alte domenii. Acest lucru se datorează următoarelor proprietăți ale izotopilor radioactivi:
· o substanta radioactiva emite continuu un anumit tip de particula iar intensitatea nu se modifica in timp;
· radiația are o anumită capacitate de penetrare;
· radioactivitatea este însoțită de eliberarea de energie;
· sub influența radiațiilor pot apărea modificări în substanța iradiată;
· radiațiile pot fi detectate în diferite moduri: cu contoare speciale de particule, fotografie etc.
LITERATURĂ
1. F.M. Diaghilev „Din istoria fizicii și viața creatorilor săi” - M.: Educație, 1986.
2. A.S. Enokhin, O.F. Kabardin și alții „Anthology on Physics” - M.: Educație, 1982.
3. P.S. Kudryavtsev. „Istoria fizicii” - M.: Educație, 1971.
4. G.Ya. Myakishev, B.B. Buhovtsev „Fizica clasa a XI-a”. - M.: Educație, 2004.
5. A.V. Peryshkin, E.V. Gutnik „Fizica clasa a IX-a”. - M.: Dropia, 2005.
6. Resurse de internet.
Revizuire
pentru un eseu de examen la fizică „Fenomenul radioactivităţii. Semnificația sa în știință, tehnologie, medicină.”
Autorul vede relevanța temei alese în posibilitatea utilizării energiei nucleare în scopuri pașnice. Izotopii radioactivi obținuți artificial și-au găsit aplicare largă în diverse domenii ale activității științifice și practice: știință, tehnologie, agricultură, industrie, medicină, arheologie etc.
Cu toate acestea, secțiunea „Introducere” nu indică relevanța și interesul autorului pentru tema aleasă a rezumatului.
Descoperirea radioactivității este explicată într-o manieră accesibilă, logică; cercetări efectuate folosind „atomi marcați”.
Formatarea rezumatului nu îndeplinește în toate cazurile cerințele:
· Paginile nu sunt numerotate;
· Fiecare secțiune nu este tipărită dintr-o pagină nouă;
· Nu există referiri la ilustrații în text;
· Secțiunea „Literatura” nu listează site-urile de resurse de Internet.
În general, în ciuda unor deficiențe minore în compilare și design, putem spune că rezumatul „Fenomenul radioactivității. Semnificația sa în știință, tehnologie și medicină merită o evaluare „bună”.
Profesor de fizică, Instituția Municipală de Învățământ „Școala Gimnazială Pobedinskaya”: ___________/L.A. Gagarina/